研究CO2的再利用有利于低碳减排的同时获得新的能源物质。如一定条件下,CO2加氢可制得甲醇: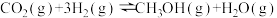
 。回答下列问题:
。回答下列问题:
(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。
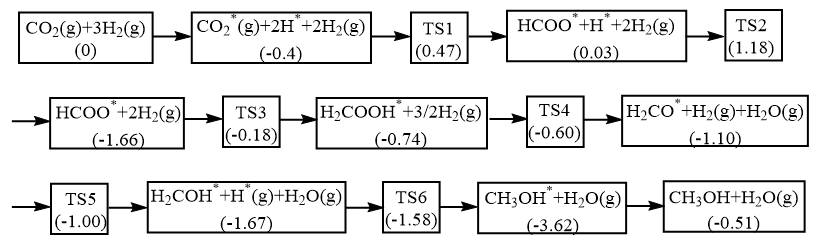
该反应
___________ 0(填“>”或“<”);该历程中总反应的决速步方程式为___________ 。
(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
①用H2表示该反应0~5min内的平均反应速率为___________ 。
②CO2的平衡转化率为___________ ;T℃时,该反应的平衡常数为___________ (保留一位小数)。
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是___________ (填标号)。
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
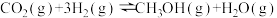
 。回答下列问题:
。回答下列问题:(1)我国科研人员研究的该反应历程如图,吸附在催化剂表面上的物种用“*”表示,“TS”表示过渡态,括号里的数字表示微粒的相对总能量(单位为eV)。

该反应

(2)T℃时,在一容积为2L的恒容密闭容器中充入2mol CO2和6molH2,测得不同时刻容器中的压强关系如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
 | 0.80 | 0.72 | 0.66 | 0.62 | 0.60 | 0.60 |
①用H2表示该反应0~5min内的平均反应速率为
②CO2的平衡转化率为
③其它条件不变,下列措施能同时增大反应速率和H2平衡转化率的是
a.升高温度 b.按原比例再充入一定量CO2和H2
c.将
 和
和 液化移出 d.缩小容器体积
液化移出 d.缩小容器体积
更新时间:2021-11-18 11:14:44
|
相似题推荐
【推荐1】碳和硫的化合物在生产生活中的应用非常广泛。
⑴用生物质热解气(主要成分为CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:
2CO(g) + SO2 (g) = S(g) + 2CO2(g) ΔH1 = +8.0kJ/mol
2CO(g) + O2 (g) = 2CO2(g) ΔH2 = -566.0kJ/mol
2H2 (g) + O2 (g) = 2H2O (g) ΔH3 = -483.6kJ/mol
则2H2 (g) + SO2 (g) = S(g) + 2 H2O (g) ΔH4 =________
⑵欲用1L Na2CO3溶液将6.99gBaSO4固体全部转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为________ 。(忽略溶液体积的变化)[已知:常温下Ksp(BaSO4)=1×10-11, Ksp(BaCO3)=1×10-10]
(3)在25 ℃时,将a mol/L的氨水溶液与0.02mol/L的HCl溶液等体积混合后溶液呈中性,则氨水的电离平衡常数Kb =________ 。
⑴用生物质热解气(主要成分为CO、CH4、H2)将SO2在高温下还原成单质硫。涉及的部分反应如下:
2CO(g) + SO2 (g) = S(g) + 2CO2(g) ΔH1 = +8.0kJ/mol
2CO(g) + O2 (g) = 2CO2(g) ΔH2 = -566.0kJ/mol
2H2 (g) + O2 (g) = 2H2O (g) ΔH3 = -483.6kJ/mol
则2H2 (g) + SO2 (g) = S(g) + 2 H2O (g) ΔH4 =
⑵欲用1L Na2CO3溶液将6.99gBaSO4固体全部转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为
(3)在25 ℃时,将a mol/L的氨水溶液与0.02mol/L的HCl溶液等体积混合后溶液呈中性,则氨水的电离平衡常数Kb =
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在碱性废水的处理中,通常用于烟道气处理。在充分燃烧的烟道中,大约含有14%的CO2,将烟道气通入碱性废水中进行中和处理,是比较先进而经济的办法,写出该处理方法的离子方程式______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】碘及其化合物在生产中应用广泛。
(1)在2HI(g) H2(g)+ I2(g)反应中,三种分于化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。
H2(g)+ I2(g)反应中,三种分于化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。
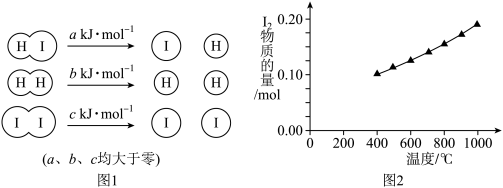
分析图1和图2,比较2a___ b+c(填"<”、“>”或“=”),理由是_________ 。
(2)碱性条件下I2可以转化为IO ,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
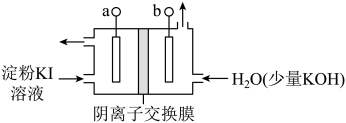
①a连接电源的_____ 极。
②结合实验现象和电极反应式说明制备KIO3的原理:___________ 。
(1)在2HI(g)
 H2(g)+ I2(g)反应中,三种分于化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。
H2(g)+ I2(g)反应中,三种分于化学键断裂时能量变化如图1所示。其他条件相同,1 mol HI在不同温度分解达平衡时,测得体系中I2的物质的量随温度变化的曲线如图2所示。
分析图1和图2,比较2a
(2)碱性条件下I2可以转化为IO
 ,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
,电解KI溶液制备KIO3的工作原理如下图所示。电解过程中观察到阳极液变蓝,一段时间后又逐渐变浅。
①a连接电源的
②结合实验现象和电极反应式说明制备KIO3的原理:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】已知在2L的密闭容器中进行如下可逆反应,各物质的有关数据如下:
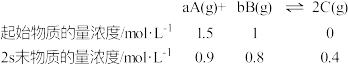
请回答下列问题。
(1)该可逆反应的化学方程式可表示为_______ 。
(2)用物质B来表示0~2s的平均反应速率为_______ 。
(3)从反应开始到2s末,A的转化率为_______ 。
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是_______ (填序号)。
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向_______ (填“反应物”或“生成物”)的方向移动。
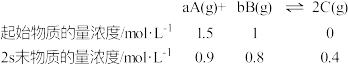
请回答下列问题。
(1)该可逆反应的化学方程式可表示为
(2)用物质B来表示0~2s的平均反应速率为
(3)从反应开始到2s末,A的转化率为
(4)下列事实能够说明上述反应在该条件下已经达到化学平衡状态的是
A.vB(消耗)=vC(生成)
B.容器内气体的总压强保持不变
C.容器内气体的密度不变
D.vA:vB:vC=3:1:2
E.容器内气体C的物质的量分数保持不变
(5)若平衡后改变温度,使得容器中气体的平均摩尔质量变大,则反应向
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】向一个固定体积的密闭容器充入2molA和1molB,发生如下反应:2A(g)+B(g) 3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
(1)用A表示2分钟内平均反应速率为_______ 。
(2)容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为_______ (填“吸热”或“放热”)反应。
(3)增大B的转化率,可采取的措施是_______ (用序号填空)
① 加入A ② 升高温度 ③ 加压 ④ 再加入1.6molA+0.8molB ⑤ 将C分离出容器
(4)若在一体积可变的容器中,该反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如下图,a点改变的条件可能是_______ ;若升高温度时,请将反应速率变化情况画在c-d处_______ 。

 3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。
3C(g)+D(g),2分钟后,反应达到平衡,C的浓度为1.2mol/L。(1)用A表示2分钟内平均反应速率为
(2)容器温度升高,平衡时混合气体的平均相对分子质量减小,则正反应为
(3)增大B的转化率,可采取的措施是
① 加入A ② 升高温度 ③ 加压 ④ 再加入1.6molA+0.8molB ⑤ 将C分离出容器
(4)若在一体积可变的容器中,该反应达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况如下图,a点改变的条件可能是

您最近一年使用:0次
填空题
|
较易
(0.85)
名校
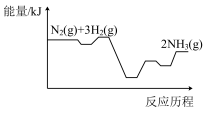
【推荐3】合成氨是人工固氮的主要手段,对人类生存、社会进步和经济发展都有着重大意义。
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是_______(填标号)。
(2)一定温度下,在 的某恒容密闭容器中,通入
的某恒容密闭容器中,通入 和
和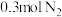 ,发生反应
,发生反应 ,
, 后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
后,该反应达到平衡,此时测得体系的总压强为起始时总压强的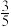 ,则:
,则:
①反应达到平衡时,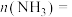
_______ mol。
② 内,
内,
_______  。
。
③为了加快该反应的速率,除加入合适的催化剂,升高温度外。还可采取的措施为_______ (写一种即可)。
(3)利用反应 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
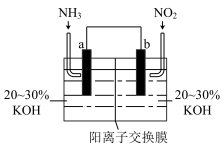
①电池工作时,电解质溶液中的 穿过阳离子交换膜向
穿过阳离子交换膜向_______ (填“a”或“b”)电极移动。
②b电极上的电极反应式为_______ 。
③电池工作一段时间后,左侧工作室溶液的pH_______ (填“变大”、“变小”或“不变”)。
④电池工作时,每转移 电子,此时右侧工作室溶液的质量将
电子,此时右侧工作室溶液的质量将_______ (填“增大”或“减小”)_______ g。
(1)下列物质间能量的变化与合成氨的能量变化(如图所示)相符的是_______(填标号)。

| A.盐酸与碳酸氢钠的反应 | B.氢氧化钡与氯化铵的反应 |
| C.铝片与稀硫酸的反应 | D.氢气与氯气的反应 |
 的某恒容密闭容器中,通入
的某恒容密闭容器中,通入 和
和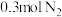 ,发生反应
,发生反应 ,
, 后,该反应达到平衡,此时测得体系的总压强为起始时总压强的
后,该反应达到平衡,此时测得体系的总压强为起始时总压强的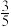 ,则:
,则:①反应达到平衡时,
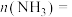
②
 内,
内,
 。
。③为了加快该反应的速率,除加入合适的催化剂,升高温度外。还可采取的措施为
(3)利用反应
 为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
为原理设计电池(如图所示,a、b电极均为惰性电极),既能实现有效消除氮氧化物的排放,减小环境污染,又能充分利用化学资源。(阳离子交换膜只允许阳离子通过)
①电池工作时,电解质溶液中的
 穿过阳离子交换膜向
穿过阳离子交换膜向②b电极上的电极反应式为
③电池工作一段时间后,左侧工作室溶液的pH
④电池工作时,每转移
 电子,此时右侧工作室溶液的质量将
电子,此时右侧工作室溶液的质量将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】反应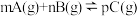 达到平衡,若升高温度,反应再次达到平衡时B的转化率变大;若减小压强,反应再次达到平衡时混合体系中C的体积分数减小。试推测:
达到平衡,若升高温度,反应再次达到平衡时B的转化率变大;若减小压强,反应再次达到平衡时混合体系中C的体积分数减小。试推测:
(1)逆反应是______________ (填“放”或“吸”)热反应。
(2)缩小体积而加压后,再次达到平衡时,与原平衡相比A的浓度_______________ (填“变大”“变小”或“不变”)。
(3)若B是有色物质,A、C是无色物质,则减小压强(增大体积),再次达到平衡时,与原平衡相比混合物的颜色_______________ (填“变深”“变浅”或“不变”)。
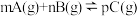 达到平衡,若升高温度,反应再次达到平衡时B的转化率变大;若减小压强,反应再次达到平衡时混合体系中C的体积分数减小。试推测:
达到平衡,若升高温度,反应再次达到平衡时B的转化率变大;若减小压强,反应再次达到平衡时混合体系中C的体积分数减小。试推测:(1)逆反应是
(2)缩小体积而加压后,再次达到平衡时,与原平衡相比A的浓度
(3)若B是有色物质,A、C是无色物质,则减小压强(增大体积),再次达到平衡时,与原平衡相比混合物的颜色
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】空气吹脱法是目前消除NH3对水体污染的重要方法。在一定条件下,向水体中加入适量NaOH固体可使NH3的脱除率增大,用平衡移动原理解释其原因:___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】在水溶液中橙红色的Cr2O72-与黄色的CrO42-有下列平衡关系:Cr2O72-+H2O 2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
(1)向上述溶液中加入NaOH溶液,溶液呈__________ 色,因为_________ 。
(2)向已加入NaOH溶液的1中再加入过量稀硫酸,则溶液呈__________ 色,因为__________ 。
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡____________________ ,溶液颜色将____________________ 。
 2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。
2CrO42-+2H+,把重铬酸钾溶于水配成稀溶液是橙色的。(1)向上述溶液中加入NaOH溶液,溶液呈
(2)向已加入NaOH溶液的1中再加入过量稀硫酸,则溶液呈
(3)向原溶液中加入Ba(NO3)2溶液(已知BaCrO4为黄色沉淀)则平衡
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)写出该反应的平衡常数表达式:K=________________ 。已知 >
>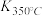 ,则该反应是
,则该反应是_____ 热反应。
(2)用NO表示从0~2 s内该反应的平均速率v=______________ 。
(3)能说明该反应已达到平衡状态的是 。
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的措施是__________ 。
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K=
 >
>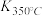 ,则该反应是
,则该反应是(2)用NO表示从0~2 s内该反应的平均速率v=
(3)能说明该反应已达到平衡状态的是 。
| A.v(NO2)=2v(O2) | B.容器内压强保持不变 |
| C.v逆(NO)=2v正(O2) | D.容器内密度保持不变 |
您最近一年使用:0次
【推荐2】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___________ 。
(2)能判断该反应是否达到化学平衡状态的依据是___________
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为____ ℃。
| t℃ | 700 | 800 | 830 | 1000 |
| K | 0.6 | 0.9 | 1.0 | 1.7 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)能判断该反应是否达到化学平衡状态的依据是
a.容器中压强不变 b.混合气体中c(CO)不变
c. 正(H2)=
正(H2)= 逆(H2O) d.c(CO2)=c(CO)
逆(H2O) d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在1L密闭容器中通入CO2、H2各2mol,在一定条件下发生反应:CO2(g)+H2(g) CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:
(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=_______ 。(写出该反应的化学平衡常数的表达式并计算出结果)
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为_______ 反应(填“吸热”或“放热”)。
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3_______ K1(填“<”或”>”或“=”)。
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应_______ (填“向正反应方向进行”或“向逆反应方向进行”或“处于平衡状态”)。
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g) CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为_______ ,此时容器内总压强与起始时的压强之比为_______ 。
 CO(g)+H2O(g),回答下列问题:
CO(g)+H2O(g),回答下列问题:(1)在830℃条件下,反应达到平衡时CO2的转化率为50%。求该条件下的化学平衡常数K1=
(2)在(1)的基础上,把体系温度降至800℃。已知该条件下的平衡常数K2=0.81,可以推知该反应的正反应为
(3)在(1)的基础上,压缩容器体积为0.5L。该条件下的平衡常数为K3。则K3
(4)830℃时,某时刻测得体系中各物质的量如下:n(CO2)=1.2mol,n(H2)=1.5mol,n(CO)=0.9mol,n(H2O)=0.9mol,则此时该反应
(5)某温度时,在2L密闭容器中发生:C(s)+H2O(g)
 CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
CO(g)+H2(g)。起始时C为2mol, H2O 为3mol,平衡时CO转化率为60%,则平衡时氢气的浓度为
您最近一年使用:0次



