从辉铋矿(主要成分为Bi2S3,含有SiO2、Cu2S、FeS2杂质)回收铋的一种工艺流程如下图所示。
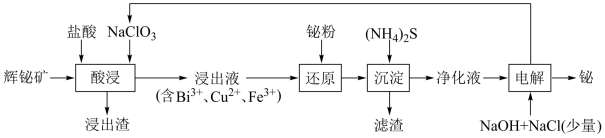
已知:i.氧化性:Cu2+>Bi3+>H+;ii.结合S2-能力:Cu2+>H+>Fe2+
(1)“酸浸”过程,需分批次的加入NaClO3以防生成Cl2。
①“浸出渣”中除硫外,还含有___________ (填化学式)。
②Bi2S3发生反应的化学方程式为___________ 。
(2)“还原”过程中Fe3+发生反应的离子方程式为___________ 。
(3)“净化液”中的阳离子除Bi3+、H+和Fe2+外,还存在有___________ (填离子符号)。
(4)“电解”装置图如下。
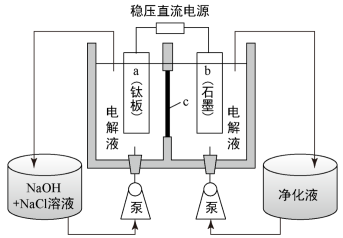
①c为___________ 离子交换膜(填“阳”或“阴”)。
②a极的电极反应式为___________ 。

已知:i.氧化性:Cu2+>Bi3+>H+;ii.结合S2-能力:Cu2+>H+>Fe2+
(1)“酸浸”过程,需分批次的加入NaClO3以防生成Cl2。
①“浸出渣”中除硫外,还含有
②Bi2S3发生反应的化学方程式为
(2)“还原”过程中Fe3+发生反应的离子方程式为
(3)“净化液”中的阳离子除Bi3+、H+和Fe2+外,还存在有
(4)“电解”装置图如下。

①c为
②a极的电极反应式为
更新时间:2021-11-13 10:24:30
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】碘及其化合物在生活中应用广泛,含有碘离子的溶液需回收处理。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列三个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)=2HI(aq)+H2SO4(aq) ΔH1
反应Ⅱ:HI(aq)= H2(g)+
H2(g)+ I2(aq) ΔH2
I2(aq) ΔH2
反应Ⅲ:2H2SO4(aq)=2SO2(g)+O2(g)+2H2O(l)
①反应:SO2(g)+2H2O(l)=H2SO4(aq)+H2(g)的ΔH=___ (用ΔH1、ΔH2表示)。
②分析上述反应,下列判断正确的是___
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2还原性比HI强
c.循环过程中需补充H2O d.循环过程中产生1molO2同时产生1molH2
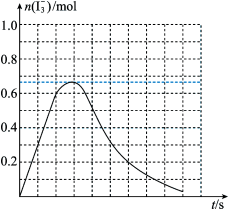
③反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq) I3-(aq),其反应速率极快且平衡常数大。现将1molSO2缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是
I3-(aq),其反应速率极快且平衡常数大。现将1molSO2缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是___ 。
(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量就能将碘单质进一步氧化成碘酸根离子(IO3-),写出氯气与碘单质反应的离子方程式:___ 。
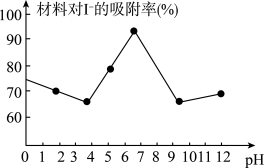
(3)科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图是不同pH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附___ (填“酸性”“中性”或“碱性”)溶液中的I-。
(4)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s) AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=
AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=___ [用c(Cl-)、Ksp(AgCl)和Ksq(AgI)表示]。该方法去除碘离子的原理是___ 。
(1)“硫碘循环”法是分解水制备氢气的研究热点,涉及下列三个反应:
反应Ⅰ:SO2(g)+I2(aq)+2H2O(l)=2HI(aq)+H2SO4(aq) ΔH1
反应Ⅱ:HI(aq)=
 H2(g)+
H2(g)+ I2(aq) ΔH2
I2(aq) ΔH2反应Ⅲ:2H2SO4(aq)=2SO2(g)+O2(g)+2H2O(l)
①反应:SO2(g)+2H2O(l)=H2SO4(aq)+H2(g)的ΔH=
②分析上述反应,下列判断正确的是
a.反应Ⅲ易在常温下进行 b.反应Ⅰ中SO2还原性比HI强
c.循环过程中需补充H2O d.循环过程中产生1molO2同时产生1molH2
③反应I发生时,溶液中存在如下平衡:I2(aq)+I-(aq)
 I3-(aq),其反应速率极快且平衡常数大。现将1molSO2缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是
I3-(aq),其反应速率极快且平衡常数大。现将1molSO2缓缓通入含1molI2的水溶液中至恰好完全反应。溶液中I3-的物质的量n(I3-)随反应时间(t)的变化曲线如图所示。开始阶段n(I3-)逐渐增大的原因是
(2)用海带提取碘时,需用氯气将碘离子氧化成单质。酸性条件下,若氯气过量就能将碘单质进一步氧化成碘酸根离子(IO3-),写出氯气与碘单质反应的离子方程式:
(3)科研小组用新型材料Ag/TiO2对溶液中碘离子进行吸附研究。如图是不同pH条件下,碘离子吸附效果的变化曲线。据此推断Ag/TiO2材料最适合吸附

(4)氯化银复合吸附剂也可有效吸附碘离子。氯化银复合吸附剂对碘离子的吸附反应为I-(aq)+AgCl(s)
 AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=
AgI(s)+Cl-(aq),反应达到平衡后溶液中c(I-)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硼化钛强度高、硬度大,广泛应用于机械制造领域;五氟化锑( )是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含
)是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含 、
、 、
、 、
、 、
、 、
、 )为原料制取硼化钛和五氟化锑的流程如图所示。
)为原料制取硼化钛和五氟化锑的流程如图所示。
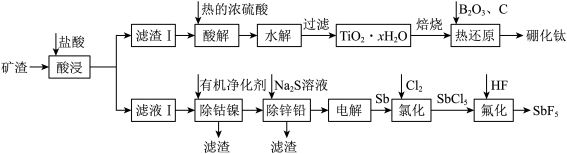
已知:① 性质较稳定,加热时可溶于浓硫酸中形成
性质较稳定,加热时可溶于浓硫酸中形成 。
。
②25℃时, 、
、 的
的 分别为
分别为 ,
,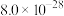 。
。
(1)“水解”步骤中对应的离子方程式为___________ 。为了使水解趋于完全,可采取的措施有___________ 。
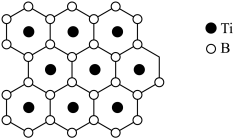
(2)硼化钛有类似石墨的层状结构,硼原子平面和钛原子平面在晶体结构中交替出现,形成二维网状结构,其投影图如下,硼化钛的化学式为___________ 。“热还原”步骤中使用电弧炉高温加热装置(1450~1550℃),每消耗1mol 转移电子数为
转移电子数为___________ 。
(3)“除钴镍”步骤中,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理表示为:
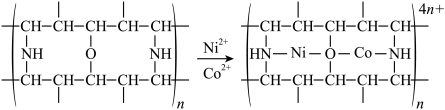
 ,
, 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为___________ 。
(4)已知滤液I中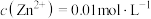 ,
,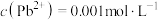 。“除锌铅”步骤中,缓慢滴加稀
。“除锌铅”步骤中,缓慢滴加稀 溶液,先产生的沉淀是(填化学式)
溶液,先产生的沉淀是(填化学式)___________ ;当 、
、 共沉时,先沉淀的物质是否已经沉淀完全(离子浓度
共沉时,先沉淀的物质是否已经沉淀完全(离子浓度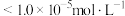 )
)___________ (填“是”或“否”)。
(5)1986年化学家用 和
和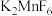 反应,首次实现了用非电解法制取
反应,首次实现了用非电解法制取 ,同时生成
,同时生成 ,已知该过程中
,已知该过程中 接受了一个
接受了一个 的电子对,请写出该反应的化学方程式
的电子对,请写出该反应的化学方程式___________ 。
 )是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含
)是一种高能氟化剂,广泛应用于制药业。工业上以一种含钛的矿渣(主要含 、
、 、
、 、
、 、
、 、
、 )为原料制取硼化钛和五氟化锑的流程如图所示。
)为原料制取硼化钛和五氟化锑的流程如图所示。
已知:①
 性质较稳定,加热时可溶于浓硫酸中形成
性质较稳定,加热时可溶于浓硫酸中形成 。
。②25℃时,
 、
、 的
的 分别为
分别为 ,
,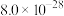 。
。(1)“水解”步骤中对应的离子方程式为
(2)硼化钛有类似石墨的层状结构,硼原子平面和钛原子平面在晶体结构中交替出现,形成二维网状结构,其投影图如下,硼化钛的化学式为
 转移电子数为
转移电子数为
(3)“除钴镍”步骤中,有机净化剂的基本组分为大分子立体网格结构的聚合物,其净化原理表示为:

 ,
, 能发生上述转化而
能发生上述转化而 不能,推测可能的原因为
不能,推测可能的原因为(4)已知滤液I中
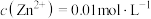 ,
,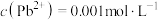 。“除锌铅”步骤中,缓慢滴加稀
。“除锌铅”步骤中,缓慢滴加稀 溶液,先产生的沉淀是(填化学式)
溶液,先产生的沉淀是(填化学式) 、
、 共沉时,先沉淀的物质是否已经沉淀完全(离子浓度
共沉时,先沉淀的物质是否已经沉淀完全(离子浓度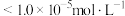 )
)(5)1986年化学家用
 和
和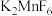 反应,首次实现了用非电解法制取
反应,首次实现了用非电解法制取 ,同时生成
,同时生成 ,已知该过程中
,已知该过程中 接受了一个
接受了一个 的电子对,请写出该反应的化学方程式
的电子对,请写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】化学小组欲从含CuCl2、NaCl及少量K2SO4的混合溶液中分离出CuCl2和NaCl,设计实验流程如下:

已知:氯化钠、氯化钾在不同温度下的溶解度如表所示:
回答下列问题:
(1)试剂甲、乙分别是______ 。
(2)向滤渣中加入试剂丙后发生反应的离子方程式是______ 。
(3)操作1的名称是_____ 。
(4)操作2包括蒸发结晶、过滤等过程。实验时需在结晶后趁热完成过滤的目的是_____ ,过滤时应首先进行的操作是______ 。
(5)取操作2所得氯化钠晶体少许溶于酒精,得乳白色液体,用一束可见光照射液体,若在入射光的侧面观察到_______ ,则证明所得液体为胶体。

已知:氯化钠、氯化钾在不同温度下的溶解度如表所示:
| 0 | 20 | 40 | 60 | 80 | 100 | ||
| 溶解度/g | NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KCl | 27.6 | 34.0 | 40.0 | 45.5 | 51.1 | 56.7 | |
回答下列问题:
(1)试剂甲、乙分别是
(2)向滤渣中加入试剂丙后发生反应的离子方程式是
(3)操作1的名称是
(4)操作2包括蒸发结晶、过滤等过程。实验时需在结晶后趁热完成过滤的目的是
(5)取操作2所得氯化钠晶体少许溶于酒精,得乳白色液体,用一束可见光照射液体,若在入射光的侧面观察到
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】为严厉打击食品生产经营中违法添加非食用物质、滥用食品添加剂,卫生部、农业部等部门联合公布了包含硫酸亚铁在内的22种“易滥用食品添加剂”名单。某同学为探究富含硫酸亚铁且保存时间较长的食品情况,设计了如下实验方案:

(1)试剂1的主要成分的化学式是________ 。
(2)加入新制氯水后溶液红色加深的原因是________ (用离子方程式表示)。
(3)该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1:溶液中的+3价铁被氧化为更高价态的铁;
假设2:_________ 。
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案:________ 。
(4)应用拓展
实验室在保存硫酸亚铁溶液时,常向其中加入少量的铁粉,原因是______ (用离子方程式表示)。

(1)试剂1的主要成分的化学式是
(2)加入新制氯水后溶液红色加深的原因是
(3)该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1:溶液中的+3价铁被氧化为更高价态的铁;
假设2:
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案:
(4)应用拓展
实验室在保存硫酸亚铁溶液时,常向其中加入少量的铁粉,原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】被世卫组织列为Al级新型高效安全消毒剂的二氧化氯(ClO2)是一种黄绿色到橙黄色的气体,易溶于水,沸点为11℃,遇热不稳定易分解发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁( )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
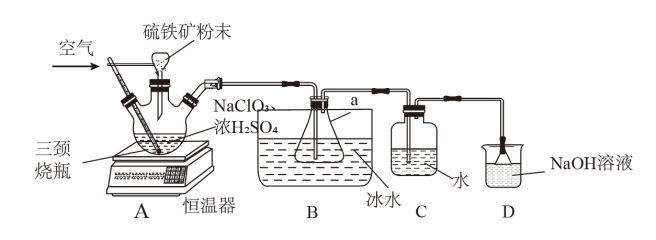
(1) 中S元素的化合价为
中S元素的化合价为___________ 价;仪器a的名称是___________ 。
(2)三颈烧瓶中发生反应的离子方程式为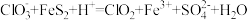 (未配平)。
(未配平)。
①该反应中被氧化的元素为___________ (填元素符号),还原产物为___________ (填化学式)。
②配平该离子方程式:___________ 。
(3)装置___________ (填“A”、“B”或“C”)为收集ClO2的装置;装置D中倒置漏斗的作用是___________ 。
(4)设计实验证明ClO2的氧化性比 的强:
的强:___________ 。
(5)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为___________ 。
 )]还原氯酸钠(
)]还原氯酸钠( )制取二氧化氯。某研究小组利用如图装置制备
)制取二氧化氯。某研究小组利用如图装置制备 ,向三颈烧瓶中加入
,向三颈烧瓶中加入 溶液、浓
溶液、浓 通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
通入空气,调节恒温器至60℃,通过固体加料器缓慢匀速加入硫铁矿粉末。请回答下列问题:
(1)
 中S元素的化合价为
中S元素的化合价为(2)三颈烧瓶中发生反应的离子方程式为
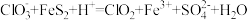 (未配平)。
(未配平)。①该反应中被氧化的元素为
②配平该离子方程式:
(3)装置
(4)设计实验证明ClO2的氧化性比
 的强:
的强:(5)将少量ClO2水溶液滴入盛有MnSO4溶液的试管中,振荡,有黑色沉淀生成,已知反应中氧化剂与还原剂的物质的量之比为2:5,则该反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
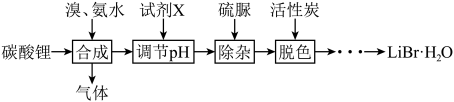
【推荐3】溴化锂是一种高效水汽吸收剂和空气湿度调节剂。工业上以碳酸锂为原料制备LiBr·H2O的流程如下:
已知:①Br2+H2O HBr+HBrO,Br2+3H2O
HBr+HBrO,Br2+3H2O 5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
(1)合成时,除生成LiBr外,还产生了2种参与大气循环的气体,写出该化学方程式:___________ 。
(2)合成时,向碳酸锂中滴加溴和氨水的顺序是___________ (填字母),可能的理由是______________ 。
a.先加氨水再滴溴 b.先滴溴再加氨水 c.边滴溴边加氨水
(3)合成所得的溶液中存在过量的溴会导致溶液pH<3,可用试剂X将溶液pH调节至8~9以除去过量的溴,则X的化学式为___________ 。
(4)加入硫脲[CS(NH2)2]的作用是除去 ,反应中硫脲表现
,反应中硫脲表现___________ (填“氧化性”或“还原性”)。
(5)已知脱色后的混合液中还含有少量的 。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,___________ 。(实验中可供选择的试剂:盐酸、氢溴酸、乙醇、蒸馏水)。


已知:①Br2+H2O
 HBr+HBrO,Br2+3H2O
HBr+HBrO,Br2+3H2O 5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。
5HBr+HBrO3;②NH3有还原性,HBrO、HBrO3均具有强氧化性。(1)合成时,除生成LiBr外,还产生了2种参与大气循环的气体,写出该化学方程式:
(2)合成时,向碳酸锂中滴加溴和氨水的顺序是
a.先加氨水再滴溴 b.先滴溴再加氨水 c.边滴溴边加氨水
(3)合成所得的溶液中存在过量的溴会导致溶液pH<3,可用试剂X将溶液pH调节至8~9以除去过量的溴,则X的化学式为
(4)加入硫脲[CS(NH2)2]的作用是除去
 ,反应中硫脲表现
,反应中硫脲表现(5)已知脱色后的混合液中还含有少量的
 。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
。溴化锂溶液的溶解度随温度变化曲线如图所示,请补充完整脱色后得到的溶液制备LiBr·H2O的实验方案:加入活性炭脱色后,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】银的冶炼有很多方法, 在《 天工开物》 均有记载, 而现代流行的“ 氰化法”, 用 NaCN溶液浸出矿石中的银的方法是最常用的方法。 该方法具备诸多优点: 银的回收率高; 对游离态和化合态的银均能浸出; 对能源消耗相对较少; 生产工艺简便等, 但氰化物通常有毒。 其炼制工艺简介如下:
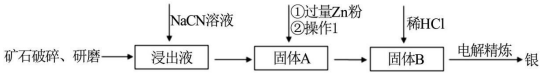
(1)矿石需要先进行破碎、 研磨, 其目的是__________ 。
(2)写出该工艺的一个明显的缺点__________ 。
(3)用 NaCN 浸泡矿石( 该矿石是辉银矿, 其主要成分是 Ag2S) 时, 反应容器处于开口状态, 产生的银以[Ag(CN)2]- 形式存在, 硫元素被氧化至最高价, 试写出主要反应的离子方程式__________ 。
(4)银往往和锌、 铜、 金等矿伴生, 故氰化法得到的银中往往因含有上述金属而不纯净, 需要进一步纯化, 从而获得纯净的银。 其中方法之一就是进行电解精炼, 在精炼过程中, 含有杂质的银作__________ 极( 填“阴” 或“阳”), 该电极上发生的主要反应式为__________ , 金以__________ 形式存在。
(5)有人提出了另外的提纯银的方案, 先将锌粉还原后的混合金属用略过量的硝酸溶解, 通过精确调整溶液的 pH 来进行金属元素分离, 已知:
①溶解后的离子浓度如下表:

②某些金属离子的氢氧化物 Ksp 如下:
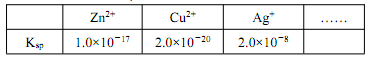
( 已知 lg2=0.3),该设计方案_______ (填“ 可行” 或“ 不可行”),其原因是_______ 。

(1)矿石需要先进行破碎、 研磨, 其目的是
(2)写出该工艺的一个明显的缺点
(3)用 NaCN 浸泡矿石( 该矿石是辉银矿, 其主要成分是 Ag2S) 时, 反应容器处于开口状态, 产生的银以[Ag(CN)2]- 形式存在, 硫元素被氧化至最高价, 试写出主要反应的离子方程式
(4)银往往和锌、 铜、 金等矿伴生, 故氰化法得到的银中往往因含有上述金属而不纯净, 需要进一步纯化, 从而获得纯净的银。 其中方法之一就是进行电解精炼, 在精炼过程中, 含有杂质的银作
(5)有人提出了另外的提纯银的方案, 先将锌粉还原后的混合金属用略过量的硝酸溶解, 通过精确调整溶液的 pH 来进行金属元素分离, 已知:
①溶解后的离子浓度如下表:

②某些金属离子的氢氧化物 Ksp 如下:
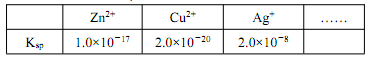
( 已知 lg2=0.3),该设计方案
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】亚氯酸钠(NaClO2)是一种强氧化性漂白剂,广泛用于纺织、印染和食品工业。它在碱性环境中稳定存在。某同学查阅资料后设计生产NaClO2的主要流程如图。
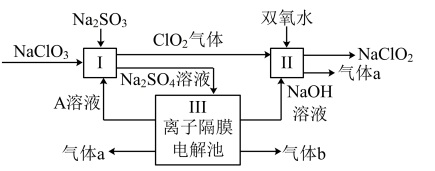
(1)I中发生反应的还原剂是___ (填化学式)。
(2)II中反应的离子方程式是___ 。
(3)A的化学式是___ ,装置III中A在___ 极区产生。
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备,反应方程式为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是___ 。
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗FeSO4的物质的量___ (填“相等”或“不相等”)。

(1)I中发生反应的还原剂是
(2)II中反应的离子方程式是
(3)A的化学式是
(4)ClO2是一种高效水处理剂,可用亚氯酸钠和稀盐酸为原料制备,反应方程式为5NaClO2+4HCl=5NaCl+4ClO2↑+2H2O。研究表明:若反应开始时盐酸浓度越大,则气体产物中Cl2的含量越大,运用氧化还原反应规律分析其原因是
(5)NaClO2变质可分解为NaClO3和NaCl。取等质量变质前后的NaClO2试样均配成溶液,分别与足量FeSO4溶液反应时,消耗FeSO4的物质的量
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】短周期元素A、B、C、D在周期表中的位置如图所示,B、D最外层电子数之和为12,回答下列问题:
(1)与元素B、D处于同一主族的第2-5周期元素单质分别与H2反应生成1 mol气态氢化物对应的热量变化如下,其中能表示该主族第四周期元素的单质生成1 mol气态氢化物所对应的热量变化是______  选填字母编号
选填字母编号 。
。
 吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。
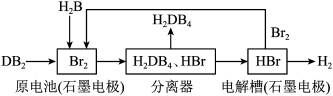
①查得:
试写出通常条件下电解槽中发生总反应的热化学方程式:______ 。
②根据资料:
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到______ ,证明分离效果较好。
③在原电池中,负极发生的反应式为______ 。
④在电解过程中,电解槽阴极附近溶液pH______ (填“变大”、“变小”或“不变”)。
⑤将该工艺流程用总反应的化学方程式表示为:________ ,该生产工艺的优点有_____ (答一点即可);缺点有____ (答一点即可)。
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入______ ,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO3-,其离子方程式为______ 。
(4)CuBr2分解的热化学方程式为:2CuBr2(s) 2CuBr(s)+Br2(g)△H=+105.4kJ/mol。在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
2CuBr(s)+Br2(g)△H=+105.4kJ/mol。在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会______ (填“增大”“不变”“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为______ 。
| A | B | |
| C | D |
 选填字母编号
选填字母编号 。
。 吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ
吸收99.7kJ b.吸收29.7kJ c.放出20.6kJ d.放出241.8kJ(2)DB2通过下列工艺流程可制化工业原料H2DB4和清洁能源H2。

①查得:
| 化学键 | H-H | Br-Br | H-Br |
| 键能(kJ/mol) | 436 | 194 | 362 |
试写出通常条件下电解槽中发生总反应的热化学方程式:
②根据资料:
| 化学式 | Ag2SO4 | AgBr |
| 溶解度(g) | 0.796 | 8.4×10-6 |
为检验分离器的分离效果,取分离后的H2DB4溶液于试管,向其中逐滴加入AgNO3溶液至充分反应,若观察到
③在原电池中,负极发生的反应式为
④在电解过程中,电解槽阴极附近溶液pH
⑤将该工艺流程用总反应的化学方程式表示为:
(3)溴及其化合物广泛应用于医药、农药、纤维、塑料阻燃剂等,回答下列问题:海水提溴过程中,向浓缩的海水中通入
(4)CuBr2分解的热化学方程式为:2CuBr2(s)
 2CuBr(s)+Br2(g)△H=+105.4kJ/mol。在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
2CuBr(s)+Br2(g)△H=+105.4kJ/mol。在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。①如反应体系的体积不变,提高反应温度,则p(Br2)将会
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为
您最近一年使用:0次
【推荐1】根据《化学反应原理》知识,按要求作答。
I.在一定条件下,以CH4和H2O为原料,通过下列反应制备甲醇(CH3OH)。
已知:①CH4+H2O(g) CO(g)+3H2(g)△H=+206.0kJ·mol-1
CO(g)+3H2(g)△H=+206.0kJ·mol-1
②CO(g)+2H2(g) CH3OH(g)△H=-129.0kJ·mol-1
CH3OH(g)△H=-129.0kJ·mol-1
(1)反应②的正反应属于___ (填“吸热”或“放热”)反应。
(2)上述两个反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向逆反应方向移动的是___ (填“①”或“②”)。
(3)在密闭容器中发生①反应,若CH4起始浓度为2.0mol·L-1,水蒸气起始浓度为3.0mol·L-1,反应进行5min后,测得CH4浓度为0.5mol·L-1,则v(CH4)=___ mol·L-1·min-1。
Ⅱ.常温下,浓度均为0.1mol·L-1的两种溶液;①氨水②NH4Cl溶液。
(4)写出①氨水中NH3·H2O的电离方程式:___ 。
(5)测得②溶液的pH<7,则溶液中c(NH )
)___ c(Cl-)(填“>”“<”或“=”),写出②溶液发生水解反应的离子方程式:___ 。
Ⅲ.如图所示装置,用惰性电极电解熔融氯化钠(2NaCl 2Na+Cl2↑)。
2Na+Cl2↑)。
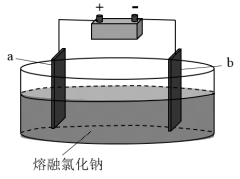
(6)通电时,C1-向___ (填“a”或“b”)电极移动,发生___ (填“氧化反应”或“还原反应”)。
(7)电解一段时间后,在两个电极上分别生成金属钠和氯气。写出生成金属钠的电极反应式:___ 。
I.在一定条件下,以CH4和H2O为原料,通过下列反应制备甲醇(CH3OH)。
已知:①CH4+H2O(g)
 CO(g)+3H2(g)△H=+206.0kJ·mol-1
CO(g)+3H2(g)△H=+206.0kJ·mol-1②CO(g)+2H2(g)
 CH3OH(g)△H=-129.0kJ·mol-1
CH3OH(g)△H=-129.0kJ·mol-1(1)反应②的正反应属于
(2)上述两个反应达到平衡后,在其它条件不变的情况下,通过减小容器体积增大压强,则化学平衡向逆反应方向移动的是
(3)在密闭容器中发生①反应,若CH4起始浓度为2.0mol·L-1,水蒸气起始浓度为3.0mol·L-1,反应进行5min后,测得CH4浓度为0.5mol·L-1,则v(CH4)=
Ⅱ.常温下,浓度均为0.1mol·L-1的两种溶液;①氨水②NH4Cl溶液。
(4)写出①氨水中NH3·H2O的电离方程式:
(5)测得②溶液的pH<7,则溶液中c(NH
 )
)Ⅲ.如图所示装置,用惰性电极电解熔融氯化钠(2NaCl
 2Na+Cl2↑)。
2Na+Cl2↑)。
(6)通电时,C1-向
(7)电解一段时间后,在两个电极上分别生成金属钠和氯气。写出生成金属钠的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】能源危机当前是一个全球性问题,“开源节流”是应对能源危机的重要举措。
(1)下列做法有助于能源“开源节流”的是_______ (填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、不使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。在通常状况下,金刚石和石墨相比较,_______ (填“金刚石”或“石墨”)更稳定,石墨的燃烧热为
_______ 。

(3)实现“碳达峰”“碳中和”目标要坚定不移,要坚持稳中求进,逐步实现。在稀硫酸中利用电催化可将 同时转化为多种燃料,其原理如图所示。
同时转化为多种燃料,其原理如图所示。

①装置甲中离子交换膜为_______ (“阳离子”或“阴离子”)交换膜。
②铜电极上产生 的电极反应式为
的电极反应式为_______ ,若铜电极上只生成5.6gCO,则铜极区溶液质量变化了_______ g。
(1)下列做法有助于能源“开源节流”的是
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源、不使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
(2)金刚石和石墨均为碳的同素异形体,它们在氧气不足时燃烧生成一氧化碳,在氧气充足时充分燃烧生成二氧化碳,反应中放出的热量如图所示。在通常状况下,金刚石和石墨相比较,


(3)实现“碳达峰”“碳中和”目标要坚定不移,要坚持稳中求进,逐步实现。在稀硫酸中利用电催化可将
 同时转化为多种燃料,其原理如图所示。
同时转化为多种燃料,其原理如图所示。
①装置甲中离子交换膜为
②铜电极上产生
 的电极反应式为
的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】SO2、CO、CO2、NOx是对环境影响较大的几种气体,对它们的合理控制和治理是优化我们生存环境的有效途径。
(1)利用电化学原理在酸性环境下将CO、SO2转化为重要化工原料,装置如图所示:
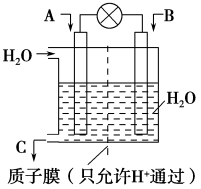
①若A为CO,B为H2,C为CH3OH,则通入CO的一极为___________ 极,该极的电极反应式为:___________ 。
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为:_______________ 。
③若A为NO,B为O2,C为HNO3,则正极的电极反应式为:_________ 。
④若用上述①作电池电解200 mL含有0.1 mol·L-1 NaCl和0.1 mol·L-1 CuSO4的混合溶液(电极均为惰性电极),当消耗标况下0.448L H2时,阳极产生的气体为_________ (填化学式),其总物质的量为_________ 。
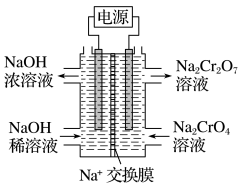
(2)根据2 +2H+⇌
+2H+⇌ +H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的
+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的_____________ 极,其电极反应式为:__________ 。
(1)利用电化学原理在酸性环境下将CO、SO2转化为重要化工原料,装置如图所示:

①若A为CO,B为H2,C为CH3OH,则通入CO的一极为
②若A为SO2,B为O2,C为H2SO4,则负极的电极反应式为:
③若A为NO,B为O2,C为HNO3,则正极的电极反应式为:
④若用上述①作电池电解200 mL含有0.1 mol·L-1 NaCl和0.1 mol·L-1 CuSO4的混合溶液(电极均为惰性电极),当消耗标况下0.448L H2时,阳极产生的气体为
(2)根据2
 +2H+⇌
+2H+⇌ +H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的
+H2O设计图示装置(均为惰性电极)电解Na2CrO4溶液制取Na2Cr2O7,图中右侧电极连接电源的
您最近一年使用:0次



