CO(g)和H2O(g)以1:2体积比分别通入到体积为2 L的恒容密闭容器中进行反应:CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
下列说法不正确的是
 CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:| 实验组 | 温度/℃ | 起始时H2O的量/mol | 平衡时CO2的量/mol | 达到平衡所需时间/min |
| ① | 650 | 4.00 | 1.30 | 50 |
| ② | 900 | 2.00 | 0.40 | 10 |
| ③ | 650 | 2.00 | 0.65 | 10 |
| A.从实验数据分析,该反应的正反应是吸热反应 |
| B.实验①中,在0-10 min内,以v(H2)表示的反应速率大于0.013 mol·L-1·min-1 |
| C.从生产效益分析,③组实验的条件最佳 |
| D.比较实验②③,说明③实验使用了更高效的催化剂 |
更新时间:2021-12-24 20:42:42
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】将 4mol A气体和 2mol B气体在 2L 固定体积的容器中混合并在一定条件下发生如下反应:2A(g)+B(g)⇌2C(g).若经2s后测得 C 的浓度为 0.6 mol•L-1,现有下列几种说法,其中正确的是
| A.用物质A表示的反应的平均速率为0.2 mol•L-1•s-1 | B.2s时物质B的浓度为0.7 mol•L-1 |
| C.用物质B表示的反应的平均速率为0.1 mol•L-1•s-1 | D.2s时物质A的转化率为70% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在密闭容器中发生反应H2(g)+I2(g)⇌2HI(g),0~5min内H2的浓度减少了0.1mol/L,则在这段时间内用HI表示的平均反应速率为
| A.0.01mol·L-1·min-1 |
| B.0.04mol·L-1·min-1 |
| C.0.2mol·L-1·min-1 |
| D.0.5mol·L-1·min-1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】在一定温度下,在2 L的恒容密闭容器中发生反应:2A(g)⇌B(g)+2C(g),反应过程中的部分数据如下表所示,下列说法正确的是
| t/min n/mol | n(A) | n(B) | n(C) |
| 0 | 2.0 | 0 | 0 |
| 2 | 1.0 | ||
| 4 | 0.8 | ||
| 6 | 0.6 |
| A.在0~2 min内,A的反应速率为0.5 mol/(L·min) |
| B.平衡状态时,C的物质的量浓度为0.6 mol/L |
| C.6 min时,反从已达到平衡状态,此时2v正(A)=v逆(B) |
| D.容器中气体的密度保持不变,说明反应已达到平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】反应N2+3H2  2NH3在密闭容器内进行。分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为v(N2)、v(H2)、v(NH3),则三者的关系正确的是
2NH3在密闭容器内进行。分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为v(N2)、v(H2)、v(NH3),则三者的关系正确的是
 2NH3在密闭容器内进行。分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为v(N2)、v(H2)、v(NH3),则三者的关系正确的是
2NH3在密闭容器内进行。分别用N2、H2、NH3三种物质在单位时间内浓度的变化表示该反应的速率为v(N2)、v(H2)、v(NH3),则三者的关系正确的是 | A.v(N2)=v(NH3) | B.3v(H2)=2v(NH3) | C.v(NH3)=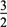 v(H2) v(H2) | D.v(H2)=3v(N2) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】恒温恒容条件下,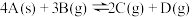 ,经
,经 ,B的浓度减少
,B的浓度减少 ,下列说法正确的是
,下列说法正确的是
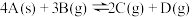 ,经
,经 ,B的浓度减少
,B的浓度减少 ,下列说法正确的是
,下列说法正确的是A.用A表示的反应速率是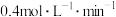 |
| B.气体的平均摩尔质量不再变化,则证明反应已经达到平衡状态 |
C. 末的反应速率 末的反应速率 |
D.分别用B、C表示反应的速率,其关系是: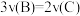 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
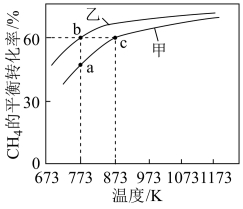
【推荐1】甲、乙均为1L的恒容密闭容器,向甲中充入1molCH4和1molCO2,乙中充入1molCH4和n molCO2,在催化剂存在下发生反应: CH4(g)+CO2(g)  2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
 2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
2CO(g)+2H2(g),测得CH4的平衡转化率随温度的变化如图所示。下列说法正确的是
| A.H2 的体积分数:φ(b)<φ(c) |
| B.773K 时,该反应的平衡常数大于12.96 |
| C.该反应的正反应是放热反应 |
| D.873K 时,向甲的平衡体系中再充入CO2、CH4各0.4mol,CO、H2各1.2 mol,平衡不发生移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是
A.H2(g)+S(s) H2S(g)恒压下充入He,化学反应速率不变 H2S(g)恒压下充入He,化学反应速率不变 |
| B.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率 |
C.N2(g)+3H2(g) 2NH3(g) △H<0,生产中采用较高温度是为了提高反应物的平衡转化率 2NH3(g) △H<0,生产中采用较高温度是为了提高反应物的平衡转化率 |
| D.一定量的锌与过量的稀硫酸反应制取氢气,为减缓反应速率,可向其中加入CH3COONa溶液 |
您最近一年使用:0次