金属铝质轻且有良好的防腐蚀性,在国防工业、生产、生活中具有非常重要的作用。下图是从铝土矿中制备铝的工艺流程:
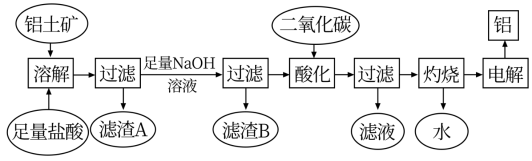
已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质;
I.依据工艺流程回答下列问题:
(1)铝土矿加入盐酸过滤后所得滤渣A的主要成分为___________ 。
(2)在工艺流程中,加入足量氢氧化钠溶液发生多个离子反应,其中发生沉淀溶解的离子反应方程式为___________ 。
(3)加入过量的二氧化碳时,生成沉淀的离子方程式为___________ 。
II.测铝土矿组分的质量分数。
(4)若铝土矿样品质量为m,对滤渣A洗涤、干燥后称重为m1;对滤渣B洗涤、干燥、灼烧后称重为m2,该方案能测得铝土矿的成份及相应的质量分数的是(写出能测出成份的化学式,并写出计算其质量分数的表达式。)___________ ,___________ 。
(5)检测滤渣A是否洗涤干净的方法是___________ 。

已知:铝土矿的主要成分是Al2O3,此外还含有少量SiO2、Fe2O3、MgO杂质;
I.依据工艺流程回答下列问题:
(1)铝土矿加入盐酸过滤后所得滤渣A的主要成分为
(2)在工艺流程中,加入足量氢氧化钠溶液发生多个离子反应,其中发生沉淀溶解的离子反应方程式为
(3)加入过量的二氧化碳时,生成沉淀的离子方程式为
II.测铝土矿组分的质量分数。
(4)若铝土矿样品质量为m,对滤渣A洗涤、干燥后称重为m1;对滤渣B洗涤、干燥、灼烧后称重为m2,该方案能测得铝土矿的成份及相应的质量分数的是(写出能测出成份的化学式,并写出计算其质量分数的表达式。)
(5)检测滤渣A是否洗涤干净的方法是
更新时间:2021-12-13 11:40:12
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】红矾钠(重铬酸钠:Na2Cr2O7·2H2O)是重要的基础化工原料。铬常见价态有+3、+6价。铬的主要自然资源是铬铁矿FeCr2O4(含有Al2O3、MgO、SiO2等杂质),实验室模拟工业以铬铁矿为原料生产红矾钠的主要流程如下:
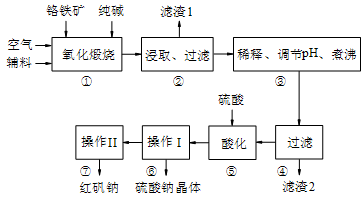
①中主要反应:4 FeCr2O4+ 8Na2CO3 + 7O2 8Na2CrO4 + 2Fe2O3+ 8CO2
8Na2CrO4 + 2Fe2O3+ 8CO2
①中副反应:Al2O3 + Na2CO3 2NaAlO2+ CO2↑,SiO2 + Na2CO3
2NaAlO2+ CO2↑,SiO2 + Na2CO3 Na2SiO3 + CO2↑
Na2SiO3 + CO2↑
请回答下列问题:
(1)FeCr2O4化学名为亚铬酸亚铁,写出它的氧化物形式________________ 。步骤“①”的反应器材质应选用__________ (填“瓷质”、“铁质”或“石英质”)。
(2)“②”中滤渣1的成分是__________ ,“③”中调pH值是_______ (填“调高”或“调低”),“④”中滤渣2的成分是___________ 。
(3)“⑤”酸化的目的是使CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:______ 。
(4)上图是Na2Cr2O7·2H2O和Na2SO4的溶解度曲线,则操作I是______ ,操作II是______ (填序号)。
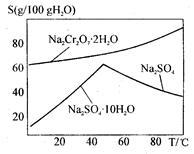
①蒸发浓缩,趁热过滤②降温结晶,过滤
(5)已知某铬铁矿含铬元素34%,进行步骤①~④中损失2%,步骤⑤~⑦中产率为92%,则1吨该矿石理论上可生产红矾钠_______ 吨(保留2位小数)。

①中主要反应:4 FeCr2O4+ 8Na2CO3 + 7O2
 8Na2CrO4 + 2Fe2O3+ 8CO2
8Na2CrO4 + 2Fe2O3+ 8CO2①中副反应:Al2O3 + Na2CO3
 2NaAlO2+ CO2↑,SiO2 + Na2CO3
2NaAlO2+ CO2↑,SiO2 + Na2CO3 Na2SiO3 + CO2↑
Na2SiO3 + CO2↑请回答下列问题:
(1)FeCr2O4化学名为亚铬酸亚铁,写出它的氧化物形式
(2)“②”中滤渣1的成分是
(3)“⑤”酸化的目的是使CrO42-转化为Cr2O72-,写出平衡转化的离子方程式:
(4)上图是Na2Cr2O7·2H2O和Na2SO4的溶解度曲线,则操作I是

①蒸发浓缩,趁热过滤②降温结晶,过滤
(5)已知某铬铁矿含铬元素34%,进行步骤①~④中损失2%,步骤⑤~⑦中产率为92%,则1吨该矿石理论上可生产红矾钠
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硒化镉(CdSe)用于电子发射器和光谱分析、光导体、半导体、光敏元件等。以镉铁矿(成分为CdO、Fe2O3、FeO及少量的Al2O3和SiO2)为原料制备硒化镉和铁红的工艺流程如图所示:

已知CdSO4易溶于水。
回答下列问题:
(1)“酸浸”时,CdO与稀硫酸反应的离子方程式为___________ 。
(2)常温下,下列物质能与滤渣1发生反应的是___________ (填序号)。
a.浓硝酸 b.碳酸钠 c.氢氟酸
(3)试剂X为___________ 。
(4)“氧化”时加入过量双氧水的目的是将溶液中的Fe2+氧化为Fe3+,检验该溶液中Fe3+的试剂是___________ 。
(5)在实验室中“灼烧”时用到的含硅酸盐的仪器有___________ (任填两种),生成的铁红的用途有___________ (任填一种)。
(6)已知镉铁矿中CdO的质量分数为64%,整个流程中镉元素的损耗率为8%,则1 t该镉铁矿可制得CdSe的质量为___________ kg。

已知CdSO4易溶于水。
回答下列问题:
(1)“酸浸”时,CdO与稀硫酸反应的离子方程式为
(2)常温下,下列物质能与滤渣1发生反应的是
a.浓硝酸 b.碳酸钠 c.氢氟酸
(3)试剂X为
(4)“氧化”时加入过量双氧水的目的是将溶液中的Fe2+氧化为Fe3+,检验该溶液中Fe3+的试剂是
(5)在实验室中“灼烧”时用到的含硅酸盐的仪器有
(6)已知镉铁矿中CdO的质量分数为64%,整个流程中镉元素的损耗率为8%,则1 t该镉铁矿可制得CdSe的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】由短周期元素组成的单质A、B、C和甲、乙、丙、丁四种化合物有图示的转换关系, 已知C为密度最小的气体。根据图示转化关系回答:
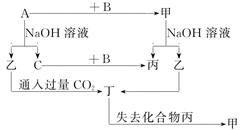
(1)若甲是电解质。写出下列物质的化学式:甲______________ ,丁_______________ 。
写出乙与过量CO2反应的离子方程式:____________________________________________ 。
(2)若甲是非电解质。写出下列物质的化学式:甲_______________ ,乙______________ 。

(1)若甲是电解质。写出下列物质的化学式:甲
写出乙与过量CO2反应的离子方程式:
(2)若甲是非电解质。写出下列物质的化学式:甲
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铝是应用广泛的金属。以铝土矿(主要成分为Al2O3,含SiO2和Fe2O3等杂质)为原料制备铝的一种工艺流程如下:

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时氧化铝反应的离子方程式为_______ 。
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH_______ (填“增大”、“不变”或“减小”)。
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是_______ 。
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为_______ ,阴极产生的物质A的化学式为_______ 。

(5)氮化铝(AlN)具有耐高温、抗冲击、导热性好的优良性质广泛应用于电子工业陶瓷工业等领域。在一定条件下,氮化铝可通过氧化铝和焦炭在氮气氛围中合成,写出该反应的化学方程式_______ ,并请用单线桥法在化学方程式上标出该反应中电子转移的方向和数目_______ 。

注:SiO2在“碱溶”时转化为铝硅酸钠沉淀。
(1)“碱溶”时氧化铝反应的离子方程式为
(2)向“过滤Ⅰ”所得滤液中加入NaHCO3溶液,溶液的pH
(3)“电解Ⅰ”是电解熔融Al2O3,电解过程中作阳极的石墨易消耗,原因是
(4)“电解Ⅱ”是电解Na2CO3溶液,原理如图所示。阳极的电极反应式为

(5)氮化铝(AlN)具有耐高温、抗冲击、导热性好的优良性质广泛应用于电子工业陶瓷工业等领域。在一定条件下,氮化铝可通过氧化铝和焦炭在氮气氛围中合成,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】煤灰的综合利用既有利于节约资源,又有利于保护环境。某粉煤灰(主要含Al2O3、Fe2O3、CaCO3等)的铝、铁分离工艺流程如下:

(1)①“酸浸”时Fe2O3发生反应的离子方程式为___________ 。
②当硫酸质量分数大于50%时,金属氧化物浸出率明显下降。其原因是___________
(2)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图1所示。“还原”操作的作用是_____ 。“沉铝”过程中加入氨水调pH的范围是_______ ,“沉铝”反应的方程式为___________ 。
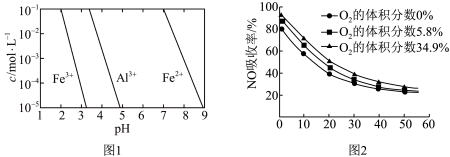
(3)“沉铝”后所得FeSO4溶液可用于烟气中NO的吸收,其原理为Fe2++2NO [Fe(NO)2]2+。
[Fe(NO)2]2+。
①由图2可知,为提高烟气中NO的吸收率,可选择烟气中O2的体积分数为___________ 。
②“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6(已知氢元素+1价、氧元素-2价)发生反应,得到N2与CO2的物质的量之比为___________ 。

(1)①“酸浸”时Fe2O3发生反应的离子方程式为
②当硫酸质量分数大于50%时,金属氧化物浸出率明显下降。其原因是
(2)有关金属离子以氢氧化物沉淀时离子浓度随pH变化如图1所示。“还原”操作的作用是

(3)“沉铝”后所得FeSO4溶液可用于烟气中NO的吸收,其原理为Fe2++2NO
 [Fe(NO)2]2+。
[Fe(NO)2]2+。①由图2可知,为提高烟气中NO的吸收率,可选择烟气中O2的体积分数为
②“再生”过程中,[Fe(NO)2]2+在微生物的作用下与C6H12O6(已知氢元素+1价、氧元素-2价)发生反应,得到N2与CO2的物质的量之比为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】CoC2O4是制备氧化钴和金属钴的原料。一种利用含钴废料(主要成分为Co2O3,含少量Fe2O3、Al2O3、MnO、CaO、MgO碳及有机物等)制取CoC2O4的工艺流程如下:
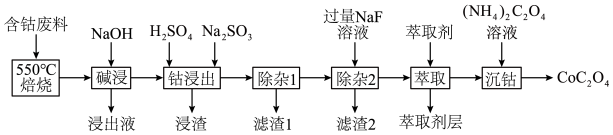
(1)为了加快“碱浸”速率,可采用的方法有________ (写一种即可)。“浸出液”的主要成分是_______ (填化学式)。
(2)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为___________ 。
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式为_______________ 。
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×10-5mol/L,则滤液中c(Mg2+)为______ [已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2) =1.05×10-10]。
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,需控制溶液的pH范围是__________ (填字母)。
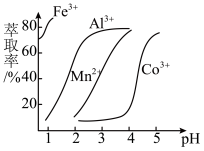
A.1.0~2.0 B.2.0~3.0 C.3.0~3.5

(1)为了加快“碱浸”速率,可采用的方法有
(2)“钴浸出”过程中Co3+转化为Co2+,反应的离子方程式为
(3)“除杂1”过程中,在40~50℃加入H2O2,写出加入H2O2反应的主要离子方程式为
(4)“除杂2”可将钙、镁离子转化为沉淀过滤除去,若所得滤液中c(Ca2+)=1.0×10-5mol/L,则滤液中c(Mg2+)为
(5)萃取剂对金属离子的萃取率与pH的关系如图所示,经过萃取可除去Mn2+,需控制溶液的pH范围是

A.1.0~2.0 B.2.0~3.0 C.3.0~3.5
您最近一年使用:0次
【推荐1】某同学拟用粗氧化铜(含少量FeO及不溶于酸的杂质)制取无水氯化铜,流程如图:
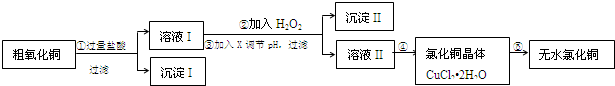
回答下列问题:
(1)步骤①中氧化铜与盐酸反应的离子方程式:_______ 。
(2)步骤②中加入H2O2的目的是_____ ,沉淀II的化学式为_______ 。
(3)已知:
步骤③中调节pH的最佳范围为________ ,调节溶液pH的试剂X可以是______ (填字母)。
A.NaOH B.CuO C.Cu(OH)2 D.NH3·H2O
(4)步骤④的操作是______ 、过滤、洗涤、干燥。为得到无水CuCl2,步骤⑤需在干燥的HCl气流中加热CuCl2·2H2O,原因是________ 。

回答下列问题:
(1)步骤①中氧化铜与盐酸反应的离子方程式:
(2)步骤②中加入H2O2的目的是
(3)已知:
| 氢氧化物开始沉淀时的pH | 氢氧化物完全沉淀时的pH | |
| Fe3+ | 1.9 | 3.2 |
| Cu2+ | 4.7 | 6.7 |
| Fe2+ | 7 | 9 |
步骤③中调节pH的最佳范围为
A.NaOH B.CuO C.Cu(OH)2 D.NH3·H2O
(4)步骤④的操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】Ce2(CO3)3可用于催化剂载体及功能材料的制备。天然独居石中,铈(Ce)主要以CePO4形式存在,还含有SiO2、Al2O3、Fe2O3、CaF2等物质。以独居石为原料制备Ce2(CO3)3·nH2O的工艺流程如下:
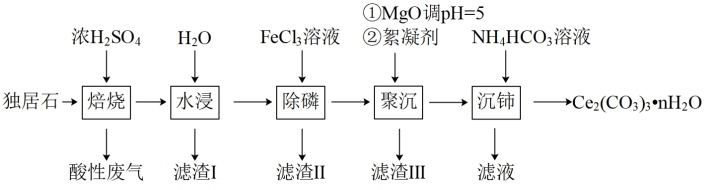
回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为_______ ;
(2)为提高“水浸”效率,可采取的措施有_______ (至少写两条);
(3)滤渣Ⅲ的主要成分是_______ (填化学式);
(4)加入絮凝剂的目的是_______ ;
(5)“沉铈”过程中,生成Ce2(CO3)3·nH2O的离子方程式为_______ 。
(6)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖(C6H12O6)和FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为_______ 。

回答下列问题:
(1)铈的某种核素含有58个质子和80个中子,该核素的符号为
(2)为提高“水浸”效率,可采取的措施有
(3)滤渣Ⅲ的主要成分是
(4)加入絮凝剂的目的是
(5)“沉铈”过程中,生成Ce2(CO3)3·nH2O的离子方程式为
(6)滤渣Ⅱ的主要成分为FePO4,在高温条件下,Li2CO3、葡萄糖(C6H12O6)和FePO4可制备电极材料LiFePO4,同时生成CO和H2O,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】碱式硫酸铁[Fe(OH)SO4]是黄褐色固体,常用作媒染剂和净水剂。一种利用废铁屑(含少量Al、Al2O3、Fe2O3 等杂质)生产碱式硫酸铁的工艺流程如图所示:
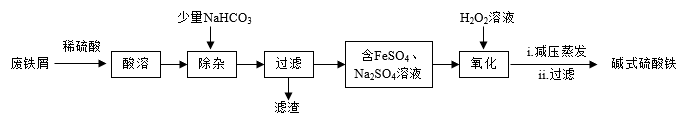
已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
②Fe(OH)2+发生电离:Fe(OH)2+ Fe3++OH-。
Fe3++OH-。
请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是___________ 。
(2)“氧化”过程中,发生反应的离子方程式为___________ ;该过程某同学选用稀硝酸代替H2O2溶液完成反应,你认为不足之处是___________ 。
(3)“氧化”过程中,若硫酸加入量过小,容易生成___________ (填化学式)沉淀;若硫酸加入量过大,不利于产品形成,试从平衡移动的角度分析原因是___________ 。
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是___________ (填字母代号)。
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液

已知:①部分金属阳离子生成氢氧化物沉淀时溶液的pH如表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀 | 7.5 | 2.3 | 3.4 |
| 沉淀完全 | 9.7 | 3.2 | 4.4 |
②Fe(OH)2+发生电离:Fe(OH)2+
 Fe3++OH-。
Fe3++OH-。请回答下列问题:
(1)加入少量NaHCO3,调节pH的范围是
(2)“氧化”过程中,发生反应的离子方程式为
(3)“氧化”过程中,若硫酸加入量过小,容易生成
(4)将所得产品加蒸馏水溶解,为检验是否含有Fe2+,最好选用的试剂是
A.氯水 B.KSCN溶液 C.K3[Fe(CN)6]溶液 D.H2O2溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某废钼镍催化剂主要含MoS2、 NiS、 Al2O3等,一种从其中回收金属元素Mo和Ni的工艺流程如图所示:

已知:
①H2MoO4是一种二元弱酸;“ 加碱焙烧”过程中有Na2MoO4生成。
②25℃时,H2CO3的Ka1=4.5×10-7, Ka2=5. 0×10-11; Ksp( CaMoO4)=4.0×10-8,Ksp(CaCO3)= 3. 2 ×10-9。
回答下列问题:
(1)“低温焙烧”过程时,粉碎后的废钼镍催化剂从炉顶进入,空气从炉底进入,其目的是_______ ;该过程中MoS2转化成MoO3,写出相关的化学方程式:_______ 。
(2)生成固体X的离子方程式为_______ 。
(3)将“含Ni固体”用稀硫酸溶解,再经_______ 、过滤、洗涤可得到NiSO4·6H2O(NiSO4的溶解度随温度的变化曲线如图所示)。
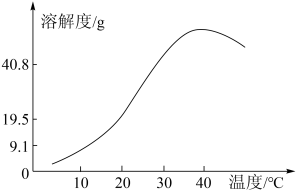
(4)“沉钼”时溶液pH与沉钼率之间的关系如图所示:

①当溶液pH小于7. 0时,沉钼率较低的原因可能为_______ 。
②“沉钼”时若条件控制不当,CaCO3也会沉淀。若“ 沉钼”时控制溶液pH=8.0,为避免CaCO3沉淀,当溶液中c( ) : c(
) : c( )=
)=_______ 时,应停止加入CaCl2溶液。

已知:
①H2MoO4是一种二元弱酸;“ 加碱焙烧”过程中有Na2MoO4生成。
②25℃时,H2CO3的Ka1=4.5×10-7, Ka2=5. 0×10-11; Ksp( CaMoO4)=4.0×10-8,Ksp(CaCO3)= 3. 2 ×10-9。
回答下列问题:
(1)“低温焙烧”过程时,粉碎后的废钼镍催化剂从炉顶进入,空气从炉底进入,其目的是
(2)生成固体X的离子方程式为
(3)将“含Ni固体”用稀硫酸溶解,再经

(4)“沉钼”时溶液pH与沉钼率之间的关系如图所示:

①当溶液pH小于7. 0时,沉钼率较低的原因可能为
②“沉钼”时若条件控制不当,CaCO3也会沉淀。若“ 沉钼”时控制溶液pH=8.0,为避免CaCO3沉淀,当溶液中c(
 ) : c(
) : c( )=
)=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氢氧化铈[Ce(OH)4]被广泛用于气敏传感器、燃料电池、催化剂等领域。实验室以精选的氟碳铈矿(主要成分为CeFCO3 )为原料制备氢氧化铈的一种工艺流程如下:
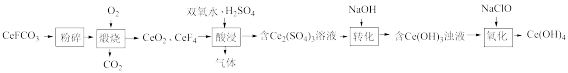
回答下列问题:
(1)“煅烧”可在_______ (填仪器名称)中进行,主要反应的化学方程式为________ ;除“粉碎”外,还可以加快“煅烧”速率的措施有_________ (只答一点即可)。
(2)实验室制取氧气。
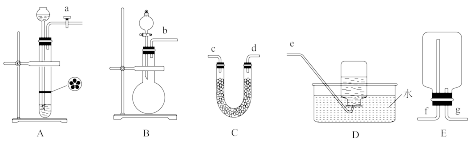
①氧气的发生装置可以选择上图中的__________ (填大写字母)。
②欲收集一瓶干燥的氧气,选择上图中的装置,按气流方向的连接顺序为:氧气的发生装置→________ (填小写字母);检验氧气已收集满的操作和现象为________ 。
(3)“酸浸”时,温度不能过高的原因为_______ ;若用盐酸代替双氧水、H2SO4的不足之处为____________ ;该步骤不能使用陶瓷容器的原因为___________________ 。
(4)“氧化”反应的化学方程式为_________________________________ 。
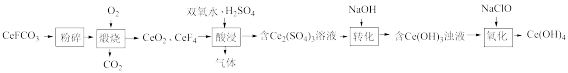
回答下列问题:
(1)“煅烧”可在
(2)实验室制取氧气。
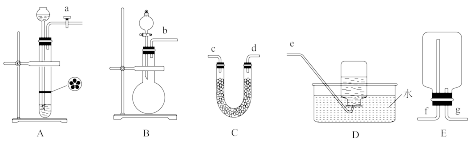
①氧气的发生装置可以选择上图中的
②欲收集一瓶干燥的氧气,选择上图中的装置,按气流方向的连接顺序为:氧气的发生装置→
(3)“酸浸”时,温度不能过高的原因为
(4)“氧化”反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】NiSO4·XH2O是一种绿色易溶于水的晶体,广泛用于镀镍、电池等,可由电镀废渣(除镍外,还含有铜、锌、铁等元素)为原料获得。操作步骤如图:
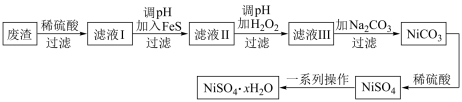
(1)在待镀件上镀镍时,待镀件应作___ 极,电镀过程中电解质溶液浓度_____ (填“增大”、“减小”、“不变”)
(2)向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质。已知FeS难溶解于水,利用溶解平衡移动原理解释加入FeS前调pH的原因____ (请用化学用语结合文字说明);当Zn2+恰好沉淀完全时,c(Zn2+)=10-5mol/L,则c(Cu2+)=_____ mol/L[已知Ksp(CuS)=1.3×10-36,Ksp(ZnS)=1.6×10-24]。
(3)滤液Ⅲ溶质的主要成分是NiSO4,流程中在滤液Ⅲ后又设计了两步,再次得到NiSO4溶液,这样设计流程的目的是_______ 。
(4)为测定NiSO4•xH2O晶体x的值,称取26.3g晶体加热至充全失去结晶水,剩余固体15.5g,则x的值等于____ 。

(1)在待镀件上镀镍时,待镀件应作
(2)向滤液Ⅰ中加入FeS是为了除去Cu2+、Zn2+等杂质。已知FeS难溶解于水,利用溶解平衡移动原理解释加入FeS前调pH的原因
(3)滤液Ⅲ溶质的主要成分是NiSO4,流程中在滤液Ⅲ后又设计了两步,再次得到NiSO4溶液,这样设计流程的目的是
(4)为测定NiSO4•xH2O晶体x的值,称取26.3g晶体加热至充全失去结晶水,剩余固体15.5g,则x的值等于
您最近一年使用:0次



