金属钛有“生物金属、海洋金属、太空金属”的美称。有些含钛的化合物在耐高温、环保或者抑菌方面有着重要的应用,钛元素也被称为“健康钛”。
(1)Ti元素位于元素周期表的___________ 区,基态原子价电子排布式为___________ 。
(2)TiCl4与SiCl4互为等电子体。SiCl4可以与N-甲基咪唑(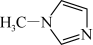 ) 发生反应。
) 发生反应。
①TiCl4分子的空间构型为___________ 。
②N-甲基咪唑分子中碳原子的杂化轨道类型为___________ , C、 N、Si的电负性由大到小的顺序为___________ , 1个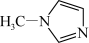 含有
含有___________ 个σ键。
(3)TiC14可以与胺形成配合物,如TiCl4 (CH3NH2)2、TiC14(H2NCH2CH2NH2)。
①TiCl4 (H2NCH2CH2NH2) 中提供电子对形成配位键的原子是___________ 。
②乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性较高的是___________ (填“Mg2+”或“Cu2+”)。
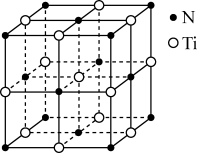
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如下图),其中阴离子(N3- )采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为apm,则r(N3- )为___________ pm。该氮化钛的密度为___________ g·cm- 3(NA为阿伏加德罗常数的值,只列计算式)。
(1)Ti元素位于元素周期表的
(2)TiCl4与SiCl4互为等电子体。SiCl4可以与N-甲基咪唑(
 ) 发生反应。
) 发生反应。①TiCl4分子的空间构型为
②N-甲基咪唑分子中碳原子的杂化轨道类型为
 含有
含有(3)TiC14可以与胺形成配合物,如TiCl4 (CH3NH2)2、TiC14(H2NCH2CH2NH2)。
①TiCl4 (H2NCH2CH2NH2) 中提供电子对形成配位键的原子是
②乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性较高的是
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似(如下图),其中阴离子(N3- )采用面心立方最密堆积方式,X-射线衍射实验测得氮化钛的晶胞参数(晶胞边长)为apm,则r(N3- )为

更新时间:2022-02-19 08:10:14
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】Ti、Na、Mg、C、N、O、Fe等元素的研究一直在进行中,其单质及化合物在诸多领域都有广泛的应用。回答下列问题:
(1)钠在火焰上灼烧的黄光是一种____ (填字母)。
A.吸收光谱B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是____ ,能量最低的是____ (填序号)。
a.1s22s22p43s13p3b.1s22s22p33s23p3c.1s22s22p63s13p1d.1s22s22p63s2
(3)Ti原子位于元素周期表中的____ 区,最高能层电子的电子云轮廓形状为____ ,其价电子排布式为____ 。与Ti同周期的过渡元素中,未成对电子数最多的的基态原子的外围电子排布图____ 。
(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是____ 。
(5)Fe3+与Fe2+的离子半径大小关系为Fe3+____ Fe2+(填“大于”或“小于”)。
(1)钠在火焰上灼烧的黄光是一种
A.吸收光谱B.发射光谱
(2)下列Mg原子的核外电子排布式中,能量最高的是
a.1s22s22p43s13p3b.1s22s22p33s23p3c.1s22s22p63s13p1d.1s22s22p63s2
(3)Ti原子位于元素周期表中的
(4)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+易被氧化成Fe3+的原因是
(5)Fe3+与Fe2+的离子半径大小关系为Fe3+
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】铁、钴、镍具有相似的性质,在化学上称为铁系元素。回答下列问题:
(1)LiCoO2、 LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为_________ ,第四电离能I4(Co) _________ I4(Fe)(填“>”或“<”),PO43-的空间构型为_________ 。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。
与CO互为等电子体的分子和离子分别为_________ 和_________ (各举一种,填化学式);在CO分子中,键与π键数目之比为_________ 。
(3)铁与K2O、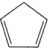 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为_________ 。二茂铁熔点为446K,不溶于水,易溶于乙醚、苯、乙醇等有机溶剂,373K即升华;从各种性质看,都表明它是典型的_________ 化合物。
(4)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。
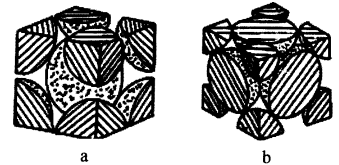
在图a所示堆积方式里铁原子的半径为rpm,则其晶胞棱长为_________ cm。
在图b所示堆积方式里铁原子的总体积占晶体体积的比例为_________ (用含圆周率π的代数式表示)
(1)LiCoO2、 LiFePO4常用作锂离子电池的正极材料。基态Co原子核外电子排布式为
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等金属羰基配合物。
与CO互为等电子体的分子和离子分别为
(3)铁与K2O、
 (环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为
(环戊二烯)在隔绝空气条件下共热可制得二茂铁[Fe(C5H5)2]。在环戊二烯中,C原子的杂化轨道类型为(4)铁单质的堆积方式有两种,其剖面图分别如图a、b所示。

在图a所示堆积方式里铁原子的半径为rpm,则其晶胞棱长为
在图b所示堆积方式里铁原子的总体积占晶体体积的比例为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】Si是优良的半导体材料:石墨是制作电极的良好材料:Cu是导电性能极佳的金属,在生活中都有着广泛的应用。回答下列问题
(1)写出CuSO4、Cu(NO3)2中阳离子的核外电子排布式___________
(2)CuSO4晶体熔点为560℃,Cu(NO3)2晶体熔点为15℃。前者比后者熔点高的原因___________
(3)Cu2O有半导体性质,不溶于水,可溶于氨水生成[Cu(NH3)2]+, 1mol[Cu(NH3)2]+中共价键的数目为___________ 个。
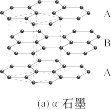
(4)石墨中C的杂化方式为___________ ,α-石墨和β-石墨结构如图(a)、(b)所示,已知:C(α-石墨,s)=C(β-石墨,s) △H=+0.586kJ·mol-1, △H数值小,易转化。请从石墨晶体结构的角度分析△H数值小的原因是___________

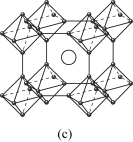
(5)高导电紫铜常用CaBx提高导电率,CaBx晶胞如图(c)所示,B原子全部组成正八面体,各个顶点通过B-B键连接成三维骨架,具有立方晶系的对称性,则x=___________ ,B原子半径为r nm,则晶胞参数a(晶胞棱长)=___________ nm。
(1)写出CuSO4、Cu(NO3)2中阳离子的核外电子排布式
(2)CuSO4晶体熔点为560℃,Cu(NO3)2晶体熔点为15℃。前者比后者熔点高的原因
(3)Cu2O有半导体性质,不溶于水,可溶于氨水生成[Cu(NH3)2]+, 1mol[Cu(NH3)2]+中共价键的数目为
(4)石墨中C的杂化方式为



(5)高导电紫铜常用CaBx提高导电率,CaBx晶胞如图(c)所示,B原子全部组成正八面体,各个顶点通过B-B键连接成三维骨架,具有立方晶系的对称性,则x=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硒(Se)是人体必需微量元素之一,含硒化合物在材料和药物领域具有重要应用。自我国科学家发现聚集诱导发光(AIE)效应以来,AIE在发光材料、生物医学等领域引起广泛关注。一种含Se的新型AIE分子IV的合成路线如图:
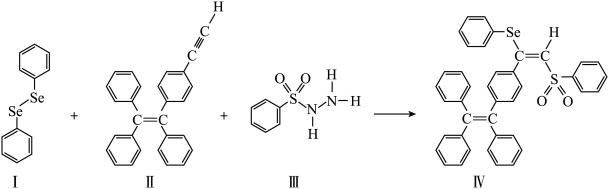
(1)Se与S同族,基态硒原子价电子排布式为_____ 。
(2) 的沸点低于H2O,其原因是
的沸点低于H2O,其原因是_____ 。
(3)关于I~III三种反应物,下列说法正确的有_____ (填标号)。
A.I中仅有σ键
B.I中的Se-Se为非极性共价键
C.II易溶于水
D.III中原子的杂化轨道类型有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有_____ 。
(5)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒,SeO 的空间结构为
的空间结构为_____ 。
(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。
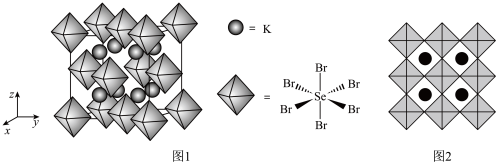
①X的化学式为_____ 。
②设X的最简式的式量为Mr,晶体密度为ρg•cm-3,则X中相邻K之间的最短距离为_____ nm(列出计算式,NA为阿伏加德罗常数的值)。

(1)Se与S同族,基态硒原子价电子排布式为
(2)
 的沸点低于H2O,其原因是
的沸点低于H2O,其原因是(3)关于I~III三种反应物,下列说法正确的有
A.I中仅有σ键
B.I中的Se-Se为非极性共价键
C.II易溶于水
D.III中原子的杂化轨道类型有sp与sp2
E.I~III含有的元素中,O电负性最大
(4)IV中具有孤对电子的原子有
(5)研究发现,给小鼠喂食适量硒酸钠(Na2SeO4)可减轻重金属铊引起的中毒,SeO
 的空间结构为
的空间结构为(6)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2。

①X的化学式为
②设X的最简式的式量为Mr,晶体密度为ρg•cm-3,则X中相邻K之间的最短距离为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用含砷、锑烟灰(主要成分为Sb2O3、As2O3,含Pb、Ag、 Cu的氧化物)制取焦锑酸钠[NaSb(OH)6]和砷酸钠晶体(Na3AsO4 ·12H2O),不仅治理了砷害污染,还可综合回收其他有价金属。其工艺流程如图所示:
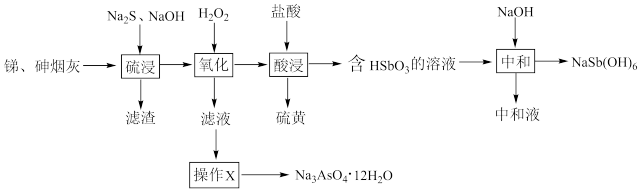
已知:①Pb、Ag、Cu的氧化物不溶于Na2S溶液。
②硫浸后,锑、砷以Na3SbS3、Na3AsS3的形式存在。
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)As的核外电子排布式是_______ , 在元素周期表中,Cu处于_______ 区。
(2)“硫浸”时,Sb2O3溶解的离子方程式为_______ 。“氧化”时氧化产物除了锑的含氧酸盐外,还有_______ (填化学式)。
(3)“操作”X为_______ 、过滤、洗涤、干燥。“中和”时生成NaSb( OH)6的化学方程式是_______ 。
(4)研究发现,电解硫浸液中的Na3SbS3-NaOH溶液,可得到单质Sb,则阴极的电极反应式为_______ 。
(5)砷的化合物砷化镓是一种重要的半导体材料,已知镓(Ga)是铝的同族元素,砷化镓的晶胞结构如图所示。该晶胞中黑球代表_______ ( 填元素符号),砷化镓的化学式为_______ ,该晶体中含有的化学键为_______ (填“共价键”“配位键”“离子键”),属于_______ 晶体。

已知:①Pb、Ag、Cu的氧化物不溶于Na2S溶液。
②硫浸后,锑、砷以Na3SbS3、Na3AsS3的形式存在。
③NaSb(OH)6易溶于热水,难溶于冷水,不溶于乙醇。
回答下列问题:
(1)As的核外电子排布式是
(2)“硫浸”时,Sb2O3溶解的离子方程式为
(3)“操作”X为
(4)研究发现,电解硫浸液中的Na3SbS3-NaOH溶液,可得到单质Sb,则阴极的电极反应式为
(5)砷的化合物砷化镓是一种重要的半导体材料,已知镓(Ga)是铝的同族元素,砷化镓的晶胞结构如图所示。该晶胞中黑球代表

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】氧族元素是元素周期表中第ⅥA族元素,包含氧(O)、硫(S)、硒(Se)、碲(Te)、钋(Po)五种元素,它们及其化合物在生产、生活中有着广泛的应用。回答下列问题:
(1)基态Se原子的核外电子排布式为___________ 。
(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为___________ ,原因是___________ 。
(3) 与
与 相比,键角较小的是
相比,键角较小的是___________ (填离子符号),原因是___________ 。
(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为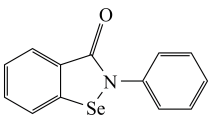 。依布硒分子中Se、C原子的杂化类型分别为
。依布硒分子中Se、C原子的杂化类型分别为___________ 、___________ 。
(1)基态Se原子的核外电子排布式为
(2)H2O、H2S、H2Se、H2Te的沸点由高到低的顺序为
(3)
 与
与 相比,键角较小的是
相比,键角较小的是(4)依布硒是一种有机硒化物,具有良好的抗炎活性,其结构简式为
 。依布硒分子中Se、C原子的杂化类型分别为
。依布硒分子中Se、C原子的杂化类型分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】金属钛被誉为“未来金属”,钛及其化合物被广泛应用于飞机、火箭、卫星、舰艇、医疗等领域。“嫦娥五号”首次实现了我国地外天体采样返回,它的成功发射标志着我国航天技术向前迈出了一大步,其制作材料中包含了 元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
(1)钛位于周期表的___________ 区,基态钛原子价电子排布式为___________ 。
(2) 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。请写出一个与
反应制得。请写出一个与 互为等电子体的微粒
互为等电子体的微粒___________ (化学式)。
(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示:
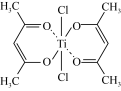
①该配合物中碳原子的杂化类型___________ 。
②该配合物中存在的化学键有___________ (填字母)。
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物 、
、 、
、 、
、 熔点依次为377℃、
熔点依次为377℃、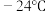 、38.3℃、153℃,其中
、38.3℃、153℃,其中 、
、 、
、 熔点依次升高的原因是
熔点依次升高的原因是___________ 。
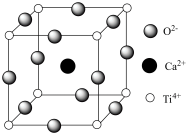
(5) 的晶胞如图所示,
的晶胞如图所示, 的配位数是
的配位数是___________ ,若 位于晶胞顶点,则
位于晶胞顶点,则 位于晶胞
位于晶胞___________ 位置,若晶胞参数为a nm,则晶体密度为___________  (列出计算式,阿伏加德罗常数用NA表示)。
(列出计算式,阿伏加德罗常数用NA表示)。
 元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。
元素。2022年2月我国科学家在《科学》杂志发表反型钙钛矿太阳能电池研究方面的最新科研成果论文,为钙钛矿电池研究开辟了新方向。(1)钛位于周期表的
(2)
 是一种储氢材料,可由
是一种储氢材料,可由 和
和 反应制得。请写出一个与
反应制得。请写出一个与 互为等电子体的微粒
互为等电子体的微粒(3)钛的某配合物可用于催化环烯烃聚合,其结构如图所示:

①该配合物中碳原子的杂化类型
②该配合物中存在的化学键有
a.共价键 b.金属键 c.配位键 d.氢键
(4)钛与卤素形成的化合物
 、
、 、
、 、
、 熔点依次为377℃、
熔点依次为377℃、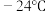 、38.3℃、153℃,其中
、38.3℃、153℃,其中 、
、 、
、 熔点依次升高的原因是
熔点依次升高的原因是(5)
 的晶胞如图所示,
的晶胞如图所示, 的配位数是
的配位数是 位于晶胞顶点,则
位于晶胞顶点,则 位于晶胞
位于晶胞 (列出计算式,阿伏加德罗常数用NA表示)。
(列出计算式,阿伏加德罗常数用NA表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】蛋白质是构成生物体的基本物质,蛋白质的组成元素主要有氢、碳、氮、氧、硫,同时还有微量元素铁、锌等。回答下列问题:
(1)在基态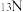 原子中,核外电子占据的最高能级的电子云轮廓图为
原子中,核外电子占据的最高能级的电子云轮廓图为________ 形。
(2)常见的含氮微粒有 、
、 、
、 等。与
等。与 互为等电子体的分子为
互为等电子体的分子为________ (写出一种)。根据价层电子对互斥理论,可推知 的空间构型为
的空间构型为________ , 比
比 更容易液化的原因是
更容易液化的原因是________ 。
(3)将足量的氨水逐滴加入到 溶液中,先生成沉淀,然后沉淀溶解生成配合物
溶液中,先生成沉淀,然后沉淀溶解生成配合物 ,该配合物中的阳离子结构式为
,该配合物中的阳离子结构式为________ ; 中的硫原子杂化方式为
中的硫原子杂化方式为________ ;用价层电子对互斥理论解释 的键角大于
的键角大于 :
:________ 。
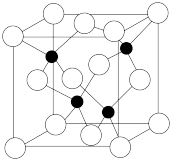
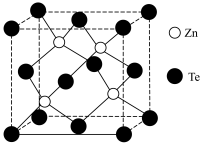
(4)碲化锌晶体有两种结构,其中一种晶胞结构如图:晶胞中与Zn原子距离最近的Te原子围成________ 形;与Te原子距离最近的Te原子有________ 个;若与Zn原子距离最近的Te原子间距为apm,则晶体密度为________  (列出计算式即可)。
(列出计算式即可)。
(1)在基态
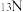 原子中,核外电子占据的最高能级的电子云轮廓图为
原子中,核外电子占据的最高能级的电子云轮廓图为(2)常见的含氮微粒有
 、
、 、
、 等。与
等。与 互为等电子体的分子为
互为等电子体的分子为 的空间构型为
的空间构型为 比
比 更容易液化的原因是
更容易液化的原因是(3)将足量的氨水逐滴加入到
 溶液中,先生成沉淀,然后沉淀溶解生成配合物
溶液中,先生成沉淀,然后沉淀溶解生成配合物 ,该配合物中的阳离子结构式为
,该配合物中的阳离子结构式为 中的硫原子杂化方式为
中的硫原子杂化方式为 的键角大于
的键角大于 :
:(4)碲化锌晶体有两种结构,其中一种晶胞结构如图:晶胞中与Zn原子距离最近的Te原子围成
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】黄铜矿是工业炼铜的原料,含有的主要元素是硫、铁、铜,请回答下列问题。
(l)基态硫原子中核外电子有____ 种空间运动状态。Fe2+的电子排布式是 ___ 。
(2)液态SO2可发生白偶电离2SO2=SO2++SO32-,SO32-的空间构型是___ ,与SO2+互为等电子体的分子有____ (填化学式,任写一种)。
(3)CuCl熔点为426℃,融化时几乎不导电,CuF的熔点为908℃,沸点1100℃,都是铜(I)的卤化物,熔沸点相差这么大的原因是___ 。
(4)乙硫醇(C2H5SH)是一种重要的合成中间体,分子中硫原子的杂化形式是____ 。乙硫醇的沸点比乙醇的沸点____ (填“高”或“低”),原因是____ 。
(5)黄铜矿主要成分X的晶胞结构及晶胞参数如图所示,X的化学式是___ ,其密度为 ___ g/cm3(阿伏加 德罗常数的值用NA表示)。

(l)基态硫原子中核外电子有
(2)液态SO2可发生白偶电离2SO2=SO2++SO32-,SO32-的空间构型是
(3)CuCl熔点为426℃,融化时几乎不导电,CuF的熔点为908℃,沸点1100℃,都是铜(I)的卤化物,熔沸点相差这么大的原因是
(4)乙硫醇(C2H5SH)是一种重要的合成中间体,分子中硫原子的杂化形式是
(5)黄铜矿主要成分X的晶胞结构及晶胞参数如图所示,X的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬(Cr)18%、含镍(Ni)8%。回答下列问题:
(1)碳的价电子层的电子排布式为____ ;石墨烯(即单层石墨)是一种碳原子构成的单层二维蜂窝状晶格结构的新材料,其中碳原子采取____ 杂化。
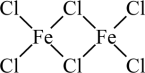
(2)铁的氯化物FeCl3蒸汽状态下以双聚分子形式存在(如图),其中Fe的配位数为____ ,双聚分子中存在配位键,提供空轨道的是____ 原子。
(3)甘氨酸亚铁[(H2NCH2COO)2Fe]中非金属元素的电负性由大到小的顺序是____ 。甘氨酸(H2NCH2COOH)比其同分异构体硝基乙烷(C2H5NO2)熔沸点高,其原因主要是____ 。
(4)FeCO3的阴离子的空间构型为____ ,写出一种与该阴离子互为等电子体的分子的化学式____ 。
(5)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为____ cm(用含NA的表达式表示)。
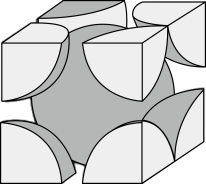
(1)碳的价电子层的电子排布式为
(2)铁的氯化物FeCl3蒸汽状态下以双聚分子形式存在(如图),其中Fe的配位数为

(3)甘氨酸亚铁[(H2NCH2COO)2Fe]中非金属元素的电负性由大到小的顺序是
(4)FeCO3的阴离子的空间构型为
(5)金属铬属于体心立方晶体(如图),已知其密度为7.2g/cm3,阿伏加德罗常数的值为NA,则晶体中铬原子的半径为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】碳、氮、氧元素的单质或化合物在很多领域有着广泛的应用。回答下列问题:
(1) 、
、 、
、 的键角由大到小的顺序是
的键角由大到小的顺序是______ 。
(2) (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为______ 。
(3)甲醇的沸点(64.7℃)介于水和甲硫醇( ,7.6℃)之间,原因是
,7.6℃)之间,原因是____________ 。
(4) (x=3,4,5,6)是一系列化合物,向含1mol
(x=3,4,5,6)是一系列化合物,向含1mol 的溶液中加入足量
的溶液中加入足量 溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
① 含有的化学键类型有
含有的化学键类型有______ (填标号)。
A.极性共价键 B.离子键 C.配位键 D.金属键 E.氢键
②能准确表示 结构的化学式为
结构的化学式为______ 。
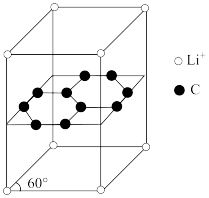
(5)锂电池负极材料晶体为 嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为
嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为______ ;其中与一个 距离最近且相等的C原子数为
距离最近且相等的C原子数为______ 。
(1)
 、
、 、
、 的键角由大到小的顺序是
的键角由大到小的顺序是(2)
 (二氟氮烯)分子中,氮原子的杂化类型为
(二氟氮烯)分子中,氮原子的杂化类型为 ,则
,则 的结构式为
的结构式为(3)甲醇的沸点(64.7℃)介于水和甲硫醇(
 ,7.6℃)之间,原因是
,7.6℃)之间,原因是(4)
 (x=3,4,5,6)是一系列化合物,向含1mol
(x=3,4,5,6)是一系列化合物,向含1mol 的溶液中加入足量
的溶液中加入足量 溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。
溶液,生成的含银物质只有难溶于硝酸的白色沉淀;过滤后,充分加热滤液,有4mol氨气逸出,且又有上述沉淀生成,两次沉淀的物质的量之比为1∶2。①
 含有的化学键类型有
含有的化学键类型有A.极性共价键 B.离子键 C.配位键 D.金属键 E.氢键
②能准确表示
 结构的化学式为
结构的化学式为(5)锂电池负极材料晶体为
 嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为
嵌入两层石墨层中导致石墨堆积方式发生改变,上下层一样,形成如图所示的晶胞结构。晶胞中锂离子和碳原子的个数之比为 距离最近且相等的C原子数为
距离最近且相等的C原子数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】铜是重要的战略资源,云南是我国铜资源储量较高的省份之一,回答下列问题:
(1)铜在周期表中位于第______ 族(填族序数),属于______ 区。
(2)铜可以形成多种配合物。
① 的核外电子排布式是
的核外电子排布式是______ ,过渡金属离子与水分子形成配合物时,若d轨道全空或全满时,化合物无颜色,否则有颜色。据此判断,
______ (填“有”或“无”)颜色。
② 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是______ , 中N原子的杂化方式是
中N原子的杂化方式是______ ,空间构型是______ 。
(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是______ 。
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为______ 。
(1)铜在周期表中位于第
(2)铜可以形成多种配合物。
①
 的核外电子排布式是
的核外电子排布式是
②
 可形成多种配合物,如
可形成多种配合物,如 ,若其中两个
,若其中两个 被
被 替换,得到的配合物只有两种结构,则
替换,得到的配合物只有两种结构,则 的空间构型是
的空间构型是 中N原子的杂化方式是
中N原子的杂化方式是(3)铜与金等金属及合金可用于生产石墨烯的催化剂,如图是一种铜金合金的晶胞示意图:

①Cu原子的配位数是
②原子坐标参数,表示晶胞内部各原子的相对位置,其中原子坐标参数A为
 ;B为
;B为 ;C为
;C为 。则D原子的坐标参数为
。则D原子的坐标参数为
您最近一年使用:0次



