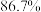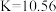在固定容积的密闭容器中,按 与
与 的物质的量之比为1∶3进行投料,发生反应
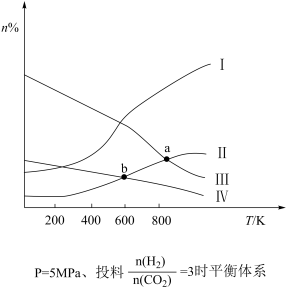
的物质的量之比为1∶3进行投料,发生反应 ,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表
,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表 。下列说法正确的是
。下列说法正确的是
 与
与 的物质的量之比为1∶3进行投料,发生反应
的物质的量之比为1∶3进行投料,发生反应 ,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表
,在5MPa下测得不同温度下平衡体系中各种气体物质的量分数(n%)如图所示,已知曲线Ⅰ代表 。下列说法正确的是
。下列说法正确的是
A.图中曲线交点a、b对应的平衡常数 |
B.图中曲线交点b对应的 转化率为40% 转化率为40% |
| C.平衡时,向体系中加入氢气,氢气转化率变大 |
D.若其他条件相同,甲为恒温恒容,乙为绝热恒容,达到平衡时 产率:甲>乙 产率:甲>乙 |
2022·河北·模拟预测 查看更多[6]
广东省广州市第二中学2022-2023学年高三 上学期(11月25日)周测化学试题湖南省怀化市沅陵县第二中学2021-2022学年高三下学期四月第一次调研考试化学试题江西省南昌市第二中学2022-2023学年高三上学期第四次考试化学试题天津市第二十五中学2022 -2023学年高二上学期期中考试化学试题(已下线)2022年湖南卷高考真题变式题(11-14)(已下线)2022年河北省新高考测评卷(七)
更新时间:2022-03-24 20:22:32
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在一密闭容器中,可逆反应:aA(g) + bB(g)  cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
 cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是
cC(g)达平衡后,测得此时C的浓度为0.6 mol/L。若保持温度不变,将容器的容积压缩为原来的2/3,当重新达平衡后,C的浓度是0.8 mol/L。下列说法正确的是| A.a + b > c | B.平衡向正反应方向移动 |
| C.物质A的转化率降低 | D.物质C的质量分数增加 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】 催化加氢合成乙烯的热化学方程式为
催化加氢合成乙烯的热化学方程式为
 ,原料初始组成
,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数
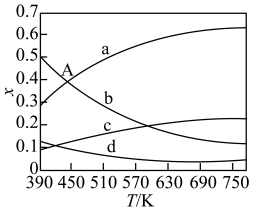
,反应达到平衡时,四种组分的物质的量分数 随温度
随温度 的变化如图所示。注:
的变化如图所示。注: 以分压表示,分压
以分压表示,分压 总压
总压 物质的量分数
物质的量分数
下列说法错误的是
 催化加氢合成乙烯的热化学方程式为
催化加氢合成乙烯的热化学方程式为
 ,原料初始组成
,原料初始组成 ,在体系压强为
,在体系压强为 ,反应达到平衡时,四种组分的物质的量分数
,反应达到平衡时,四种组分的物质的量分数 随温度
随温度 的变化如图所示。注:
的变化如图所示。注: 以分压表示,分压
以分压表示,分压 总压
总压 物质的量分数
物质的量分数
下列说法错误的是
A.当反应达到平衡时,若其它条件不变,增大压强,则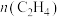 变大 变大 |
B.表示 、 、 变化的曲线分别是d、c, 变化的曲线分别是d、c, |
C.点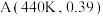 对应温度下,反应的平衡常数 对应温度下,反应的平衡常数 (单位已省略) (单位已省略) |
| D.反应往往伴随副反应,一定温度和压强条件下,为了提高反应速率和乙烯选择性,应当选择对生成乙烯反应催化活性更高的催化剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】向一恒容密闭容器中加入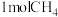 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比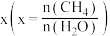 随温度的变化曲线如图所示。下列说法错误的是
随温度的变化曲线如图所示。下列说法错误的是
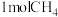 和一定量的
和一定量的 ,发生反应:
,发生反应: 。
。 的平衡转化率按不同投料比
的平衡转化率按不同投料比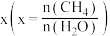 随温度的变化曲线如图所示。下列说法错误的是
随温度的变化曲线如图所示。下列说法错误的是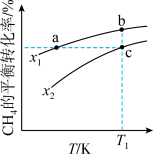
A.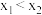 |
B.反应速率: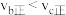 |
C.点a、b、c对应的平衡常数: |
D.反应温度为 ,当容器内压强不变时,反应达到平衡状态 ,当容器内压强不变时,反应达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】异丁醇催化脱水制备异丁烯主要涉及以下2个反应。研究一定压强下不同含水量的异丁醇在恒压反应器中的脱水反应,得到了异丁烯的平衡产率随温度的变化结果如图。
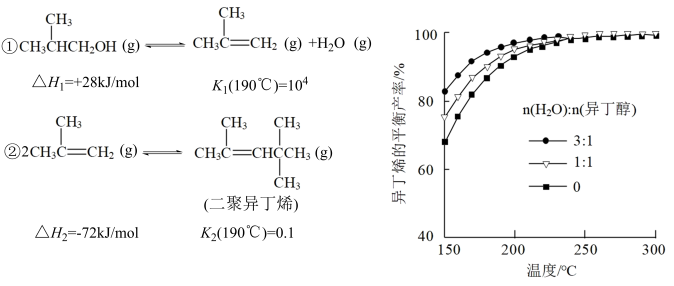
| A.其他条件不变时,在催化剂的活性温度内,升高温度有利于异丁烯的制备 |
B.高于190℃时,温度对异丁烯的平衡产率影响不大的原因是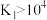 、 、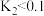 |
C.190℃时,增大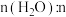 (异丁醇),不利于反应②的进行 (异丁醇),不利于反应②的进行 |
D.若只有异丁烯、水和二聚异丁烯生成,则初始物质浓度 与流出物质浓度c之间存在: 与流出物质浓度c之间存在: (异丁醇)=c(异丁烯)+2c(二聚异丁烯) (异丁醇)=c(异丁烯)+2c(二聚异丁烯) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】二甲醚催化制备乙醇主要涉及以下两个反应:
反应I: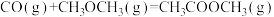

反应II: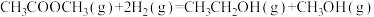
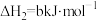
反应I、II的平衡常数的对数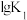 、
、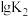 与温度的关系如图1所示:固定
与温度的关系如图1所示:固定 、
、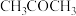 、
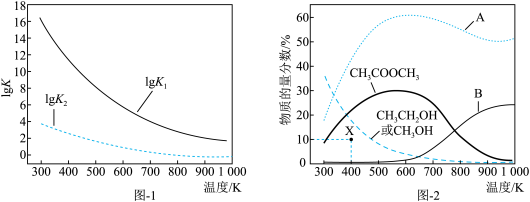
、 的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
反应I:
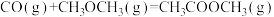

反应II:
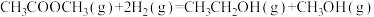
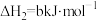
反应I、II的平衡常数的对数
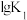 、
、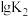 与温度的关系如图1所示:固定
与温度的关系如图1所示:固定 、
、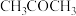 、
、 的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
的原料比、体系压强不变的条件下,同时发生反应I、II,平衡时各物质的物质的量分数随温度的变化如图2所示。下列说法正确的是
A. |
B.测得X点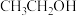 的物质的量分数是10%,则X点反应II有: 的物质的量分数是10%,则X点反应II有: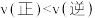 |
C.由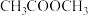 的曲线知,600K后升高温度对反应I的影响程度小于对反应II的影响程度 的曲线知,600K后升高温度对反应I的影响程度小于对反应II的影响程度 |
D.曲线A表示 的物质的量分数随温度的变化 的物质的量分数随温度的变化 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】羰基硫(COS)可作为一种粮食熏蒸剂,能防止某些昆虫、线虫和真菌的危害。在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡: CO(g)+H2S(g) COS(g)+H2(g) ,K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g) ,K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
 COS(g)+H2(g) ,K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是
COS(g)+H2(g) ,K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是| A.升高温度,H2S浓度增加,表明该反应的△H>0 |
| B.随着反应的进行,混合气体的密度逐渐减小 |
| C.反应前H2S物质的量为7mol |
| D.CO的平衡转化率为80% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】相同温度下体积均为2L的两个恒容容器中发生可逆反应:2SO2(g)+O2(g) 2SO3(g) △H=-196kJ·mol-1,实验测得有关数据如下表:
2SO3(g) △H=-196kJ·mol-1,实验测得有关数据如下表:
下列叙述不正确的是
 2SO3(g) △H=-196kJ·mol-1,实验测得有关数据如下表:
2SO3(g) △H=-196kJ·mol-1,实验测得有关数据如下表:| 容器编号 | 起始时各物质物质的量/mol | 达平衡时体系能量的变化 | ||
| SO2 | O2 | SO3 | ||
| ① | 2 | 1 | 0 | 放热156.8 kJ |
| ② | 0.6 | 0.3 | 1.4 | Q(Q>0) |
| A.容器①中达到平衡时,O2的转化率为80% |
| B.Q=19.6kJ |
| C.容器①、②中反应的平衡常数相等,K=80 |
| D.相同温度下,起始时向容器中充入0.8 mol SO2、0.4 mol O2和3.2 mol SO3,反应达到平衡前v(正)>v(逆) |
您最近一年使用:0次

 xC(g)+D(s)
xC(g)+D(s)
 的密闭容器中充入一定量
的密闭容器中充入一定量 ,发生反应
,发生反应
 。若在
。若在 时,通入
时,通入 ,
, 时达到平衡状态;
时达到平衡状态;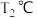 时,通入
时,通入 ,
, 时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。
时达到平衡状态。已知反应过程中有关物质的物质的量随时间的变化曲线如图所示。

 的平均反应速率为
的平均反应速率为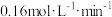
 的平衡转化率约为
的平衡转化率约为