据《科学》报道,中国科学家首次实现超导体(Bi2Te3/NBSe2)中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为___________ 。基态Se原子核外电子云轮廓图呈哑铃形的能级上共有___________ 个电子。
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子( )的平面结构简式如图所示:
)的平面结构简式如图所示:
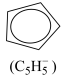
①C、H、Cl的电负性由大到小的顺序为___________ 。
② 中C原子的杂化类型是
中C原子的杂化类型是___________ 。
③已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为___________ 。
(3) 的空间构型为
的空间构型为___________ 。
(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为___________ 。
(1)Bi与P位于同主族,基态P原子的价层电子排布式为
(2)二氯二茂铌的组成为(C5H5)2NbCl2.环戊二烯阴离子(
 )的平面结构简式如图所示:
)的平面结构简式如图所示:
①C、H、Cl的电负性由大到小的顺序为
②
 中C原子的杂化类型是
中C原子的杂化类型是③已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为(3)
 的空间构型为
的空间构型为(4)四氟化铌(NbF4)的熔点为72℃,它的晶体类型为
更新时间:2022-03-25 17:55:27
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】写出下列元素基态原子的电子排布式:
(1)N_______ 。
(2)Ca_______ 。
(3)26Fe_______ 。
(1)N
(2)Ca
(3)26Fe
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】基态 原子的价电子排布式为
原子的价电子排布式为______ , 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为______ 。
 原子的价电子排布式为
原子的价电子排布式为 、
、 、
、 的沸点由高到低的顺序依次为
的沸点由高到低的顺序依次为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】铁氮化合物(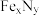 )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某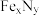 的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。
(1) 基态核外电子排布式为
基态核外电子排布式为_______ 。
(2)丙酮(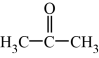 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是_______ ,1mol丙酮分子中含有σ键的数目为______________ 。
(3)C、H、O三种元素的电负性由小到大的顺序为_____ 。
(4)乙醇的沸点高于丙酮,这是因为_______ 。
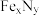 )在磁记录材料领域有着广泛的应用前景。某
)在磁记录材料领域有着广泛的应用前景。某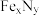 的制备需铁、氮气、丙酮和乙醇参与。
的制备需铁、氮气、丙酮和乙醇参与。(1)
 基态核外电子排布式为
基态核外电子排布式为(2)丙酮(
 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(3)C、H、O三种元素的电负性由小到大的顺序为
(4)乙醇的沸点高于丙酮,这是因为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】许多元素及它们的化合物在科学研究和工业生产中具有许多用途,请回答下列有关问题:
(1)某同学画出基态碳原子的核外电子排布图: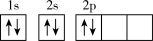 ,该电子排布图违背了
,该电子排布图违背了_______ ;CH 、-CH3、CH
、-CH3、CH 都是重要的有机反应中间体,CH
都是重要的有机反应中间体,CH 的VSEPR模型为
的VSEPR模型为_______ 。
(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为___________ 。
(3)基态溴原子的价层电子排布图为________ ,用价层电子对互斥理论推断SnBr2分子中Sn—Br的键角___________ 120°(填“>”、“<”或“=”)。
(4)CN-能与多种金属离子形成配合物,例如,工业冶炼金的原理:2[Zn(CN)2]-+Zn=2Au+[Zn(CN)4]2-。与CN-互为等电子体的分子有___________ (只写一种),1mol[Zn(CN)4]2-中含_____ molσ键。
(5)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是___________ 。
(1)某同学画出基态碳原子的核外电子排布图:
 ,该电子排布图违背了
,该电子排布图违背了 、-CH3、CH
、-CH3、CH 都是重要的有机反应中间体,CH
都是重要的有机反应中间体,CH 的VSEPR模型为
的VSEPR模型为(2)CH4中共用电子对偏向C,SiH4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为
(3)基态溴原子的价层电子排布图为
(4)CN-能与多种金属离子形成配合物,例如,工业冶炼金的原理:2[Zn(CN)2]-+Zn=2Au+[Zn(CN)4]2-。与CN-互为等电子体的分子有
(5)类卤素(SCN)2对应的酸有两种,理论上硫氰酸(H-S-C≡N)的沸点低于异硫氰酸(H-N=C=S)的沸点,其原因是
您最近一年使用:0次
【推荐3】N、P两种元素位于元素周期表第VA族。请回答下列问题:
(1)基态氮原子的电子排布式为________ ;基态氮原子的价层电子的轨道表示式为________ 。
(2)基态磷原子中,其占据的最高能层的符号是________ ;基态磷原子占据的最高能级共有________ 个原子轨道,其形状是________ 。
(3)电负性:N________ P(填>或<)。
(4)雷酸汞曾被用作起爆药,雷酸汞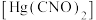 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为________ >________ >________ (填元素符号)。
(1)基态氮原子的电子排布式为
(2)基态磷原子中,其占据的最高能层的符号是
(3)电负性:N
(4)雷酸汞曾被用作起爆药,雷酸汞
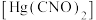 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】元素X和Y属于同一主族。负二价的元素X和氢形成的化合物在通常状况下是一种液体,其中X的质量分数约为88.9%;元素X和元素Y可以形成两种化合物,在这两种化合物中,X的质量分数分别为50%和60%。
(1)写出基态Y原子的电子排布式:___________ 。
(2)在X和Y两种元素形成的化合物中:
①X的质量分数为50%的化合物的化学式为___________ ;该分子的中心原子发生___________ 杂化,分子构型为___________ 。
②X的质量分数为60%的化合物的化学式为___________ ;该分子的中心原子发生___________ 杂化,分子构型为___________ 。
(3)由元素X、Y和氢三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式___________ 、___________ ,两种酸的阴离子分别为___________ 和___________ ,其立体构型分别为___________ 和___________ 。
(4)在由氢元素与X元素形成的化合物中,含有非极性键的是___________ (写分子式),分子构型为V形的是___________ (写分子式)。
(1)写出基态Y原子的电子排布式:
(2)在X和Y两种元素形成的化合物中:
①X的质量分数为50%的化合物的化学式为
②X的质量分数为60%的化合物的化学式为
(3)由元素X、Y和氢三种元素形成的化合物常见的有两种,其水溶液均呈酸性,试分别写出其分子式
(4)在由氢元素与X元素形成的化合物中,含有非极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】元素As与N同族。预测As的氢化物分子的立体结构为___________ ,其沸点比NH3的___________ (填“高”或“低”),其判断理由是___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】回答下列问题。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2___________ ;AlBr3(共价分子)___________ 。
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:
平面形分子___________ ,三角锥形分子___________ ,四面体形分子___________ 。
(1)利用VSEPR模型推断分子或离子的立体构型。
CS2
(2)有两种活性反应中间体微粒,它们的微粒中均含有1个碳原子和3个氢原子。请依据下面给出的这两种微粒的球棍模型,写出相应的化学式:

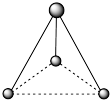
平面形分子
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是_____ 。
(2)立方BN和立方AlN均为共价晶体,结构相似,BN的熔点高于AlN的原因为_____ 。
(3)我国科学家研制成功的一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。Cd与Zn位于同一副族,且Cd在Zn的下一周期。已知ZnS熔点为2830℃、CdS熔点为1750℃、ZnS熔点更高的原因为______ 。
(4)“掺杂”能够提高电极的电导率和结构稳定性。MgF2是常用的掺杂剂,其熔点高于MgCl2的原因为______ 。
(5)Co及与其同周期同族的两种元素的二价氧化物的晶体类型相同,其熔点由高到低的顺序为_____ (用化学式表示)。
(6)PbF4的熔点显著高于PbCl4的原因是_____ 。
(1)CuSO4的熔点为560℃,Cu(NO3)2的熔点为115℃,CuSO4熔点更高的原因是
(2)立方BN和立方AlN均为共价晶体,结构相似,BN的熔点高于AlN的原因为
(3)我国科学家研制成功的一种纳米半导体材料可以高效实现光化学转换,该种材料主要成分为硫化镉和硫化锌。Cd与Zn位于同一副族,且Cd在Zn的下一周期。已知ZnS熔点为2830℃、CdS熔点为1750℃、ZnS熔点更高的原因为
(4)“掺杂”能够提高电极的电导率和结构稳定性。MgF2是常用的掺杂剂,其熔点高于MgCl2的原因为
(5)Co及与其同周期同族的两种元素的二价氧化物的晶体类型相同,其熔点由高到低的顺序为
(6)PbF4的熔点显著高于PbCl4的原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】20世纪前,人们以为_____________ 是所有化学物质能够保持其性质的最小粒子,物质固、液、气三态的相互转化只是_____________ 距离发生了变化。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】常见的典型分子晶体
(1)所有_____________ :如H2O、H2S、NH3、CH4、HX(卤化氢)等。
(2)部分_____________ :如X2(卤素单质)、O2、H2、S8、P4、C60、稀有气体等。
(3)部分_____________ :如CO2、SO2、NO2、P4O6、P4O10等。
(4)几乎所有的_____________ :如H2SO4、HNO3、H3PO4、H2SiO3等。
(5)绝大多数_____________ :如苯、四氯化碳、乙醇、冰醋酸、蔗糖等。
(1)所有
(2)部分
(3)部分
(4)几乎所有的
(5)绝大多数
您最近一年使用:0次



