Ⅰ.铁是地壳中含量第二位的金属元素,其单质、合金及众多的化合物在生产生活中都有广泛的应用,请回答下问题:
(1)写出铁元素在周期表中的位置:_____ ;写出Fe2+的价电子排布式_____ 。
(2)某种铁的化合物俗称“绿矾”,化学式为FeSO4•7H2O,“绿矾”中SO 的空间构型为
的空间构型为____ (用文字描述),其中S的杂化轨道类型为_____ 。
Ⅱ.铁能形成多种配合物,其中一种配合物Fe(CO)5的熔点为-20℃,沸点为103℃,可用于制备纯铁,请回答下列问题:
(3)Fe(CO)5晶体类型属于____ 晶体,配体为:____ 。
(4)价电子数和原子数相同的分子、离子或原子团互称为等电子体,往往具有相似的化学键和构型,请写出与CO互为等电子体的一种阴离子的电子式:____ 。
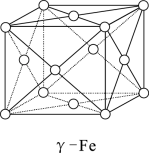
(5)γ—Fe晶体的晶胞为立方晶胞,结构如图所示,其晶胞边长为apm,则γ—Fe单质的密度为____ g/cm3(设NA为阿伏加德罗常数的值,列出算式即可)
(1)写出铁元素在周期表中的位置:
(2)某种铁的化合物俗称“绿矾”,化学式为FeSO4•7H2O,“绿矾”中SO
 的空间构型为
的空间构型为Ⅱ.铁能形成多种配合物,其中一种配合物Fe(CO)5的熔点为-20℃,沸点为103℃,可用于制备纯铁,请回答下列问题:
(3)Fe(CO)5晶体类型属于
(4)价电子数和原子数相同的分子、离子或原子团互称为等电子体,往往具有相似的化学键和构型,请写出与CO互为等电子体的一种阴离子的电子式:
(5)γ—Fe晶体的晶胞为立方晶胞,结构如图所示,其晶胞边长为apm,则γ—Fe单质的密度为

更新时间:2022-04-18 21:07:31
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】氮、磷、钾是农作物生长的必须营养元素,磷和钙都是促成骨骼和牙齿的钙化不可缺少的营养元素。回答下列问题:
(1)基态K的核外电子排布式为____________ ,基态N的价电子排布图为____________ 。
(2)元素的第一电离能:Ca________ (填“>”或“<”)P。
(3)白磷P4在CS2中的溶解度________ (填“大于”或“小于”)在水中的溶解度,N4是氮的一种新型单质,若N4分子结构类似于白磷P4,则N的杂化方式为________ 。
(4)下表是几种碳酸盐的热分解温度和阳离子半径:
根据上表数据分析碳酸钡分解温度最高的原因是_______________________
(5)常温下PCl5是一种白色晶体,晶体结构为氯化铯型,由A、B两种离子构成。已知A、B两种离子分别与CCl4、SF6互为等电子体,则A、B两种离子的符号分别为________ 、________ 。
(6)用晶体的X射线衍射法可以测得阿伏加 德罗常数的值。已知金属钙的晶胞为面心立方(如图)晶胞,晶胞边长为d pm;又知钙的密度为ρ g/cm3,则一个钙晶胞的质量为________ (用d、ρ表示,下同)g,阿伏加 德罗常数的值为______________ (化成最简式)。

(1)基态K的核外电子排布式为
(2)元素的第一电离能:Ca
(3)白磷P4在CS2中的溶解度
(4)下表是几种碳酸盐的热分解温度和阳离子半径:
| 碳酸盐 | CaCO3 | SrCO3 | BaCO3 |
| 热分解温度/℃ | 900 | 1172 | 1360 |
| 阳离子半径/pm | 99 | 112 | 135 |
根据上表数据分析碳酸钡分解温度最高的原因是
(5)常温下PCl5是一种白色晶体,晶体结构为氯化铯型,由A、B两种离子构成。已知A、B两种离子分别与CCl4、SF6互为等电子体,则A、B两种离子的符号分别为
(6)用晶体的X射线衍射法可以测得阿伏加 德罗常数的值。已知金属钙的晶胞为面心立方(如图)晶胞,晶胞边长为d pm;又知钙的密度为ρ g/cm3,则一个钙晶胞的质量为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】【化学—选修3:物质结构与性质】A、B、C、D、E、F均属前四周期且原子序数依次增大的六种元素,其中A、B、C是同一周期相邻的三种元素,C的氢化物水溶液呈碱性;D的基态原子3p轨道上有3个未成对电子;E、F为副族元素,4s能级均只有一个电子。回答下列问题:
(1)A、B、C三种元素按电负性由小到大的顺序是_________ (用元素符号表示)。
(2)B与氧原子能形成四原子阴离子,其中B的杂化方式为_____________ ;C的三氯化物分子的立体构型为____________________________________ 。
(3)任写一种与BC—离子互为等电子体的离子__________________ (写出化学式)。
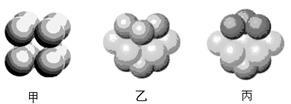
(4)F原子的外围电子排布式为_____________ ,F晶体中原子的堆积方式是下图中的_________ (填写“甲”、“乙”或“丙”)。
(5)E的离子可以形成多种配合物,将ECl3溶液蒸发浓缩,析出深绿色晶体。该晶体中E3+、Cl—、H2O的物质的量之比为1∶3∶6,且E的配位数为6。向1.0mol该晶体的溶液中加入足量AgNO3溶液产生143.5g白色沉淀,则该配合物的化学式为__________________________ 。
(6)AD是一种耐磨材料,其结构与金刚石相似,下图为其晶体结构单元,它可由A的三溴化物和D的三溴化物于高温下在氢气的氛围中合成。

①写出合成AD的化学方程式:________________________ 。
②已知晶体中A与D原子的最近距离为a pm,则该晶体密度的表达式为_________ g/cm3。(不需化简,阿伏加德罗常数为NA)
(1)A、B、C三种元素按电负性由小到大的顺序是
(2)B与氧原子能形成四原子阴离子,其中B的杂化方式为
(3)任写一种与BC—离子互为等电子体的离子
(4)F原子的外围电子排布式为

(5)E的离子可以形成多种配合物,将ECl3溶液蒸发浓缩,析出深绿色晶体。该晶体中E3+、Cl—、H2O的物质的量之比为1∶3∶6,且E的配位数为6。向1.0mol该晶体的溶液中加入足量AgNO3溶液产生143.5g白色沉淀,则该配合物的化学式为
(6)AD是一种耐磨材料,其结构与金刚石相似,下图为其晶体结构单元,它可由A的三溴化物和D的三溴化物于高温下在氢气的氛围中合成。

①写出合成AD的化学方程式:
②已知晶体中A与D原子的最近距离为a pm,则该晶体密度的表达式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】可以由下列反应合成三聚氰胺:CaO+3C CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[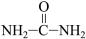 ],尿素合成三聚氰胺。
],尿素合成三聚氰胺。
(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:____________________________ ;CaCN2中阴离子为CN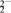 ,与CN22-互为等电子体的分子有CO2和
,与CN22-互为等电子体的分子有CO2和________ (填化学式),由此可以推知CN22-的空间构型为_______ 。
(2)尿素分子中C原子采取________ 杂化。
(3)三聚氰胺(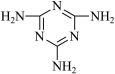 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (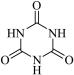 )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过__________ 结合,在肾脏内易形成结石。
(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为________ ,Ca2+采取的堆积方式为____________________________ ,每个Ca2+周围距离最近且相等的Ca2+有________ 个。
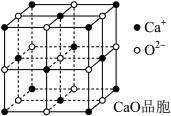
(5)CaO晶体和MgO晶体的晶格能分别为:CaO 3401 kJ·mol-1、MgO 3916 kJ·mol-1。导致两者晶格能差异的主要原因是___________________________________ 。
(6)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n=______________
 CaC2+CO↑,CaC2+N2
CaC2+CO↑,CaC2+N2 CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[
CaCN2+C,CaCN2+2H2O===NH2CN+Ca(OH)2,NH2CN与水反应生成尿素[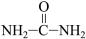 ],尿素合成三聚氰胺。
],尿素合成三聚氰胺。(1)写出与Ca在同一周期且最外层电子数相同、内层排满电子的基态原子的电子排布式:
 ,与CN22-互为等电子体的分子有CO2和
,与CN22-互为等电子体的分子有CO2和(2)尿素分子中C原子采取
(3)三聚氰胺(
 )俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 (
)俗称“蛋白精”。动物摄入三聚氰胺和三聚氰酸 ( )后,三聚氰酸与三聚氰胺分子相互之间通过
)后,三聚氰酸与三聚氰胺分子相互之间通过(4)CaO晶胞如图所示,CaO晶体中Ca2+的配位数为

(5)CaO晶体和MgO晶体的晶格能分别为:CaO 3401 kJ·mol-1、MgO 3916 kJ·mol-1。导致两者晶格能差异的主要原因是
(6)配位化合物K3[Fe(CN)n]遇亚铁离子会产生蓝色沉淀,因此可用于检验亚铁离子,已知铁原子的最外层电子数和配体提供电子数之和为14,求n=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(物质结构与性质)
Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素D的基态原子电子排布式___________________ 。
(2)元素A、B形成的单质中,______ 对应的单质熔点更高,原因是_________________ 。
(3)写出C的最高价氧化物的水化物与B的最高价氧化物的水化物反应的化学方程式_______________ 。
(4)元素D可以形成化学式为D(NH3)5BrSO4,配位数均为6的两种配合物。若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为____________ 。
Ⅱ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。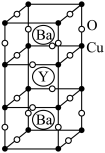
(5)根据图示晶胞结构,推算晶体中Y,Ba,Cu和O原子个数比,确定其化学式为________ 。
Ⅲ.BF3与一定量的水形成晶体Q [(H2O)2·BF3],Q在一定条件下可转化为R:
(6)晶体Q中各种微粒间的作用力不涉及________ (填字母)。
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
(7)R中阳离子的空间构型为________ ,阴离子的中心原子轨道采用_____ 杂化。
Ⅰ.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。

试回答下列问题:
(1)请写出元素D的基态原子电子排布式
(2)元素A、B形成的单质中,
(3)写出C的最高价氧化物的水化物与B的最高价氧化物的水化物反应的化学方程式
(4)元素D可以形成化学式为D(NH3)5BrSO4,配位数均为6的两种配合物。若往其中一种配合物的溶液中加入BaCl2溶液时,无明显现象,若加入AgNO3溶液时,产生淡黄色沉淀,则该配合物的化学式为
Ⅱ.钇钡铜氧的晶胞结构如图。研究发现,此高温超导体中的铜元素有两种价态:+2价和+3价。

(5)根据图示晶胞结构,推算晶体中Y,Ba,Cu和O原子个数比,确定其化学式为
Ⅲ.BF3与一定量的水形成晶体Q [(H2O)2·BF3],Q在一定条件下可转化为R:

(6)晶体Q中各种微粒间的作用力不涉及
a.离子键
b.共价键
c.配位键
d.金属键
e.氢键
f.范德华力
(7)R中阳离子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】2019年1月3日,中国“嫦娥四号”探测器成功着陆在月球背面的预选着陆区,实现了人类探测器首次月被软着陆。“嫦娥四号”降落月球时的第一眼画面,由探测器搭载的降落相机拍摄。这个降落相机镜筒由钛合金制作。回答下列问题:
(1)Ti(BH4)2是一种储氢材料。
①基态Ti2+的价电子排布图(轨道表达式)为__________ ;钛元素位于周期表的_______ 区。
②BH4-的空间构型是_______________ ,B原子的杂化方式___________ 。
③BH4-中,含有___________ (填标号)。
a.σ键b.π键c.氢键d.配位键e.离子键
(2)与钛同周期的ⅡB族和ⅢA族两种元素中第一电离能较大的是___________ (写元素符号),原因是_________________________________ 。
(3)—种以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:在高温下,向金红石与焦炭的泡合物中通入Cl2,得到TiCl4和一种可燃性气体;然后在稀有气体氛围和加热的条件下,用镁与TiCl4反应可得到钛。
①请写出上述制备过程的化学方程式:___________________ 、_________________ 。
②中间产物TiCl4是一种洛剂,常温下呈液态,分子结构与CCl4相似,也能与CCl4均匀混合,请解释TiCl4与CCl4均匀混合的原因:_____________________________ 。
(4)单质钛与单质Zn、Mg的堆积方式相同,这种堆积方式称为:__________________ 。若钛原子半径为rpm,NA表示阿伏伽德罗常数的值,钛的密度为___________ g•cm-3(列出计算式)
(1)Ti(BH4)2是一种储氢材料。
①基态Ti2+的价电子排布图(轨道表达式)为
②BH4-的空间构型是
③BH4-中,含有
a.σ键b.π键c.氢键d.配位键e.离子键
(2)与钛同周期的ⅡB族和ⅢA族两种元素中第一电离能较大的是
(3)—种以金红石(主要成分TiO2)为原料生产金属钛的步骤主要有:在高温下,向金红石与焦炭的泡合物中通入Cl2,得到TiCl4和一种可燃性气体;然后在稀有气体氛围和加热的条件下,用镁与TiCl4反应可得到钛。
①请写出上述制备过程的化学方程式:
②中间产物TiCl4是一种洛剂,常温下呈液态,分子结构与CCl4相似,也能与CCl4均匀混合,请解释TiCl4与CCl4均匀混合的原因:
(4)单质钛与单质Zn、Mg的堆积方式相同,这种堆积方式称为:
您最近一年使用:0次
【推荐3】回答下列问题
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为___________ ,电负性O___________ F;其中氧原子的杂化方式为___________ 。
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。 空间结构是
空间结构是___________ ;X与Z形成化合物中含有的化学键是___________ 。
(3) 的空间结构为
的空间结构为___________ 。(用文字描述,下同): 的空间结构是
的空间结构是___________ 。
(4)在BF3分子中: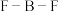 的键角是
的键角是___________ ,B原子的杂化轨道类型为___________ ,BF3和过量NaF作用可生成NaBF4, 的空间结构为
的空间结构为___________ 。
(5)钠在火焰上灼烧产生的黄光是一种___________ (填字母)。
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为___________ ;其中π键与σ键的个数比为___________ 。
(7)基态S原子价电子排布式___________ ;S原子的核外电子运动状态有___________ 种,空间运动状态有___________ 种:能量最高的轨道的电子云的形状是___________ 。
(1)F2通入稀NaOH溶液中可生成OF2,OF2空间结构为
(2)X、Y、Z为短周期元素且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成NH3;Z基态原子的M层与K层电子数相等。
 空间结构是
空间结构是(3)
 的空间结构为
的空间结构为 的空间结构是
的空间结构是(4)在BF3分子中:
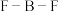 的键角是
的键角是 的空间结构为
的空间结构为(5)钠在火焰上灼烧产生的黄光是一种
A.吸收光谱 B.发射光谱
(6)已知(CN)2是直线形分子,且有对称性,则(CN)2分子的结构式为
(7)基态S原子价电子排布式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】向盛有硫酸铜溶液的试管中滴加氨水,先生成蓝色难溶物,继续滴加氨水,难溶物溶解,得到深蓝色透明溶液。
(1)下列对此现象的说法正确的是___________(填序号)。
(2)写出实验过程中的离子方程式:
①___________ ②___________
(3)铜可以形成一种离子化合物 ,若要确定
,若要确定 是晶体还是非晶体,最科学的方法是对其进行
是晶体还是非晶体,最科学的方法是对其进行___________ 实验,该化合物的中心离子是___________ ;阴离子的空间构型是___________ ,该化合物加热时首先失去的组分是 ,原因是
,原因是___________ 。
(1)下列对此现象的说法正确的是___________(填序号)。
A.反应后溶液中不存在任何沉淀,所以反应前后 的浓度不变 的浓度不变 |
B.沉淀溶解后,生成深蓝色的配离子 |
C.在 中, 中, 提供孤电子对, 提供孤电子对, 中的N原子提供空轨道 中的N原子提供空轨道 |
D.向反应后的溶液中加入乙醇,溶液没有发生变化,因为 不会与乙醇发生反应 不会与乙醇发生反应 |
①
(3)铜可以形成一种离子化合物
 ,若要确定
,若要确定 是晶体还是非晶体,最科学的方法是对其进行
是晶体还是非晶体,最科学的方法是对其进行 ,原因是
,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铜铟硒太阳能电池是多元化合物太阳能电池中的一种。其中的Cu(In,Ga)Se2是一种性能优良的太阳光吸收材料。回答下列问题:
(1)基态Se原子价电子的轨道排布图为___________ ,第四周期元素的基态原子中,未成对电子数与基态铜原子相同且位于P区的元素有___________ (填原子符号)。
(2)向CuSO4溶液中逐滴加入过量浓氨水,得到深蓝色溶液,向深蓝色溶液中通入SO2,至溶液呈微酸性时,Cu2+被还原并生成白色沉淀和(NH4)2SO4。化学分析表明白色沉淀中含五种元素,且白色沉淀晶体里有分别呈三角锥形和四面体形的两种离子。深蓝色溶液中阳离子的结构为___________ (标出其中的配位键),白色沉淀的晶体中这两种离子的化学式为___________ 。
(3)在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离域π键,或大π键。下列微粒中存在离域π键的是___________ (填序号)。
① ②H2Se ③SeO2 ④H3BO3
②H2Se ③SeO2 ④H3BO3
(4)P与Cu、Ge形成的一种化合物也是一种光伏材料,其晶胞结构如图所示(P都在晶胞内)。该晶胞的底面边长为a pm,高为b pm。
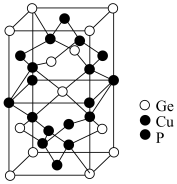
①该化合物的化学式为___________ (最简式)。晶体中与Cu原子距离最近的P原子的数目为___________ 。
②设化合物的最简式的式量为M,晶体的密度为___________ g/cm3 (列出算式,NA为阿伏加德罗常数的值)。
(1)基态Se原子价电子的轨道排布图为
(2)向CuSO4溶液中逐滴加入过量浓氨水,得到深蓝色溶液,向深蓝色溶液中通入SO2,至溶液呈微酸性时,Cu2+被还原并生成白色沉淀和(NH4)2SO4。化学分析表明白色沉淀中含五种元素,且白色沉淀晶体里有分别呈三角锥形和四面体形的两种离子。深蓝色溶液中阳离子的结构为
(3)在多原子分子中如有相互平行的p轨道,它们连贯重叠在一起构成一个整体,p电子在多个原子间运动形成π型化学键,这种不局限在两个原子之间的π键称为离域π键,或大π键。下列微粒中存在离域π键的是
①
 ②H2Se ③SeO2 ④H3BO3
②H2Se ③SeO2 ④H3BO3(4)P与Cu、Ge形成的一种化合物也是一种光伏材料,其晶胞结构如图所示(P都在晶胞内)。该晶胞的底面边长为a pm,高为b pm。

①该化合物的化学式为
②设化合物的最简式的式量为M,晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】乙二胺(H2NCH2CH2NH2)能与硫酸铜溶液反应形成一种紫色的溶液,其溶质为配合物[Cu(en)2(H2O)2] SO4,其中的en为乙二胺分子,该配合物中N原子均与Cu2+形成了配位键。回答下列问题:
(1)基态二价铜离子的外围电子排布式为____ 。
(2)该配合物中Cu2+的配位数为____ ,配体中所有元素电负性由强到弱排列的顺序是____ 。
(3) [Cu(en)2(H2O)2]2+最可能的空间构型为____ (填正确答案标号)。
A.平面正方形B.平面六边形C.四面体形D.八面体形
(4)1 mol [Cu(en)2(H2O)2]2+中所含共价键的个数是____ ,乙二胺分子中N原子和C原子的杂化方式分别为____ 、____ 。
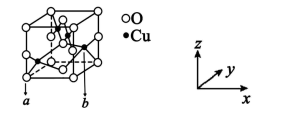
(5)已知铜的某种氧化物晶胞结构如下图所示,该晶体熔点1 326℃,熔化状态下能够导电。
①该铜的氧化物的化学式为____ ;
②已知a点的坐标参数为(0,0,0),则b点的坐标参数为____ ;
③若Cu2+与O2-最短核间距为npm,则该晶体的密度为______ g ▪cm-3(阿伏加德罗常数用NA表示)。
(1)基态二价铜离子的外围电子排布式为
(2)该配合物中Cu2+的配位数为
(3) [Cu(en)2(H2O)2]2+最可能的空间构型为
A.平面正方形B.平面六边形C.四面体形D.八面体形
(4)1 mol [Cu(en)2(H2O)2]2+中所含共价键的个数是
(5)已知铜的某种氧化物晶胞结构如下图所示,该晶体熔点1 326℃,熔化状态下能够导电。
①该铜的氧化物的化学式为
②已知a点的坐标参数为(0,0,0),则b点的坐标参数为
③若Cu2+与O2-最短核间距为npm,则该晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
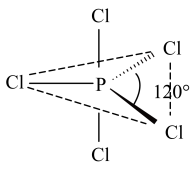
【推荐1】白磷(P4)是磷的单质之一,与卤素单质反应生成卤化磷。卤化磷通常有三卤化磷和五卤化磷(PCl5分子结构如图所示,其中Cl原子有两种不同位置)。回答下列问题:_____ 。P、S、Cl的第一电离能由小到大顺序为_____ 。
(2)PCl5水解产生一种无色油状中间产物POCl3,该分子的空间结构为_____ 。
(3)PCl5中P的轨道杂化类型为_____(填字母标号)。
(4)三卤化磷的熔点见下表,分析变化趋势及原因是_____ 。
(5)PCl5晶体呈CsCl(晶胞结构如下图)型构造,其中含有等量的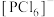 和正四面体形的
和正四面体形的_____ (填化学式),两者之间形成_____ 键。晶胞中含有的P原子的个数为_____ 。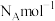 ,则该晶体密度为
,则该晶体密度为_____  (用含NA、a的式子表示)。
(用含NA、a的式子表示)。
(2)PCl5水解产生一种无色油状中间产物POCl3,该分子的空间结构为
(3)PCl5中P的轨道杂化类型为_____(填字母标号)。
| A.sp3 | B.sp3d | C.d2sp3 | D.dsp2 |
| 三卤化磷 | PF3 | PCl3 | PBr3 | PI3 |
| 熔点/℃ | -151.5 | -93.6 | -41.5 | 61.2 |
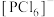 和正四面体形的
和正四面体形的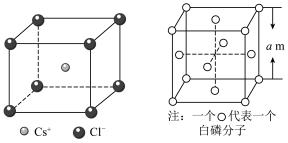
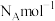 ,则该晶体密度为
,则该晶体密度为 (用含NA、a的式子表示)。
(用含NA、a的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】医学研究发现,人体中部分钛、镁等矿物质,可能会积匿在内脏中。砖家称该现象为“积匿钛镁”。铁作为人体所必需的元素之一,维持着人体的各种生命活动。回答以下问题:
(1)钛位于元素周期表的_______ 。
(2)在补铁时,人所摄入的铁(离子态)的基态价电子轨道表示式为_______ 。
(3)人体中积匿的镁(离子态)可用Kun醇(可表示为[iKun]OH)进行去除,Kun醇中羟基的中心原子杂化方式为_______ 。
(4) 与
与 、
、 反应可制取
反应可制取 ;
; 中
中 键占全部共价键的
键占全部共价键的_______ (填百分数)。 分子中正负电荷中心
分子中正负电荷中心_______ (填“重合”或“不重合”)。
(5)人体内可能形成图1所示的配合物。其配位数为_______ ,Ti的配位原子有_______ ,该配合物中_______ (填“存在”或“不存在”)氢键。
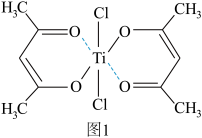
(6)图2是由Mg、Al与O形成的一种晶胞,其化学式为_______ , 所处的位置有
所处的位置有_______ 。

(1)钛位于元素周期表的
(2)在补铁时,人所摄入的铁(离子态)的基态价电子轨道表示式为
(3)人体中积匿的镁(离子态)可用Kun醇(可表示为[iKun]OH)进行去除,Kun醇中羟基的中心原子杂化方式为
(4)
 与
与 、
、 反应可制取
反应可制取 ;
; 中
中 键占全部共价键的
键占全部共价键的 分子中正负电荷中心
分子中正负电荷中心(5)人体内可能形成图1所示的配合物。其配位数为

(6)图2是由Mg、Al与O形成的一种晶胞,其化学式为
 所处的位置有
所处的位置有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】M是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y的负一价离子的最外层电子数与次外层的相同。回答下列问题:
(1)单质M的晶体类型为_______ 。
(2)元素Y基态原子的核外电子排布式为_______ ,元素Y的含氧酸中,酸性最强的是_______ (写化学式),该酸根离子的立体构型为_______ 。
(3)M与Y形成的一种化合物的立方晶胞如图所示。
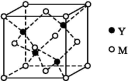
①已知晶胞参数a=0.542 nm,此晶体的密度为_______ g·cm-3。(写出计算式,不要求计算结果。设阿伏加德罗常数的值为NA)
②该化合物难溶于水但易溶于氨水,其原因是_______ 。
③此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为_______ 。
(1)单质M的晶体类型为
(2)元素Y基态原子的核外电子排布式为
(3)M与Y形成的一种化合物的立方晶胞如图所示。

①已知晶胞参数a=0.542 nm,此晶体的密度为
②该化合物难溶于水但易溶于氨水,其原因是
③此化合物的氨水溶液遇到空气则被氧化为深蓝色,深蓝色溶液中阳离子的化学式为
您最近一年使用:0次



