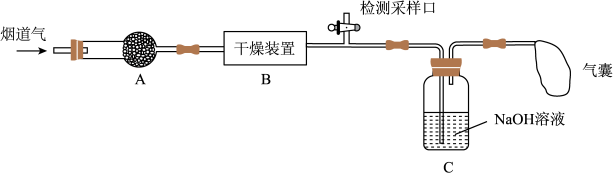
研究性学习小组对某工厂排出的烟道气(主要成分为NO、NO2、N2、粉尘和少量水蒸气)进行处理,实验装置如图:
已知:NO、NO2能与NaOH溶液发生如下反应:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+ NaNO3+H2O;但NO不能单独与NaOH溶液反应。
(1)实验时在装置A的干燥管中放置一团棉花,吸收粉尘。装置B的干燥装置中应盛放的试剂为____ (填字母)。
a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO4•5H2O)
(2)气体在被装置C中的NaOH溶液吸收前,需在检测采样口测定气体中NO和NO2的含量。为确保NO和NO2气体能够被NaOH溶液完全吸收,则需控制参加反应的NO和NO2物质的量比值为____ (填字母)。
a.≥1 b.=1 c.≤1
(3)若进入装置C的气体中NO和NO2物质的量比值不符合(2)中要求,则气囊中除含有N2外,可能含有少量NO气体。甲同学设计了喷淋吸收塔装置(如图所示),用NaClO溶液来进一步处理NO气体。
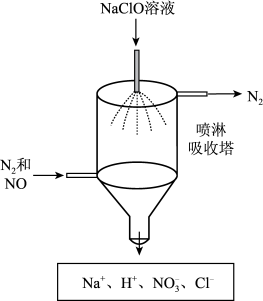
①NaClO溶液吸收NO时发生反应的离子方程式为____ 。
②该装置的优点是____ 。
(4)装置C的吸收液中NO 、NO
、NO 直接排放也会造成水体污染。乙同学设计了以下实验将溶液中
直接排放也会造成水体污染。乙同学设计了以下实验将溶液中 、NO
、NO 转化为N2,实现氮的脱除,具体步骤如下:
转化为N2,实现氮的脱除,具体步骤如下:
①向装置C的吸收液中加入适量H2O2溶液,充分反应后,蒸发浓缩,得到c(NO )为0.1000mol·L-1的溶液甲。写出H2O2溶液将吸收液中的NO
)为0.1000mol·L-1的溶液甲。写出H2O2溶液将吸收液中的NO 氧化为NO
氧化为NO 的离子方程式:
的离子方程式:____ 。
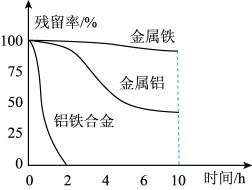
②量取三份50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中将溶液甲中的NO 还原为N2,从而实现脱氮,溶液中NO
还原为N2,从而实现脱氮,溶液中NO 的残留率(残留率=
的残留率(残留率=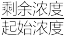 ×100%)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
×100%)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是____ 。

已知:NO、NO2能与NaOH溶液发生如下反应:NO+NO2+2NaOH=2NaNO2+H2O、2NO2+2NaOH=NaNO2+ NaNO3+H2O;但NO不能单独与NaOH溶液反应。
(1)实验时在装置A的干燥管中放置一团棉花,吸收粉尘。装置B的干燥装置中应盛放的试剂为
a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO4•5H2O)
(2)气体在被装置C中的NaOH溶液吸收前,需在检测采样口测定气体中NO和NO2的含量。为确保NO和NO2气体能够被NaOH溶液完全吸收,则需控制参加反应的NO和NO2物质的量比值为
a.≥1 b.=1 c.≤1
(3)若进入装置C的气体中NO和NO2物质的量比值不符合(2)中要求,则气囊中除含有N2外,可能含有少量NO气体。甲同学设计了喷淋吸收塔装置(如图所示),用NaClO溶液来进一步处理NO气体。

①NaClO溶液吸收NO时发生反应的离子方程式为
②该装置的优点是
(4)装置C的吸收液中NO
 、NO
、NO 直接排放也会造成水体污染。乙同学设计了以下实验将溶液中
直接排放也会造成水体污染。乙同学设计了以下实验将溶液中 、NO
、NO 转化为N2,实现氮的脱除,具体步骤如下:
转化为N2,实现氮的脱除,具体步骤如下:①向装置C的吸收液中加入适量H2O2溶液,充分反应后,蒸发浓缩,得到c(NO
 )为0.1000mol·L-1的溶液甲。写出H2O2溶液将吸收液中的NO
)为0.1000mol·L-1的溶液甲。写出H2O2溶液将吸收液中的NO 氧化为NO
氧化为NO 的离子方程式:
的离子方程式:②量取三份50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中将溶液甲中的NO
 还原为N2,从而实现脱氮,溶液中NO
还原为N2,从而实现脱氮,溶液中NO 的残留率(残留率=
的残留率(残留率=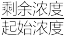 ×100%)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
×100%)与反应时间的关系如图所示。0~2h内,铝铁合金的脱氮效率比金属铝、金属铁要高得多,其可能原因是
更新时间:2022-04-22 14:56:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】根据下列框图回答问题(答题时方程式中的M、E用所对应的元素符号表示):
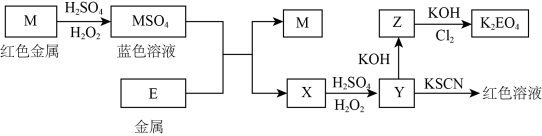
(1)写出M、E的化学式:M___________ ;E__________ ;
(2)M溶于稀H2SO4和H2O2混合液的化学方程式:_________________ ,若参加反应H2O2为1mol,转移电子为__________ mol。
(3)某同学取X的溶液,用稀硫酸酸化并在空气中放置一段时间后,加入KI—淀粉溶液,溶液变为蓝色。写出与上述变化过程相关的离子方程式:_______________ 、_________________ 。
(4)写出Cl2将Z氧化为K2EO4的化学方程式:_____________________________ 。

(1)写出M、E的化学式:M
(2)M溶于稀H2SO4和H2O2混合液的化学方程式:
(3)某同学取X的溶液,用稀硫酸酸化并在空气中放置一段时间后,加入KI—淀粉溶液,溶液变为蓝色。写出与上述变化过程相关的离子方程式:
(4)写出Cl2将Z氧化为K2EO4的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某生产企业的工业废水中含有FeSO4和CuSO4.为了变废为宝,技术人员计划从该废水中回收FeSO4和金属Cu,工艺流程如图所示。回答下列问题:
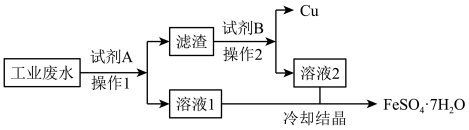
(1)“操作1”与“操作2”的名称为________ ,在实验室中进行该操作时,所需要的玻璃仪器除烧杯外,还有_______ 。
(2)加入试剂A的目的是将Cu2+全部转化为Cu,以便回收铜单质,发生反应的离子方程式为______ 。
(3)溶液1加入过量氯水后发生反应的离子方程式为________ 。
(4)“滤渣”的成分为______ ,加入的试剂B为_______ (填化学式)。
(5)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是___________ 。
(6)B小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。试剂:酸化的0.5 mol·L-1 溶液1,5% H2O2溶液
①上述实验中H2O2溶液与溶液1反应的离子方程式是___________ 。
②产生气泡的原因是___________ 。

(1)“操作1”与“操作2”的名称为
(2)加入试剂A的目的是将Cu2+全部转化为Cu,以便回收铜单质,发生反应的离子方程式为
(3)溶液1加入过量氯水后发生反应的离子方程式为
(4)“滤渣”的成分为
(5)A小组同学要鉴别“溶液2”中的金属阳离子,所需实验操作及实验现象是
(6)B小组同学设计如下实验,研究亚铁盐与H2O2溶液的反应。试剂:酸化的0.5 mol·L-1 溶液1,5% H2O2溶液
| 操作 | 现象 |
| 取2 mL酸化的溶液1于试管中,加入5滴5% H2O2溶液 | 溶液立即变为棕黄色,稍后,产生气泡。 |
| 向反应后的溶液中加入KSCN溶液 | 溶液变红 |
②产生气泡的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属钻广泛应用于航空航天、电器制造等领域,是一种重要的战略金属。以含钴废料(主要成分为 ,含有少量
,含有少量 、
、 、
、 和Ti的化合物)为原料制备
和Ti的化合物)为原料制备 的流程如下图所示:
的流程如下图所示:

回答下列问题:
(1)“酸浸”过程中, 发生反应的离子方程式为
发生反应的离子方程式为_____ 。
(2)“滤渣1”的成分是_____ (填化学式)。
(3)“除钛”时, 生成
生成 的离子方程式为
的离子方程式为_____ 。
(4)“调pH”时,pH越低,“除钙”时所需 越多,原因是
越多,原因是_____ ;若“调pH至3.7”后的滤液中,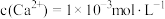 ,除钙率达到
,除钙率达到 ,“除钙”后滤液中
,“除钙”后滤液中
_____  。[已知:
。[已知: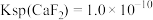 ]
]
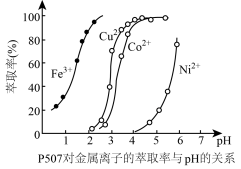
(5)已知:萃取率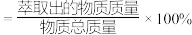 。萃取剂P507对金属离子的萃取率与溶液pH的关系如图所示,则萃取应选择的最佳pH在
。萃取剂P507对金属离子的萃取率与溶液pH的关系如图所示,则萃取应选择的最佳pH在_____ 左右。若用等体积有机萃取剂连续萃取三次,每次萃取率均为 ,则经过三次萃取后,
,则经过三次萃取后, 的总萃取率为
的总萃取率为_____ 。
 ,含有少量
,含有少量 、
、 、
、 和Ti的化合物)为原料制备
和Ti的化合物)为原料制备 的流程如下图所示:
的流程如下图所示:
回答下列问题:
(1)“酸浸”过程中,
 发生反应的离子方程式为
发生反应的离子方程式为(2)“滤渣1”的成分是
(3)“除钛”时,
 生成
生成 的离子方程式为
的离子方程式为(4)“调pH”时,pH越低,“除钙”时所需
 越多,原因是
越多,原因是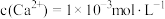 ,除钙率达到
,除钙率达到 ,“除钙”后滤液中
,“除钙”后滤液中
 。[已知:
。[已知: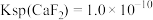 ]
](5)已知:萃取率
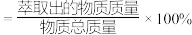 。萃取剂P507对金属离子的萃取率与溶液pH的关系如图所示,则萃取应选择的最佳pH在
。萃取剂P507对金属离子的萃取率与溶液pH的关系如图所示,则萃取应选择的最佳pH在 ,则经过三次萃取后,
,则经过三次萃取后, 的总萃取率为
的总萃取率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】亚硝酸钙是一种重要的化工原料,可作为水泥添加剂,防锈剂等。某兴趣小组拟利用以下装置制备Ca(NO2)2并测定产品的纯度(夹持及加热装置略)。
已知:①Ca(OH)2+NO+NO2=Ca(NO2)2+H2O
②2Ca(OH)2+4NO2=Ca(NO2)2+Ca(NO3)2+2H2O
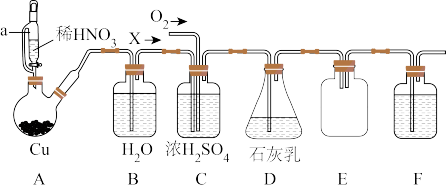
(1)仪器a的名称是____ ,B的作用是____ ,F中盛放的试剂是____ 。
(2)A中发生反应的离子方程式为____ 。
(3)C中通入的O2的量应为X的 ,若
,若 <
< ,会导致
,会导致____ ;若 >
> ,会导致
,会导致____ 。
(4)实验中可通过调节气体X流速来控制其与O2通入量的比,调节流速的方法有____ (任答一种)。
(5)充分反应后,经分离提纯得到Ca(NO2)2,设计如下方案测定产品中Ca(NO2)2的纯度(杂质不参与以下反应):准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,加入过量的c1mol·L-1的KI溶液、淀粉溶液,然后滴加稀硫酸,用c2mol·L-1的Na2S2O3溶液滴定,平行滴定3次,平均消耗VmL的Na2S2O3溶液。
(在酸性条件下:2NO +4H++2I-=2NO↑+I2+2H2O,I2+2S2O
+4H++2I-=2NO↑+I2+2H2O,I2+2S2O =2I-+S4O
=2I-+S4O )
)
①滴定至终点的现象是____ 。
②Ca(NO2)2的纯度为____ 。
已知:①Ca(OH)2+NO+NO2=Ca(NO2)2+H2O
②2Ca(OH)2+4NO2=Ca(NO2)2+Ca(NO3)2+2H2O

(1)仪器a的名称是
(2)A中发生反应的离子方程式为
(3)C中通入的O2的量应为X的
 ,若
,若 <
< ,会导致
,会导致 >
> ,会导致
,会导致(4)实验中可通过调节气体X流速来控制其与O2通入量的比,调节流速的方法有
(5)充分反应后,经分离提纯得到Ca(NO2)2,设计如下方案测定产品中Ca(NO2)2的纯度(杂质不参与以下反应):准确称取mgCa(NO2)2样品放入锥形瓶中,加适量水溶解,加入过量的c1mol·L-1的KI溶液、淀粉溶液,然后滴加稀硫酸,用c2mol·L-1的Na2S2O3溶液滴定,平行滴定3次,平均消耗VmL的Na2S2O3溶液。
(在酸性条件下:2NO
 +4H++2I-=2NO↑+I2+2H2O,I2+2S2O
+4H++2I-=2NO↑+I2+2H2O,I2+2S2O =2I-+S4O
=2I-+S4O )
)①滴定至终点的现象是
②Ca(NO2)2的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某课外活动小组为了探究铜与稀硝酸反应产生的是 气体,设计了如下实验:
气体,设计了如下实验:

回答下列问题:
(1)仪器a的名称为_______ 。
(2)装置A制取 的目的是
的目的是_______ 。
(3)当_______ (填某装置中出现的实验现象)时,关闭K,将装置B中铜丝插入稀硝酸,并微热之,装置B中生成 时发生反应的离子方程式为
时发生反应的离子方程式为_______ 。
(4)验证装置B中生成的是 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为_______ 。
(5)若产生的氮氧化物尾气用 溶液吸收,主要反应为
溶液吸收,主要反应为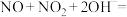
 。
。
①下列措施能提高 和
和 吸收率的是
吸收率的是_______ (填字母)。
A.微微加热装置B,加快气流速率
B.在实验过程中补充适量 溶液
溶液
C.在干燥管末端加一个多孔球泡
②实验结束时,装置内的 被完全吸收,若装置B中生成
被完全吸收,若装置B中生成 气体的体积为
气体的体积为 ,注射器内空气有
,注射器内空气有 (氧气体积按
(氧气体积按 计算),则最终生成的
计算),则最终生成的 的物质的量约为
的物质的量约为_______ (装置内气体的摩尔体积均视为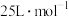 )。
)。
 气体,设计了如下实验:
气体,设计了如下实验:
回答下列问题:
(1)仪器a的名称为
(2)装置A制取
 的目的是
的目的是(3)当
 时发生反应的离子方程式为
时发生反应的离子方程式为(4)验证装置B中生成的是
 气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为
气体,某同学将注射器F中的空气推入装置E中,装置E中出现的实验现象为(5)若产生的氮氧化物尾气用
 溶液吸收,主要反应为
溶液吸收,主要反应为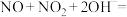
 。
。①下列措施能提高
 和
和 吸收率的是
吸收率的是A.微微加热装置B,加快气流速率
B.在实验过程中补充适量
 溶液
溶液C.在干燥管末端加一个多孔球泡
②实验结束时,装置内的
 被完全吸收,若装置B中生成
被完全吸收,若装置B中生成 气体的体积为
气体的体积为 ,注射器内空气有
,注射器内空气有 (氧气体积按
(氧气体积按 计算),则最终生成的
计算),则最终生成的 的物质的量约为
的物质的量约为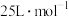 )。
)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某处工厂排出的烟道气中含氮氧化物(主要为NO、NO2)、粉尘和少量水蒸气。课外兴趣活动小组对该工厂排出的烟道气进行处理,并检测其氮氧化物含量,实验装置如图所示:
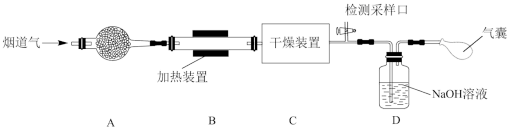
(1)装置A中放置无碱玻璃棉,其目的是除去___________ 。为保证检测的准确性,装置C中盛放的化学试剂可以是___________ (填字母)。
a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO4·5H2O)
(2)装置D中主要发生:2NaOH+2NO2=NaNO2+NaNO3+H2O;2NaOH+NO+NO2=2NaNO2+H2O
①若反应后尾气无残留,则参加反应的NO2、NO物质的量比值为_______ (填字母)。
a.≥1 b.≤1 c.任意值
②可使用适量酸性H2O2溶液,将溶液中的NO2-全部氧化为NO3-,发生反应的离子方程式是___________ 。
(3)溶液中NO3-直接排放在水体中也会造成污染,现用活泼金属将溶液中NO3-转化为N2,实现氮元素的脱除,具体步骤如下:
步骤一、取适量(2)中H2O2处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO3-)为0.100mol·L-1的溶液甲。
步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行氮脱除。
步骤三、重复实验2~3次,溶液中NO3-的残留情况与反应时间的关系如图所示。
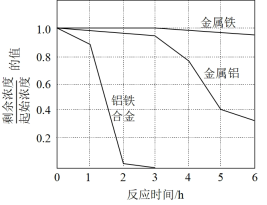
①金属铝和金属铁在0~3h内,NO3-的脱除效率均很低,几乎没被脱除,其可能的原因是___________ 。
②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因________ 。
(4)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生成NO3-和Cl-,发生反应的离子方程式是___________ 。

(1)装置A中放置无碱玻璃棉,其目的是除去
a.碱石灰 b.浓硫酸 c.五水合硫酸铜(CuSO4·5H2O)
(2)装置D中主要发生:2NaOH+2NO2=NaNO2+NaNO3+H2O;2NaOH+NO+NO2=2NaNO2+H2O
①若反应后尾气无残留,则参加反应的NO2、NO物质的量比值为
a.≥1 b.≤1 c.任意值
②可使用适量酸性H2O2溶液,将溶液中的NO2-全部氧化为NO3-,发生反应的离子方程式是
(3)溶液中NO3-直接排放在水体中也会造成污染,现用活泼金属将溶液中NO3-转化为N2,实现氮元素的脱除,具体步骤如下:
步骤一、取适量(2)中H2O2处理后的溶液,调节pH至中性,蒸发浓缩,得到c(NO3-)为0.100mol·L-1的溶液甲。
步骤二、现量取50mL溶液甲,分别用金属铝、金属铁和铝铁合金在45℃、惰性气体氛围中对溶液乙进行氮脱除。
步骤三、重复实验2~3次,溶液中NO3-的残留情况与反应时间的关系如图所示。

①金属铝和金属铁在0~3h内,NO3-的脱除效率均很低,几乎没被脱除,其可能的原因是
②0~3h内铝铁合金的氮脱除效率比金属铝、金属铁大得多,其可能的原因
(4)气囊用来储存处理后气体,其中可能含少量NO气体,可用酸性NaClO溶液来处理。HClO氧化NO生成NO3-和Cl-,发生反应的离子方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工厂采用如下工艺处理镍钴矿(硫酸浸取液中含Ni2+、Co2+、Fe2+、Fe3+、Mg2+和Mn2+),实现镍、钴、镁元素的回收,流程如图1所示。

已知:
回答下列问题:
(1)用硫酸浸取镍钴矿时,下列措施可以提高浸取速率的是______(填字母)。
(2)“氧化”时,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5)。Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为______ 。 (H2SO5的电离第一步完全,第二步微弱)。用石灰乳调节pH=4,检验氧化后的滤液中是否仍存在Fe3+的方法是______ 。
(3)“氧化”时保持空气通入速率不变,Mn(Ⅱ)氧化率与时间关系如图2所示。SO2体积分数为______ 时,Mn(Ⅱ)氧化速率最大。

(4)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为______ 。
(5)“沉钴镍”时钴镍恰好完全沉淀时溶液中c(OH-)=______  (离子浓度
(离子浓度 时沉淀完全)。
时沉淀完全)。
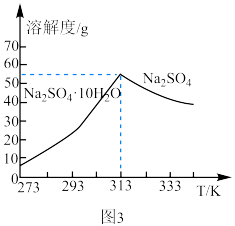
(6)已知 及
及 的溶解度曲线如图3所示,从“上层清液”中制得
的溶解度曲线如图3所示,从“上层清液”中制得 的具体操作是
的具体操作是______ 、过滤﹑洗涤、干燥。

已知:
| 物质 |  |  |  |  |
 |  |  |  | 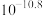 |
(1)用硫酸浸取镍钴矿时,下列措施可以提高浸取速率的是______(填字母)。
| A.适当升高温度 | B.适当增大硫酸浓度 |
| C.适当延长浸取时间 | D.将镍钴矿粉碎 |
(2)“氧化”时,混合气在金属离子的催化作用下产生具有强氧化性的过一硫酸(H2SO5)。Mn2+被H2SO5氧化为MnO2,该反应的离子方程式为
(3)“氧化”时保持空气通入速率不变,Mn(Ⅱ)氧化率与时间关系如图2所示。SO2体积分数为

(4)“沉钴镍”中得到的Co(Ⅱ)在空气中可被氧化成CoO(OH),该反应的化学方程式为
(5)“沉钴镍”时钴镍恰好完全沉淀时溶液中c(OH-)=
 (离子浓度
(离子浓度 时沉淀完全)。
时沉淀完全)。(6)已知
 及
及 的溶解度曲线如图3所示,从“上层清液”中制得
的溶解度曲线如图3所示,从“上层清液”中制得 的具体操作是
的具体操作是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以菱镁矿(主要成分为MgCO3,含少量FeCO3等)为原料制备高纯氧化镁的流程如下:
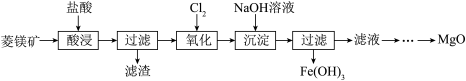
(1)采用搅拌、______ 、适当增大盐酸的浓度等措施可以提高“酸浸”率。
(2)“氧化”过程中发生反应的化学方程式为________ 。
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是________ 。
(4)“滤液”中继续加入NaOH溶液,______ 、________ 、灼烧,制得氧化镁。
(5)工业可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO,写出该反应的化学方程式:____ 。取少量制得的该物质溶于某种液体溶剂中(两者不反应),能说明有纳米MgO存在的简单方法是____ 。

(1)采用搅拌、
(2)“氧化”过程中发生反应的化学方程式为
(3)“沉淀”时需严格控制NaOH溶液的用量,其目的是
(4)“滤液”中继续加入NaOH溶液,
(5)工业可用氯化镁和碳酸铵为原料,采用直接沉淀法制备纳米MgO,写出该反应的化学方程式:
您最近一年使用:0次
【推荐3】汽车尾气中含有CO、NOx等有害气体。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:___________ 。
(2)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下, N2和O2完全反应生成NO的热化学方程式为___________ 。
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
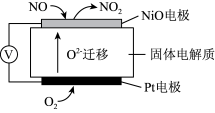
①NiO电极上发生的是___________ 反应(填“氧化”或“还原”)。
②外电路中,电子的流动方向是从___________ 电极流出(填NiO或Pt);Pt电极上的电极反应式为___________ 。
(4)一种新型催化剂能使NO和CO发生反应:2NO + 2CO ⇌ 2CO2 + N2。
某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,
①请将表中数据补充完整:A___________ ;B___________ 。
②能验证温度对化学反应速率影响规律的实验是___________ (填实验序号)。
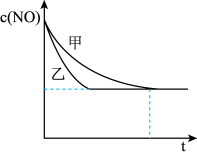
③实验I和实验II中,c(NO)随时间t的变化曲线如图所示,其中表示实验II的曲线是___________ (填“甲”或“乙”)。
(1)NOx能形成酸雨,写出NO2转化为HNO3的化学方程式:
(2)汽车尾气中NO生成过程的能量变化示意图如下:

该条件下, N2和O2完全反应生成NO的热化学方程式为
(3)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:

①NiO电极上发生的是
②外电路中,电子的流动方向是从
(4)一种新型催化剂能使NO和CO发生反应:2NO + 2CO ⇌ 2CO2 + N2。
某同学设计了三组实验,部分实验条件已经填在下表中。已知增大催化剂的比表面积可提高该反应速率。为了验证温度、催化剂的比表面积对化学反应速率的影响规律,
| 实验 编号 | t (℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | B | 124 |
| III | 350 | A | 5.80×10-3 | 82 |
①请将表中数据补充完整:A
②能验证温度对化学反应速率影响规律的实验是
③实验I和实验II中,c(NO)随时间t的变化曲线如图所示,其中表示实验II的曲线是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氢气是一种清洁能源,请根据实验室和工业上制氢及氢气性质回答相关问题。
I.实验室用稀硫酸与锌粒(黄豆粒大小)制取氢气时加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)少量硫酸铜溶液可以加快氢气生成速率的原因是______________ ;
(2)要加快上述实验中产生氢气的速率,还可采取的措施有______ 、_______ (列举两种措施)。
(3)当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因____________ 。
II.工业上海水制氢气的新技术:2H2O 2H2↑+O2↑。试回答下列问题:
2H2↑+O2↑。试回答下列问题:
(1)分解海水的反应属于_____ 反应(填“放热”或“吸热”)。
(2)某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为:A极是2H2+2O2-―4e-=2H2O,B极是O2+4e-=2O2-,则A极是电池的____ 极。
(3)氢气的储存比较困难,最近科学家研究出一种环保,安全的储氢方法,其原理可表示为:NaHCO3+H2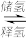 HCOONa+H2O。下列有关说法正确的是
HCOONa+H2O。下列有关说法正确的是____ 。
A 储氢释氢过程均无能量变化 B 该反应属于可逆反应
C 储氢过程中,NaHCO3被还原 D 释氢过程中,每消耗0.1 mol H2O放出2.24 L的H2
I.实验室用稀硫酸与锌粒(黄豆粒大小)制取氢气时加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)少量硫酸铜溶液可以加快氢气生成速率的原因是
(2)要加快上述实验中产生氢气的速率,还可采取的措施有
(3)当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因
II.工业上海水制氢气的新技术:2H2O
 2H2↑+O2↑。试回答下列问题:
2H2↑+O2↑。试回答下列问题:(1)分解海水的反应属于
(2)某种氢氧燃料电池是用固体金属化合物陶瓷作电解质,两极上发生的电极反应分别为:A极是2H2+2O2-―4e-=2H2O,B极是O2+4e-=2O2-,则A极是电池的
(3)氢气的储存比较困难,最近科学家研究出一种环保,安全的储氢方法,其原理可表示为:NaHCO3+H2
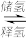 HCOONa+H2O。下列有关说法正确的是
HCOONa+H2O。下列有关说法正确的是A 储氢释氢过程均无能量变化 B 该反应属于可逆反应
C 储氢过程中,NaHCO3被还原 D 释氢过程中,每消耗0.1 mol H2O放出2.24 L的H2
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学生为了探究Zn与硫酸反应过程中的速率变化,在100mL稀硫酸中加入足量的Zn粒,用排水集气法收集反应放出的H2,实验记录如下(累计值):
(1)哪一时间段(指0~1、1~2、2~3、3~4、4~5min)反应速率最大________ ,原因是_________ 。
(2)哪一时间段的反应速率最小_________ ,原因是____________ 。
(3)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①硫酸铜溶液可以加快氢气生成速率的原因是____________ 。
②当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因____________ 。
(4)要加快上述实验中气体产生的速率,还可采取的措施有________ (答两种)。
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标况下) | 50 | 120 | 232 | 290 | 310 |
(2)哪一时间段的反应速率最小
(3)该同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。
①硫酸铜溶液可以加快氢气生成速率的原因是
②当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
(4)要加快上述实验中气体产生的速率,还可采取的措施有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】以Al和不同的铜盐溶液间的反应为实验对象,探索Al与不同铜盐溶液反应的多样性。
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:____________________________
经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:_____________________
③请写出60s后反应进一步加快可能的原因(写出两条)_____________________________
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用。
假设二:________________________
(3)为进一步研究上述假设,设计如下实验:
_____________________________________
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:______________________________________
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:______________________________________
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:_________________
实验 | 向试管中加入2ml溶液 | 实验现象 |
| 实验Ⅰ:0.5mol/LCuCl2溶液 | 15s:大量气泡且有红色物质析出 60s:反应进一步加快且反应剧烈放热,液体几乎沸腾 120s:铝片反应完,试管中析出大量蓬松的红色物质 |
| 实验Ⅱ:0.5mol/LCuSO4溶液 | 15s 无明显现象 60s:铝片表面有极少气泡 120s:有少量气泡溢出,铝片边缘有很少红色物质生成 |
(1)对实验Ⅰ进行研究②④
①实验Ⅰ中生成红色物质的离子方程式为:
经检验实验Ⅰ中产生的气体为氢气,用离子方程式解释溶液中存在H+的原因:
③请写出60s后反应进一步加快可能的原因(写出两条)
(2)对实验Ⅱ进行研究
实验Ⅱ反应明显比实验Ⅰ缓慢,说明Al与不同的铜盐溶液反应呈现多样性,其原因可能有:
假设一:SO42-对Al与Cu2+的置换反应存在一定的抑制作用。
假设二:
(3)为进一步研究上述假设,设计如下实验:
实验 | 向试管中加入2mL溶液 | 实验现象 |
| 实验Ⅲ:0.5mol/LCuCl2溶液+1g Na2SO4固体 | 加入 Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 |
| 实验Ⅳ:0.5mol/L CuCl2溶液+5g Na2SO4固体 | 加入Na2SO4固体后速率几乎不变,仍有大量气泡产生,红色物质生成且剧烈放热,铝片反应完全,溶液沸腾 | |
| 实验Ⅴ:0.5mol/LCuSO4溶液+0.02mol NaCl固体 | 未加入 NaCl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 | |
| 实验Ⅵ:0.5mol/LCuSO4溶液+ | 未加入 NH4Cl固体前几乎没现象,加入后,铝片表面迅速产生大量气体和红色物质,溶液温度上升至沸腾,铝反应完全 |
其中,实验Ⅰ与实验Ⅲ、Ⅳ做对比,结论为:
其中,实验Ⅱ与实验Ⅴ、Ⅵ做对比,结论为:
(4)请设计实验证明Cl-对Al与H+的反应同样起到相似的作用:
您最近一年使用:0次