化合物I(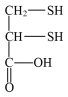 )易与Cu2+结合生成化合物II(
)易与Cu2+结合生成化合物II( )。请回答:
)。请回答:
(1)Cu原子的M电子层中有_______ 个能级,Cu原子的核外电子排布式为_______ 。
(2)下列说法正确的是_______。
(3)化合物I中同周期的两种元素的电负性大小为_______ 。
(4)金属铜的熔点高于钾的原因是_______ 。
(5)Cu可以形成一种离子化合物 。若要确定它是晶体还是非晶体,最科学的方法是对它进行
。若要确定它是晶体还是非晶体,最科学的方法是对它进行_______ 实验;其阴离子的空间构型是_______ 。
(6)CX4的熔沸点如下表所示:
分析上述三种CX4的熔沸点变化原因:_______ 。
 )易与Cu2+结合生成化合物II(
)易与Cu2+结合生成化合物II( )。请回答:
)。请回答:(1)Cu原子的M电子层中有
(2)下列说法正确的是_______。
| A.化合物I中S原子采取sp3杂化 | B.化合物I中碳原子的杂化类型有sp3和sp2 |
| C.化合物II中C-C-C键角是180° | D.化合物II中存在离子键和共价键 |
(4)金属铜的熔点高于钾的原因是
(5)Cu可以形成一种离子化合物
 。若要确定它是晶体还是非晶体,最科学的方法是对它进行
。若要确定它是晶体还是非晶体,最科学的方法是对它进行(6)CX4的熔沸点如下表所示:
| CX4 |  |  | 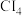 |
| 熔点/℃ | -22.8 | 88 | 170 |
| 沸点/℃ | 76.8 | 190 | 329 |
更新时间:2022-06-24 22:04:31
|
相似题推荐
【推荐1】金属钛(Ti)被誉为“21世纪金属”,具有良好的生物相容性,它兼具铁的高强度和铝的低密度。其单质和化合物具有广泛的应用价值。氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品。以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图)。

图中的M是短周期金属元素,M的部分电离能如下表所示:
请回答下列问题:
(1)Ti的基态原子外围电子排布式为___________ 。
(2)纳米TiO2是一种应用广泛的催化剂,用纳米TiO2催化的反应实例如图所示。化合物甲的分子中采取sp2方式杂化的碳原子有___________ 个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为___________ 。

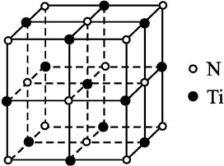
(3)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为___________ g·cm-3(NA为阿伏加德罗常数的值,只列计算式)。该晶体中与N原子距离相等且最近的N原子有___________ 个。

图中的M是短周期金属元素,M的部分电离能如下表所示:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/(kJ·mol-1) | 738 | 1451 | 7733 | 10540 | 13630 |
(1)Ti的基态原子外围电子排布式为
(2)纳米TiO2是一种应用广泛的催化剂,用纳米TiO2催化的反应实例如图所示。化合物甲的分子中采取sp2方式杂化的碳原子有

(3)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为

您最近一年使用:0次
【推荐2】 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有___________ 种;O、S、Cl电负性由大到小的顺序是___________ 。
(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是___________ (填化学式);键长 最长的是
最长的是___________ (填化学式)。已知:配离子的颜色与 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
___________  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是___________ 。
(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为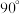 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为___________ 。若阿伏加德罗常数的值为 ,化合物
,化合物 的密度
的密度
___________  (用含
(用含 的代数式表示)。
的代数式表示)。
 、
、 、
、 、
、 组成的化合物
组成的化合物 通过
通过 空位的掺杂可引入载流子诱发超导,
空位的掺杂可引入载流子诱发超导, 的晶体结构和氧原子沿
的晶体结构和氧原子沿 轴的投影如图所示。回答下列问题:
轴的投影如图所示。回答下列问题: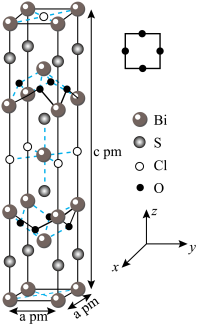
 原子中
原子中 层上的电子空间运动状态有
层上的电子空间运动状态有(2)氮族元素氢化物(MH3)NH3、PH3、AsH3、SbH3、BiH3键角H-M-H最大的是
 最长的是
最长的是 电子跃迁的分裂能大小有关,1个电子从较低的
电子跃迁的分裂能大小有关,1个电子从较低的 轨道跃迁到较高能量的
轨道跃迁到较高能量的 轨道所需的能量为
轨道所需的能量为 的分裂能,用符号
的分裂能,用符号 表示。分裂能
表示。分裂能
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是(3)A属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
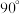 ,该晶胞中Bi原子的配位数为
,该晶胞中Bi原子的配位数为 ,化合物
,化合物 的密度
的密度
 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】氮和氧是构建化合物的常见元素。
(1)下列说法正确的是___________。
(2)①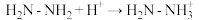 ,其中
,其中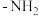 的
的 原子杂化方式为
原子杂化方式为___________ ;比较键角 中的-NH2
中的-NH2_____ H2N-NH 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由___________ 。
②将 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是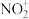 。比较氧化性强弱:NO
。比较氧化性强弱:NO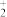
_____ HNO3(填“>”、“<”或“=”);写出A中阴离子的结构式___________ 。
已知: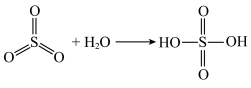
(1)下列说法正确的是___________。
A.电负性: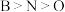 | B.离子半径: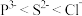 |
C.第一电离能: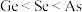 | D.基态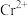 的简化电子排布式: 的简化电子排布式: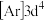 |
(2)①
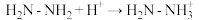 ,其中
,其中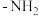 的
的 原子杂化方式为
原子杂化方式为 中的-NH2
中的-NH2 中的-NH
中的-NH (填“>”、“<”或“=”),请说明理由
(填“>”、“<”或“=”),请说明理由②将
 与
与 按物质的量之比
按物质的量之比 发生化合反应生成A,测得A由2种微粒构成,其中之一是
发生化合反应生成A,测得A由2种微粒构成,其中之一是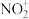 。比较氧化性强弱:NO
。比较氧化性强弱:NO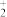
您最近一年使用:0次
【推荐1】下表是元素周期表的一部分,表中所列字母分别代表一种元素。试回答下列问题:
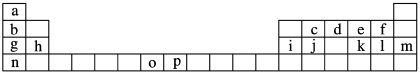
(1)请写出n元素基态原子的电子排布式:___________ 。
(2)o、p两元素的部分电离能数据列于下表:
比较两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,其原因是
再失去一个电子难,其原因是___________ 。
(3)第三周期8种元素按单质熔点高低的顺序排列如图(Ⅰ)所示,其中电负性最大的是___________ (填图中的序号)。

(4)表中所列的某主族元素的电离能情况如图(Ⅱ)所示,则该元素是___________ (填元素符号)。

(5)基态i原子核外电子云有___________ 种不同的伸展方向,共有___________ 种不同能级的电子,有___________ 种不同运动状态的电子。
(6)第四周期中最外层仅有1个电子的所有基态原子的元素为___________ ,第四周期中,3d轨道半充满的元素符号是___________ 。

(1)请写出n元素基态原子的电子排布式:
(2)o、p两元素的部分电离能数据列于下表:
| 元素 | o | p | |
 | 717 | 759 | |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子难,其原因是
再失去一个电子难,其原因是(3)第三周期8种元素按单质熔点高低的顺序排列如图(Ⅰ)所示,其中电负性最大的是

(4)表中所列的某主族元素的电离能情况如图(Ⅱ)所示,则该元素是

(5)基态i原子核外电子云有
(6)第四周期中最外层仅有1个电子的所有基态原子的元素为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】已知a~f是原子序数依次增大前四周期的六种元素,a元素原子核外电子只有一种自旋取向;b元素原子最高能级的不同轨道都有电子且自旋方向相同;c元素原子的价层电子排布为 ,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用
,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用元素符号 表示):
(1)e元素基态原子占据的最高能级共有_________ 个原子轨道,其形状是_________ ;f元素位于周期表的_________ 区,其基态原子的电子排布式为_________ 。
(2)a、b、c三种元素的电负性由大到小的顺序为_________ 。
(3)b、c、d、e四种元素的第一电离能由大到小的顺序为_________ 。
(4)下图是a~f中某种元素的部分电离能,由此判断该元素是_________ 。
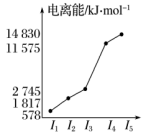
表1:Mn、Fe的部分电离能
(5)比较表1中Mn、Fe两元素的 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子
再失去一个电子_________ (填“易”或“难”)。你的解释是_________ 。
 ,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用
,d元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;e与d的最高能层数相同,但其价电子层电子数等于其电子层数;f元素原子最外层只有1个电子,次外层内的所有轨道的电子均成对。请回答下列问题(答题时涉及a~f元素,要用(1)e元素基态原子占据的最高能级共有
(2)a、b、c三种元素的电负性由大到小的顺序为
(3)b、c、d、e四种元素的第一电离能由大到小的顺序为
(4)下图是a~f中某种元素的部分电离能,由此判断该元素是

表1:Mn、Fe的部分电离能
| 元素 | Mn | Fe | |
电离能/kJ·mol |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
 、
、 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子
再失去一个电子
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】呋喃(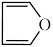 )和吡咯(
)和吡咯(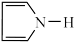 )是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
)是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
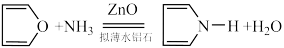
回答下列问题:
(1)呋喃和吡咯所含元素中:电负性最大的是___________ (填元素符号),第一电离能最大的元素的基态原子电子排布图是______________________ 。
(2)呋喃分子中,碳原子的杂化方式是___________ ,1mol吡咯分子中含________ molσ键。
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是___________ (填元素符号);H2O的空间构型为___________ ;写出一种与NH3互为等电子体的阳离子:___________ (填化学式)。
(4)NH3的相对分子质量比N2O的小,但其沸点却比N2O的高,其主要原因是___________ 。
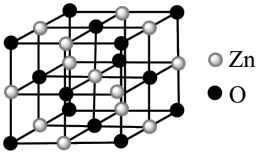
(5)ZnO晶体随着环境条件的改变能形成不同结构的晶体,其中一种的晶胞结构如图所示,已知该ZnO晶体密度为ag·cm-3,NA表示阿伏伽德罗常数。则该晶体中与Zn2+等距离且最近的Zn2+共有___________ 个,该ZnO晶胞中相邻两个O2-之间的距离为___________ nm。
 )和吡咯(
)和吡咯( )是较常见的杂环化合物呋喃通过下列反应可转化为吡咯:
)是较常见的杂环化合物呋喃通过下列反应可转化为吡咯: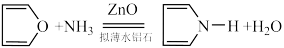
回答下列问题:
(1)呋喃和吡咯所含元素中:电负性最大的是
(2)呋喃分子中,碳原子的杂化方式是
(3)NH3与H2O可与Zn2+形成配合物[Zn(NH3)3(H2O)]2+。与Zn2+形成配位键的原子是
(4)NH3的相对分子质量比N2O的小,但其沸点却比N2O的高,其主要原因是
(5)ZnO晶体随着环境条件的改变能形成不同结构的晶体,其中一种的晶胞结构如图所示,已知该ZnO晶体密度为ag·cm-3,NA表示阿伏伽德罗常数。则该晶体中与Zn2+等距离且最近的Zn2+共有

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】碳(C)、铜(Cu)、锡(Sn)及其化合物有许多用途。回答下列问题。
(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为_______ 。
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)___ I2(S)(填“>”、“<”或“=”),原因是_ 。PH3分子的热稳定性比NH3______ (填“强”或“弱”)。
(3)1mol苯中含 键的数目为
键的数目为______ 。CH3CH2COOH中C的杂化方式有______ ;
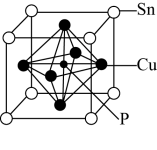
(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为__________ nm,该晶体密度为______ g cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。

(1)在元素周期表里,锡和碳同族,锡位于第五周期。基态锡原子的最外层电子排布式为
(2)磷化铜(Cu3P2)用于制造磷青铜,磷青铜是含少量锡、磷的铜合金。磷化铜与水反应产生有毒的磷化氢(PH3)气体,P、S的第二电离能(I2)的大小关系为I2(P)
(3)1mol苯中含
 键的数目为
键的数目为(4)磷青铜晶体的晶胞结构如图所示,该晶体中P原子与最近的Cu原子的核间距为anm,该晶体中P原子位于由铜原子形成的正八面体的空隙中,则该正八面体的边长为
 cm-3(用含NA的代数式表示)。
cm-3(用含NA的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】(1)写出基态镍原子的电子排布式______ .与其同周期的基态原子的M 层电子全充满的元素位于周期表的_____ 区; 基态原子变成激发态原子产生的光谱叫_________ 光谱。
(2)丙酮(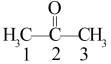 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为____________ ;与CS2互为等电子体的阴离子是____ (写一种);CO32-的立体构型是________ 。
(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成_____ mol AgCl沉淀。H2O分子的键角比H2S分子的键角大,原因是_________ 。
(4)如图所示为GaAs的晶胞结构。
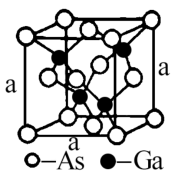
①一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是______
②已知晶胞棱长a=5.64×10-10m.则该晶胞密度为ρ=_______ 。
(2)丙酮(
 )分子中2号碳原子的杂化方式为
)分子中2号碳原子的杂化方式为(3)含0.1mol[Cr(H2O)Cl]Cl2·H2O的水溶液与足量硝酸银溶液反应生成
(4)如图所示为GaAs的晶胞结构。

①一个镓原子周围所有距离最近且相等的砷原子形成的空间构型是
②已知晶胞棱长a=5.64×10-10m.则该晶胞密度为ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】某催化剂材料中包含了Fe、Cr、Ni、C等多种元素。回答下列问题:
(1)基态铁原子的价电子排布式为_______ 。
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的_______ 区。
(3)实验室常用KSCN溶液、苯酚(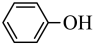 )检验Fe,其中N、O、S的第一电离能由大到小的顺序为
)检验Fe,其中N、O、S的第一电离能由大到小的顺序为_______ (用元素符号表示),苯酚中碳原子的杂化轨道类型为_______ 。
(4)铁元素能与CO形成五羰基铁[Fe(CO)5],Fe(CO)5可用作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含_______ molσ键,与CO互为等电子体的一种离子的化学式为_______ 。
(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的_______ 空隙和_______ 空隙(填几何空间构型);若C60分子的坐标参数分别为A(0,0,0),B( ,0,
,0, ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为_______ 。
(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为_______ ,晶胞参数为428pm,则晶体密度为_______ g/cm3(NA表示阿伏伽德罗常数的值,列出表达式)。

(1)基态铁原子的价电子排布式为
(2)与Cr同周期且基态原子最外层电子数相同的元素,可能位于周期表中的
(3)实验室常用KSCN溶液、苯酚(
 )检验Fe,其中N、O、S的第一电离能由大到小的顺序为
)检验Fe,其中N、O、S的第一电离能由大到小的顺序为(4)铁元素能与CO形成五羰基铁[Fe(CO)5],Fe(CO)5可用作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含
(5)碳的一种同素异形体的晶体可采取非最密堆积,然后在空隙中插入金属离子获得超导体。如图为一种超导体的面心立方晶胞,C60分子占据顶点和面心处,K+占据的是C60分子围成的
 ,0,
,0, ),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为
),C(1,1,1)等,则距离A位置最近的阳离子的原子坐标参数为(6)Ni可以形成多种氧化物,其中一种NiaO晶体晶胞结构为NaCl型,由于晶体缺陷,a的值为0.88,且晶体中的Ni分别为Ni2+、Ni3+,则晶体中Ni2+与Ni3+的最简整数比为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】I.如图所示为NaCl晶胞结构示意图,回答下列问题。

(1)该晶体中,在每个 周围与它距离最近且相等的
周围与它距离最近且相等的 共有
共有_______ 个。
(2)晶体中重复的基本结构单元叫晶胞。在NaCl晶胞中,正六面体的顶点上、面上、棱上的 或
或 为该晶胞与其相邻的晶胞所共有,一个晶胞中
为该晶胞与其相邻的晶胞所共有,一个晶胞中 的个数为
的个数为_______ 。
(3)设NaCl的摩尔质量为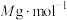 ,NaCl晶体的密度为
,NaCl晶体的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。NaCl晶体中两个钠离子间的最近距离为
。NaCl晶体中两个钠离子间的最近距离为_______ cm。
II.第ⅤA族元素及其化合物在生产、生活中用途广泛。
(4)苯胺( )的晶体类型是
)的晶体类型是_______ 。
(5)两种氧化物的熔点如下表所示,解释表中氧化物之间熔点差异的原因:_______ 。
(6)乙二胺( )是一种有机化合物,乙二胺能与
)是一种有机化合物,乙二胺能与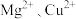 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是_______ ,其中与乙二胺形成的化合物稳定性相对较高的是_______ (填“ ”或“
”或“ ”)。
”)。

(1)该晶体中,在每个
 周围与它距离最近且相等的
周围与它距离最近且相等的 共有
共有(2)晶体中重复的基本结构单元叫晶胞。在NaCl晶胞中,正六面体的顶点上、面上、棱上的
 或
或 为该晶胞与其相邻的晶胞所共有,一个晶胞中
为该晶胞与其相邻的晶胞所共有,一个晶胞中 的个数为
的个数为(3)设NaCl的摩尔质量为
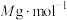 ,NaCl晶体的密度为
,NaCl晶体的密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 。NaCl晶体中两个钠离子间的最近距离为
。NaCl晶体中两个钠离子间的最近距离为II.第ⅤA族元素及其化合物在生产、生活中用途广泛。
(4)苯胺(
 )的晶体类型是
)的晶体类型是(5)两种氧化物的熔点如下表所示,解释表中氧化物之间熔点差异的原因:
| 氧化物 |  | 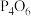 |
| 熔点/℃ | -75.5 | 23.8 |
(6)乙二胺(
 )是一种有机化合物,乙二胺能与
)是一种有机化合物,乙二胺能与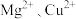 等金属离子形成稳定环状离子,其原因是
等金属离子形成稳定环状离子,其原因是 ”或“
”或“ ”)。
”)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力。
(1)太阳能热水器中常使用一种以镍或镍合金(含铁)空心球为吸收剂的太阳能吸热涂层,铁、镍基态原子未成对电子数各为_____________ 、________________ 。
(2)C60可用作储氢材料,已知金刚石中的C-C键的键长为0.154 nm,C60中C-C键键长为0.140~0.145 nm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?_________ ,阐述理由:________________________________________________________________________ 。C60晶体(其结构模型如图)中每个C60分子周围与它距离最近且等距离的C60分子有_____ 个。
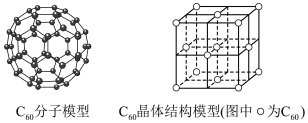
(3)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如下图所示,分子中碳原子轨道的杂化类型为_________ ;1 mol C60分子中σ键的数目为________ 。科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图所示,该物质在低温时是一种超导体。该物质的K原子和C60分子的个数比为________ 。
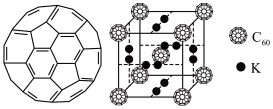
(4)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是______________ 。Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则Si60分子中π键的数目为______ 个。
(5)请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是:________________________________________________________________________ 。
(1)太阳能热水器中常使用一种以镍或镍合金(含铁)空心球为吸收剂的太阳能吸热涂层,铁、镍基态原子未成对电子数各为
(2)C60可用作储氢材料,已知金刚石中的C-C键的键长为0.154 nm,C60中C-C键键长为0.140~0.145 nm,有同学据此认为C60的熔点高于金刚石,你认为是否正确?

(3)富勒烯衍生物由于具有良好的光电性能,在太阳能电池的应用上具有非常光明的前途。富勒烯(C60)的结构如下图所示,分子中碳原子轨道的杂化类型为

(4)继C60后,科学家又合成了Si60、N60,C、Si、N原子电负性由大到小的顺序是
(5)请解释如下现象:熔点:Si60>N60>C60,而破坏分子所需要的能量: N60>C60>Si60,其原因是:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】碳及其化合物广泛存在于自然界中。回答下列问题:
(1)在基态14C原子中,核外存在____ 对自旋相反的电子。
(2)碳在形成化合物时,其键型以共价键为主,原因是____ 。
(3)CS2分子中,共价键的类型有____ ,C原子的杂化轨道类型是____ 。
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于____ 晶体。
(5)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:.

①在石墨烯晶体中,每个C原子连接___ 个六元环,每个六元环占有____ 个C原子。
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接____ 个六元环,六元环中最多有____ 个C原子在同一平面。
(1)在基态14C原子中,核外存在
(2)碳在形成化合物时,其键型以共价键为主,原因是
(3)CS2分子中,共价键的类型有
(4)CO能与金属Fe形成Fe(CO)5,该化合物的熔点为253K,沸点为376K,其固体属于
(5)碳有多种同素异形体,其中石墨烯与金刚石的晶体结构如图所示:.

①在石墨烯晶体中,每个C原子连接
②在金刚石晶体中,C原子所连接的最小环也为六元环,每个C原子连接
您最近一年使用:0次



