磷酸铁 常用作电极材料,以硫铁矿(主要成分是
常用作电极材料,以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的流程如下:
)为原料制备磷酸铁的流程如下:

已知:a.该工艺条件下,几种金属离子沉淀的pH如下表所示:
b. 难溶于水。
难溶于水。
(1)焙烧过程中为提高化学反应速率,可采取的措施是_______ (至少写一条)。
(2)用 还原
还原 的离子方程式为
的离子方程式为_______ 。
(3)用 调节pH的范围是
调节pH的范围是_______ ,以达到除铝的目的。
(4)除铝后加过量 溶液的目的是
溶液的目的是_______ 。
 常用作电极材料,以硫铁矿(主要成分是
常用作电极材料,以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的流程如下:
)为原料制备磷酸铁的流程如下:
已知:a.该工艺条件下,几种金属离子沉淀的pH如下表所示:
| 金属氢氧化物 |  |  |  |
| 开始沉淀pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀pH | 4.1 | 9.7 | 5.2 |
b.
 难溶于水。
难溶于水。(1)焙烧过程中为提高化学反应速率,可采取的措施是
(2)用
 还原
还原 的离子方程式为
的离子方程式为(3)用
 调节pH的范围是
调节pH的范围是(4)除铝后加过量
 溶液的目的是
溶液的目的是
更新时间:2022-06-25 07:43:55
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐1】某硫酸厂以硫铁矿焙烧后的烧渣(主要成分为Fe2O3、SiO2、Al2O3)为原料制取铵明矾晶体[NH4A1(SO4)2·12H2O]的一种工艺流程如图。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:_______ 。
(2)“试剂I”为_______ (填试剂名称),“滤渣b”为_______ (填化学式)。
(3)写出“滤液a”和NaOH溶液反应的离子方程式:_______ 、_______ 。
(4)“滤渣c”的化学式为_______ ,证明铁元素已沉淀完全的实验方法是_______ 。
(5)向NaAlO2溶液中通入足量CO2的离子方程式为_______ 。
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、_______ (填操作名称)、洗涤、干燥。

已知:①SiO2是酸性氧化物,难溶于水,酸浸时不发生反应。
②AI(OH)3固体可溶于NaOH等强碱溶液。
请回答下列问题:
(1)写出Fe2O3的一种常见用途:
(2)“试剂I”为
(3)写出“滤液a”和NaOH溶液反应的离子方程式:
(4)“滤渣c”的化学式为
(5)向NaAlO2溶液中通入足量CO2的离子方程式为
(6)从铵明矾溶液中获得铵明矾晶体的实验操作依次为蒸发浓缩、冷却结晶、
您最近一年使用:0次
【推荐2】ZrO2是重要的耐高温材料,可用作陶瓷遮光剂和良好的催化剂。天然锆英石(ZrSiO4含有铁、铝、铜等金属元素的氧化物杂质,工业以锆英石为原料制备ZrO2的工艺流程如图:
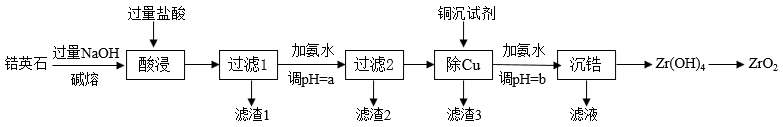
已知:
①锆英石能与烧碱高温反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表:
(1)锆英石碱熔时需要粉碎,其目的是___ 。
(2)ZrSiO4中Zr的化合价为___ 。滤渣2的主要成分为___ 。
(3)“碱熔”过程中ZrSiO4发生反应的化学方程式___ 。
(4)本流程使用NaCN除铜,若盐酸溶解后溶液中c(Cu2+)=0.01mol∙L-1,当溶液中Cu2+开始沉淀时,c(CN-)=___ 。(已知Ksp[Cu(CN)2]=4×10-10)
(5)向除Cu后所得滤液中加氨水调pH=b,发生的离子方程式为___ 。
(6)过滤时需要用到的玻璃仪器___ 。
(7)由氢氧化锆制备高纯二氧化锆的方法是___ 。

已知:
①锆英石能与烧碱高温反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表:
| 离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 完全沉淀时pH | 3.2 | 5.2 | 8.0 |
(2)ZrSiO4中Zr的化合价为
(3)“碱熔”过程中ZrSiO4发生反应的化学方程式
(4)本流程使用NaCN除铜,若盐酸溶解后溶液中c(Cu2+)=0.01mol∙L-1,当溶液中Cu2+开始沉淀时,c(CN-)=
(5)向除Cu后所得滤液中加氨水调pH=b,发生的离子方程式为
(6)过滤时需要用到的玻璃仪器
(7)由氢氧化锆制备高纯二氧化锆的方法是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】工业上常采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3制取七水合硫酸亚铁(FeSO4·7H2O),设计流程如图:

(1)溶解烧渣选用的足量的酸的名称是___ 。
(2)固体1的主要成分是___ 。
(3)加入药品X后,溶液1中主要反应的离子方程式为___ 。
(4)从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解,经过、___ 、___ 过滤等步骤得到晶体。
(5)有同学认为在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O,你认为这一方案___ (填写“可行”或“不可行”)。

(1)溶解烧渣选用的足量的酸的名称是
(2)固体1的主要成分是
(3)加入药品X后,溶液1中主要反应的离子方程式为
(4)从溶液2得到FeSO4·7H2O产品的过程中,须控制条件防止其氧化和分解,经过、
(5)有同学认为在溶液1中直接加NaOH至过量,得到的沉淀用硫酸溶解,其溶液经结晶分离也可得到FeSO4·7H2O,你认为这一方案
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】孔雀石的主要成分为CuCO3·Cu(OH)2。某同学设计从孔雀石中冶炼铜的方案如下:

回答下列问题:
(1)将孔雀石粉碎的目的是__________ ,加入过量稀硫酸, 可观察到的现象是__________ 。
(2)操作a的名称是__________ ,在滤液中加入过量铁粉发生的反应有__________ 、__________ (用离子方程式表示)。
(3)A的化学式为__________ ,在悬浊液中加入A的目的是__________ 。
(4)从滤液中获得铜的另外一种方案是2CuSO4+2H2O 2Cu+O2↑+2H2SO4。现有111 kg CuCO3·Cu(OH)2,通过这种方案理论上可以制取
2Cu+O2↑+2H2SO4。现有111 kg CuCO3·Cu(OH)2,通过这种方案理论上可以制取__________ kg铜。

回答下列问题:
(1)将孔雀石粉碎的目的是
(2)操作a的名称是
(3)A的化学式为
(4)从滤液中获得铜的另外一种方案是2CuSO4+2H2O
 2Cu+O2↑+2H2SO4。现有111 kg CuCO3·Cu(OH)2,通过这种方案理论上可以制取
2Cu+O2↑+2H2SO4。现有111 kg CuCO3·Cu(OH)2,通过这种方案理论上可以制取
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】规范、科学处置废旧锂离子电池具有重要的环保意义和经济价值。废旧锂离子电池的正极材料主要含有 及少量Al、Fe等,处理该废料的一种工艺流程如图所示。
及少量Al、Fe等,处理该废料的一种工艺流程如图所示。

已知:① 难溶于水。
难溶于水。
②相关金属离子形成氢氧化物沉淀的pH如下表所示。
③ 的溶解度(S)随温度(T)的变化曲线如下图所示。
的溶解度(S)随温度(T)的变化曲线如下图所示。

(1)“放电处理”有助于锂元素在正极的回收,电池放电时的总反应为 ,则此时正极的电极反应式为
,则此时正极的电极反应式为_______ 。
(2)“碱溶”所得滤液中大量存在的阴离子为 和
和_______ 。
(3)为提高“酸溶”的速率,可采取的措施有_______ (任写一条)。
(4)“酸溶”过程中所用 的量远高于理论用量,原因为
的量远高于理论用量,原因为_______ ;若用浓盐酸代替 和
和 的混合液,产生的问题是
的混合液,产生的问题是_______ 。
(5)“调pH”时,用氨水调节pH的范围为_______ 。
(6)“沉钴”过程中发生反应的化学方程式为_______ 。
(7)“沉锂”后,洗涤所得 沉淀要使用
沉淀要使用_______ (填“热水”或“冷水”),理由为______ 。
 及少量Al、Fe等,处理该废料的一种工艺流程如图所示。
及少量Al、Fe等,处理该废料的一种工艺流程如图所示。
已知:①
 难溶于水。
难溶于水。②相关金属离子形成氢氧化物沉淀的pH如下表所示。
 |  |  | |
| 开始沉淀的pH | 2.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 3.7 | 9.6 | 9.0 |
 的溶解度(S)随温度(T)的变化曲线如下图所示。
的溶解度(S)随温度(T)的变化曲线如下图所示。
(1)“放电处理”有助于锂元素在正极的回收,电池放电时的总反应为
 ,则此时正极的电极反应式为
,则此时正极的电极反应式为(2)“碱溶”所得滤液中大量存在的阴离子为
 和
和(3)为提高“酸溶”的速率,可采取的措施有
(4)“酸溶”过程中所用
 的量远高于理论用量,原因为
的量远高于理论用量,原因为 和
和 的混合液,产生的问题是
的混合液,产生的问题是(5)“调pH”时,用氨水调节pH的范围为
(6)“沉钴”过程中发生反应的化学方程式为
(7)“沉锂”后,洗涤所得
 沉淀要使用
沉淀要使用
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
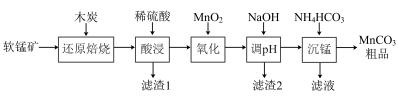
【推荐3】碳酸锰(MnCO3)是制造电信器材的软磁铁氧体,也用作含锰的催化剂,瓷釉、涂料和清漆的颜料等。利用软锰矿(主要成分是MnO2还含有Fe2O3、CaCO3、CuO等杂质)制备碳酸锰的流程如下图所示:
②部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
(1)“还原焙烧”中,MnO2转化为MnO,如果是在实验室中进行该项操作,装软锰矿的仪器名称是___________ 。
(2)滤渣1的主要成分有木炭、___________ 、___________ 。
(3)“调pH”时, pH控制的范围为______ ≤pH<______ 。
(4)“沉锰”时发生反应的离子方程式为___________ ; 此步骤需加热, 温度不能太高也不能太低, 原因是___________ 。
(5) 中存在过氧键(-O-O-),
中存在过氧键(-O-O-),  中S的化合价为
中S的化合价为___________ ;实验室可以用  溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式
溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式___________ 。
(6)在600~700℃下,将一定量的 MnCO3置于空气中加热至恒重,此时测得固体的质量残留率为68.70%,则该反应中固体产物的化学式为___________ 。

②部分阳离子以氢氧化物形式沉淀时溶液的pH范围如下表:
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Cu(OH)2 | Mn(OH)2 |
| 开始沉淀时的 pH | 7.5 | 2.7 | 4.2 | 8.3 |
| 完全沉淀时的pH | 9.7 | 3.7 | 7.4 | 9.8 |
(1)“还原焙烧”中,MnO2转化为MnO,如果是在实验室中进行该项操作,装软锰矿的仪器名称是
(2)滤渣1的主要成分有木炭、
(3)“调pH”时, pH控制的范围为
(4)“沉锰”时发生反应的离子方程式为
(5)
 中存在过氧键(-O-O-),
中存在过氧键(-O-O-),  中S的化合价为
中S的化合价为 溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式
溶液来检验 Mn2+是否完全发生反应,写出对应的离子方程式(6)在600~700℃下,将一定量的 MnCO3置于空气中加热至恒重,此时测得固体的质量残留率为68.70%,则该反应中固体产物的化学式为
您最近一年使用:0次
【推荐1】实验室以工业废渣(主要含CaSO4∙2H2O,还含少量SiO2、Al2O3、FeO、Fe2O3)为原料制取(NH4)2SO4晶体和轻质CaCO3,其实验流程如下:
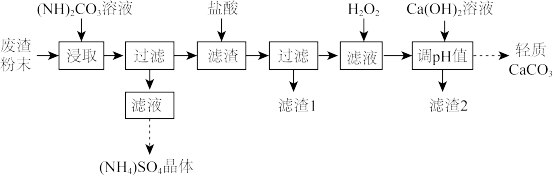
已知:①金属离子形成氢氧化物沉淀的pH范围(pH=8.5时Al(OH)3开始溶解)
②已知常温下,Ksp(CaSO4)=4.8×10-5,Ksp(CaCO3)=3×10-9
回答下列问题:
(1)废渣粉末“浸取”时,主要反应的离子方程式为_____________________________ 。实验时需向(NH4)2CO3溶液中加入适量浓氨水的目的是______________________ 。
(2)废渣粉末“浸取”时,反应温度需控制在60~70℃,合适的加热方式为_________ 。若温度过高将会导致CaSO4的转化率下降,其原因是_______________________ 。
(3)滤渣1成分是_______________ (填化学式)。
(4)加适量H2O2的作用是________________________________ (用离子方程式表示)。“调pH值”除铁和铝时,应调节溶液的pH范围为_________________ 。

已知:①金属离子形成氢氧化物沉淀的pH范围(pH=8.5时Al(OH)3开始溶解)
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ |
| 开始沉淀时pH | 3.4 | 2.7 | 7.6 | 11.3 |
| 完全沉淀时pH | 4.7 | 3.7 | 9.6 | / |
②已知常温下,Ksp(CaSO4)=4.8×10-5,Ksp(CaCO3)=3×10-9
回答下列问题:
(1)废渣粉末“浸取”时,主要反应的离子方程式为
(2)废渣粉末“浸取”时,反应温度需控制在60~70℃,合适的加热方式为
(3)滤渣1成分是
(4)加适量H2O2的作用是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
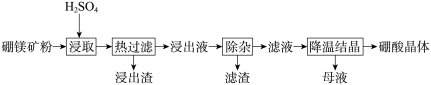
【推荐2】硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(2MgO•B2O3•H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
②298K下,常见金属氢氧化物的溶度积常数如下表:
(1)“浸取”时2MgO•B2O3•H2O发生的反应的化学方程式为___________ 。
(2)“浸取”后,采用“热过滤”的目的是___________ ,“浸出渣”的成分为___________ (填化学式)。
(3)“浸出液”显酸性, “除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是___________ 。
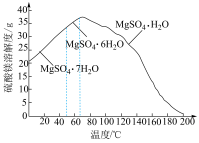
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是___________。
| 温度 |  |  |  |  |
| 溶解度 | 5.0g | 8.7g | 14.8g | 40.2g |
| Fe(OH)3 | Al(OH)3 | Fe(OH)2 | Mg(OH)2 |
 | 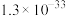 | 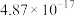 | 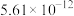 |
(1)“浸取”时2MgO•B2O3•H2O发生的反应的化学方程式为
(2)“浸取”后,采用“热过滤”的目的是
(3)“浸出液”显酸性, “除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4·H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是___________。
| A.升温结晶 | B.降温结晶 | C.加压升温结晶 | D.降压降温结晶 |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】某火电厂收捕到的粉煤灰的主要成分为SiO2、Al2O3、FeO、Fe2O3、MgO、TiO2等。研究小组对其进行综合处理的流程如下:
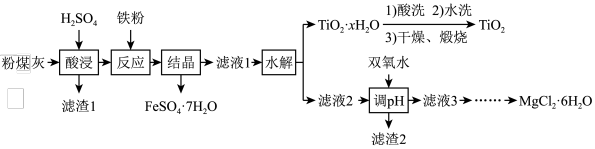
已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO 和一种阳离子。
和一种阳离子。
②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有___________ (任写一种)。
(2)钛元素发生“水解”反应的离子方程式为___________ 。
(3)加入双氧水的目的是___________ 。滤渣2中的成分分别为Al(OH)3和___________ ,Al(OH)3沉淀完全时(溶液中离子浓度小于10−5mol/L),溶液中的c(OH−)为___________ 。
(4)将MgCl2·6H2O制成无水MgCl2时应注意___________ 。
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因___________ 。

已知:①“酸浸”后钛主要以TiOSO4形式存在,强电解质TiOSO4在溶液中仅能电离SO
 和一种阳离子。
和一种阳离子。②常温下,Ksp[Al(OH)3]=8.0×10−35,Ksp[Fe(OH)3]=4.0×10−38,Ksp[Mg(OH)2]=5.61×10−12。
③滤液1中仍有Fe2+剩余
(1)为了提高粉煤灰浸出速率,在“酸浸”时可采取的措施有
(2)钛元素发生“水解”反应的离子方程式为
(3)加入双氧水的目的是
(4)将MgCl2·6H2O制成无水MgCl2时应注意
(5)某同学以石墨为两个电极,电解MgCl2溶液以制取金属镁。你认为他能否获得成功?并用化学方程式解释原因
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】硼酸( )为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含
)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含 、
、 及少量
及少量 、
、 )为原料生产硼酸的工艺流程如下:
)为原料生产硼酸的工艺流程如下:

已知:
① 在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
②有关金属离子开始沉淀和沉淀完全的pH见下表
(1)写出硼元素在周期表中的位置___________ ;
(2)“酸浸”时生成 的化学方程式为
的化学方程式为___________ ;
(3)“热过滤”的目的是___________ ;
(4)“固体1”的主要成分是___________ (写化学式);
(5)从绿色化学角度考虑,试剂A宜选择___________ ,作用是___________ (用离子方程式表示);
(6)“氧化”后将溶液pH调节至6,目的是___________ ;
(7)“母液”中的溶质主要有___________ ,___________ 。
 )为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含
)为白色粉末状结晶,大量用于玻璃工业,可以改善玻璃制品的耐热、透明性能提高机械强度,缩短熔融时间。以硼镁矿(含 、
、 及少量
及少量 、
、 )为原料生产硼酸的工艺流程如下:
)为原料生产硼酸的工艺流程如下:
已知:
①
 在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。
在20℃,40℃,60℃,100℃时溶解度依次为5.0g,8.7g,14.8g,40.2g。②有关金属离子开始沉淀和沉淀完全的pH见下表
 |  |  |  | |
| 开始沉淀时 | 3.8 | 5.8 | 2.2 | 10.6 |
| 完全沉淀时 | 5.2 | 9.7 | 3.2 | 12.4 |
(2)“酸浸”时生成
 的化学方程式为
的化学方程式为(3)“热过滤”的目的是
(4)“固体1”的主要成分是
(5)从绿色化学角度考虑,试剂A宜选择
(6)“氧化”后将溶液pH调节至6,目的是
(7)“母液”中的溶质主要有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】钛白(TiO2)是一种重要的白色颜料和瓷器釉料。以攀枝花钛铁矿(主要含TiO2和FeO,另有少量Fe2O3、MgO、SiO2、Al2O3、CaO、MnO2)为原料制取钛白的工艺流程如下:
②“水解”过程所得偏钛酸H2TiO3(白色)呈两性,也可写作TiO(OH)2。
回答下列问题:
(1)“酸浸”前通常将钛铁矿处理为粒度为150微米左右的矿粉,其目的是___________ 。酸浸时MnO2被还原成Mn2+,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(2)“固相酸解”过程中硫酸浓度和浸出温度对钛、铁浸出率的影响分别如图1、图2所示。根据图示,选用质量分数为___________ 的浓硫酸为宜,温度高于80℃时钛的浸出率显著下降,其原因是___________ 。___________ 的溶液和浸出渣。
(4)“水解”过程若不加入EDTA,得到的偏钛酸呈黄色且形貌不规则,加入EDTA后黄色会消除,则加入EDTA的作用是___________ 。已知Ksp(H2TiO3)=1×10-29,若要让TiO2+水解完全(离子浓度小于1×10-5mol·L-1),应控制pH不低于___________ 。
(5)阳极氧化法制备TiO2纳米管是以钛箔作阳极,氢氟酸作电解质溶液,制备包括两个过程:
①电解使阳极形成TiO2薄膜阻挡层,其电极反应式为___________ ;
②TiO2被HF局部刻蚀生成[TiF6]2-形成大量孔痕,其离子方程式为___________ 。

②“水解”过程所得偏钛酸H2TiO3(白色)呈两性,也可写作TiO(OH)2。
回答下列问题:
(1)“酸浸”前通常将钛铁矿处理为粒度为150微米左右的矿粉,其目的是
(2)“固相酸解”过程中硫酸浓度和浸出温度对钛、铁浸出率的影响分别如图1、图2所示。根据图示,选用质量分数为

(4)“水解”过程若不加入EDTA,得到的偏钛酸呈黄色且形貌不规则,加入EDTA后黄色会消除,则加入EDTA的作用是
(5)阳极氧化法制备TiO2纳米管是以钛箔作阳极,氢氟酸作电解质溶液,制备包括两个过程:
①电解使阳极形成TiO2薄膜阻挡层,其电极反应式为
②TiO2被HF局部刻蚀生成[TiF6]2-形成大量孔痕,其离子方程式为
您最近一年使用:0次




