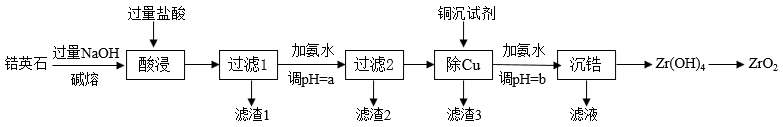
ZrO2是重要的耐高温材料,可用作陶瓷遮光剂和良好的催化剂。天然锆英石(ZrSiO4含有铁、铝、铜等金属元素的氧化物杂质,工业以锆英石为原料制备ZrO2的工艺流程如图:
已知:
①锆英石能与烧碱高温反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表:
(1)锆英石碱熔时需要粉碎,其目的是___ 。
(2)ZrSiO4中Zr的化合价为___ 。滤渣2的主要成分为___ 。
(3)“碱熔”过程中ZrSiO4发生反应的化学方程式___ 。
(4)本流程使用NaCN除铜,若盐酸溶解后溶液中c(Cu2+)=0.01mol∙L-1,当溶液中Cu2+开始沉淀时,c(CN-)=___ 。(已知Ksp[Cu(CN)2]=4×10-10)
(5)向除Cu后所得滤液中加氨水调pH=b,发生的离子方程式为___ 。
(6)过滤时需要用到的玻璃仪器___ 。
(7)由氢氧化锆制备高纯二氧化锆的方法是___ 。

已知:
①锆英石能与烧碱高温反应生成可溶于水的Na2ZrO3,Na2ZrO3与酸反应生成ZrO2+。
②部分离子在实验条件下开始沉淀和完全沉淀时的pH如表:
| 离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀时pH | 1.9 | 3.3 | 6.2 |
| 完全沉淀时pH | 3.2 | 5.2 | 8.0 |
(2)ZrSiO4中Zr的化合价为
(3)“碱熔”过程中ZrSiO4发生反应的化学方程式
(4)本流程使用NaCN除铜,若盐酸溶解后溶液中c(Cu2+)=0.01mol∙L-1,当溶液中Cu2+开始沉淀时,c(CN-)=
(5)向除Cu后所得滤液中加氨水调pH=b,发生的离子方程式为
(6)过滤时需要用到的玻璃仪器
(7)由氢氧化锆制备高纯二氧化锆的方法是
更新时间:2020-11-21 14:36:19
|
相似题推荐
解答题-工业流程题
|
较易
(0.85)
名校
【推荐1】工业上用铝土矿(主要成分为A12O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:

(1)试剂X是_______________ ,过滤操作的主要玻璃仪器有烧杯、漏斗、_____ 。为了提高经济效益,滤渣还可以用来________ (写一种)。
(2)写出反应②的离子方程式__________________ 。
(3)工业上还可以用提取到的Al2O3为原料,与焦炭、氯气加热制备无水氯化铝,当生成1molAlCl3时消耗0.75mol焦炭,写出发生反应的化学方程式_____________ 。

(1)试剂X是
(2)写出反应②的离子方程式
(3)工业上还可以用提取到的Al2O3为原料,与焦炭、氯气加热制备无水氯化铝,当生成1molAlCl3时消耗0.75mol焦炭,写出发生反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】铝元素在自然界中主要存在于铝土矿(主要成分为Al2O3,还含有Fe2O3、FeO、SiO2)中。工业上用铝土矿制备铝的某种化合物的工艺流程如下。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的操作方法为:____ 。
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为___________ (填选项编号)。
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、___________ (填操作名称)、过滤、洗涤。
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填选项编号)。

(1)在滤液A中加入漂白液,目的是氧化除铁,所得滤液B显酸性。
①检验滤液B中是否还含有铁元素的操作方法为:
②将滤液B中的铝元素以沉淀形式析出,可选用的最好试剂为
a.氢氧化钠溶液 b.硫酸溶液 c.氨水 d.二氧化碳
③由滤液B制备氯化铝晶体涉及的操作为:边滴加浓盐酸边蒸发浓缩、
(2)SiO2和NaOH焙烧制备硅酸钠,可采用的装置为___________(填选项编号)。
A. | B. | C. | D. |
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】以高硫铝土矿(主要成分为Al2O3、Fe2O3、SiO2,少量FeS2和金属硫酸盐)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如下

已知矿粉焙烧过程中FeS2与O2反应生成Fe2O3和SO2
(1)工业上为了加快“碱浸速率,可采取的措施有:__________________ (任写2点);
“碱浸”时涉及硅元素的化学反应方程式为:________________________________ 。
(2)向“过滤”得到的滤液中通入过量CO2后,铝元素存在的形式为化学式___________ (填化学式 )。“过滤”操作需要用到的玻璃仪器有:烧杯、_________ 、________ 。
(3)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,“焙烧”过程理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=___________________ 。
(4)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于600℃硫去除率=(1- )×100%
)×100%

700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是______________________________________ 。

已知矿粉焙烧过程中FeS2与O2反应生成Fe2O3和SO2
(1)工业上为了加快“碱浸速率,可采取的措施有:
“碱浸”时涉及硅元素的化学反应方程式为:
(2)向“过滤”得到的滤液中通入过量CO2后,铝元素存在的形式为化学式
(3)“过滤”得到的滤渣中含大量的Fe2O3。Fe2O3与FeS2混合后在缺氧条件下焙烧生成Fe3O4和SO2,“焙烧”过程理论上完全反应消耗的n(FeS2)∶n(Fe2O3)=
(4)添加1%CaO和不添加CaO的矿粉焙烧,其硫去除率随温度变化曲线如图所示。
已知:多数金属硫酸盐的分解温度都高于600℃硫去除率=(1-
 )×100%
)×100%
700℃焙烧时,添加1%CaO的矿粉硫去除率比不添加CaO的矿粉硫去除率低,其主要原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】钕铁硼(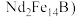 磁铁因其超强的磁性被誉为“永磁之王”,已知某钕铁硼废料中主要成分为
磁铁因其超强的磁性被誉为“永磁之王”,已知某钕铁硼废料中主要成分为 等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物,一种利用钕铁硼废料制取
等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物,一种利用钕铁硼废料制取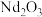 和
和 的工艺流程如图所示:
的工艺流程如图所示: 价;
价;
②某些金属氢氧化物沉淀完全(离子浓度 )时的
)时的 如表所示:
如表所示:
回答下列问题:
(1)钕铁硼废料“浸出”前需“预处理”,粉碎后,再除去表面的矿物油污,除去矿物油污可以选择的试剂是___________(填选项字母)。
(2)“滤渣2”为 ,写出其在空气中“煅烧”的化学方程式:
,写出其在空气中“煅烧”的化学方程式:___________ .
(3)“滤渣3”的主要成分是___________ (填化学式);在“萃取”步骤中假设萃取前调节 ,有机萃取剂用
,有机萃取剂用 表示,发生萃取的反应可表示为
表示,发生萃取的反应可表示为 ,若
,若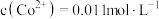 ,多次萃取后水相中的
,多次萃取后水相中的 ,则钴的萃取率为
,则钴的萃取率为______ (结果保留小数点后一位,溶液体积变化忽略不计)。
(4)若溶液中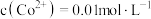 ,加入试剂2调节
,加入试剂2调节 的范围是
的范围是___________ (忽略过程中溶液体积变化);假设“滤液1”步骤中加入的试剂有 ,当
,当 6时,处理铁的离子方程式为
6时,处理铁的离子方程式为___________ 。
(5)在“沉钴”过程中生成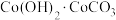 的离子方程式为
的离子方程式为___________ 。
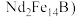 磁铁因其超强的磁性被誉为“永磁之王”,已知某钕铁硼废料中主要成分为
磁铁因其超强的磁性被誉为“永磁之王”,已知某钕铁硼废料中主要成分为 等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物,一种利用钕铁硼废料制取
等金属单质,还含有不溶于水和盐酸的硼、硅酸盐及硫化物,一种利用钕铁硼废料制取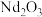 和
和 的工艺流程如图所示:
的工艺流程如图所示:
 价;
价;②某些金属氢氧化物沉淀完全(离子浓度
 )时的
)时的 如表所示:
如表所示:| 沉淀 |  |  |  |  |  |  |
沉淀完全时的 | 5.2 | 3.2 | 9.4 | 9.5 | 10.1 | 8.5 |
(1)钕铁硼废料“浸出”前需“预处理”,粉碎后,再除去表面的矿物油污,除去矿物油污可以选择的试剂是___________(填选项字母)。
| A.纯碱溶液 | B. 溶液 溶液 | C.苯 | D.稀硫酸 |
(2)“滤渣2”为
 ,写出其在空气中“煅烧”的化学方程式:
,写出其在空气中“煅烧”的化学方程式:(3)“滤渣3”的主要成分是
 ,有机萃取剂用
,有机萃取剂用 表示,发生萃取的反应可表示为
表示,发生萃取的反应可表示为 ,若
,若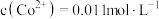 ,多次萃取后水相中的
,多次萃取后水相中的 ,则钴的萃取率为
,则钴的萃取率为(4)若溶液中
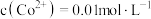 ,加入试剂2调节
,加入试剂2调节 的范围是
的范围是 ,当
,当 6时,处理铁的离子方程式为
6时,处理铁的离子方程式为(5)在“沉钴”过程中生成
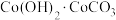 的离子方程式为
的离子方程式为
您最近一年使用:0次
【推荐2】工业废水中常含有一定量的Cr2O 和CrO
和CrO ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法。该法的工艺流程为:CrO
 Cr2O
Cr2O
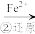 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓
(1)流程第①步存在平衡:2 CrO +2H+⇌ Cr2O
+2H+⇌ Cr2O +H2O,能说明第①步反应达平衡状态的是
+H2O,能说明第①步反应达平衡状态的是_____ 。(填序号)
A.Cr2O 和CrO
和CrO 的浓度相同 B.2v Cr2O
的浓度相同 B.2v Cr2O =v CrO
=v CrO C.溶液的颜色不变
C.溶液的颜色不变
(2)流程第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L时溶液的pH为_____ 。
方法2:电解法
该法用Fe做电极电解含Cr2O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。请用电极反应方程式解释下列原因:
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。请用电极反应方程式解释下列原因:
(3)用Fe做电极的原因是_____ ,在阴极附近溶液pH升高的原因是_____ 。
 和CrO
和CrO ,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。
,它们会对人类及生态系统产生很大的伤害,必须进行处理。常用的处理方法有两种。方法1:还原沉淀法。该法的工艺流程为:CrO

 Cr2O
Cr2O
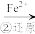 Cr3+
Cr3+ Cr(OH)3↓
Cr(OH)3↓(1)流程第①步存在平衡:2 CrO
 +2H+⇌ Cr2O
+2H+⇌ Cr2O +H2O,能说明第①步反应达平衡状态的是
+H2O,能说明第①步反应达平衡状态的是A.Cr2O
 和CrO
和CrO 的浓度相同 B.2v Cr2O
的浓度相同 B.2v Cr2O =v CrO
=v CrO C.溶液的颜色不变
C.溶液的颜色不变(2)流程第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L时溶液的pH为
方法2:电解法
该法用Fe做电极电解含Cr2O
 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。请用电极反应方程式解释下列原因:
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。请用电极反应方程式解释下列原因:(3)用Fe做电极的原因是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐3】金属钴是一种非常稀缺的金属之一,具有耐高温、高压的特性,可应用于催化剂。电池方面,电子设备和航空设备中。某钴矿石的主要成分包括 、
、 、
、 和
和 。由该矿石制
。由该矿石制 固体的方法如图(部分分离操作省略):
固体的方法如图(部分分离操作省略):
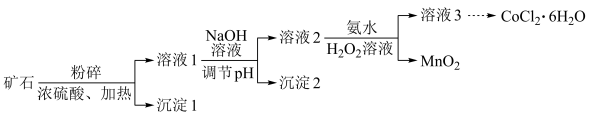
资料:25℃时有关金属离子沉淀的相关PH见下表
(1)上述矿石溶解过程中,粉碎的目的是___________ 。
(2) 溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括
溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括 、
、 和
和___________ 。
(3)沉淀2是___________ ,此时调节溶液的pH范围是___________ 。
(4)①已知:当c(Co2+)≤1×10-5mol/L时可认为 完全沉淀,则
完全沉淀,则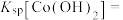
___________ 。
②溶液2中加入氨水和 溶液,发生反应的离子方程式为:
溶液,发生反应的离子方程式为:___________ 。
(5)溶液3中加入 溶液生成
溶液生成 沉淀,沉淀剂若选择
沉淀,沉淀剂若选择 ,所得到的沉淀中可能会混有
,所得到的沉淀中可能会混有___________ 。
 、
、 、
、 和
和 。由该矿石制
。由该矿石制 固体的方法如图(部分分离操作省略):
固体的方法如图(部分分离操作省略):
资料:25℃时有关金属离子沉淀的相关PH见下表
| 离子 |  |  |  |
| 开始沉淀时的PH | 1.9 | 7.15 | 8.2 |
| 沉淀完全时的PH | 2.8 | 9.15 | 10.2 |
(1)上述矿石溶解过程中,粉碎的目的是
(2)
 溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括
溶于浓硫酸是非氧化还原反应,溶液1中阳离子包括 、
、 和
和(3)沉淀2是
(4)①已知:当c(Co2+)≤1×10-5mol/L时可认为
 完全沉淀,则
完全沉淀,则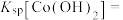
②溶液2中加入氨水和
 溶液,发生反应的离子方程式为:
溶液,发生反应的离子方程式为:(5)溶液3中加入
 溶液生成
溶液生成 沉淀,沉淀剂若选择
沉淀,沉淀剂若选择 ,所得到的沉淀中可能会混有
,所得到的沉淀中可能会混有
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】某工厂用废铜铁合金制取生产油漆的颜料铁红(Fe2O3),并回收铜的流程如下:
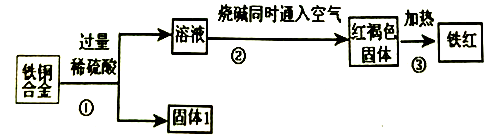
完成下列问题:
(1) 上述三个过程中发生了氧化还原反应的是____________ (填符号①②③)。
(2) 固体1的名称______ ;红褐色固体的化学式______ 。
(3) 写出整个②过程发生反应的离子方程式:______ ;______ ;______ 。

完成下列问题:
(1) 上述三个过程中发生了氧化还原反应的是
(2) 固体1的名称
(3) 写出整个②过程发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】硫代硫酸钠是一种重要的化工产品,易溶于水,在酸性环境中易分解,溶解度随温度升高显著增大,其稀溶液与BaCl2溶液混合无沉淀生成。工业上可用2Na2S+Na2CO3+4SO2=3Na2S2O3+CO2制得。某兴趣小组利用如图装置拟制备 (Na2S2O3∙5H2O)。
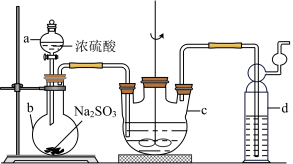
回答下列问题。
(1)仪器a的名称是_______ ,d中的试剂是_______ (填编号)。
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)Na2SO3(aq)裸露在空气中易变质,检验其已经变质的实验操作是:_______ 。
(3)实验过程中,三颈烧瓶中的澄清溶液先变浑浊,后变澄清时生成大量的 一段时间后,再次出现少量浑浊,此时须立刻停止通入
一段时间后,再次出现少量浑浊,此时须立刻停止通入 。为了保证Na2S2O3∙5H2O的产量,实验中通入的SO2不能过量,原因是
。为了保证Na2S2O3∙5H2O的产量,实验中通入的SO2不能过量,原因是_______ 。
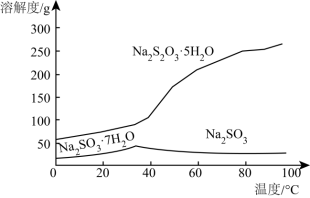
(4)实际工业生产中制得的 溶液中常混有少量
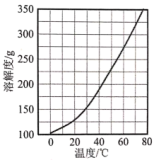
溶液中常混有少量 ,结合溶解度曲线(下图),获得
,结合溶解度曲线(下图),获得 ·
· 的操作是
的操作是_______ 。
(5)为了测定产品纯度。以淀粉作指示剂,通过用碘标准溶液滴定Na2S2O3∙5H2O产品配制的溶液,计算Na2S2O3∙5H2O含量。
①滴定前,有关滴定管的正确操作顺序为 (填编号):检查活塞是否漏水→蒸馏水洗涤→_______→_______→_______→_______→_______ →开始滴定
A.装入滴定液至零刻度以上 B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡 D.用滴定液润洗2至3次 E.记录起始读数
②判断滴定反应达到终点现象是:当加入最后一滴碘标准溶液,锥形瓶内液体_______ ,且半分钟内部恢复原色。

回答下列问题。
(1)仪器a的名称是
A.稀H2SO4 B.NaOH溶液 C.饱和NaHSO3溶液
(2)Na2SO3(aq)裸露在空气中易变质,检验其已经变质的实验操作是:
(3)实验过程中,三颈烧瓶中的澄清溶液先变浑浊,后变澄清时生成大量的
 一段时间后,再次出现少量浑浊,此时须立刻停止通入
一段时间后,再次出现少量浑浊,此时须立刻停止通入 。为了保证Na2S2O3∙5H2O的产量,实验中通入的SO2不能过量,原因是
。为了保证Na2S2O3∙5H2O的产量,实验中通入的SO2不能过量,原因是(4)实际工业生产中制得的
 溶液中常混有少量
溶液中常混有少量 ,结合溶解度曲线(下图),获得
,结合溶解度曲线(下图),获得 ·
· 的操作是
的操作是
(5)为了测定产品纯度。以淀粉作指示剂,通过用碘标准溶液滴定Na2S2O3∙5H2O产品配制的溶液,计算Na2S2O3∙5H2O含量。
①滴定前,有关滴定管的正确操作顺序为 (填编号):检查活塞是否漏水→蒸馏水洗涤→_______→_______→_______→_______→_____
A.装入滴定液至零刻度以上 B.调整滴定液液面至零刻度或零刻度以下
C.排除气泡 D.用滴定液润洗2至3次 E.记录起始读数
②判断滴定反应达到终点现象是:当加入最后一滴碘标准溶液,锥形瓶内液体
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】某学生欲用下列装置制取纯净的 固体。其中
固体。其中 是
是 发生装置,
发生装置, 为气体净化装置,
为气体净化装置, 硬质玻璃管中装有细铁丝网,
硬质玻璃管中装有细铁丝网, 为干燥的空广口瓶,烧杯
为干燥的空广口瓶,烧杯 为尾气吸收装置。
为尾气吸收装置。

试回答:
(1)该装置中的一处明显错误是___________ 。
(2)D中所装试剂为___________ ,C装置的作用是___________ 。
(3)A中发生反应的化学方程式是___________ 。G中发生反应的离子方程式是___________ 。
(4)若用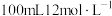 盐酸跟足量
盐酸跟足量 充分反应,生成的
充分反应,生成的 体积(标准状况)
体积(标准状况)___________ (填“大于”“小于”或“等于”) 。
。
(5)若用所制取的 固体制成
固体制成 胶体,
胶体, 胶体分散质粒子
胶体分散质粒子___________ (填“能”或“不能”)通过滤纸孔隙;在 胶体中逐滴加入稀盐酸,现象是
胶体中逐滴加入稀盐酸,现象是___________ 。
 固体。其中
固体。其中 是
是 发生装置,
发生装置, 为气体净化装置,
为气体净化装置, 硬质玻璃管中装有细铁丝网,
硬质玻璃管中装有细铁丝网, 为干燥的空广口瓶,烧杯
为干燥的空广口瓶,烧杯 为尾气吸收装置。
为尾气吸收装置。
试回答:
(1)该装置中的一处明显错误是
(2)D中所装试剂为
(3)A中发生反应的化学方程式是
(4)若用
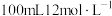 盐酸跟足量
盐酸跟足量 充分反应,生成的
充分反应,生成的 体积(标准状况)
体积(标准状况) 。
。(5)若用所制取的
 固体制成
固体制成 胶体,
胶体, 胶体分散质粒子
胶体分散质粒子 胶体中逐滴加入稀盐酸,现象是
胶体中逐滴加入稀盐酸,现象是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐2】我国化学家侯德榜发明了联合制碱法,对世界制碱工业做出了巨大贡献。联合制碱法的主要过程如下(部分物质已略去)。

已知:
①氨气极易溶于水,1体积水可溶解800体积氨气。
②几种盐的溶解度。
(1)写出过程①的化学方程式___________ 。原料有两种气体,应先通入___________ (填“ ”或“
”或“ ”),原因是
”),原因是__________________ 。
(2)操作①中析出 的原因是
的原因是___________ 。
a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)制取的碱固体中还混有小苏打,如何除去杂质,写出化学方程式___________________ 。
(4)“侯氏制碱法”中除水外,能够循环利用的物质是___________ (填化学式)。
(5)检验产品碳酸钠中含有氯化钠,请你把以下实验方案补充完整:
操作:取少量试样溶于水中,再滴加___________ 。
现象:___________ 。

已知:
①氨气极易溶于水,1体积水可溶解800体积氨气。
②几种盐的溶解度。
| 物质 | NaCl |  |  |  |
| 溶解度 | 36.0 | 21.7 | 9.6 | 37.2 |
(1)写出过程①的化学方程式
 ”或“
”或“ ”),原因是
”),原因是(2)操作①中析出
 的原因是
的原因是a.碳酸氢钠难溶于水
b.碳酸氢钠受热易分解
c.碳酸氢钠的溶解度相对较小,所以在溶液中首先结晶析出
(3)制取的碱固体中还混有小苏打,如何除去杂质,写出化学方程式
(4)“侯氏制碱法”中除水外,能够循环利用的物质是
(5)检验产品碳酸钠中含有氯化钠,请你把以下实验方案补充完整:
操作:取少量试样溶于水中,再滴加
现象:
您最近一年使用:0次
【推荐3】钴酸锂(LiCoO2)电池是一种应用广泛的新型电源,已知:①钴酸锂(LiCoO2)电池中还含有铝箔、石墨、塑料等,②在酸性溶液中LiCoO2的氧化性强于H2O2。利用如图工艺流程回收废旧电池中的金属资源。
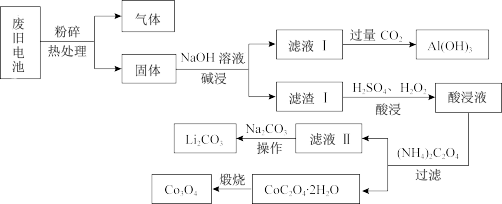
(1)粉碎废旧电池后热处理可以除去_______ (填物质的名称)。
(2)用硫酸酸浸时要控制温度为80℃,原因是_______ ,写出酸浸时发生的主要氧化还原反应的化学方程式_______ 。
(3)在空气中煅烧二水合草酸钴需要用到的仪器是_______ (填字母)。
A.蒸发皿 B.玻璃棒 C.烧杯 D. 瓷坩埚
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见表。为了减少碳酸锂的损失,图中“操作”应为蒸发结晶、__________ ,90℃时Ksp(Li2CO3)的值为______ 。

(1)粉碎废旧电池后热处理可以除去
(2)用硫酸酸浸时要控制温度为80℃,原因是
(3)在空气中煅烧二水合草酸钴需要用到的仪器是
A.蒸发皿 B.玻璃棒 C.烧杯 D. 瓷坩埚
(4)已知Li2CO3微溶于水,其饱和溶液的浓度与温度关系见表。为了减少碳酸锂的损失,图中“操作”应为蒸发结晶、
| 温度/℃ | 10 | 30 | 60 | 90 |
| 浓度/mol·L-1 | 0.21 | 0.17 | 0.14 | 0.10 |
您最近一年使用:0次