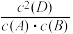在温度为T1条件下,在三个容积均为1L的恒容密闭容器中仅发生反应: ,实验测得:
,实验测得: ,
, 。
。
已知: 为速率常数,仅受温度的影响。下列说法正确的是
为速率常数,仅受温度的影响。下列说法正确的是
 ,实验测得:
,实验测得: ,
, 。
。| 容器编号 | 起始浓度/(mol/L) | 平衡浓度/(mol/L) | ||
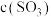 | 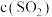 | 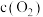 | 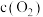 | |
| Ⅰ | 0.6 | 0 | 0 | 0.2 |
| Ⅱ | 0.3 | 0.5 | 0.2 | |
| Ⅲ | 0 | 0.5 | 0.35 | |
 为速率常数,仅受温度的影响。下列说法正确的是
为速率常数,仅受温度的影响。下列说法正确的是| A.T1时,该反应的平衡常数的值为1 |
B.容器Ⅱ初始状态时,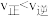 |
C.当温度改变为T2时,若 ,则 ,则 |
D.容器Ⅲ中达到平衡时, |
更新时间:2022-06-30 22:04:28
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】反应N2O4(g) 2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
2NO2(g)在温度为T1、T2(T1<T2)时达到平衡,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.A、C两点的反应速率:A>C |
| B.B、C两点的气体的平均相对分子质量:B<C |
| C.A、C两点气体的颜色:A浅,C深 |
| D.保持容器体积不变,再充入NO2气体,NO2的体积分数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
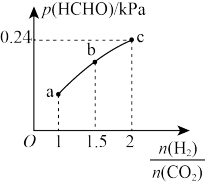
【推荐2】在T℃时,向容积为2L的恒容密闭容器中充入1molCO2和一定量的H2发生反应:CO2(g)+2H2(g)⇌HCHO(g)+H2O(g) ;∆H<0,若起始时容器内气体压强为1.2 kPa,达到平衡时,HCHO的分压与起始的 关系如图所示:下列说法不正确的是
关系如图所示:下列说法不正确的是
 关系如图所示:下列说法不正确的是
关系如图所示:下列说法不正确的是
| A.b点的化学平衡常数KP≈3.5 |
| B.容器内H2O的体积分数保持不变,说明达到平衡状态 |
C.若5min到达c点,则v(H2)= 0.24mol L-1 L-1 min-1 min-1 |
| D.c点时,再加入CO2(g)和H2O(g),使二者分压均增大0.05 kPa,α(H2)增大 |
您最近一年使用:0次
【推荐3】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:CH3OH(g)+CO(g) CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是
 CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是| 容器编号 | 温度(K) | 起始物质的量(mol) | 平衡时CH3COOH的物质的量(mol) | 平衡常数 | ||
| n(CH3OH) | n (CO) | n (CH3COOH) | ||||
| Ⅰ | 530 | 0.05 | 0.05 | 0 | 0.025 | K1 |
| Ⅱ | 530 | 0.03 | 0.03 | 0.006 | K2 | |
| Ⅲ | 510 | 0 | 0 | 0.05 | K3 | |
| A.达平衡时,容器Ⅰ中平衡常数K1 =40 |
| B.达平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小 |
| C.达平街时,容器Ⅰ中CH3OH转化率与容器Ⅲ中CH3COOH转化率之和小于1 |
| D.K1>K2>K3 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在一定温度下,将气体X与气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X( g)+Y( g)⇌2Z(g)△H<0,一段时间后达到平衡.反应过程中测定的数据如表:下列说法正确的是( )
| t∕min | 2 | 4 | 7 | 9 |
| n(Y)∕mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A.反应前4min的平均反应速率υ(Z)=0.0125mol•L-1•min-1 |
| B.其他条件不变,降低温度,反应达到新平衡前υ(逆)>υ(正) |
| C.其他条件不变,再向体系中冲入1L氦气,使体系压强增大,则υ(逆)与υ(正)同等程度增大 |
| D.该温度下此反应的平衡常数K=1.44 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表:
下列说法正确的是
 时,向容积为2L的恒容密闭容器中充入一定量的CO和
时,向容积为2L的恒容密闭容器中充入一定量的CO和 ,发生如下反应:
,发生如下反应: 。反应过程中测定的部分数据见下表:
。反应过程中测定的部分数据见下表: 反应时间 | 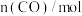 | 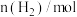 |
| 0 | 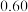 | 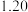 |
| 20 | 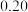 | |
| 30 |  |
A.反应在 内的平均速率为 内的平均速率为 |
B.保持其他条件不变,升高温度,平衡时 ,则反应的 ,则反应的 |
C.保持其他条件不变,再向平衡体系中同时通入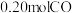 、 、 、 、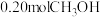 ,达到新平衡前 ,达到新平衡前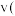 正 正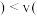 逆 逆 |
D.相同温度下,若起始时向容器中充入 ,达到平衡时 ,达到平衡时 转化率大于 转化率大于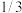 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在盛有足量A的体积可变的密闭容器中,保持压强一定,加入B,发生反应:A(s)+2B(g) 4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
 4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是
4C(g)+D(g);△H<0.在一定温度、压强下达到平衡。平衡时C的物质的量与加入的B的物质的量的变化关系如图.下列说法正确的是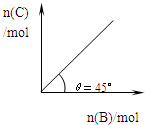
| A.当温度升高后,则图中θ>45° |
| B.平衡时B的转化率为50% |
| C.若保持温度压强不变,再加入B,则平衡后正、逆反应速率均逐渐增大 |
| D.若保持温度压强不变,再加入B,则平衡后反应体系气体密度减小 |
您最近一年使用:0次
【推荐2】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s) 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如表所示,已知Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,下列说法正确的是| 压强/MPa 体积分数/% 温度/℃ | 1.0 | 2.0 | 3.0 |
| 810 | 54.0 | a | b |
| 915 | c | 75.0 | d |
| 1000 | e | f | 83.0 |
| A.b>f |
| B.平衡常数K(1000℃)<K(810℃) |
| C.915℃、2.0MPa该反应的平衡常数为Kp=4.5MPa |
| D.1000℃、3.0MPa时E的转化率为83% |
您最近一年使用:0次

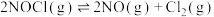 。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是
。反应tmin后,三个容器中NOCl的转化率如图中A、B、C三点。下列叙述正确的是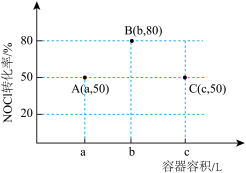
 C(s)+xD(g)
C(s)+xD(g)