以软锰矿(含 和少量
和少量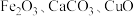 )和辉铜矿(含
)和辉铜矿(含 和少量
和少量 、
、 )为原料生产高纯
)为原料生产高纯 和
和 的工艺流程如下:
的工艺流程如下:
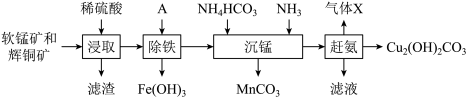
已知有关金属离子形成氢氧化物沉淀的pH范围如下:
(1)“浸取”所得滤渣经 提取后可获得一种淡黄色副产品,则滤渣的主要成分是
提取后可获得一种淡黄色副产品,则滤渣的主要成分是_______ (填化学式)。浸取时,发生主要反应的离子方程式为_______ 。
(2)试剂A最好选用_______ (填序号),其调节溶液pH的范围是_______ 。
A.氨水 B.CuO C.NaOH
(3)上述流程中可循环利用的物质是_______ 。除铁后检验溶液中是否含有 的试剂名称是
的试剂名称是_______ ;研究发现,若软锰矿和辉铜矿中不含 ,浸取速率明显变慢,浸取速率明显变慢的可能原因除了
,浸取速率明显变慢,浸取速率明显变慢的可能原因除了 有氧化性外,还可能是
有氧化性外,还可能是_______ 。
(4)“沉锰”所得溶液中铜元素主要以 形式存在,则生成
形式存在,则生成 的离子方程式是
的离子方程式是_______ 。
 和少量
和少量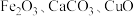 )和辉铜矿(含
)和辉铜矿(含 和少量
和少量 、
、 )为原料生产高纯
)为原料生产高纯 和
和 的工艺流程如下:
的工艺流程如下:
已知有关金属离子形成氢氧化物沉淀的pH范围如下:
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 7.5 | 2.7 | 5.6 | 8.3 |
| 沉淀完全的pH | 9.0 | 3.7 | 6.7 | 9.8 |
 提取后可获得一种淡黄色副产品,则滤渣的主要成分是
提取后可获得一种淡黄色副产品,则滤渣的主要成分是(2)试剂A最好选用
A.氨水 B.CuO C.NaOH
(3)上述流程中可循环利用的物质是
 的试剂名称是
的试剂名称是 ,浸取速率明显变慢,浸取速率明显变慢的可能原因除了
,浸取速率明显变慢,浸取速率明显变慢的可能原因除了 有氧化性外,还可能是
有氧化性外,还可能是(4)“沉锰”所得溶液中铜元素主要以
 形式存在,则生成
形式存在,则生成 的离子方程式是
的离子方程式是
更新时间:2022-07-12 20:45:31
|
相似题推荐
【推荐1】某小组同学探究Cu和H2O2的反应,进行如下实验。
实验ⅰ:向装有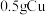 的烧杯中加入
的烧杯中加入 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
(1)蓝色固体是_______ (填化学式)。
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料: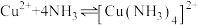 (深蓝色)
(深蓝色)
(2)实验中ⅱ:溶液变蓝的原因是_______ (用化学用语解释)。
(3)实验ⅲ中:
①深蓝色溶液含有 ,其中提供空轨道的微粒是
,其中提供空轨道的微粒是_______ ,提供孤电子对的原子是_______ 。
②对比实验ⅰ和ⅲ,为探究氨水对 的还原性或
的还原性或 氧化性的影响,利用下图装置继续实验。
氧化性的影响,利用下图装置继续实验。
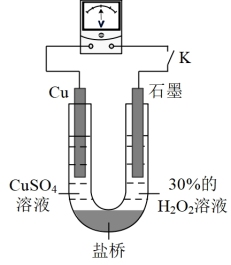
已知:电压大小反映了物质氧化性与还原性强弱的差异;差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论是_______ ,结合化学用语解释c中电压增大的原因_______ 。利用该方法也可证明酸性增强可提高 的氧化性,导致
的氧化性,导致 溶解速率加快。
溶解速率加快。
(4)对比实验ii和iii,实验iii中产生氧气速率明显更快,可能的原因是_______ 。
(5)基于以上实验,影响Cu与 反应速率的因素有
反应速率的因素有_______ 。
实验ⅰ:向装有
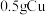 的烧杯中加入
的烧杯中加入 溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。
溶液,一段时间内无明显现象,10小时后,溶液中有少量蓝色浑浊,Cu片表面附着少量蓝色固体。(1)蓝色固体是
针对该反应速率较慢,小组同学查阅资料,设计并完成了下列实验。
资料:
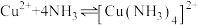 (深蓝色)
(深蓝色)| 装置 | 序号 | 试剂a | 现象 |
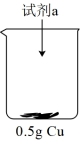 | ⅱ |  与 与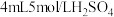 混合液 混合液 |  表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 表面很快生产少量气泡,溶液逐渐变蓝,产生较多气泡 |
| ⅲ |  与 与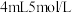 氨水混合液 氨水混合液 | 溶液立即变为深蓝色,产生大量气泡, 表面有少量蓝色不溶物 表面有少量蓝色不溶物 |
(3)实验ⅲ中:
①深蓝色溶液含有
 ,其中提供空轨道的微粒是
,其中提供空轨道的微粒是②对比实验ⅰ和ⅲ,为探究氨水对
 的还原性或
的还原性或 氧化性的影响,利用下图装置继续实验。
氧化性的影响,利用下图装置继续实验。
已知:电压大小反映了物质氧化性与还原性强弱的差异;差异越大,电压越大
a.K闭合时,电压为x。
b.向U型管右侧溶液中滴加氨水后,电压不变。
c.继续向U型管左侧溶液中滴加氨水后,电压增大了y。
该实验的结论是
 的氧化性,导致
的氧化性,导致 溶解速率加快。
溶解速率加快。(4)对比实验ii和iii,实验iii中产生氧气速率明显更快,可能的原因是
(5)基于以上实验,影响Cu与
 反应速率的因素有
反应速率的因素有
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】综合利用CO2和CO是科学家研究的热点课题。
(1)CO用于处理大气污染物N2O所发生的反应为:CO(g)+N2O(g)⇌ CO2(g)+N2(g) 。几种物质的相对能量如表:
。几种物质的相对能量如表:
①
_______  。
。
②有人提出上述反应可以用“Fe+”作催化剂。其总反应分两步进行:
第一步: ;
;
第二步:_______ (写化学方程式)。
第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应活化能_______ 第一步反应活化能(填“大于”“小于”或“等于”)。
(2)在实验室采用 测定空气中CO的含量。在密闭容器中充入足量的
测定空气中CO的含量。在密闭容器中充入足量的 粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:

①相对曲线a,曲线b仅改变一个条件,改变的条件可能是_______ 。
②在此温度下,该可逆反应的平衡常数
_______ (用含x的代数式表示)。
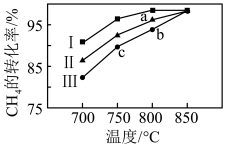
(3)CH4超干重整CO2技术可得到富含CO的化工原料。反应为CH4(g)+CO2(g)⇌ 2CO(g)+2H2(g) =−49.0 kJ·mol−1
=−49.0 kJ·mol−1
其他条件不变,在不同催化剂(I、II、III)作用下,反应进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态_______ (填“是”或“不是”)平衡状态;b点CH4的转化率高于c点,原因是_______ 。
(1)CO用于处理大气污染物N2O所发生的反应为:CO(g)+N2O(g)⇌ CO2(g)+N2(g)
 。几种物质的相对能量如表:
。几种物质的相对能量如表:| 物质 |  | 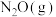 |  |  |
相对能量( ) ) | 283 | 475.5 | 0 | 393.5 |

 。
。②有人提出上述反应可以用“Fe+”作催化剂。其总反应分两步进行:
第一步:
 ;
;第二步:
第二步反应不影响总反应达到平衡所用时间,由此推知,第二步反应活化能
(2)在实验室采用
 测定空气中CO的含量。在密闭容器中充入足量的
测定空气中CO的含量。在密闭容器中充入足量的 粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
粉末和一定量的CO,发生反应:I2O5(s)+5CO(g)⇌ 5CO2(g)+I2(s)。测得CO的转化率如图所示:
①相对曲线a,曲线b仅改变一个条件,改变的条件可能是
②在此温度下,该可逆反应的平衡常数

(3)CH4超干重整CO2技术可得到富含CO的化工原料。反应为CH4(g)+CO2(g)⇌ 2CO(g)+2H2(g)
 =−49.0 kJ·mol−1
=−49.0 kJ·mol−1其他条件不变,在不同催化剂(I、II、III)作用下,反应进行相同时间后,CH4的转化率随反应温度的变化如图所示。a点所代表的状态

您最近一年使用:0次
【推荐3】我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g) C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1
③2CO(g) CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1
反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=____ kJ•mol-1。
(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图1所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为_____ 。

(3)CO2的电化学催化还原具有条件温和、对环境友好的优点。Cu对CO2的电还原有一定的催化作用。在0.1mol•L-1CuSO4/H2SO4溶液中,改变沉积时间,进行恒电位沉积制备纳米Cu电极。图2是根据不同沉积时间制备的纳米Cu电极的循环伏安曲线作出的CO2的还原峰电流(峰电流越大,表明纳米Cu电极催化效果越好)与沉积时间的关系图,沉积时间超过50s,进一步延长沉积时间,纳米Cu电极催化效果减弱的原因是____ 。

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为____ mol•L-1。
[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
(5)章根强课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoⅡ表示),测试结果表明,该CoⅡ在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoⅡ/CoI反应路径(如图3)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoⅡ供激发电子将CoⅡ还原为CoI,_____ 。(结合图示,描述CO2还原为CO的过程)

(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g)
 C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1③2CO(g)
 CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图1所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为

(3)CO2的电化学催化还原具有条件温和、对环境友好的优点。Cu对CO2的电还原有一定的催化作用。在0.1mol•L-1CuSO4/H2SO4溶液中,改变沉积时间,进行恒电位沉积制备纳米Cu电极。图2是根据不同沉积时间制备的纳米Cu电极的循环伏安曲线作出的CO2的还原峰电流(峰电流越大,表明纳米Cu电极催化效果越好)与沉积时间的关系图,沉积时间超过50s,进一步延长沉积时间,纳米Cu电极催化效果减弱的原因是

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为
[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
(5)章根强课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoⅡ表示),测试结果表明,该CoⅡ在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoⅡ/CoI反应路径(如图3)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoⅡ供激发电子将CoⅡ还原为CoI,

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐1】难溶性杂岗石 (K2SO4·MgSO4·2CaSO4·2H2O) 在水中在如下平衡: K2SO4·MgSO4·2CaSO4·2H2O(s) =2Ca2++ 2K++ Mg2++4SO +2H2O采用饱和Ca(OH)2溶液浸杂卤石制备 K2SO4工艺流程如下:
+2H2O采用饱和Ca(OH)2溶液浸杂卤石制备 K2SO4工艺流程如下:
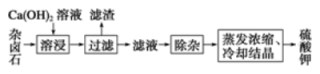
回答下列问题:
(1)滤渣的主要成分有___________ 和___________ 以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂岗石浸出K+的原因___________
(3)“溶浸”中,K+的浸出率结果如图所示。由图可知,当K+的浸出率为70%时。可以采用的实验条件为___________

(4)“除杂”中,先加入___________ 溶液,经搅拌等操作后,过滤,再加入___________ 溶液,调滤液pH至中性。
(5)以可溶性碳酸盐为溶浸剂,溶浸过程中会发生: CaSO4(s)+CO (ag)⇌CaCO3(s)+ SO
(ag)⇌CaCO3(s)+ SO (ag)
(ag)
已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5.此温度下,该反应的平衡常数K=___________ 。
 +2H2O采用饱和Ca(OH)2溶液浸杂卤石制备 K2SO4工艺流程如下:
+2H2O采用饱和Ca(OH)2溶液浸杂卤石制备 K2SO4工艺流程如下:
回答下列问题:
(1)滤渣的主要成分有
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂岗石浸出K+的原因
(3)“溶浸”中,K+的浸出率结果如图所示。由图可知,当K+的浸出率为70%时。可以采用的实验条件为

(4)“除杂”中,先加入
(5)以可溶性碳酸盐为溶浸剂,溶浸过程中会发生: CaSO4(s)+CO
 (ag)⇌CaCO3(s)+ SO
(ag)⇌CaCO3(s)+ SO (ag)
(ag)已知298K时,Ksp(CaCO3)=2.80×10-9,Ksp(CaSO4)=4.90×10-5.此温度下,该反应的平衡常数K=
您最近一年使用:0次
【推荐2】某种电镀污泥主要含有碲化亚铜(Cu2Te)、三氧化二铬(Cr2O3)以及少量的金(Au),可以用于制取Na2Cr2O7溶液、金属铜和粗碲等,以实现有害废料的资源化利用,工艺流程如下:
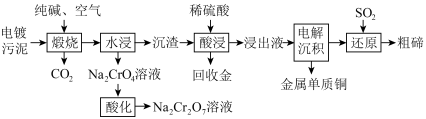
已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2 2CuO+TeO2。
2CuO+TeO2。
(1)煅烧时,Cr2O3发生反应的化学方程式为______ 。
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有____ (填化学式)。
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:

通过冷却结晶能析出大量K2Cr2O7的原因是_________ 。
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O 被还原为Cr3+)
被还原为Cr3+)
①氧化还原滴定过程中的离子方程式为________ 。
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为_____ %。[已知M(K2Cr2O7)=294 g·mol-1,计算结果保留三位有效数字]。
(5)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?____ (填“是”或“否”)。{已知:Ksp[Fe(OH)3]=4.0×10-38, Ksp[Cr(OH)3]=6.0×10-31}

已知:煅烧时,Cu2Te发生的反应为Cu2Te+2O2
 2CuO+TeO2。
2CuO+TeO2。(1)煅烧时,Cr2O3发生反应的化学方程式为
(2)浸出液中除了含有TeOSO4(在电解过程中不反应)外,还可能含有
(3)工业上用重铬酸钠(Na2Cr2O7)母液生产重铬酸钾(K2Cr2O7)的工艺流程如图所示:

通过冷却结晶能析出大量K2Cr2O7的原因是
(4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.50 g配成250 mL溶液,用移液管取出25.00 mL于锥形瓶中,加入足量稀硫酸酸化后,再加入几滴指示剂,用0.1000 mol·L-1硫酸亚铁铵(NH4)2Fe(SO4)2标准液进行滴定,重复进行二次实验。(已知Cr2O
 被还原为Cr3+)
被还原为Cr3+)①氧化还原滴定过程中的离子方程式为
②若三次实验消耗(NH4)2Fe(SO4)2标准液的平均体积为25.00 mL,则所得产品中K2Cr2O7的纯度为
(5)上述流程中K2Cr2O7发生氧化还原反应后所得溶液中除含有Cr3+外,还含有一定浓度的Fe3+杂质,可通过加碱调pH的方法使两者转化为沉淀。已知c(Cr3+)=3×10-5 mol·L-1,则当溶液中开始析出Cr(OH)3沉淀时Fe3+是否沉淀完全?
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】利用钒钛磁铁矿冶炼后产生的钒渣(主要含 、
、 、
、 及少量可溶性磷酸盐)生产
及少量可溶性磷酸盐)生产 的工艺流程如下,回答下列问题:
的工艺流程如下,回答下列问题:
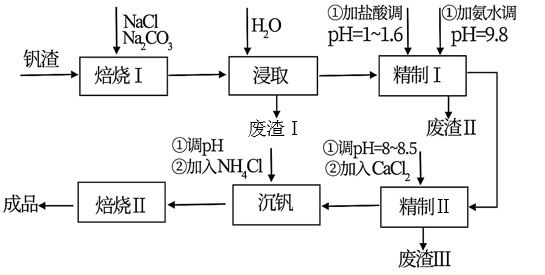
已知: 、
、 、
、 可与
可与 、NaCl组成的混合钠盐在高温下反应,并转化为
、NaCl组成的混合钠盐在高温下反应,并转化为 、
、 、
、 等可溶性钠盐。
等可溶性钠盐。
(1)焙烧I包括氧化和钠化成盐两个过程,氧化的目的是获得 ,写出氧化过程中
,写出氧化过程中 发生反应的化学方程式
发生反应的化学方程式___________ ;废渣I的主要成分是___________ 。
(2)精制I加入 后,写出相关的离子反应方程式:
后,写出相关的离子反应方程式:___________ 、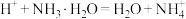 ,溶液中
,溶液中
___________ 。[已知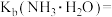
 ]
]
(3)精制II中加入 溶液除去磷酸盐,pH过小时影响除磷效果的原因是
溶液除去磷酸盐,pH过小时影响除磷效果的原因是___________ 。
(4)沉钒所得 沉淀需进行洗涤,洗涤时除去的阴离子主要是
沉淀需进行洗涤,洗涤时除去的阴离子主要是___________ 。 在500℃时焙烧脱氨制得产品,反应方程式为
在500℃时焙烧脱氨制得产品,反应方程式为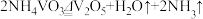 。但脱氨过程中,部分
。但脱氨过程中,部分 会被
会被 转化成
转化成 ,反应中氧化剂与还原剂物质的量之比为3:2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3:2,该反应的化学方程式为___________ 。
 、
、 、
、 及少量可溶性磷酸盐)生产
及少量可溶性磷酸盐)生产 的工艺流程如下,回答下列问题:
的工艺流程如下,回答下列问题:
已知:
 、
、 、
、 可与
可与 、NaCl组成的混合钠盐在高温下反应,并转化为
、NaCl组成的混合钠盐在高温下反应,并转化为 、
、 、
、 等可溶性钠盐。
等可溶性钠盐。(1)焙烧I包括氧化和钠化成盐两个过程,氧化的目的是获得
 ,写出氧化过程中
,写出氧化过程中 发生反应的化学方程式
发生反应的化学方程式(2)精制I加入
 后,写出相关的离子反应方程式:
后,写出相关的离子反应方程式: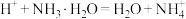 ,溶液中
,溶液中
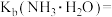
 ]
](3)精制II中加入
 溶液除去磷酸盐,pH过小时影响除磷效果的原因是
溶液除去磷酸盐,pH过小时影响除磷效果的原因是(4)沉钒所得
 沉淀需进行洗涤,洗涤时除去的阴离子主要是
沉淀需进行洗涤,洗涤时除去的阴离子主要是 在500℃时焙烧脱氨制得产品,反应方程式为
在500℃时焙烧脱氨制得产品,反应方程式为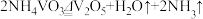 。但脱氨过程中,部分
。但脱氨过程中,部分 会被
会被 转化成
转化成 ,反应中氧化剂与还原剂物质的量之比为3:2,该反应的化学方程式为
,反应中氧化剂与还原剂物质的量之比为3:2,该反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】铂、钴、镍及其化合物在工业和医药等领域有重要应用。回答下列问题:
(1)筑波材料科学国家实验室发现了在 下呈现超导性的晶体
下呈现超导性的晶体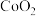 ,其具有层状结构。
,其具有层状结构。
①晶体中原子 与
与 的配位数之比为
的配位数之比为________ ;
②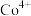 的价层电子的轨道表示式为
的价层电子的轨道表示式为________ 。
(2)配合物 常温下为液态,易溶于
常温下为液态,易溶于 等有机溶剂。固态
等有机溶剂。固态 属于
属于_________ 晶体。
(3)某镍配合物结构如图所示。
①分子内含有的化学键有_________ (填序号)。
A.氢键 B.共价键 C.离子键 D.配位键 E.金属键
②配合物中 、
、 、
、 三种元素原子的第一电离能由大到小的顺序是
三种元素原子的第一电离能由大到小的顺序是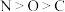 ,试从原子结构解释为什么同周期元素原子的第一电离能
,试从原子结构解释为什么同周期元素原子的第一电离能 :
:________ 。
(4)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。
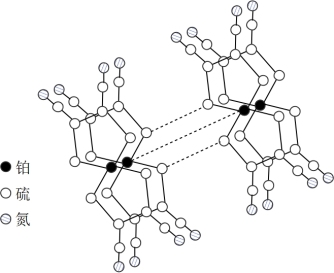
①“分子金属”可以导电,是因为_________ 能沿着其中的金属原子链流动。
② “分子金属”中,铂原子是否以 的方式杂化?
的方式杂化?________ (填“是”或“否”),其理由是_________ 。
(5)金属铂晶体中,铂原子的堆积方式类似于 晶胞中的钠离子或氯离子的堆积方式,其晶胞沿
晶胞中的钠离子或氯离子的堆积方式,其晶胞沿 、
、 或
或 轴的投影图如图所示,金属铂的密度为
轴的投影图如图所示,金属铂的密度为 ,则晶胞参数
,则晶胞参数
________  (列计算式)。
(列计算式)。

(1)筑波材料科学国家实验室发现了在
 下呈现超导性的晶体
下呈现超导性的晶体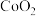 ,其具有层状结构。
,其具有层状结构。①晶体中原子
 与
与 的配位数之比为
的配位数之比为②
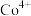 的价层电子的轨道表示式为
的价层电子的轨道表示式为(2)配合物
 常温下为液态,易溶于
常温下为液态,易溶于 等有机溶剂。固态
等有机溶剂。固态 属于
属于(3)某镍配合物结构如图所示。

①分子内含有的化学键有
A.氢键 B.共价键 C.离子键 D.配位键 E.金属键
②配合物中
 、
、 、
、 三种元素原子的第一电离能由大到小的顺序是
三种元素原子的第一电离能由大到小的顺序是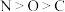 ,试从原子结构解释为什么同周期元素原子的第一电离能
,试从原子结构解释为什么同周期元素原子的第一电离能 :
:(4)某研究小组将平面型的铂配合物分子进行层状堆砌,使每个分子中的铂原子在某一方向上排列成行,构成能导电的“分子金属”,其结构如图所示。

①“分子金属”可以导电,是因为
② “分子金属”中,铂原子是否以
 的方式杂化?
的方式杂化?(5)金属铂晶体中,铂原子的堆积方式类似于
 晶胞中的钠离子或氯离子的堆积方式,其晶胞沿
晶胞中的钠离子或氯离子的堆积方式,其晶胞沿 、
、 或
或 轴的投影图如图所示,金属铂的密度为
轴的投影图如图所示,金属铂的密度为 ,则晶胞参数
,则晶胞参数
 (列计算式)。
(列计算式)。
您最近一年使用:0次
【推荐2】固体化合物X由3种元素组成。某学习小组进行了如下实验:

请回答:
(1)X的化学式___________ 。
(2)固体混合物Y的成分___________ (填化学式)。
(3)X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到绿色溶液,该反应的化学方程式是___________ 。
(4)绿色溶液加水稀释变蓝色,是因为生成了___________ 。(填离子的化学式)。

请回答:
(1)X的化学式
(2)固体混合物Y的成分
(3)X与浓盐酸反应产生黄绿色气体,固体完全溶解,得到绿色溶液,该反应的化学方程式是
(4)绿色溶液加水稀释变蓝色,是因为生成了
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】Cu3N具有良好的电学和光学性能,在电子工业领域、航空航天领域、国防领域、通讯领域以及光学工业等领域中,发挥着广泛的、不可替代的作用。
(1)Cu+的核外电子排布式为__________ ;N元素与O元素的第一电离能比较:N____ O(填“>”、“<”或“=”)。
(2)与N3-含有相同电子数的四原子分子的空间构型为____________________ 。
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(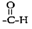 )碳原子的杂化方式为
)碳原子的杂化方式为_________ 。
(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式_________ 。
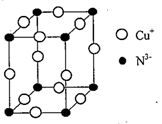
(5)Cu3N 的晶胞结构如图所示,N3-的配位数为________ ;若晶胞棱长为anm,NA表示阿伏伽德罗常数的值,则Cu3N的密度p=______ g/cm3[用含a和NA 的式子表示,Mr(Cu3N)=206]
 .
.
(1)Cu+的核外电子排布式为
(2)与N3-含有相同电子数的四原子分子的空间构型为
(3)在Cu催化作用下,乙醇可被空气氧化为乙醛(CH3CHO),乙醛分子中醛其(
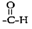 )碳原子的杂化方式为
)碳原子的杂化方式为(4)[Cu(H2O)4]2+为平面正方形结构,其中的两个H2O被C1-取代可生成Cu(H2O)2Cl2,试画出其具有极性的分子的结构式
(5)Cu3N 的晶胞结构如图所示,N3-的配位数为
 .
.
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】 是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是
是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是 ,其中含铝、硅、铜、锰等氧化物及油脂等杂质,一种以该下脚料为原料提取
,其中含铝、硅、铜、锰等氧化物及油脂等杂质,一种以该下脚料为原料提取 的工艺流程如图:
的工艺流程如图:

已知: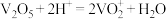 ;
;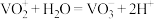 。
。
回答下列问题:
(1)“焙烧”可以除去油脂,还有一个作用是_______ 。
(2)将焙烧冷却后的固体残留物进行“粉碎”,其目的是_______ 。
(3)“滤渣1”的主要成分是_______ (写化学式)。
(4)“沉锰”反应的离子方程式是_______ 。
(5)“浓缩结晶”时,需要加入过量 ,其原因是
,其原因是_______ 。
(6)煅烧偏钒酸铵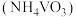 时,固体(取
时,固体(取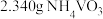 )质量的减少量随温度变化的曲线如图所示:
)质量的减少量随温度变化的曲线如图所示:
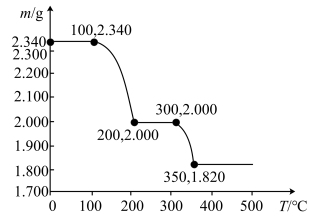
100~200℃时产生的一种气体的化学式为_______ ,300~350℃时发生反应的化学方程式为_______ 。
 是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是
是硫酸生产中的催化剂,某种含钒工业下脚料主要成分是 ,其中含铝、硅、铜、锰等氧化物及油脂等杂质,一种以该下脚料为原料提取
,其中含铝、硅、铜、锰等氧化物及油脂等杂质,一种以该下脚料为原料提取 的工艺流程如图:
的工艺流程如图:
已知:
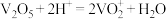 ;
;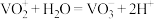 。
。回答下列问题:
(1)“焙烧”可以除去油脂,还有一个作用是
(2)将焙烧冷却后的固体残留物进行“粉碎”,其目的是
(3)“滤渣1”的主要成分是
(4)“沉锰”反应的离子方程式是
(5)“浓缩结晶”时,需要加入过量
 ,其原因是
,其原因是(6)煅烧偏钒酸铵
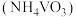 时,固体(取
时,固体(取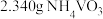 )质量的减少量随温度变化的曲线如图所示:
)质量的减少量随温度变化的曲线如图所示:
100~200℃时产生的一种气体的化学式为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】工业上以碳酸锰矿(主要成分为 ,含少量
,含少量 、
、 、CuO、
、CuO、 、
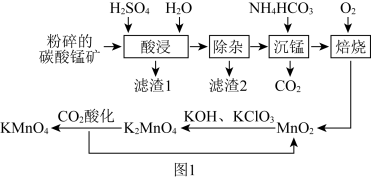
、 等杂质)为主要原料制备高锰酸钾的流程如图1所示。
等杂质)为主要原料制备高锰酸钾的流程如图1所示。
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀时的pH如表所示。
②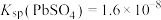 ;
; 。
。
(1)常温下,“酸浸”工序中,向粉碎的碳酸锰矿中加入一定体积的水,在搅拌下缓慢加入质量分数高于90%的硫酸。锰元素的浸出率与反应条件的关系如图2、3、4所示。

根据上述图象可知“酸浸”选择的最佳条件为_______ 。
(2)“除杂”工序中具体步骤如下:
①先加入 将
将 氧化,该反应的离子方程式为
氧化,该反应的离子方程式为_______ 。
②为除去铁元素和铝元素,加入CaO调节溶液的pH不小于_______ 。
③再加入CaS除去 、
、 后,最后加入NaF溶液,除去
后,最后加入NaF溶液,除去_______ ,此步骤中再次除铅的原因为由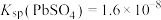 可知,溶液中仍含有
可知,溶液中仍含有 。
。
(3)“沉锰”工序中反应的化学方程式为_______ 。
(4)“焙烧”工序中反应的化学方程式为_______ 。
(5)若在实验室模拟图1中由二氧化锰制备高锰酸钾的过程,称量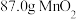 样品,经多次循环氧化,最终得到的产品质量为63.2g,则高锰酸钾的产率是
样品,经多次循环氧化,最终得到的产品质量为63.2g,则高锰酸钾的产率是_______ 。
 ,含少量
,含少量 、
、 、CuO、
、CuO、 、
、 等杂质)为主要原料制备高锰酸钾的流程如图1所示。
等杂质)为主要原料制备高锰酸钾的流程如图1所示。
已知:①常温下,溶液中金属离子开始沉淀和完全沉淀时的pH如表所示。
| 金属离子 |  |  |  |  |  |  |
| 开始沉淀pH | 1.5 | 3.3 | 6.5 | 4.2 | 8.0 | 8.3 |
| 完全沉淀pH | 3.7 | 5.2 | 9.7 | 6.7 | 8.8 | 9.8 |
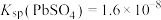 ;
; 。
。(1)常温下,“酸浸”工序中,向粉碎的碳酸锰矿中加入一定体积的水,在搅拌下缓慢加入质量分数高于90%的硫酸。锰元素的浸出率与反应条件的关系如图2、3、4所示。

根据上述图象可知“酸浸”选择的最佳条件为
(2)“除杂”工序中具体步骤如下:
①先加入
 将
将 氧化,该反应的离子方程式为
氧化,该反应的离子方程式为②为除去铁元素和铝元素,加入CaO调节溶液的pH不小于
③再加入CaS除去
 、
、 后,最后加入NaF溶液,除去
后,最后加入NaF溶液,除去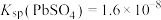 可知,溶液中仍含有
可知,溶液中仍含有 。
。(3)“沉锰”工序中反应的化学方程式为
(4)“焙烧”工序中反应的化学方程式为
(5)若在实验室模拟图1中由二氧化锰制备高锰酸钾的过程,称量
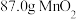 样品,经多次循环氧化,最终得到的产品质量为63.2g,则高锰酸钾的产率是
样品,经多次循环氧化,最终得到的产品质量为63.2g,则高锰酸钾的产率是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】重铬酸钾(K2Cr2O7)在皮革、火柴印染化学、电镀等方面应用广泛。工业上对制革工业污泥中(主要含有Cr3+、Fe3+、Fe2+、Al3+等)Cr元素的回收与再利用工艺如图:
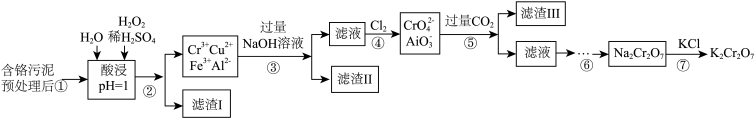
已知:①Al(OH)3与Cr(OH)3性质相似。
②2CrO42-+2H+ Cr2O72-+H2O。
Cr2O72-+H2O。
③有关物质的溶解度曲线如图。

回答下列问题:
(1)含铬污泥预处理包括高温煅烧粉碎等步骤,其中高温煅烧的目的是__ (写一条即可),滤渣III的成分是__ (填化学式)。
(2)步骤③中操作需要的玻璃仪器有__ ,步骤①加入H2O2的作用是__ 。
(3)步骤⑦反应能够发生的原因是__ ,写出步骤④的反应离子方程式:__ 。
(4)为测定产品中K2Cr2O7的含量,某兴趣小组将mg产品溶于水配制为500mL溶液,准确量取50.00mL,加入稀硫酸酸化,然后加入过量的KI充分还原,加___ 作指示剂,到达终点消耗30.00mL0.0500mol·L-1的Na2S2O3溶液。则该次生产的样品中K2Cr2O7含量为__ %。(已知:Cr2O72-+6I-+14H+=2Cr3++3I2+7H2O,2Na2S2O3+I2=Na2S4O6+2NaI)

已知:①Al(OH)3与Cr(OH)3性质相似。
②2CrO42-+2H+
 Cr2O72-+H2O。
Cr2O72-+H2O。③有关物质的溶解度曲线如图。

回答下列问题:
(1)含铬污泥预处理包括高温煅烧粉碎等步骤,其中高温煅烧的目的是
(2)步骤③中操作需要的玻璃仪器有
(3)步骤⑦反应能够发生的原因是
(4)为测定产品中K2Cr2O7的含量,某兴趣小组将mg产品溶于水配制为500mL溶液,准确量取50.00mL,加入稀硫酸酸化,然后加入过量的KI充分还原,加
您最近一年使用:0次



