我国对世界郑重承诺:2030年前实现碳达峰,2060年前实现碳中和,而研发CO2的碳捕捉和碳利用技术则是关键。
(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g) C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1
②CO2(g)+H2(g) CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1
③2CO(g) CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1
反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=____ kJ•mol-1。
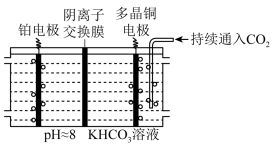
(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图1所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为_____ 。

(3)CO2的电化学催化还原具有条件温和、对环境友好的优点。Cu对CO2的电还原有一定的催化作用。在0.1mol•L-1CuSO4/H2SO4溶液中,改变沉积时间,进行恒电位沉积制备纳米Cu电极。图2是根据不同沉积时间制备的纳米Cu电极的循环伏安曲线作出的CO2的还原峰电流(峰电流越大,表明纳米Cu电极催化效果越好)与沉积时间的关系图,沉积时间超过50s,进一步延长沉积时间,纳米Cu电极催化效果减弱的原因是____ 。

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为____ mol•L-1。
[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
(5)章根强课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoⅡ表示),测试结果表明,该CoⅡ在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoⅡ/CoI反应路径(如图3)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoⅡ供激发电子将CoⅡ还原为CoI,_____ 。(结合图示,描述CO2还原为CO的过程)

(1)大气中的CO2主要来自于煤、石油及其他含碳化合物的燃烧,CH4与CO2重整是CO2利用的研究热点之一。该重整反应体系主要涉及以下反应:
①CH4(g)
 C(s)+2H2(g) ΔH1=akJ•mol-1
C(s)+2H2(g) ΔH1=akJ•mol-1②CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2=bkJ•mol-1
CO(g)+H2O(g) ΔH2=bkJ•mol-1③2CO(g)
 CO2(g)+C(s) ΔH3=ckJ•mol-1
CO2(g)+C(s) ΔH3=ckJ•mol-1反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的ΔH=
2CO(g)+2H2(g)的ΔH=(2)多晶Cu是目前唯一被实验证实能高效催化CO2还原为烃类(如C2H4)的金属。如图1所示,电解装置中分别以多晶Cu和Pt为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后KHCO3浓度基本保持不变,温度控制在10℃左右。生成C2H4的电极反应式为

(3)CO2的电化学催化还原具有条件温和、对环境友好的优点。Cu对CO2的电还原有一定的催化作用。在0.1mol•L-1CuSO4/H2SO4溶液中,改变沉积时间,进行恒电位沉积制备纳米Cu电极。图2是根据不同沉积时间制备的纳米Cu电极的循环伏安曲线作出的CO2的还原峰电流(峰电流越大,表明纳米Cu电极催化效果越好)与沉积时间的关系图,沉积时间超过50s,进一步延长沉积时间,纳米Cu电极催化效果减弱的原因是

(4)常温下,以NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。用1LNa2CO3溶液将2.33gBaSO4固体全都转化为BaCO3,再过滤,所用的Na2CO3溶液的物质的量浓度至少为
[已知:常温下Ksp(BaSO4)=1×10-11,Ksp(BaCO3)=1×10-10;忽略溶液体积变化]
(5)章根强课题组通过温和的自光刻技术制备出富含氧空位的Co(CO3)0.5(OH)•0.11H2O纳米线(用CoⅡ表示),测试结果表明,该CoⅡ在可见光下具有优异的光催化CO2还原活性。分析表明,该CO2还原催化机理为典型的CoⅡ/CoI反应路径(如图3)。首先,光敏剂([Ru(bpy)3]2+)通过可见光照射被激发到激发态([Ru(bpy)3]2+*),随后([Ru(bpy)3]2+*)被TEOA淬灭得到([Ru(bpy)3]+)还原物种,该还原物种将向CoⅡ供激发电子将CoⅡ还原为CoI,

更新时间:2022-12-08 20:15:08
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
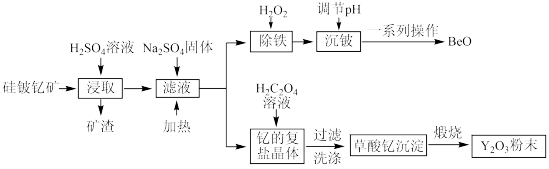
【推荐1】钇的常见化合价为+3价,我国蕴藏着丰富的硅铍钇矿,其主要成分为一种铍钇的硅酸盐(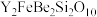 ),工业上通过如图所示生产流程可获得氧化钇和氧化铍。
),工业上通过如图所示生产流程可获得氧化钇和氧化铍。
已知:① 呈两性,
呈两性,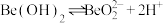
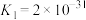 ;
;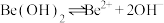
 。
。
②25℃时,相关金属离子形成氢氧化物沉淀的pH范围如下表:
(1)硅铍钇矿石(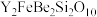 )中铁元素的价态为
)中铁元素的价态为_______ ,浸取时金属元素形成硫酸盐,则浸取后钇的产物为_______ (填化学式)。
(2)矿渣的成分为 ,酸化过程必须在较高温度下进行,若温度低会导致浸取率低,其原因是
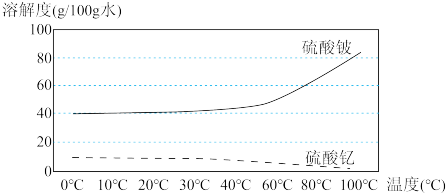
,酸化过程必须在较高温度下进行,若温度低会导致浸取率低,其原因是_______ ,图为硫酸钇和硫酸铍的溶解度随温度变化的曲线,浸取时最佳温度范围为_______ (填序号)。
A.10~20℃ B.20~30℃ C.40~50℃ D.80~100℃
(3)加入双氧水并同时调节pH除去铁,采取适当加热有利于铁的除去,其原因除了加快氧化速率,另一个原因是_______ 。
(4)除铁时需要控制pH范围是_______ ,通过计算说明沉铍时选择用氨水作为沉淀剂,而不选用NaOH溶液的原因是_______ 。
(5)草酸钇煅烧发生分解反应,产物中有两种气体,化学方程式为_______ 。
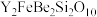 ),工业上通过如图所示生产流程可获得氧化钇和氧化铍。
),工业上通过如图所示生产流程可获得氧化钇和氧化铍。
已知:①
 呈两性,
呈两性,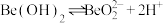
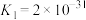 ;
;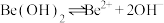
 。
。②25℃时,相关金属离子形成氢氧化物沉淀的pH范围如下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
 | 2.1 | 3.1 |
 | 6.2 | 8.4 |
(1)硅铍钇矿石(
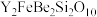 )中铁元素的价态为
)中铁元素的价态为(2)矿渣的成分为
 ,酸化过程必须在较高温度下进行,若温度低会导致浸取率低,其原因是
,酸化过程必须在较高温度下进行,若温度低会导致浸取率低,其原因是A.10~20℃ B.20~30℃ C.40~50℃ D.80~100℃

(3)加入双氧水并同时调节pH除去铁,采取适当加热有利于铁的除去,其原因除了加快氧化速率,另一个原因是
(4)除铁时需要控制pH范围是
(5)草酸钇煅烧发生分解反应,产物中有两种气体,化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐2】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示(条件及物质未标出)。

(1)已知: 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
___________ 。
(2)工业中 和
和 制备甲醇的方程式为
制备甲醇的方程式为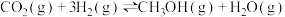 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为___________ 。
(3)某温度下,将 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
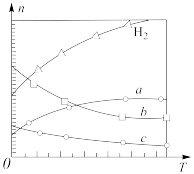
①该反应的ΔH___________ (填“>”或“<”)。
②曲线c表示的物质为___________ 。
③为提高 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是___________ 。

(1)已知:
 、CO、
、CO、 的标准燃烧热(ΔH)分别为
的标准燃烧热(ΔH)分别为 、
、 、
、 ,则上述流程中第一步反应
,则上述流程中第一步反应 的
的
(2)工业中
 和
和 制备甲醇的方程式为
制备甲醇的方程式为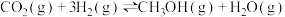 ,某温度下,将
,某温度下,将 和
和 充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下
充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下表,该温度下 的平衡转化率为
的平衡转化率为| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
 | 0.90 | 0.85 | 0.836 | 0.81 | 0.80 | 0.80 |
 和
和 按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得
按物质的量之比1:3通入压强为8MPa的恒压密闭容器中,发生(2)中反应,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数为
的平衡转化率为50%,则该反应条件下的平衡常数为
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)
 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: 。在0.1MPa时,按
。在0.1MPa时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
①该反应的ΔH
②曲线c表示的物质为
③为提高
 的平衡转化率,除改变温度外,还可采取的措施是
的平衡转化率,除改变温度外,还可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】氮元素也与碳元素一样存在一系列氢化物,如NH3、N2H4、N3H5、N4H6等。请回答下列有关问题:
(1)上述氮的系列氢化物的通式为____________ 。
(2)已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,查阅文献资料,化学键键能如下表:
①氨分解反应NH3(g)
 N2(g)+
N2(g)+ H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的活化能Ea2=
NH3(g)的活化能Ea2=___________ 。
②氨气完全燃烧生成氮气和气态水的热化学方程式为__________________________ 。
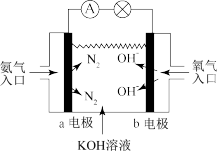
③如右图是氨气燃料电池示意图。a电极的电极反应式为________________ 。
(3)已知NH3·H2O为一元弱碱。N2H4·H2O为二元弱碱,在水溶液中的一级电离方程式表示为:N2H4·H2O+H2O N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为__________________ ;溶液中离子浓度由大到小的排列顺序为___________________ 。
(4)通过计算判定(NH4)2SO3溶液的酸碱性(写出计算过程)________________________ 。(已知:氨水Kb=1.8×10-5;H2SO3 Ka1=1.3×10-2 Ka2=6.3×10-8)。
(1)上述氮的系列氢化物的通式为
(2)已知:2H2(g)+O2(g)=2H2O(g) △H=-483.6kJ·mol-1,查阅文献资料,化学键键能如下表:
化学键 | H-H | N=N | N-H |
E/kJ·mol-1 | 436 | 946 | 391 |

 N2(g)+
N2(g)+ H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
H2(g)的活化能Ea1=300kJ·mol-1,则合成氨反应
 N2(g)+
N2(g)+ H2(g)
H2(g) NH3(g)的活化能Ea2=
NH3(g)的活化能Ea2=②氨气完全燃烧生成氮气和气态水的热化学方程式为
③如右图是氨气燃料电池示意图。a电极的电极反应式为

(3)已知NH3·H2O为一元弱碱。N2H4·H2O为二元弱碱,在水溶液中的一级电离方程式表示为:N2H4·H2O+H2O
 N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为
N2H5·H2O++OH-。则可溶性盐盐酸肼(N2H6Cl2)第一步水解的离子方程式为(4)通过计算判定(NH4)2SO3溶液的酸碱性(写出计算过程)
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】甲烷是一种清洁燃料,与水制氢和天然气脱硫具有重要的现实意义。回答下列问题:
Ⅰ.一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
①
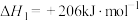
②
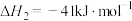
恒定压强为100kPa时,将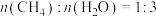 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。

______  ,反应在
,反应在______ 条件下能自发进行。
(2)600℃时, 的平衡分压为
的平衡分压为______ kPa,反应②的物质的量分数的平衡常数
______ (用物质的量分数代替平衡浓度计算,保留2位有效数字)。
(3)系统中q的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:______ 。
Ⅱ.H2S与 重整,不但可以消除污染,还可以制氢。主要反应如下:
重整,不但可以消除污染,还可以制氢。主要反应如下: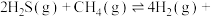
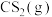
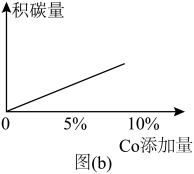
 。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
(4)图(a)为800℃、 催化剂条件下投入等量
催化剂条件下投入等量 ,不同投料比分别达到平衡时
,不同投料比分别达到平衡时 转化率、平均反应速率图。C组图像中平均速率最低的原因可能是
转化率、平均反应速率图。C组图像中平均速率最低的原因可能是______ ;相同质量的同种催化剂,在载体上的分散度越高,催化作用越强,原因是______ 。______ 反应(填化学方程式)。
Ⅰ.一定条件下,甲烷和水蒸气催化制氢主要有如下两个反应:
①

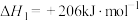
②

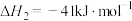
恒定压强为100kPa时,将
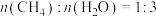 的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。
的混合气体投入反应器中,平衡时,各组分的物质的量分数与温度的关系如图所示。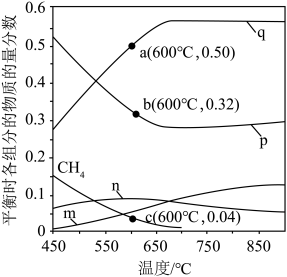


 ,反应在
,反应在(2)600℃时,
 的平衡分压为
的平衡分压为
(3)系统中q的含量在700℃左右出现峰值,试从化学平衡的角度解释出现峰值的原因:
Ⅱ.H2S与
 重整,不但可以消除污染,还可以制氢。主要反应如下:
重整,不但可以消除污染,还可以制氢。主要反应如下: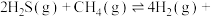
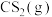
 。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。
。在研究反应发生的适宜条件时,Co助剂有稳定催化剂的作用。(4)图(a)为800℃、
 催化剂条件下投入等量
催化剂条件下投入等量 ,不同投料比分别达到平衡时
,不同投料比分别达到平衡时 转化率、平均反应速率图。C组图像中平均速率最低的原因可能是
转化率、平均反应速率图。C组图像中平均速率最低的原因可能是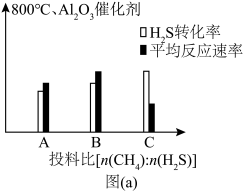
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】中学教材对Cu与 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
Ⅰ.利用如图装置完成Cu与 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.___________ ;
(2)用化学方程式解释C中液面上方为红棕色气体的原理___________ ;
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为___________ ;
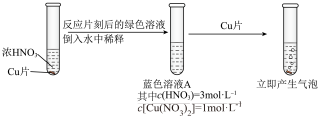
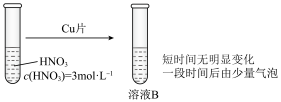
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
分析蓝色溶液A的成分后,学习小组探究蓝色溶液A与铜片能够立即发生反应的原因。
实验验证:
(4)将少量硫酸铜固体加入到 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证___________ (填化学式)对该反应是否有催化作用。该同学这样做不能得出该物质不是催化剂的正确结论,还应该考虑___________ 和___________ 的影响;
(5)某同学又提出可能是 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为___________ (写实验操作及现象)。
 的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.
的反应进行了讲解,但深入研究时用到了控制变量法(即有多个变量时,应该控制其他变量不变,只允许一个变量发生变化的研究方法),设计了如下的实验装置,并探讨了一些值得思考的问题.Ⅰ.利用如图装置完成Cu与
 制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
制取氮氧化物的反应.实验过程中可观察到装置B中液面上方为无色气体,C中液面上方为红棕色气体.
(2)用化学方程式解释C中液面上方为红棕色气体的原理
(3)将分液漏斗中液体换为稀硫酸和硝酸钠混合液也出现了溶解现象。此时烧瓶中发生反应的离子方程式为
Ⅱ.深入研究时,有同学观察到了以下现象:实验1中蓝色溶液A遇铜片立即产生气泡;而相同条件下实验2中3mol/L硝酸遇铜片短时间内无明显变化,一段时间后才有少量气泡产生。实验操作如下:
| 实验1 |
|
| 实验2 |
|
实验验证:
(4)将少量硫酸铜固体加入到
 硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证
硝酸中,溶液呈蓝色,放入铜片,无明显变化。该同学这样做是为了验证(5)某同学又提出可能是
 对该反应有催化作用。为了得出该结论,应该补充的实验为
对该反应有催化作用。为了得出该结论,应该补充的实验为
您最近一年使用:0次
【推荐3】Fe、Co、Cu等金属在回收利用 和污水处理等多个领域都具有应用价值。回答下列问题:
和污水处理等多个领域都具有应用价值。回答下列问题:
(1) 在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
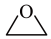 (g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g)
(g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g) 
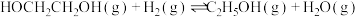
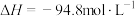
获取乙二醇的反应历程可分为如下2步:
I.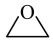
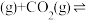
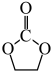 (g)
(g) 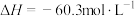
II.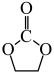 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。
①步骤II的热化学方程式是:_______ 。
②研究反应温度对EC加氢的影响(反应时间均为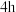 ),实验数据见下表:
),实验数据见下表:
由上表可知,温度越高,EC的转化率越高,原因是_______ 。温度升高到220℃时,乙二醇的产率反而降低,原因是_______ 。
(2)多晶 是目前唯一被实验证实能高效催化
是目前唯一被实验证实能高效催化 还原为烃类(如
还原为烃类(如 )的金属。如图所示,电解装置中分别以多晶
)的金属。如图所示,电解装置中分别以多晶 和
和 为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后
为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后 浓度基本保持不变,温度控制在10℃左右,生成
浓度基本保持不变,温度控制在10℃左右,生成 的电极反应式为
的电极反应式为_______ 。
(3) 与
与 反应如果用
反应如果用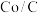 作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将
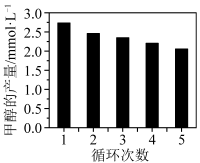
作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将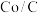 催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因:
催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因:_______ 。(Co的性质与 相似)
相似)
(4)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。
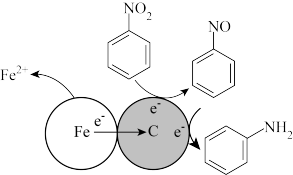
该物质转化示意图可以描述为_______ 。
 和污水处理等多个领域都具有应用价值。回答下列问题:
和污水处理等多个领域都具有应用价值。回答下列问题:(1)
 在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。
在金属催化剂作用下可以直接转化为乙二醇和甲醇,但若反应温度过高,乙二醇会深度加氢生成乙醇。 (g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g)
(g)+CO2(g)+3H2(g)⇌HOCH2CH2OH(g)+CH3OH(g) 
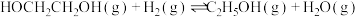
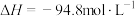
获取乙二醇的反应历程可分为如下2步:
I.

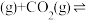
 (g)
(g) 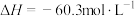
II.
 加氢生成乙二醇与甲醇。
加氢生成乙二醇与甲醇。①步骤II的热化学方程式是:
②研究反应温度对EC加氢的影响(反应时间均为
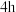 ),实验数据见下表:
),实验数据见下表:| 反应温度/℃ |  的转化率/% 的转化率/% | 乙二醇的产率/% |
| 160 | 23.8 | 23.2 |
| 180 | 62.1 | 60.9 |
| 200 | 99.9 | 94.7 |
| 220 | 99.9 | 92.4 |
(2)多晶
 是目前唯一被实验证实能高效催化
是目前唯一被实验证实能高效催化 还原为烃类(如
还原为烃类(如 )的金属。如图所示,电解装置中分别以多晶
)的金属。如图所示,电解装置中分别以多晶 和
和 为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后
为电极材料,用阴离子交换膜分隔开阴、阳极室,反应前后 浓度基本保持不变,温度控制在10℃左右,生成
浓度基本保持不变,温度控制在10℃左右,生成 的电极反应式为
的电极反应式为
(3)
 与
与 反应如果用
反应如果用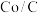 作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将
作为催化剂,可以得到含有少量甲酸的甲醇。为研究催化剂的催化效率,将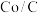 催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因:
催化剂循环使用,相同条件下,随着循环使用次数的增加,甲醇产量如图所示,试推测甲醇产量变化的原因: 相似)
相似)
(4)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。

该物质转化示意图可以描述为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】磷酸铁( )常用作电极材料。以硫铁矿(主要成分是
)常用作电极材料。以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的流程如下:
)为原料制备磷酸铁的流程如下:
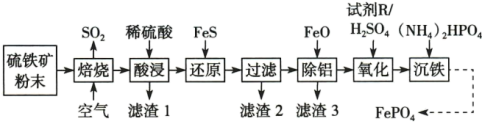
已知几种金属离子沉淀的 如下表所示:
如下表所示:
请回答下列问题:
(1)滤渣3的主要成分是___________ (写出化学式)。
(2)用 还原
还原 的目的是
的目的是___________ ,加入 的作用是
的作用是___________ (用离子方程式表示)。
(3)试剂R宜选择___________(填字母)。
(4)检验“氧化”之后溶液是否含 的操作是
的操作是___________ 。
(5)已知常温下,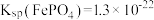 。“沉铁”中为了使
。“沉铁”中为了使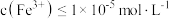 ,
,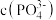 最小为
最小为___________  。
。
 )常用作电极材料。以硫铁矿(主要成分是
)常用作电极材料。以硫铁矿(主要成分是 ,含少量
,含少量 、
、 和
和 )为原料制备磷酸铁的流程如下:
)为原料制备磷酸铁的流程如下:
已知几种金属离子沉淀的
 如下表所示:
如下表所示:| 金属氢氧化物 |  |  |  |
开始沉淀的 | 2.3 | 7.5 | 4.0 |
完全沉淀的 | 4.1 | 9.7 | 5.2 |
请回答下列问题:
(1)滤渣3的主要成分是
(2)用
 还原
还原 的目的是
的目的是 的作用是
的作用是(3)试剂R宜选择___________(填字母)。
| A.高锰酸钾 | B.稀硝酸 | C.双氧水 | D.次氯酸钠 |
 的操作是
的操作是(5)已知常温下,
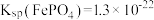 。“沉铁”中为了使
。“沉铁”中为了使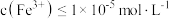 ,
,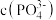 最小为
最小为 。
。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】锂离子电池正极材料的回收利用具有重大的现实意义。将废旧钴酸锂电池经过放电、拆解等操作后获得正极材料(主要成分是LiCoO2、铝箔和炭黑等),可采用湿法治金工艺回收正极材料中的金属,其流程如下:
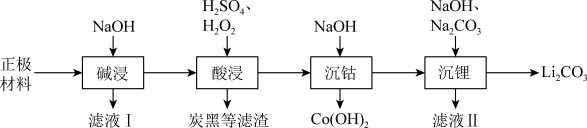
(1)钴酸锂中Co元素的化合价为___________ 。
(2)加快碱浸的可行性措施是___________ 。(任意写一条)
(3)滤液I中的主要成分除了NaOH还有___________ 。(写化学式)
(4)“酸浸”中发生反应的离子方程式是___________ ;在酸浸过程中不使用盐酸做浸出剂的原因可能是___________ 。
(5)常温下,“沉钴”时加入碱使溶液pH = 8.5,此时溶液中c(Co2+)=___________ 。(已知:Ksp[Co(OH)2]=2×10-15)
(6)该工艺得到的Co(OH)2和Li2CO3混合后在空气中于800℃煅烧可进行LiCoO2材料再生,写出LiCoO2材料再生的化学方程式___________ 。

(1)钴酸锂中Co元素的化合价为
(2)加快碱浸的可行性措施是
(3)滤液I中的主要成分除了NaOH还有
(4)“酸浸”中发生反应的离子方程式是
(5)常温下,“沉钴”时加入碱使溶液pH = 8.5,此时溶液中c(Co2+)=
(6)该工艺得到的Co(OH)2和Li2CO3混合后在空气中于800℃煅烧可进行LiCoO2材料再生,写出LiCoO2材料再生的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐3】工业上以碳酸锰矿(主要成分为MnCO3,另含FeO、Fe2O3、CaO等杂质)为主要原料生产锰酸锂(LiMn2O4)的工艺流程如下:

已知:部分离子沉淀的pH值。
(1)为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③_____ 等。
(2)氧化时发生的离子方程式:_________ 。
(3)加入CaO“除铁”的原理是____________ 。
(4)加入MnF2为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol·L-1,则Ca2+的浓度为________ mol·L-1[常温时,Ksp(CaF2)=2.7×10-11]。
(5)“锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5 h,然后升温至600~750℃,保温24 h,自然冷却至室温得产品。升温到515℃时,开始有CO2产生,比预计碳酸锂的分解温度(723℃)低得多。可能的原因是________ 。

已知:部分离子沉淀的pH值。
| 离子 | 开始沉淀的pH值 | 沉淀完全时的pH值 |
| Mn2+ | 8.8 | 10.8 |
| Fe2+ | 7.5 | 9.5 |
| Fe3+ | 2.2 | 3.5 |
(1)为了提高碳酸锰矿浸出的速率,在“酸浸”时可采取的措施有:①适当升高温度;②搅拌;③
(2)氧化时发生的离子方程式:
(3)加入CaO“除铁”的原理是
(4)加入MnF2为了除去溶液中的Ca2+,若控制溶液中F-浓度为3×10-3mol·L-1,则Ca2+的浓度为
(5)“锂化”是将MnO2和Li2CO3按4∶1的物质的量比配料,球磨3~5 h,然后升温至600~750℃,保温24 h,自然冷却至室温得产品。升温到515℃时,开始有CO2产生,比预计碳酸锂的分解温度(723℃)低得多。可能的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】废气中的H2S可用电解、Fe2(SO4)3吸收和活性炭吸附氧化等多种方法脱除。
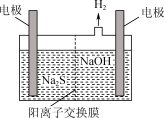
(1)电解法脱除:将烧碱吸收H2S后的溶液加入如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S;(n-1)S+S2-= S 。
。___________ 。
② 电解后阳极区溶液用稀硫酸酸化得到硫单质,其离子方程式为___________ 。
(2)Fe2(SO4)3吸收脱除:用Fe2(SO4)3溶液吸收H2S,其反应后的溶液可在硫杆菌作用下实现吸收液的再生。
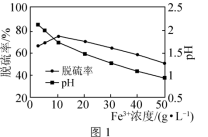
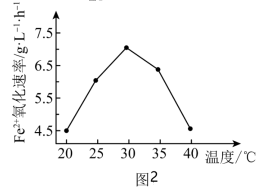
① 用Fe2(SO4)3吸收液脱除H2S的原理经历三步。第一步:H2S(g)⇌H2S(aq);第二步:H2S⇌H++HS-;第三步:HS-+2Fe3+= S↓+2Fe2++H+。一定条件下,Fe3+质量浓度及该溶液起始pH与脱硫率的关系如图1所示。当Fe3+质量浓度大于10 g·L-1时,随着Fe3+质量浓度的增大,脱硫率逐渐降低。其原因是___________ 。_______ 。___________ 。___________ 。
② 若水膜过厚,H2S的氧化去除率减小的原因是___________ 。
(1)电解法脱除:将烧碱吸收H2S后的溶液加入如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S;(n-1)S+S2-= S
 。
。
② 电解后阳极区溶液用稀硫酸酸化得到硫单质,其离子方程式为
(2)Fe2(SO4)3吸收脱除:用Fe2(SO4)3溶液吸收H2S,其反应后的溶液可在硫杆菌作用下实现吸收液的再生。
① 用Fe2(SO4)3吸收液脱除H2S的原理经历三步。第一步:H2S(g)⇌H2S(aq);第二步:H2S⇌H++HS-;第三步:HS-+2Fe3+= S↓+2Fe2++H+。一定条件下,Fe3+质量浓度及该溶液起始pH与脱硫率的关系如图1所示。当Fe3+质量浓度大于10 g·L-1时,随着Fe3+质量浓度的增大,脱硫率逐渐降低。其原因是
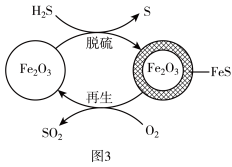
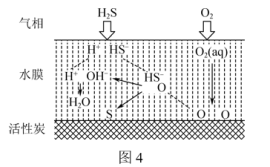
② 若水膜过厚,H2S的氧化去除率减小的原因是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.利用电化学方法可以将CO2有效地转化为HCOO−,装置如图所示。
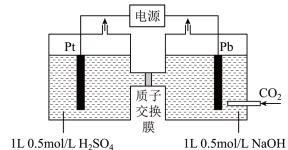
(1)①在该装置中,右侧Pt电极的电极反应式为_______ 。
②装置工作时,阴极除有HCOO−生成外,还可能生成副产物H2降低电解效率。已知:电解效率= ×100%;若测得阴极区内的c(HCOO−)=0.03mol/L,电解效率为75%,则阴极和阳极生成的气体在标准状况下的体积总共
×100%;若测得阴极区内的c(HCOO−)=0.03mol/L,电解效率为75%,则阴极和阳极生成的气体在标准状况下的体积总共_______ mL。(忽略电解前后溶液的体积变化)
Ⅱ.CH4与CO2的干法重整(DRM)反应可同时转化两种温室气体,并制备CO和H2.主要反应如下:
反应Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1;
反应Ⅱ:CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g) ΔH2;
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
已知:反应I、Ⅱ的自发均需高温条件。
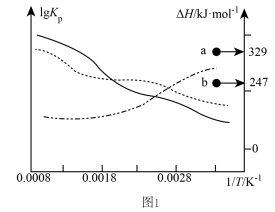
(2)上述三个反应的平衡常数Kp、ΔH与温度T关系如图1所示。图中a点代表的是_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)反应的ΔH,ΔH3=_______ kJ⋅mol−1。
(3)向密闭容器中,通入3molCO2和1molCH4,若仅考虑上述反应,平衡时CO2、CH4、CO、H2的物质的量随温度T的变化如图2所示。900K时,CH4的物质的量分数为_______ ,用各物质的物质的量分数表示反应Ⅲ的平衡常数Kx=_______ 。900K后随温度升高,H2物质的量减少的原因为_______ 。

(4)DRM反应目前普遍存在的一个难题是积碳,该过程与两个反应有关:①CH4→NiC+2H2 ΔH>0;②2CO⇌C+CO2 ΔH<0。目前积碳问题的解决方案主要有两种:A.提高原料气中CO2的占比;B.在常规的Ni催化剂中添加MgO,使其在催化剂表面与Ni形成共熔物。试解释这两种方法可以有效抑制积碳的原因_______ (答出两条即可)。

(1)①在该装置中,右侧Pt电极的电极反应式为
②装置工作时,阴极除有HCOO−生成外,还可能生成副产物H2降低电解效率。已知:电解效率=
 ×100%;若测得阴极区内的c(HCOO−)=0.03mol/L,电解效率为75%,则阴极和阳极生成的气体在标准状况下的体积总共
×100%;若测得阴极区内的c(HCOO−)=0.03mol/L,电解效率为75%,则阴极和阳极生成的气体在标准状况下的体积总共Ⅱ.CH4与CO2的干法重整(DRM)反应可同时转化两种温室气体,并制备CO和H2.主要反应如下:
反应Ⅰ:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1;
反应Ⅱ:CH4(g)+3CO2(g)⇌4CO(g)+2H2O(g) ΔH2;
反应Ⅲ:CO(g)+H2O(g)⇌CO2(g)+H2(g) ΔH3
已知:反应I、Ⅱ的自发均需高温条件。
(2)上述三个反应的平衡常数Kp、ΔH与温度T关系如图1所示。图中a点代表的是

(3)向密闭容器中,通入3molCO2和1molCH4,若仅考虑上述反应,平衡时CO2、CH4、CO、H2的物质的量随温度T的变化如图2所示。900K时,CH4的物质的量分数为

(4)DRM反应目前普遍存在的一个难题是积碳,该过程与两个反应有关:①CH4→NiC+2H2 ΔH>0;②2CO⇌C+CO2 ΔH<0。目前积碳问题的解决方案主要有两种:A.提高原料气中CO2的占比;B.在常规的Ni催化剂中添加MgO,使其在催化剂表面与Ni形成共熔物。试解释这两种方法可以有效抑制积碳的原因
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】中国科学家首次实现了二氧化碳到淀粉的从头合成,相关成果北京时间9月24日由国际知名学术期刊《科学》在线发表,因此 的捕集及其资源化利用成为科学家研究的重要课题。
的捕集及其资源化利用成为科学家研究的重要课题。
Ⅰ.二氧化碳合成“合成气”
(1)捕获的高浓度 能与
能与 制备合成气
制备合成气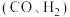 ,该过程主要涉及以下反应:
,该过程主要涉及以下反应:
①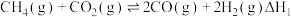
②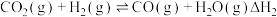
③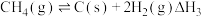
④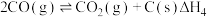
根据盖斯定律,反应①的
___________ (写出代数式即可)。
Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原 时,采用高浓度的
时,采用高浓度的 抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图所示。阴极发生的反应为:
抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图所示。阴极发生的反应为:_______ ;每转移 电子,阳极生成
电子,阳极生成___________  气体(标准状况)
气体(标准状况) 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
A.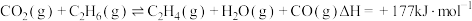 (主反应)
(主反应)
B.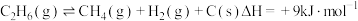 (副反应)
(副反应)
其中,反应 的反应历程可分为如下两步:
的反应历程可分为如下两步:
a.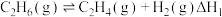 (反应速率较快)
(反应速率较快)
b.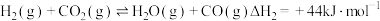 (反应速率较慢)
(反应速率较慢)
密闭容器中充入 和
和 合成
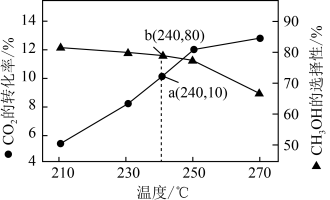
合成 ,发生主反应,温度对催化剂
,发生主反应,温度对催化剂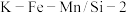 性能的影响如图所示,工业生产综合各方面的因素,反应选择
性能的影响如图所示,工业生产综合各方面的因素,反应选择 的原因是
的原因是_______ 。
主反应:
副反应:
某一刚性容器中充入 和
和 ,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性
,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性 。
。 平衡时,生成的
平衡时,生成的 的物质的量是
的物质的量是___________ 。
Ⅳ.新型二氧化碳固定法
(5)某课题组设计一种新型的固定 方法,如图所示。若原料用
方法,如图所示。若原料用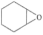 ,则产物为
,则产物为___________ 。
 的捕集及其资源化利用成为科学家研究的重要课题。
的捕集及其资源化利用成为科学家研究的重要课题。Ⅰ.二氧化碳合成“合成气”
(1)捕获的高浓度
 能与
能与 制备合成气
制备合成气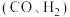 ,该过程主要涉及以下反应:
,该过程主要涉及以下反应:①
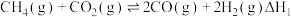
②
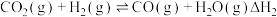
③
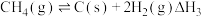
④
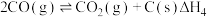
根据盖斯定律,反应①的

Ⅱ.二氧化碳合成低碳烯烃
(2)用可再生能源电还原
 时,采用高浓度的
时,采用高浓度的 抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图所示。阴极发生的反应为:
抑制酸性电解液中的析氢反应来提高乙烯的生成率,装置如图所示。阴极发生的反应为: 电子,阳极生成
电子,阳极生成 气体(标准状况)
气体(标准状况)
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:A.
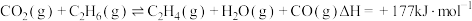 (主反应)
(主反应)B.
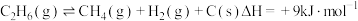 (副反应)
(副反应)其中,反应
 的反应历程可分为如下两步:
的反应历程可分为如下两步:a.
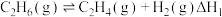 (反应速率较快)
(反应速率较快)b.
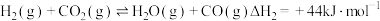 (反应速率较慢)
(反应速率较慢)密闭容器中充入
 和
和 合成
合成 ,发生主反应,温度对催化剂
,发生主反应,温度对催化剂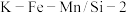 性能的影响如图所示,工业生产综合各方面的因素,反应选择
性能的影响如图所示,工业生产综合各方面的因素,反应选择 的原因是
的原因是
主反应:

副反应:

某一刚性容器中充入
 和
和 ,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性
,在催化剂存在条件下进行反应,测得温度与平衡转化率、产物选择性的关系如图所示。已知:选择性 。
。
 平衡时,生成的
平衡时,生成的 的物质的量是
的物质的量是Ⅳ.新型二氧化碳固定法
(5)某课题组设计一种新型的固定
 方法,如图所示。若原料用
方法,如图所示。若原料用 ,则产物为
,则产物为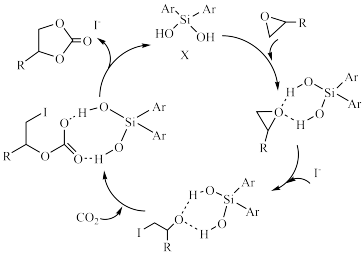
您最近一年使用:0次