NA为阿伏加德罗常数的值。下列有关说法正确的是
| A.室温下,22. 4L乙烷中含有的碳原子数小于2NA |
B.1L 0.1mol/L NH4Cl溶液中 的数目为0.1NA 的数目为0.1NA |
| C.标准状况下,11. 2L CHCl3中所含的氯原子数为1. 5NA |
| D.室温下,27g Al与足量浓硫酸反应,转移的电子数为3NA |
更新时间:2022-07-01 21:40:40
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】设 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是A. 含有的质子数为 含有的质子数为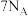 |
B.标准状况下, 和 和 的混合气体中所含分子数为 的混合气体中所含分子数为 |
C. 金属钠在氧气中完全燃烧生成 金属钠在氧气中完全燃烧生成 ,失去的电子数目为 ,失去的电子数目为 |
D.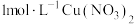 溶液中含有硝酸根离子的数目为 溶液中含有硝酸根离子的数目为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.32 g氧气所含的原子数目为NA |
| B.18 g水所含的原子数目为NA |
| C.在常温下22.4 L氢气所含的原子数目为NA |
| D.2.3 g金属钠变为钠离子时失电子数为0.1 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设NA表示阿伏加德罗常数的值,下列叙述正确的是
| A.常温常压下4.6g NO2和N2O4混合气体所含原子总数为0.3NA |
| B.标准状况下,22.4L SO3的分子数为NA |
| C.将标准状况下11.2L的Cl2通入足量水中发生反应,转移的电子总数为0.5NA |
| D.电解58.5 g熔融的NaCl,能产生22.4 L氯气(标准状况)、23.0 g金属钠 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】若NA表示阿伏加 德罗常数的值,下列叙述中正确的是
| A.常温下,9.2gNO2和N2O4的混合气体中含有的氮原子数目为0.2NA |
| B.22.4L N2与CO组成的混合气体所含有的电子数为14NA |
| C.0.1mol/L K2CO3溶液中所含K+数目为0.2NA |
| D.在反应KClO3+6HCl=KCl+3Cl2↑+3H2O中,每生成3molCl2转移的电子数为6NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列推断正确的是
| 选项 | 事实 | 结论 |
| A | 可用饱和FeCl3溶液制备Fe(OH)3胶体 | Fe3+有氧化性 |
| B | 铝箔在酒精灯火焰上加热熔化但不滴落 | 铝箔表面氧化铝熔点高于铝 |
| C | Cl2的水溶液可以导电 | Cl2是电解质 |
| D | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验的现象与对应结论均正确的是
| 选项 | 操 作 | 现 象 | 结论 |
| A | 将浓硫酸滴到蔗糖表面 | 固体变黑膨胀 | 浓硫酸只表现脱水性 |
| B | 常温下将Al片放入浓硝酸中 | 无明显现象 | Al与浓硝酸不反应 |
| C | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| D | 将盐酸滴入Na2CO3溶液中 | 产生气泡 | Cl的非金属性比C强 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。

A.过程I将 转化为NH3: 转化为NH3: +OH- +OH- NH3↑+H2O NH3↑+H2O |
| B.过程II将残留的NH3∙H2O转化N2:3ClO-+2NH3∙H2O=3Cl-+N2↑+5H2O |
C.过程III将残留的NaClO转化NaCl:ClO-+SO =Cl-+SO =Cl-+SO |
D.Na2SO3溶液呈碱性的原因:SO +2H2O=H2SO3+2OH- +2H2O=H2SO3+2OH- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】测定0.1
 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:
实验过程中,取①、④时刻的溶液,加入盐酸酸化的 溶液做对比实验,④产生白色沉
溶液做对比实验,④产生白色沉
淀多。下列说法不正确 的是

 溶液先升温再降温过程中的pH,数据如下表:
溶液先升温再降温过程中的pH,数据如下表:时刻 | ① | ② | ③ | ④ |
温度/℃ | 25 | 30 | 40 | 25 |
pH | 9.66 | 9.52 | 9.37 | 9.25 |
 溶液做对比实验,④产生白色沉
溶液做对比实验,④产生白色沉淀多。下列说法
A. 溶液中共有7种微粒 溶液中共有7种微粒 |
B.④产生的白色沉淀是 |
C.①与④的 值相等 值相等 |
D.①→③的过程中,温度对水解平衡的影响比 的影响更大 的影响更大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】“84”消毒液(有效成分为NaClO)可用于消毒和漂白。下列对于实验现象的分析不正确的是
| 实验目的 |  6mL“84”消毒液+2滴石蕊试液 |  6mL“84”消毒液+2滴石蕊试液 |  6mL“84”消毒液+2滴石蕊试液 |
| 现象 | 混合后溶液呈蓝色, 一段时间后蓝色褪去 | 混合后溶液呈紫色,紫色迅速褪去,无气体产生 | 混合后溶液呈红色,红色迅速褪去,并产生大量气体,该气体能使湿润的淀粉碘化钾试纸变蓝 |
| A.对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO-+H+=HClO |
| B.实验③中产生的气体是Cl2,由HClO分解得到:2HClO=Cl2↑+H2O |
| C.湿润的淀粉碘化钾试纸变蓝是因为发生了置换反应生成了碘单质(I2) |
| D.加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用 |
您最近一年使用:0次

 ,下列说法不正确的是
,下列说法不正确的是

