铬是不锈钢的合金元素之一,目前被广泛应用于冶金、化工等领域。
(1)基态Cr原子价层电子的电子排布式为_______ 。
(2)金属铬的第二电离能(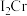 )和锰的第二电离能(
)和锰的第二电离能(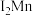 )分别为1590.6kJ/mol、1509.0kJ/mol,
)分别为1590.6kJ/mol、1509.0kJ/mol,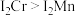 的原因是
的原因是_______ 。
(3) 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为_______ 。
(4)Cr的一种配合物结构如图所示,该配合物阳离子中Cr的配位数为_______ ,阴离子 的空间构型为
的空间构型为_______ 。
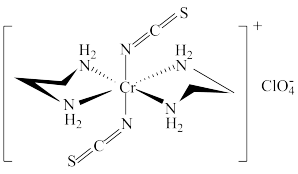
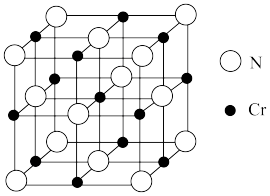
(5)氮化铬晶体的晶胞结构如图所示,若N与Cr核间距离为a pm( ),则氮化铬的密度为
),则氮化铬的密度为_______ g·cm-3。
(1)基态Cr原子价层电子的电子排布式为
(2)金属铬的第二电离能(
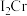 )和锰的第二电离能(
)和锰的第二电离能(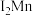 )分别为1590.6kJ/mol、1509.0kJ/mol,
)分别为1590.6kJ/mol、1509.0kJ/mol,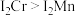 的原因是
的原因是(3)
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是因为
的熔点(1100℃)低得多,这是因为(4)Cr的一种配合物结构如图所示,该配合物阳离子中Cr的配位数为
 的空间构型为
的空间构型为
(5)氮化铬晶体的晶胞结构如图所示,若N与Cr核间距离为a pm(
 ),则氮化铬的密度为
),则氮化铬的密度为
21-22高二下·浙江湖州·期末 查看更多[4]
浙江省湖州市2021-2022学年高二下学期期末调研测试化学试题浙江省舟山市舟山中学2021-2022学年高三上学期开学考试化学试题(已下线)2023年1月浙江省普通高校招生选考科目考试化学仿真模拟试卷A(已下线)专题02 物质结构专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)
更新时间:2022-07-05 18:00:48
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国科学家合成有机-无机“杂化分子”,进而制备“弹性陶瓷塑料”过程如下。

(1)碳酸钙中各元素电负性从大到小的顺序为___________ 。
(2)理论上参加反应的碳酸钙寡聚体和硫辛酸的物质的量之比为___________ 。
(3)“弹性陶瓷塑料”相较于单一材料具有更好的性能,其微观结构如图。

①杂化分子在120℃时仅断开___________ (填“C-S键”或“S-S键”),加压至l10MPa的目的是___________ ,便于重新成键,进一步交联,形成“弹性陶瓷塑料”。
②对比橡胶,___________ (填微粒间作用力)主导的无机骨架有刚性支撑作用,抗压性好:对比陶瓷,由于___________ 片段(填片段名称)交联的结构起弹性缓冲作用,回弹率好。
(4)若合成时直接采用过饱和碳酸钙溶液,将得到一种碳酸钙晶体,其晶胞结构如图。该晶胞中氧原子的个数为___________ ,密度为___________  。(列出计算式,阿伏加德罗常数的值为
。(列出计算式,阿伏加德罗常数的值为 )
)


(1)碳酸钙中各元素电负性从大到小的顺序为
(2)理论上参加反应的碳酸钙寡聚体和硫辛酸的物质的量之比为
(3)“弹性陶瓷塑料”相较于单一材料具有更好的性能,其微观结构如图。

①杂化分子在120℃时仅断开
②对比橡胶,
(4)若合成时直接采用过饱和碳酸钙溶液,将得到一种碳酸钙晶体,其晶胞结构如图。该晶胞中氧原子的个数为
 。(列出计算式,阿伏加德罗常数的值为
。(列出计算式,阿伏加德罗常数的值为 )
)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】锂一磷酸氧铜电池正极的活性物质是Cu4O(PO4)2,可通过下列反应制备: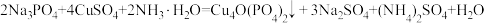 。回答下列问题:
。回答下列问题:
(1)铜位于周期表中_____ 区,与Cu同周期的元素中,与铜原子最外层电子数相等的元素还有_____ (填元素符号)。
(2)上述方程式中涉及的N、O、P、S元素第一电离能由小到大的顺序为________ ,电负性由小到大的顺序为______ 。
(3)常见含硫的微粒有SO2、SO3、 等,
等, 的空间构型为
的空间构型为________ ;SO2、SO3杂化轨道类型相同,但键角SO3大于SO2,原因是_______ 。
(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则[Cu(CN)4]2-中σ键与π键的数目之比为_______ 。
(5)铜的晶胞结构如图所示。
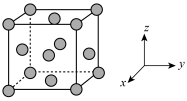
①铜晶胞在x轴方向的投影图是_____ (填标号)。
A.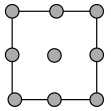 B.
B. 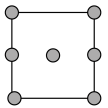
C.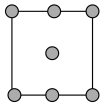 D.
D. 
②假设铜晶胞参数为anm,铜晶体的密度为bg·cm-3,则铜的相对原子质量为_____ (设NA为阿伏加德罗常数的值,用含a、b、NA的代数式表示)。
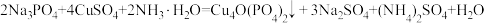 。回答下列问题:
。回答下列问题:(1)铜位于周期表中
(2)上述方程式中涉及的N、O、P、S元素第一电离能由小到大的顺序为
(3)常见含硫的微粒有SO2、SO3、
 等,
等, 的空间构型为
的空间构型为(4)在硫酸铜溶液中加入过量KCN,生成配合物[Cu(CN)4]2-,则[Cu(CN)4]2-中σ键与π键的数目之比为
(5)铜的晶胞结构如图所示。

①铜晶胞在x轴方向的投影图是
A.
 B.
B. 
C.
 D.
D. 
②假设铜晶胞参数为anm,铜晶体的密度为bg·cm-3,则铜的相对原子质量为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】K、Al、Si、Cu、N i均为重要的合金材料,在工业生产、科技、国防领域有着广泛的用途,请回答下列问题:
(1)K元素处于元素周期表的_____ 区。
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是______ (填标号)。
A. [Ne] B. [Ne]
B. [Ne]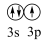 C. [Ne]
C. [Ne] 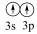 D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是_____________ 。
(4)一些化合物的熔点如下表所示:
解释表中化合物之间熔点差异的原因________________________________ 。
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是_______ 。
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式_________ 。
③1mol[Ni (NH3)6]SO4中含有δ键的数目为___________ 。
④NH3的VSEPR模型为____ ;NH3、SO42-的中心原子的杂化类型分别为___ 、___ 。
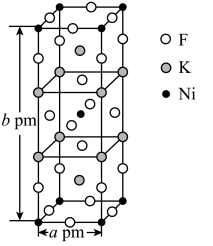
(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=______ g·cm-3(用代数式表示)。
(1)K元素处于元素周期表的
(2)下列状态的铝中,电离最外层一个电子所需能量最大的是
A. [Ne]
 B. [Ne]
B. [Ne] C. [Ne]
C. [Ne]  D. [Ne]
D. [Ne]
(3)从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因是
(4)一些化合物的熔点如下表所示:
| 化合物 | NaCl | KCl | SiO2 |
| 熔点/°C | 801 | 770 | 1723 |
解释表中化合物之间熔点差异的原因
(5)NiSO4溶于氨水形成[Ni (NH3)6]SO4。
①N、O、S三种元素中电负性最大的是
②写出一种与[Ni (NH3)6]SO4中的阴离子互为等电子体的分子的分子式
③1mol[Ni (NH3)6]SO4中含有δ键的数目为
④NH3的VSEPR模型为

(6)K、Ni、F三种元素组成的一种晶体的长方体晶胞结构如图所示。若NA为阿伏加 德罗常数的值,该晶体的密度ρ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】 、
、 是近年来常用的高温表层超导材料,其母体常
是近年来常用的高温表层超导材料,其母体常 。请回答下列与之相关的问题:
。请回答下列与之相关的问题:
(1)基态 原子的电子排布式为
原子的电子排布式为__________ , 的第一电离能比
的第一电离能比 大,其原因
大,其原因__________ 。
(2) 为白色结晶粉末,熔点2020℃。
为白色结晶粉末,熔点2020℃。 的晶体类型为
的晶体类型为__________ , 的空间构型为
的空间构型为__________ 。
(3)用 做电极材料,通过光电解可将
做电极材料,通过光电解可将 和
和 催化合成
催化合成 ,其工作原理如图所示,羟基自由基
,其工作原理如图所示,羟基自由基 的电子式为
的电子式为__________ , 、
、 、
、 中键角的大小顺序为
中键角的大小顺序为__________ 。

(4) 、
、 、
、 形成的一种新型超导材料的晶胞如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。
形成的一种新型超导材料的晶胞如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。 原子①的坐标为
原子①的坐标为 ,
, 原子②的坐标为
原子②的坐标为 ,
, 原子③的坐标为
原子③的坐标为 ,则
,则 原子④的坐标为
原子④的坐标为__________ ;已知晶胞参数如图所示,晶胞棱边夹角均为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为__________  (列式表示)。
(列式表示)。

 、
、 是近年来常用的高温表层超导材料,其母体常
是近年来常用的高温表层超导材料,其母体常 。请回答下列与之相关的问题:
。请回答下列与之相关的问题:(1)基态
 原子的电子排布式为
原子的电子排布式为 的第一电离能比
的第一电离能比 大,其原因
大,其原因(2)
 为白色结晶粉末,熔点2020℃。
为白色结晶粉末,熔点2020℃。 的晶体类型为
的晶体类型为 的空间构型为
的空间构型为(3)用
 做电极材料,通过光电解可将
做电极材料,通过光电解可将 和
和 催化合成
催化合成 ,其工作原理如图所示,羟基自由基
,其工作原理如图所示,羟基自由基 的电子式为
的电子式为 、
、 、
、 中键角的大小顺序为
中键角的大小顺序为
(4)
 、
、 、
、 形成的一种新型超导材料的晶胞如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。
形成的一种新型超导材料的晶胞如图所示,以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。 原子①的坐标为
原子①的坐标为 ,
, 原子②的坐标为
原子②的坐标为 ,
, 原子③的坐标为
原子③的坐标为 ,则
,则 原子④的坐标为
原子④的坐标为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则晶体的密度为
,则晶体的密度为 (列式表示)。
(列式表示)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某矿渣的主要成分为 ,杂质包括
,杂质包括 、
、 、FeO、
、FeO、 ,工业上用该矿渣获取铜和胆矾的操作流程如图:
,工业上用该矿渣获取铜和胆矾的操作流程如图:

已知:① 。
。
②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
(1)胆矾在金属冶炼、化工、药用等领域都有着重要用途。写出基态 的核外电子排布式:
的核外电子排布式:___________ 。 的空间结构为
的空间结构为___________ 。
(2)固体混合物A中的成分是___________ 。
(3)洗涤 粗产品不能用大量水洗,而用少量乙醇冲洗,其优点是
粗产品不能用大量水洗,而用少量乙醇冲洗,其优点是___________ 。
(4)用NaClO调pH可以生成沉淀B,其离子方程式为___________ 。
(5)25℃时,可用___________ (填化学式)调pH可以生成沉淀C,利用题中所给信息分析 的范围为
的范围为___________ 。 的
的 的数量级为
的数量级为___________ 。(若溶液中某离子浓度小于 ,可视为该离子已沉淀完全。)
,可视为该离子已沉淀完全。)
 ,杂质包括
,杂质包括 、
、 、FeO、
、FeO、 ,工业上用该矿渣获取铜和胆矾的操作流程如图:
,工业上用该矿渣获取铜和胆矾的操作流程如图:
已知:①
 。
。②部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示:
| 沉淀物 |  |  |  |  |
| 开始沉淀pH | 5.4 | 4.0 | 2.7 | 5.8 |
| 完全沉淀pH | 6.7 | 5.2 | 3.2 | 8.8 |
 的核外电子排布式:
的核外电子排布式: 的空间结构为
的空间结构为(2)固体混合物A中的成分是
(3)洗涤
 粗产品不能用大量水洗,而用少量乙醇冲洗,其优点是
粗产品不能用大量水洗,而用少量乙醇冲洗,其优点是(4)用NaClO调pH可以生成沉淀B,其离子方程式为
(5)25℃时,可用
 的范围为
的范围为 的
的 的数量级为
的数量级为 ,可视为该离子已沉淀完全。)
,可视为该离子已沉淀完全。)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】回答下列问题:
(1)Xe是第五周期的稀有气体元素,与 形成的
形成的 室温下易升华。
室温下易升华。 中心原子的价层电子对数为
中心原子的价层电子对数为_______ ,下列对 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是_______ (填标号)。
A. B.
B. C.
C. D.
D.
(2)已知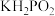 是次磷酸的正盐,
是次磷酸的正盐, 的结构式为
的结构式为_______ ,其中P采取_______ 杂化方式。
(3)氨硼烷在催化剂作用下水解释放氢气: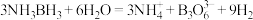 。
。 的结构为
的结构为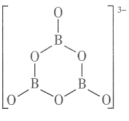 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由_______ 变为_______ 。
(4)乙二胺 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是_______ 、_______ 。
(1)Xe是第五周期的稀有气体元素,与
 形成的
形成的 室温下易升华。
室温下易升华。 中心原子的价层电子对数为
中心原子的价层电子对数为 中心原子杂化方式推断合理的是
中心原子杂化方式推断合理的是A.
 B.
B. C.
C. D.
D.
(2)已知
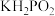 是次磷酸的正盐,
是次磷酸的正盐, 的结构式为
的结构式为(3)氨硼烷在催化剂作用下水解释放氢气:
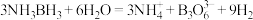 。
。 的结构为
的结构为 。在该反应中,B原子的杂化轨道类型由
。在该反应中,B原子的杂化轨道类型由(4)乙二胺
 是一种有机化合物,分子中氮、碳的杂化类型分别是
是一种有机化合物,分子中氮、碳的杂化类型分别是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】非线性光学晶体在信息、激光技术、医疗、国防等领域具有重要应用价值。我国科学家利用 Cs2CO3、XO2(X=Si、Ge)和 H3BO3首次合成了组成为 CsXB3O7的非线性光学晶体。回答下列问题:
(1)C、O、Si 三种元素电负性由大到小的顺序为_______ ;第一电离能I1(Si) ___ I1(Ge)(填>或<)。
(2)基态Ge 原子简化核外电子排布式为_________ ;SiO2、 GeO2 具有类似的晶体结构, 其中熔点较高的是 __________ , 原因是 _________ 。
(3)如图为硼酸晶体的片层结构,其中硼的杂化方式为____________ 。

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为 apm、b pm、c pm。如图为沿 y 轴投影的晶胞中所有 Cs 原子的分布图和原子分数坐标。CsSiB3O7的摩尔质量为 M g•mol-1,设 NA为阿伏加 德罗常数的值,则CsSiB3O7晶体的密度为_________ g•cm-3(用代数式表示)。

(1)C、O、Si 三种元素电负性由大到小的顺序为
(2)基态Ge 原子简化核外电子排布式为
(3)如图为硼酸晶体的片层结构,其中硼的杂化方式为

(4)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为 apm、b pm、c pm。如图为沿 y 轴投影的晶胞中所有 Cs 原子的分布图和原子分数坐标。CsSiB3O7的摩尔质量为 M g•mol-1,设 NA为阿伏加 德罗常数的值,则CsSiB3O7晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知Mn、Fe、Co是组成合金的重要元素,P、S、Cl是农药中的重要元素。回答下列问题:
(1)Mn元素位于元素周期表的______ 区,基态锰原子的价电子排布图为_____ 。
(2)P、S、Cl三种元素的第一电离能由大到小顺序为________ 。
(3)已知NH3的沸点高于PH3,原因是________ 。
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为: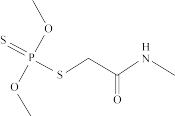 ,其中N原子的杂化类型为
,其中N原子的杂化类型为________ 。
(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为_______ 。
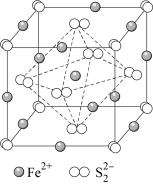
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S 的数目为
的数目为_____ 。如可用晶胞参数为单位长度建立的坐标系表示晶胞中各原子的位置,并称作原子分数坐标,则该晶胞中体心Fe2+的坐标为__________ 。
(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =______ (用d、NA表示a)。
(1)Mn元素位于元素周期表的
(2)P、S、Cl三种元素的第一电离能由大到小顺序为
(3)已知NH3的沸点高于PH3,原因是
(4)农药“乐果”中的主要成分O,O-二甲基-S-(N-甲基氨基甲酰甲基)二硫代磷酸酯的分子结构为:
 ,其中N原子的杂化类型为
,其中N原子的杂化类型为(5)已知P4(白磷)为正四面体结构,与氧气反应生成非极性分子P4O10,其中P在空间的相对位置不变,则P4O10中σ键和π键的数目之比为
(6)已知一种立方型FeS2晶体的晶胞如图所示,则与体心Fe2+距离最近且等距离的S
 的数目为
的数目为(7)已知该立方型FeS2晶体的晶胞参数为a pm,密度为d g·cm-3, 阿伏加德罗常数的值为NA,则a与d的关系是a =

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】[化学—选修物质结构与性质]
铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为 ,基态Fe原子的价电子排布式为 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是 ,Fe(CO)5在空气中燃烧后剩余固体呈红棕色,其化学方程式为 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是 ,配体中提供孤对电子的原子是 。
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有 形成。
a.离子键 b.配位键 c.非极性键 d.б键
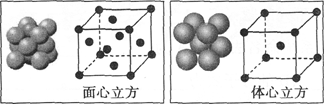
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为 ,面心立方堆积与体心立方堆积的两种铁晶体的密度之比为 (写出已化简的比例式即可)。
铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为:[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。
请回答下列问题:
(1)C、N、O的电负性由大到小的顺序为 ,基态Fe原子的价电子排布式为 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是 ,Fe(CO)5在空气中燃烧后剩余固体呈红棕色,其化学方程式为 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型是 ,配体中提供孤对电子的原子是 。
(4)用[Cu(NH3)2]OOCCH3除去CO的反应中,肯定有 形成。
a.离子键 b.配位键 c.非极性键 d.б键
(5)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为 ,面心立方堆积与体心立方堆积的两种铁晶体的密度之比为 (写出已化简的比例式即可)。

您最近一年使用:0次



