已知 与
与 的
的 分别为
分别为 与
与 。实验桌上有4杯水溶液,分别为(1)
。实验桌上有4杯水溶液,分别为(1)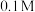 的
的 、(2)
、(2) 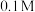 的
的 、(3)
、(3) 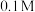 的
的 与(4)
与(4) 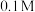 的
的 。若将等体积(1)与(2)混合得溶液甲,等体积(1)与(3)混合得溶液乙,等体积(1)与(4)混合得溶液丙,则溶液甲、乙与丙的
。若将等体积(1)与(2)混合得溶液甲,等体积(1)与(3)混合得溶液乙,等体积(1)与(4)混合得溶液丙,则溶液甲、乙与丙的 浓度由小至大的顺序为何?
浓度由小至大的顺序为何?
 与
与 的
的 分别为
分别为 与
与 。实验桌上有4杯水溶液,分别为(1)
。实验桌上有4杯水溶液,分别为(1)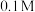 的
的 、(2)
、(2) 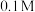 的
的 、(3)
、(3) 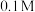 的
的 与(4)
与(4) 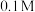 的
的 。若将等体积(1)与(2)混合得溶液甲,等体积(1)与(3)混合得溶液乙,等体积(1)与(4)混合得溶液丙,则溶液甲、乙与丙的
。若将等体积(1)与(2)混合得溶液甲,等体积(1)与(3)混合得溶液乙,等体积(1)与(4)混合得溶液丙,则溶液甲、乙与丙的 浓度由小至大的顺序为何?
浓度由小至大的顺序为何?| A.甲<乙<丙 |
| B.乙<甲<丙 |
| C.丙<乙<甲 |
| D.甲<丙<乙 |
| E.丙<甲<乙 |
更新时间:2022-08-16 16:59:38
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】常温下 的电离常数为
的电离常数为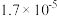 ,该温度下用
,该温度下用 的醋酸溶液滴定
的醋酸溶液滴定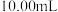 等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积
等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积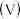 与溶液中
与溶液中 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是
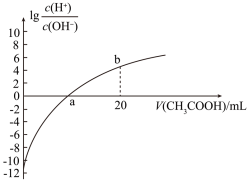
 的电离常数为
的电离常数为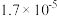 ,该温度下用
,该温度下用 的醋酸溶液滴定
的醋酸溶液滴定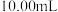 等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积
等物质的量浓度的碱ROH,滴定过程中加入醋酸的体积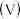 与溶液中
与溶液中 的关系如图所示。下列说法中正确的是
的关系如图所示。下列说法中正确的是

| A.b点溶液显碱性 |
B.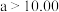 |
C.ROH 的电离方程式为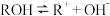 |
D. 时, 时,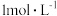 的醋酸溶液中 的醋酸溶液中 的浓度约为 的浓度约为 已知 已知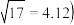 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向 A、B两支试管中各加入2 mL10%的H2O2溶液,向B试管中加入2滴1 mol·L-1FeCl3溶液 | B试管中产生气泡快 | 当其它条件不变时,催化剂可以改变化学反应速率 |
| B | 蒸干并灼烧AlCl3溶液 | 得到白色固体 | 获得Al2O3固体 |
| C | 分别将1 mL pH=3的HA和HB溶液加水稀释至100 mL,测溶液pH | pH(HA)>pH(HB) | 酸性:HA<HB |
| D | 向某溶液中滴加 K3[Fe(CN)6]溶液 | 产生蓝色沉淀 | 溶液中存在Fe2+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,向 溶液中逐滴加入
溶液中逐滴加入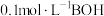 (一元碱)溶液,同时分别测得溶液的pH和导电能力随加入BOH溶液体积的变化如图所示。下列说法错误的是
(一元碱)溶液,同时分别测得溶液的pH和导电能力随加入BOH溶液体积的变化如图所示。下列说法错误的是

 溶液中逐滴加入
溶液中逐滴加入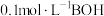 (一元碱)溶液,同时分别测得溶液的pH和导电能力随加入BOH溶液体积的变化如图所示。下列说法错误的是
(一元碱)溶液,同时分别测得溶液的pH和导电能力随加入BOH溶液体积的变化如图所示。下列说法错误的是
| A.c点和m点对应同一溶液 |
B. |
C.b点对应溶液中一定存在 |
D.水的电离程度: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,有关盐酸与醋酸溶液的说法正确的是( )
| A.pH=2.0 的盐酸和醋酸溶液,等体积混合后溶液的 pH >2.0 |
| B.浓度为0.1 mol·L -1 等体积的盐酸和醋酸溶液加水稀释 10 倍后,c( Cl-)> c(CH3COO- ) |
| C.相同浓度的两溶液,分别与NaOH 固体反应后呈中性的溶液中(忽略溶液体积变化):c(CH3COO-)=c(Cl- ) |
| D.等浓度的盐酸和醋酸与足量的锌反应产生气体的体积(同温同压时)相同 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知室温时,NaHA水溶液呈酸性,NaHB水溶液呈碱性。下列有关说法正确的是
A.NaHA溶液中一定存在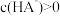 |
B.NaHB溶液中的离子浓度关系为 |
| C.H2A的电离常数Ka2一定大于H2B的电离常数Ka1 |
D.NaHB溶液加水稀释时 一定减小 一定减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知: ;
;  。25℃时,向某浓度的
。25℃时,向某浓度的 溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中
溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是

 ;
;  。25℃时,向某浓度的
。25℃时,向某浓度的 溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中
溶液中逐滴滴加一定浓度的NaOH溶液,所得溶液中 、
、 、
、 三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是
三种微粒的物质的量分数(δ)与溶液pH的关系如图所示。下列说法错误的是
A.曲线3表示的微粒是 |
| B.25℃时,Kal/ Ka2=1000 |
C.溶液的pH=1.2时,溶液中有c(Na+)+c(H+)=c(OH-)+c( ) ) |
D.溶度的pH=4.2时,溶液中有c(Na+)+c(H+)=c(OH-)+2c( ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关电解质溶液的说法正确的是
A.在25℃下, 的 的 与 与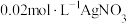 溶液等体积混合,有白色沉淀生成 溶液等体积混合,有白色沉淀生成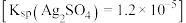 |
B.室温下,弱酸的酸式盐NaHA的溶液中存在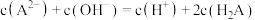 |
C.某温度下, 与 与 的电离常数相等,稀醋酸铵溶液中: 的电离常数相等,稀醋酸铵溶液中: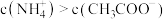 |
D. 溶液中: 溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】常温下,向20mL0.01mol·L-1的NaOH溶液中逐滴加入0.01mol·L-1的CH3COOH溶液,溶液中水所电离出的c(OH-)的对数随加入 CH3COOH溶液的体积变化如图所示,下列说法正确的是
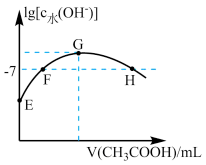

| A.F点溶液显中性 |
| B.若G点由水电离出的c(OH-)=2.24×10-6mol·L-1,则Ka(CH3COOH)≈1×10-6 |
| C.H点离子浓度关系为c( CH3COO-)=c(Na+)>c(H+)=c(OH-) |
| D.E点由水电离的c(H+)=10-3mol·L-1 |
您最近一年使用:0次



