钴是一种重要战略物质,由钴催化剂废料(含Co2O3、Fe2O3、CuO等杂质)制备CoCO3和高效净水剂黄钠铁矾[NaFe3(SO4)2(OH)6]的工艺流程如图所示:

已知:(i)氧化性:Co3+> >Fe3+。
>Fe3+。
(ii)CoCO3、Co(OH)2、黄钠铁矾[NaFe3(SO4)2 (OH)6]均难溶于水。
(1)写出两条提高还原含钴废催化剂时浸取率的措施_______ 。
(2)“还原浸出”中,Co2O3被Na2SO3还原的化学方程式为_______ 。
(3)“氧化”中,被氧化的离子有_______ 。
(4)如图表示几种含铁物质稳定存在时与溶液和温度的关系,其中阴影部分表示黄钠铁矾。若工艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制溶液的pH范围为_______ 。

(5)若选用MnS“除铜”,计算常温下“除铜”反应的平衡常数K=_______ [已知常温下,Ksp(MnS)=2.6 ×10-13,Kp (CuS)=1.3×10-36]。
(6)“沉钴”时,加入小苏打发生反应的离子反应方程式为_______ ,不宜用 Na2CO3代替NaHCO3的原因是_______ 。

已知:(i)氧化性:Co3+>
 >Fe3+。
>Fe3+。(ii)CoCO3、Co(OH)2、黄钠铁矾[NaFe3(SO4)2 (OH)6]均难溶于水。
(1)写出两条提高还原含钴废催化剂时浸取率的措施
(2)“还原浸出”中,Co2O3被Na2SO3还原的化学方程式为
(3)“氧化”中,被氧化的离子有
(4)如图表示几种含铁物质稳定存在时与溶液和温度的关系,其中阴影部分表示黄钠铁矾。若工艺在100℃左右进行,为使铁转化为黄钠铁矾,应控制溶液的pH范围为

(5)若选用MnS“除铜”,计算常温下“除铜”反应的平衡常数K=
(6)“沉钴”时,加入小苏打发生反应的离子反应方程式为
2022·四川乐山·一模 查看更多[5]
(已下线)化学(全国乙卷理综卷)-学易金卷:2023年高考第一次模拟考试卷江苏省泰州中学2022-2023学年高三上学期第一次月度检测化学试题江苏省如东高级中学2023届高三上学期期初学情检测化学试题甘肃省张掖市高台县第一中学2022-2023学年高三上学期开学第一次检测化学试题四川省乐山市高中2022届第一次调研考试理综化学试题
更新时间:2022-08-25 21:22:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】研究性学习小组对某硫酸亚铁晶体(FeSO4·xH2O)热分解研究,该小组同学称取ag硫酸亚铁晶体样品按图1高温加热,使其完全分解,对所得产物进行探究,并通过称量装置B质量测出x的值。
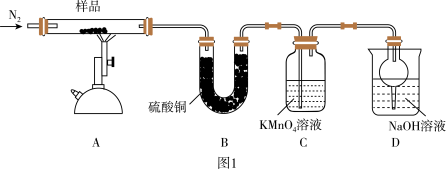
(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水。
(2)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体氧化铁。
(3)装置C中高锰酸钾溶液褪色,说明产物中存在气体______ 。
(4)实验中要持续通入氮气,否则测出的x会_____ (填“偏大”、“偏小”或“不变”)。
(5)从理论上分析得出硫酸亚铁分解还生成另一物质三氧化硫,写出硫酸亚铁分解的化学方程式________ 。
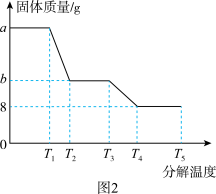
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量分解温度的关系如图2,根据图2中有关数据,可计算出FeSO4·xH2O中的x=______ 。


(1)装置B中硫酸铜粉末变蓝,质量增加12.6g,说明产物中有水。
(2)硫酸亚铁晶体完全分解后装置A中还残留红棕色固体氧化铁。
(3)装置C中高锰酸钾溶液褪色,说明产物中存在气体
(4)实验中要持续通入氮气,否则测出的x会
(5)从理论上分析得出硫酸亚铁分解还生成另一物质三氧化硫,写出硫酸亚铁分解的化学方程式
(6)某研究所利用SDTQ600热分析仪对硫酸亚铁晶体(FeSO4·xH2O)进行热分解,获得相关数据,绘制成固体质量分解温度的关系如图2,根据图2中有关数据,可计算出FeSO4·xH2O中的x=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】铁元素属于过渡元素,在化学反应中最外层和次外层均可失去电子。铁在化合物中通常显+2价、+3价。
实验甲组用如图所示的装置制备白色的

供选择的试剂有:①铁粉 ②稀硫酸 ③NaOH溶液
(1)装置I中加入___________ (填写编号)
(2)本实验成功的关键是___________ 。
A.实验过程隔绝空气(氧气) B.实验过程空气(氧气)充足
若控制不当,将会生成___________ 色的 沉淀。反应的化学方程式为
沉淀。反应的化学方程式为___________ 。
(3)待装置Ⅱ中a处收集到的 纯净后,如何操作会得到白色的
纯净后,如何操作会得到白色的 沉淀?
沉淀?_______ 。
实验乙组用如下实验步骤探究 和
和 的性质
的性质
(4)分别取一定量 、
、 固体,均配制成
固体,均配制成 的溶液。为防止
的溶液。为防止 溶液被氧化,可向溶液中加入
溶液被氧化,可向溶液中加入___________ 。
A.铁片 B.酸性 溶液
溶液
(5)取 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红。书写
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红。书写 溶液与氯水反应的离子方程式。
溶液与氯水反应的离子方程式。___________ 。
(6)取 溶液,向其中加入
溶液,向其中加入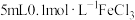 溶液,充分振荡。分别取2mL混合溶液进行如下实验:
溶液,充分振荡。分别取2mL混合溶液进行如下实验:
通过实验①可知两种溶液混合___________ 反应(“发生”或“不发生”)。结合题干和实验②的实验结论,你能得出什么结论?___________ 。
实验甲组用如图所示的装置制备白色的


供选择的试剂有:①铁粉 ②稀硫酸 ③NaOH溶液
(1)装置I中加入
(2)本实验成功的关键是
A.实验过程隔绝空气(氧气) B.实验过程空气(氧气)充足
若控制不当,将会生成
 沉淀。反应的化学方程式为
沉淀。反应的化学方程式为(3)待装置Ⅱ中a处收集到的
 纯净后,如何操作会得到白色的
纯净后,如何操作会得到白色的 沉淀?
沉淀?实验乙组用如下实验步骤探究
 和
和 的性质
的性质(4)分别取一定量
 、
、 固体,均配制成
固体,均配制成 的溶液。为防止
的溶液。为防止 溶液被氧化,可向溶液中加入
溶液被氧化,可向溶液中加入A.铁片 B.酸性
 溶液
溶液(5)取
 溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红。书写
溶液,加入几滴氯水,再加入1滴KSCN溶液,溶液变红。书写 溶液与氯水反应的离子方程式。
溶液与氯水反应的离子方程式。(6)取
 溶液,向其中加入
溶液,向其中加入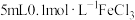 溶液,充分振荡。分别取2mL混合溶液进行如下实验:
溶液,充分振荡。分别取2mL混合溶液进行如下实验:| 实验序号 | 加入试剂 | 现象 | 结论 |
| ① |  溶液 溶液 |  层呈现紫色 层呈现紫色 | |
| ② | 1滴KSCN溶液 | 溶液变红 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯化亚铜(CuCl)是一种重要化工原料,难溶于水,在潮湿空气中易水解氧化。回答下列问题:
(1)向 与NaCl的混合溶液中通入
与NaCl的混合溶液中通入 即可制得CuCl,制备过程中主要发生了以下三步反应,请写出第三步的化学反应方程式:
即可制得CuCl,制备过程中主要发生了以下三步反应,请写出第三步的化学反应方程式:


___________ 。
(2)CuCl在含一定浓度 溶液中会部分溶解,存在如下平衡:
溶液中会部分溶解,存在如下平衡:
 ,溶液中
,溶液中 和
和 的关系如图。
的关系如图。

①上述反应在B点的平衡常数
___________  。
。
②使图中的A点变为B点的措施可以是___________ 。
(3)利用CuCl难溶于水的性质,可以除去水溶液中的 。
。
①除 的方法是向含
的方法是向含 的溶液同时加入Cu和
的溶液同时加入Cu和 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
②若用Zn替换Cu可加快除 速率,但需控制溶液的pH。若pH过低,除
速率,但需控制溶液的pH。若pH过低,除 效果下降的原因是
效果下降的原因是___________ 。
(4)产品纯度的测定:准确称取氯化亚铜产品2.3900g,溶于过量的 溶液中得250mL待测液,从中量取25.00mL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用
溶液中得250mL待测液,从中量取25.00mL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用 硫酸铈[Ce(SO4)2]标准溶液滴定至终点,共完成三次滴定,每次消耗
硫酸铈[Ce(SO4)2]标准溶液滴定至终点,共完成三次滴定,每次消耗 溶液体积见下表。产品中CuCl的质量分数为
溶液体积见下表。产品中CuCl的质量分数为___________ %。(已知: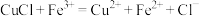 ,
, )
)
若未用标准溶液润洗滴定管,则会使测定结果___________ (填“偏大”、“偏小”或“不变”)。
(1)向
 与NaCl的混合溶液中通入
与NaCl的混合溶液中通入 即可制得CuCl,制备过程中主要发生了以下三步反应,请写出第三步的化学反应方程式:
即可制得CuCl,制备过程中主要发生了以下三步反应,请写出第三步的化学反应方程式:

(2)CuCl在含一定浓度
 溶液中会部分溶解,存在如下平衡:
溶液中会部分溶解,存在如下平衡:
 ,溶液中
,溶液中 和
和 的关系如图。
的关系如图。
①上述反应在B点的平衡常数

 。
。②使图中的A点变为B点的措施可以是
(3)利用CuCl难溶于水的性质,可以除去水溶液中的
 。
。①除
 的方法是向含
的方法是向含 的溶液同时加入Cu和
的溶液同时加入Cu和 ,该反应的离子方程式为
,该反应的离子方程式为②若用Zn替换Cu可加快除
 速率,但需控制溶液的pH。若pH过低,除
速率,但需控制溶液的pH。若pH过低,除 效果下降的原因是
效果下降的原因是(4)产品纯度的测定:准确称取氯化亚铜产品2.3900g,溶于过量的
 溶液中得250mL待测液,从中量取25.00mL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用
溶液中得250mL待测液,从中量取25.00mL于锥形瓶中,加入2滴邻菲罗啉指示剂,立即用 硫酸铈[Ce(SO4)2]标准溶液滴定至终点,共完成三次滴定,每次消耗
硫酸铈[Ce(SO4)2]标准溶液滴定至终点,共完成三次滴定,每次消耗 溶液体积见下表。产品中CuCl的质量分数为
溶液体积见下表。产品中CuCl的质量分数为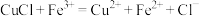 ,
, )
)| 1 | 2 | 3 | |
| 消耗硫酸铈标准溶液的体积(mL) | 23.85 | 24.35 | 23.95 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】镀镍生产过程中产生的酸性硫酸镍废液(含有Fe2+、Zn2+、Mg2+、Ca2+等杂质离子),通过精制提纯可制备高纯硫酸镍,部分流程如图:
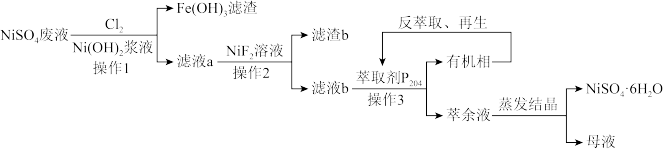
资料1:25℃时,生成氢氧化物沉淀的pH
注:金属离子的起始浓度为0.1mol/L.
资料2:25℃时,Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9,ZnF2易溶于水。
资料3:P204(二乙基己基磷酸)萃取金属离子的反应为:x +Mx+
+Mx+
 M+xH+
M+xH+
(1)操作1、2的名称是____ ,操作3的名称是____ 。
(2)操作1中加入Cl2的主要目的是____ 。
(3)NiF2溶液参与反应的离子方程式是____ 。杂质离子沉淀完全时,溶液中c(F-)=____ mol/L(c(杂质离子)≤10-5mol/L即可视为沉淀完全)。
(4)滤液b中含有的微粒主要有____ 。
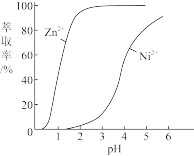
(5)在硫酸盐溶液中,P204对某些金属离子的萃取率与pH关系如图所示,在一定范围内,随着pH升高,萃取率升高的原因是____ 。
(6)在母液中加入其它物质,可制备操作1中所需Ni(OH)2浆液,写出制备的离子方程式____ 。

资料1:25℃时,生成氢氧化物沉淀的pH
| Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Mg(OH)2 | Ca(OH)2 | Ni(OH)2 | |
| 开始沉淀时 | 6.3 | 1.5 | 6.2 | 9.1 | 11.8 | 6.9 |
| 完全沉淀时 | 8.3 | 2.8 | 8.2 | 11.1 | 13.8 | 8.9 |
注:金属离子的起始浓度为0.1mol/L.
资料2:25℃时,Ksp(CaF2)=4×10-11,Ksp(MgF2)=9×10-9,ZnF2易溶于水。
资料3:P204(二乙基己基磷酸)萃取金属离子的反应为:x
 +Mx+
+Mx+
 M+xH+
M+xH+(1)操作1、2的名称是
(2)操作1中加入Cl2的主要目的是
(3)NiF2溶液参与反应的离子方程式是
(4)滤液b中含有的微粒主要有
(5)在硫酸盐溶液中,P204对某些金属离子的萃取率与pH关系如图所示,在一定范围内,随着pH升高,萃取率升高的原因是

(6)在母液中加入其它物质,可制备操作1中所需Ni(OH)2浆液,写出制备的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】废弃物的综合利用既有利于节约资源,又有利于保护环境。实验室利用废旧铜片回收Cu并制备绿矾晶体的部分实验过程如下:

已知: I2+2S2O =S4O
=S4O +2I-
+2I-
(1)①铜片溶解时加入H2O2的作用是___________ (用化学方程式表示)
②铜片溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是___________
(2)某学习小组用“间接碘量法”测定试样A中Cu2+ (不含能与I- 发生反应的杂质)的浓度。过程如下:取20.00mL试样于锥形瓶中,加入过量KI.固体,充分反应,生成白色沉淀。用0.1000mol/L的Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液10.00 mL。
①可选用___________ 作滴定指示剂,滴定终点的现象是___________
②CuCl2溶液与KI反应的离子方程式为___________
③试样A中c(Cu2+)为___________ mol/L
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、 Au等杂质)的电解精炼,下列说法正确的是___________
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(4)①从滤液B中制取绿矾晶体的实验操作为___________
②某溶液中c(Fe3+)= 0.100mol/L, c(Cu2+)= 0.200mol/L。要实现Fe3+沉淀完全而Cu2+保持不变,可控制溶液pH范围为___________

已知: I2+2S2O
 =S4O
=S4O +2I-
+2I-| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2 ×10-20 | 4.0 ×10-38 | 1.7 ×10-7 | 1.3 ×10-12 |
(1)①铜片溶解时加入H2O2的作用是
②铜片溶解完全后,需将溶液中过量的H2O2除去。除去H2O2的简便方法是
(2)某学习小组用“间接碘量法”测定试样A中Cu2+ (不含能与I- 发生反应的杂质)的浓度。过程如下:取20.00mL试样于锥形瓶中,加入过量KI.固体,充分反应,生成白色沉淀。用0.1000mol/L的Na2S2O3标准溶液滴定,到达滴定终点时,消耗Na2S2O3标准溶液10.00 mL。
①可选用
②CuCl2溶液与KI反应的离子方程式为
③试样A中c(Cu2+)为
(3)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、 Au等杂质)的电解精炼,下列说法正确的是
a.电能全部转化为化学能
b.粗铜接电源正极,发生氧化反应
c.溶液中Cu2+向阳极移动
d.利用阳极泥可回收Ag、Pt、Au等金属
(4)①从滤液B中制取绿矾晶体的实验操作为
②某溶液中c(Fe3+)= 0.100mol/L, c(Cu2+)= 0.200mol/L。要实现Fe3+沉淀完全而Cu2+保持不变,可控制溶液pH范围为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯[主要成分为Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等]生产硫酸镍、碳酸钴的工艺流程如图。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
回答下列问题:
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法___________________ (写一种)。
(2)沉淀A的主要成分___________ ,步骤②调pH的范围为___________ ,证明沉淀A已经洗净的实验操作为______________ 。
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是__________ 。
(4)步骤④离子方程式___________ ,若用盐酸代替H2SO4和H2O2的混合液也能达到目的,从环保角度分析不采用盐酸的原因:___________________________ 。
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为___________________ 。
(6)步骤⑧的操作为___________________ 。

已知:部分金属阳离子以氢氧化物的形式沉淀时溶液的pH见表:
| 金属阳离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时pH(金属阳离子浓度<10-5mol/L) | 9.0 | 3.2 | 4.7 | 9.2 | 9.15 |
(1)步骤①用稀硫酸浸取金属电极芯前,提高浸取率方法
(2)沉淀A的主要成分
(3)将“母液1”的pH调至3~4,再加入NaClO,NaClO的作用是
(4)步骤④离子方程式
(5)步骤⑤中“母液3”与NaHCO3溶液反应的离子方程式为
(6)步骤⑧的操作为
您最近一年使用:0次
【推荐2】Mo、Co均为重要战略性金属。以Al2O3为载体的钴钼废催化剂中含CoS、MoS2及少量Fe、Si、Ca等元素的物质,经系列处理可制取CoCO3、(NH4)2MoO4,工艺流程如图所示:

已知:①“焙烧”后各元素转化为相应氧化物,“酸浸”后钼元素转化为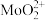 。
。
②常温下, ,
, ,
,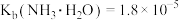 。
。
③金属离子开始沉淀和完全沉淀时pH范围:Al3+(3.7~4.7),Fe3+(1.9~3.2), Co2+(7.2~9.2)。
(1)MoS2在空气中焙烧的化学方程式为___________ 。焙烧过程中采用多层逆流(空气从炉底进入,固体粉末从炉顶进入),该操作的优点为___________ 。
(2)“滤渣1”的主要成分为___________ 。“滤渣2”的主要成分为Fe(OH)3和Al(OH)3,“调pH”中调节pH的合理范围为___________ 。
(3)“水相”经萃取后得钴的有机相,存在平衡: ,然后加反萃取剂进行反萃取,可得含Co2+的水溶液,可作为反萃取剂的一种常用物质为
,然后加反萃取剂进行反萃取,可得含Co2+的水溶液,可作为反萃取剂的一种常用物质为___________ (写化学式)溶液。
(4)“沉钴”过程中为防止CoCO3转化为Co(OH)2,需控制溶液pH,转化过程存在平衡: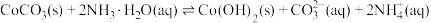 ,该反应的平衡常数K=
,该反应的平衡常数K=___________ (结果保留一位小数)。
(5)氮化钼量子点可应用于电池及催化领域,其晶胞结构如图所示,氮化钼的化学式为___________ ,钼原子周围距离最近的氮原子有___________ 个。若晶胞密度为ρg∙cm-3,则晶胞参数a=___________ nm(设NA为阿伏加德罗常数的值)


已知:①“焙烧”后各元素转化为相应氧化物,“酸浸”后钼元素转化为
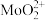 。
。②常温下,
 ,
, ,
,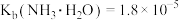 。
。③金属离子开始沉淀和完全沉淀时pH范围:Al3+(3.7~4.7),Fe3+(1.9~3.2), Co2+(7.2~9.2)。
(1)MoS2在空气中焙烧的化学方程式为
(2)“滤渣1”的主要成分为
(3)“水相”经萃取后得钴的有机相,存在平衡:
 ,然后加反萃取剂进行反萃取,可得含Co2+的水溶液,可作为反萃取剂的一种常用物质为
,然后加反萃取剂进行反萃取,可得含Co2+的水溶液,可作为反萃取剂的一种常用物质为(4)“沉钴”过程中为防止CoCO3转化为Co(OH)2,需控制溶液pH,转化过程存在平衡:
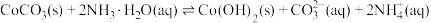 ,该反应的平衡常数K=
,该反应的平衡常数K=(5)氮化钼量子点可应用于电池及催化领域,其晶胞结构如图所示,氮化钼的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】钴被誉为战略物资,有出色的性能和广泛的应用。以水钴矿(主要成分为Co2O3、CoO、CuO、Fe2O3、CaO、MgO、NiO和SiO2等)为原料制备CoCl2·6H2O的工艺流程如图所示:
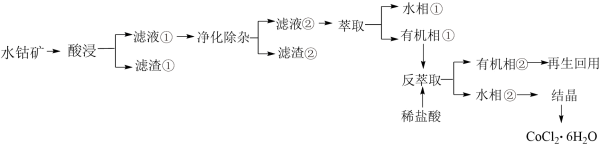
回答下列问题:
Ⅰ.“酸浸”
(1)钴的浸出率随酸浸时间、温度的变化关系如下图所示。综合考虑成本,应选择的最佳工艺条件为_________ 、_________ ;滤渣①的主要成分为__________ 。

(2)Co2O3与浓硫酸反应生成CoSO4,化学方程式为______________________________ 。
Ⅱ.“净化除杂”分三步完成:
(3)除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,离子方程式为____________________________________ 。
(4)除钙、镁:加入适量NaF,当Mg2+恰好完全被除去(离子浓度等于10-5mol·L-1)时,c(Ca2+)=_____________ mol·L-1(取两位有效数字)。已知:Ksp(MgF2)=7.4×10-11,Ksp(CaF2)=1.5×10-10。
(5)除铜:加入适量Na2S2O3,发生反应2CuSO4+2Na2S2O3+2H2O=Cu2S↓+S↓+2Na2SO4+2H2SO4,该反应的还原产物为___________ 。
Ⅲ.“萃取和反萃取”
(6)“水相①”中的主要溶质是Na2SO4和________ (写化学式)。
(7)实验室称取100g原料(含钴11.80%),反萃取时得到浓度为0.036mol·L-1的CoCl2溶液5L,忽略损耗,钴的产率=______ (产率=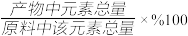 )。
)。

回答下列问题:
Ⅰ.“酸浸”
(1)钴的浸出率随酸浸时间、温度的变化关系如下图所示。综合考虑成本,应选择的最佳工艺条件为

(2)Co2O3与浓硫酸反应生成CoSO4,化学方程式为
Ⅱ.“净化除杂”分三步完成:
(3)除铁:加入适量Na2SO4固体,析出淡黄色晶体黄钠铁矾Na2Fe6(SO4)4(OH)12,离子方程式为
(4)除钙、镁:加入适量NaF,当Mg2+恰好完全被除去(离子浓度等于10-5mol·L-1)时,c(Ca2+)=
(5)除铜:加入适量Na2S2O3,发生反应2CuSO4+2Na2S2O3+2H2O=Cu2S↓+S↓+2Na2SO4+2H2SO4,该反应的还原产物为
Ⅲ.“萃取和反萃取”
(6)“水相①”中的主要溶质是Na2SO4和
(7)实验室称取100g原料(含钴11.80%),反萃取时得到浓度为0.036mol·L-1的CoCl2溶液5L,忽略损耗,钴的产率=
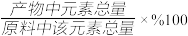 )。
)。
您最近一年使用:0次


 溶液完全转化为沉淀C的实验现象为
溶液完全转化为沉淀C的实验现象为 ,写出相应的离子方程式:
,写出相应的离子方程式:

