Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为____ 。
A. B.
B.
C.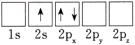 D.
D.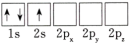
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是____ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是____ ,中心原子的杂化形式为____ 。LiAlH4中,存在下列给出的____ 。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为____ kJ/mol,O=O键能为____ kJ/mol,Li2O晶格能为____ kJ/mol。
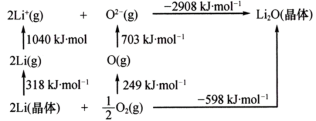
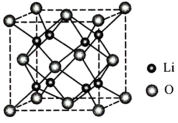
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为____ g•cm-3(列出计算式即可)。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为
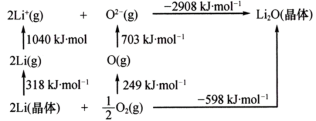
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为

更新时间:2022-09-19 08:37:46
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】按要求填空。
(1)下列原子或离子的电子排布式或排布图正确的是_______ (填序号,下同),违反能量最低原理的是_______ ,违反洪特规则的是_______ ,违反泡利原理的是_______ 。
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:
④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C: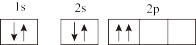
(2) 互为等电子体的离子为
互为等电子体的离子为_______ (只写一个);
(3)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为_______ ;
(4)BF3能与NH3反应生成BF3·NH3.BF3·NH3中B原子的杂化轨道类型为_______ ,B与N之间形成_______ 键。硼酸(H3BO3)在水溶液中能与水反应生成[B(OH)4]-而体现一元弱酸的性质,[B(OH)4]-中B的原子杂化类型为_______ ,不考虑空间构型,[B(OH)4]-的结构可用示意图表示为_______ ;
(5)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为_______ ;
A.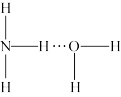 B.
B.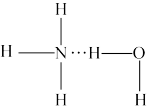 C.
C.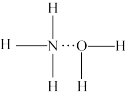 D.
D.
氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺(H2NCl),分子结构类似于NH3,H2NCl分子的空间构型为_______ ,电子式为_______ ,H2NCl中氯的化合价为_______ 。
(1)下列原子或离子的电子排布式或排布图正确的是
①Ca2+:1s22s22p63s23p6
②F-:1s22s23p6
③P:

④Cr:1s22s22p63s23p63d44s2
⑤Fe:1s22s22p63s23p63d64s2
⑥Mg2+:1s22s22p6
⑦C:
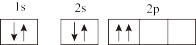
(2)
 互为等电子体的离子为
互为等电子体的离子为(3)Ni与CO能形成配合物Ni(CO)4,该分子中π键与σ键个数比为
(4)BF3能与NH3反应生成BF3·NH3.BF3·NH3中B原子的杂化轨道类型为
(5)氨气溶于水时,大部分NH3与H2O以氢键(用“…”表示)结合形成NH3·H2O分子。根据氨水的性质可推知NH3·H2O的结构式为
A.
 B.
B. C.
C. D.
D.
氨水和次氯酸盐溶液在弱碱性介质中反应可生成氯胺(H2NCl),分子结构类似于NH3,H2NCl分子的空间构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】下图是元素周期表的一部分,图中所列字母分别代表一种化学元素。回答下列问题:
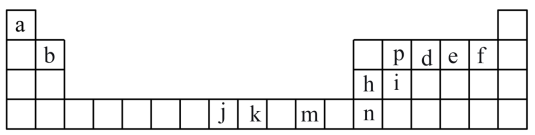
(1)下列正确的是___________。
(2)已知高温下化合物 比化合物
比化合物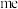 更稳定,试从
更稳定,试从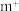 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因___________ 。
(3)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与 溶液反应的离子方程式
溶液反应的离子方程式___________ 。
(4)下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。

分析上图回答下列问题:
①推测ⅣA族 与
与 的沸点大小为
的沸点大小为
___________  (填“>”或“<”)。
(填“>”或“<”)。
②接近水的沸点的水蒸气的相对分子质量测定值比按化学式 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为___________ 。
③ 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,通过
,通过___________ 的实验分析方法可测出 的键长键角信息。
的键长键角信息。

(1)下列正确的是___________。
A.原子半径 | B.第一电离能 |
C.电负性 | D.最高价氧化物的水化物的酸性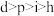 |
 比化合物
比化合物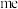 更稳定,试从
更稳定,试从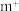 离子的核外电子排布的角度解释原因
离子的核外电子排布的角度解释原因(3)根据对角线规则,b与h的化学性质相似,请写出b的最高价氧化物对应的水化物与
 溶液反应的离子方程式
溶液反应的离子方程式(4)下图为第ⅤA族、ⅥA、ⅦA族元素简单氢化物沸点随周期数的递变趋势图。

分析上图回答下列问题:
①推测ⅣA族
 与
与 的沸点大小为
的沸点大小为
 (填“>”或“<”)。
(填“>”或“<”)。②接近水的沸点的水蒸气的相对分子质量测定值比按化学式
 计算出的相对分子质量大一些,原因为
计算出的相对分子质量大一些,原因为③
 常用于制备半导体材料,
常用于制备半导体材料, 与足量的
与足量的 加热可反应得到
加热可反应得到 ,通过
,通过 的键长键角信息。
的键长键角信息。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)已知BA5为离子化合物,写出其电子式______________________________ 。
(2)B基态原子中能量最高的电子,其电子云在空间有________ 个方向,原子轨道呈________ 形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布为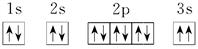 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了_____________________________________ 。
(4)G位于________ 族________ 区,价电子排布式为________ 。
(5)检验F元素的方法是________ ,请用原子结构的知识解释产生此现象的原因是_____________________________________________________________ 。
| A元素的核外电子数和电子层数相等,也是宇宙中最丰富的元素 |
| B元素原子的核外p电子数比s电子数少1 |
| C原子的第一至第四电离能分别是 I1=738 kJ/mol;I2=1 451 kJ/mol;I3=7 733 kJ/mol;I4=10 540 kJ/mol |
| D原子核外所有p轨道全满或半满 |
| E元素的主族序数与周期数的差为4 |
| F是前四周期中电负性最小的元素 |
| G在周期表的第七列 |
(1)已知BA5为离子化合物,写出其电子式
(2)B基态原子中能量最高的电子,其电子云在空间有
(3)某同学根据上述信息,推断C基态原子的核外电子排布为
 该同学所画的电子排布图违背了
该同学所画的电子排布图违背了(4)G位于
(5)检验F元素的方法是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】以NaOH、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: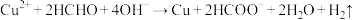
(1)基态Cu原子的价层电子排布式为___________ 。
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的___________ 性。
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是___________ 。
a.HCHO、 均属于极性分子
均属于极性分子
b.HCHO与 之间能形成氢键
之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、HCHO、
、HCHO、 三种微粒,空间结构为三角形的是
三种微粒,空间结构为三角形的是___________ 。
(4)为防止 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和 。
。
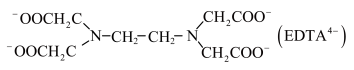
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是___________ 。
(5)锏—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区,Ni位于___________ 区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
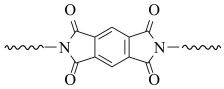
上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①聚酰亚胺在碱性条件下会发生水解
②___________
(7)有机化合物的合成通常使用催化剂,一种催化剂 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:
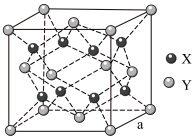
①Y原子为___________ (填元素符号)。与每个Y原子距离最近且等距的X原子有___________ 个
②晶胞边长为a nm,阿伏伽德罗常数为 ,则该晶体的密度
,则该晶体的密度
___________  (列出计算式,
(列出计算式,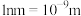 ,
, 的摩尔质量为123
的摩尔质量为123  )。
)。
 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: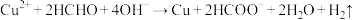
(1)基态Cu原子的价层电子排布式为
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
a.HCHO、
 均属于极性分子
均属于极性分子b.HCHO与
 之间能形成氢键
之间能形成氢键c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、HCHO、
、HCHO、 三种微粒,空间结构为三角形的是
三种微粒,空间结构为三角形的是(4)为防止
 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和 。
。
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是(5)锏—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区,Ni位于
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:

上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①聚酰亚胺在碱性条件下会发生水解
②
(7)有机化合物的合成通常使用催化剂,一种催化剂
 晶体的晶胞示意图如下:
晶体的晶胞示意图如下:
①Y原子为
②晶胞边长为a nm,阿伏伽德罗常数为
 ,则该晶体的密度
,则该晶体的密度
 (列出计算式,
(列出计算式,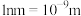 ,
, 的摩尔质量为123
的摩尔质量为123  )。
)。
您最近一年使用:0次
【推荐2】铁被誉为“第一金属”,铁及其化合物广泛应用于生活、生产、国防等领域。
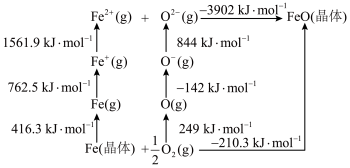
(1)已知:元素的一个基态的气态原子得到一个电子形成-1价气态阴离子时所放出的能量称为该元素的第一电子亲和能,用E1表示。从-1价的气态阴离子再得到1个电子,成为-2价的气态阴离子所放出的能量称为第二电子亲和能E2,依此类推。FeO是离子晶体,其晶格能可通过如下的Born-Haber循环计算得到。__________ kJ/mol,FeO的晶格能为__________ kJ/mol,基态O原子E1____________ E2(填“大于”或“小于”),从原子结构角度解释_________ 。
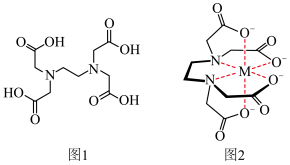
(2)乙二胺四乙酸又叫做EDTA(图1),是化学中一种良好的配合剂,形成的配合物叫做螯合物。EDTA在配位滴定中经常用到,一般是测定金属离子的含量。已知:EDTA配离子结构(图2)。____________ ,EDTANa-Fe(Ⅲ)是一种螯合物,六个配位原子在空间构型为____________ 。EDTANa-Fe(Ⅲ)的化学键除了σ键和配位键外,还存在____________ 。
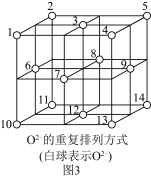
(3)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O 围成的正四面体空隙和如3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,O2-数与正四面体空隙数(包括被填充的)之比为__________ ,有__________ %的正八面体空隙填充阳离子。Fe3O4晶胞的八分之一是图示结构单元(图3),晶体密度为5.18 g/cm3,则该晶胞参数a=____________ pm。(写出计算表达式)
(1)已知:元素的一个基态的气态原子得到一个电子形成-1价气态阴离子时所放出的能量称为该元素的第一电子亲和能,用E1表示。从-1价的气态阴离子再得到1个电子,成为-2价的气态阴离子所放出的能量称为第二电子亲和能E2,依此类推。FeO是离子晶体,其晶格能可通过如下的Born-Haber循环计算得到。
(2)乙二胺四乙酸又叫做EDTA(图1),是化学中一种良好的配合剂,形成的配合物叫做螯合物。EDTA在配位滴定中经常用到,一般是测定金属离子的含量。已知:EDTA配离子结构(图2)。
(3)Fe3O4晶体中,O2-的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的O 围成的正四面体空隙和如3、6、7、8、9、12的O2-围成的正八面体空隙。Fe3O4中有一半的Fe3+填充在正四面体空隙中,另一半Fe3+和Fe2+填充在正八面体空隙中,则Fe3O4晶体中,O2-数与正四面体空隙数(包括被填充的)之比为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】元素周期表反映了元素性质的周期性变化规律。请根据短周期元素在周期表中的位置、结构和相关性质,回答下列问题:
(1)第VIA族元素形成的氢化物中沸点最高的是_________ (用分子式表示),原因是__________ ,该分子的空间构型为_________ 。
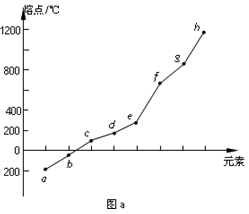
(2)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中E的化学式为______ ;第三周期元素单质的熔点(℃)变化如图a所示,其中h的元素符号为__________ 。
(3)第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为__________ g。
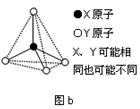
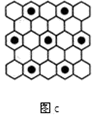
(4)碳元素的某种单质具有平面层状结构,该单质的名称为__________ ;同一层中的原子构成许多的正六边形,单质与熔融的钾相互作用,形成某种青铜色的物质(其中的元素钾用“●”表示),原子分布如图c所示,该物质的化学式为__________ 。
(1)第VIA族元素形成的氢化物中沸点最高的是
(2)第二周期元素中,除Be、B、Ne三种元素外,其他元素的氢化物沸点如下表所示,其中E的化学式为
| 氢化物 | A | B | HF | D | E |
| 沸点/℃ | 1317 | 100 | 19.5 |  33.35 33.35 |  164 164 |

(3)第二、第三周期的某些元素能形成单质甲和化合物乙,它们具有图b所示的结构单元,甲和乙的晶体类型相同,甲的某种同素异形体与乙在高温时能发生置换反应生成h的单质和CO。若该反应生成的h的单质含有1 mol共价键,则参加反应的乙的质量为

(4)碳元素的某种单质具有平面层状结构,该单质的名称为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】钛白粉是一种重要的无机化工颜料,主要成分为二氧化钛( ),一种以含
),一种以含 、CaO、
、CaO、 等杂质的钛铁矿(
等杂质的钛铁矿( )为原料制备钛白粉的工艺流程如图所示。
)为原料制备钛白粉的工艺流程如图所示。 不溶于水和稀酸;
不溶于水和稀酸;
②“酸浸”后钛元素主要以 形式存在;
形式存在;
③ ,当溶液中
,当溶液中 '时可认为
'时可认为 完全除去。
完全除去。
回答下列问题:
(1)请写出加快“酸浸”速率的一个措施:_____ 。
(2)“酸浸”时, 发生反应的化学方程式为
发生反应的化学方程式为_______ 。
(3)“滤渣”①的主要成分是______ (填化学式)。
(4)流程中加入铁粉的目的是把体系中的 还原成
还原成 ,冷却结晶析出
,冷却结晶析出 晶体。体系中的
晶体。体系中的 还可以用调节pH的方法除去,设酸浸后体系中
还可以用调节pH的方法除去,设酸浸后体系中 ,常温下
,常温下 开始沉淀的pH为
开始沉淀的pH为______ 。
(5)经处理后,流程中可循环利用的物质除Fe外,还有______ (填化学式)。
(6)碳化钛晶胞结构如图所示,碳化钛的化学式为_______ ,碳原子距离最近且相等的碳原子的数目为_____ 。晶胞边长参数 ,则晶体的密度
,则晶体的密度
_______  (列出计算式,不要求化简)。
(列出计算式,不要求化简)。
 ),一种以含
),一种以含 、CaO、
、CaO、 等杂质的钛铁矿(
等杂质的钛铁矿( )为原料制备钛白粉的工艺流程如图所示。
)为原料制备钛白粉的工艺流程如图所示。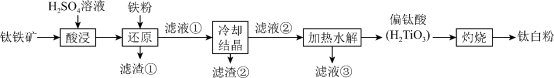
 不溶于水和稀酸;
不溶于水和稀酸;②“酸浸”后钛元素主要以
 形式存在;
形式存在;③
 ,当溶液中
,当溶液中 '时可认为
'时可认为 完全除去。
完全除去。回答下列问题:
(1)请写出加快“酸浸”速率的一个措施:
(2)“酸浸”时,
 发生反应的化学方程式为
发生反应的化学方程式为(3)“滤渣”①的主要成分是
(4)流程中加入铁粉的目的是把体系中的
 还原成
还原成 ,冷却结晶析出
,冷却结晶析出 晶体。体系中的
晶体。体系中的 还可以用调节pH的方法除去,设酸浸后体系中
还可以用调节pH的方法除去,设酸浸后体系中 ,常温下
,常温下 开始沉淀的pH为
开始沉淀的pH为(5)经处理后,流程中可循环利用的物质除Fe外,还有
(6)碳化钛晶胞结构如图所示,碳化钛的化学式为
 ,则晶体的密度
,则晶体的密度
 (列出计算式,不要求化简)。
(列出计算式,不要求化简)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】锗及其化合物广泛用于半导体、催化剂、光伏、制药工业。回答下列问题:
(1)锗的基态原子核外电子排布式为_______ 。
(2)硅、锗、铅的氯化物的熔点如下表:
① 的分子空间构型为
的分子空间构型为_______ 。
②熔点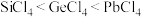 的原因是
的原因是_______ 。
(3)有机锗被称为“生命的奇效元素”,在医疗上具有重要应用。一种锗的有机配合物合成方法如下:
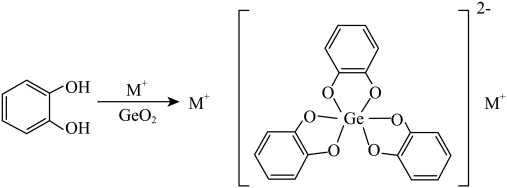
该有机配合物中锗的配位数为_______ ,其阴离子中C、 、O元素的第一电离能从大到小顺序为
、O元素的第一电离能从大到小顺序为_______ 。
(4)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):
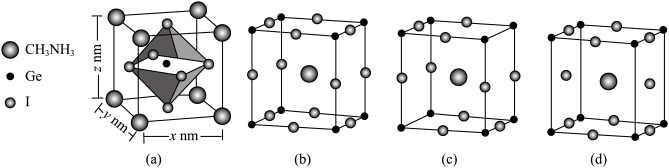
①该锗化合物晶胞的表示方式有多种,图中_______ (填“b”“c”或“d”)图也能表示此化合物的晶胞。
②用 表示阿伏加德罗常数的数值,计算晶胞(a)密度为
表示阿伏加德罗常数的数值,计算晶胞(a)密度为_______  (用含x、y、z和
(用含x、y、z和 的式子表示)。
的式子表示)。
(1)锗的基态原子核外电子排布式为
(2)硅、锗、铅的氯化物的熔点如下表:
| 物质 |  |  | 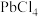 |
熔点( ) ) | 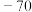 | 约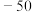 |  |
①
 的分子空间构型为
的分子空间构型为②熔点
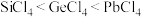 的原因是
的原因是(3)有机锗被称为“生命的奇效元素”,在医疗上具有重要应用。一种锗的有机配合物合成方法如下:

该有机配合物中锗的配位数为
 、O元素的第一电离能从大到小顺序为
、O元素的第一电离能从大到小顺序为(4)一种含锗的化合物应用于太阳能电池,其晶胞为长方体,结构如图(a):

①该锗化合物晶胞的表示方式有多种,图中
②用
 表示阿伏加德罗常数的数值,计算晶胞(a)密度为
表示阿伏加德罗常数的数值,计算晶胞(a)密度为 (用含x、y、z和
(用含x、y、z和 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。
(1)下列选项的电子排布式中,属于激发态氟原子的有___(填标号)。
(2)氰气[(CN)2]具有一部分类似卤素单质的性质,称为拟卤素。它的分子中每个原子最外层都达到8电子结构,则(CN)2分子中σ键、π键的个数之比为___ ,C的杂化轨道类型为_____ 。
(3)卤素离子可形成多种配合物。某种钴的配合物,其化学式可表示为CoCl3·4NH3·H2O。在含l mol该物质的溶液中,加入足量AgNO3溶液,能生成2 mol AgCl;经X射线衍射实验确定,中心离子的配位数是6。该配合物中配离子的化学式为___ 。
(4)金属镓的卤化物熔点如表:
GaF3熔点比GaCl3熔点高很多,原因是___ 。
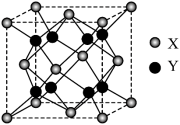
(5)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构为立方体,如图所示。其中X代表的离子是_____ ;该立方晶胞的边长为a pm,正负离子的最小核间距为___ pm。
(1)下列选项的电子排布式中,属于激发态氟原子的有___(填标号)。
| A.1s22s22p43s1 | B.1s22s22p43d2 | C.1s22s12p5 | D.1s22s22p33p2 |
(3)卤素离子可形成多种配合物。某种钴的配合物,其化学式可表示为CoCl3·4NH3·H2O。在含l mol该物质的溶液中,加入足量AgNO3溶液,能生成2 mol AgCl;经X射线衍射实验确定,中心离子的配位数是6。该配合物中配离子的化学式为
(4)金属镓的卤化物熔点如表:
| GaF3 | GaCl3 | GaBr3 | |
| 熔点/℃ | > 1000 | 77.75 | 122.3 |
(5)萤石(CaF2)是自然界中常见的含氟矿物,其晶胞结构为立方体,如图所示。其中X代表的离子是

您最近一年使用:0次
【推荐1】1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
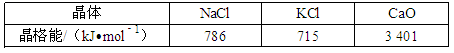
4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是__ .
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.

①写出基态Cu原子的核外电子排布式__ ;金属铜采用下列__ (填字母代号)堆积方式.
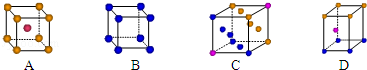
②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)__ .
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响__ .
④SO42﹣的空间构型是________ .
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
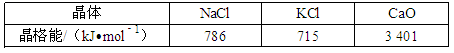
4种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如下,其中配位键和氢键均采用虚线表示.

①写出基态Cu原子的核外电子排布式

②写出胆矾晶体中水合铜离子的结构简式(必须将配位键表示出来)
③水分子间存在氢键,请你列举两点事实说明氢键对水的性质的影响
④SO42﹣的空间构型是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(1)已知A和B均为第3周期元素,其原子的第一至第四电离能如下表所示:
A通常显___ 价,A的电负性____ B的电负性(填“>”“<”或“=”)。
(2)紫外光的光子所具有的能量约为399kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因_____ 。
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是____ 。
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
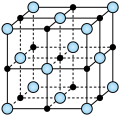
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:____ 。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有____ 个。
(4)金属阳离子含有的未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是____ 。
(5)某配合物的分子结构如图所示,其分子内不含有___ (填序号)。

A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键
(6)科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中的CO2。若有1molCH4生成,则有___ molσ键和___ molπ键断裂。
| 电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
| A | 578 | 1817 | 2745 | 11578 |
| B | 738 | 1451 | 7733 | 10540 |
A通常显
(2)紫外光的光子所具有的能量约为399kJ·mol-1。根据下表有关蛋白质分子中重要化学键的信息,说明人体长时间照射紫外光后皮肤易受伤害的原因
| 共价键 | C-C | C-N | C-S |
| 键能/kJ·mol-1 | 347 | 305 | 259 |
组成蛋白质的最简单的氨基酸中的碳原子杂化类型是
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:

| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
则该4种离子晶体(不包括NaCl)熔点从高到低的顺序是:
(4)金属阳离子含有的未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是
(5)某配合物的分子结构如图所示,其分子内不含有

A.离子键 B.极性键 C.金属键 D.配位键 E.氢键 F.非极性键
(6)科学家设计反应:CO2+4H2→CH4+2H2O以减小空气中的CO2。若有1molCH4生成,则有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
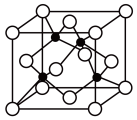
【推荐3】(1)铜的氢化物的晶体结构如图所示,写出此氢化物在氯气中燃烧的化学方程式:__ 。
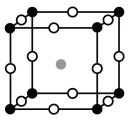
(2)如图为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是__ (填离子符号)。
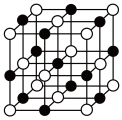
(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示)
已知3种离子晶体的晶格能数据如下表:
则这4种离子晶体(NaCl)熔点从高到低的顺序是___ 。其中MgO晶体中一个Mg2+周围和它最邻近且等距离的Mg2+有__ 个。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点都比金属Ca高,原因为__ 。
(5)BeO晶体也是制备氟硼铍酸钾晶体的原料,其晶胞结构如下图所示。
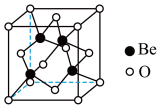
设O与Be的最近距离为a pm,用NA表示阿伏加德罗常数的值,则BeO晶体的密度为___ g·cm-3

(2)如图为F-与Mg2+、K+形成的某种离子晶体的晶胞,其中“○”表示的离子是

(3)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示)

已知3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点都比金属Ca高,原因为
(5)BeO晶体也是制备氟硼铍酸钾晶体的原料,其晶胞结构如下图所示。

设O与Be的最近距离为a pm,用NA表示阿伏加德罗常数的值,则BeO晶体的密度为
您最近一年使用:0次



