内蒙古达拉特旗第一中学2022-2023学年高三上学期开学考试理综化学试题
内蒙古
高三
开学考试
2022-09-21
121次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
内蒙古达拉特旗第一中学2022-2023学年高三上学期开学考试理综化学试题
内蒙古
高三
开学考试
2022-09-21
121次
整体难度:
适中
考查范围:
常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.65)
解题方法
2. 下列离子方程式中正确的是
A.浓氢氧化钠溶液与空气短时间接触:OH—+CO2=HCO |
| B.将石灰加入稀硫酸中:2H++CaO=Ca2++H2O |
C.向碘化钾与碘酸钾的混合溶液中加入硫酸:I—+IO +6H+=I2+3H2O +6H+=I2+3H2O |
| D.酸性硫酸亚铁溶液久置后变黄:4Fe2++4H++O2=4Fe3++2H2O |
【知识点】 离子方程式的正误判断解读 Fe2+的还原性解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
3. 随着研究的深入和技术的发展,化学逐渐渗透到了生活的各个方面,下列说法正确的是
| A.使用洁净的细铁丝蘸取儿童服用的葡萄糖酸钙溶液在酒精灯火焰上进行灼烧,可以观察到火焰的颜色变为砖红色 |
| B.南方地区湿度较大,工匠们将锡制艺术品表面镀上锌保护层,目的是利用牺牲阴极的阳极保护法阻碍电化学腐蚀的发生 |
| C.化石燃料除燃烧外,还可以通过化学反应制得多种产品,在诸多利用方法中,煤的干馏、气化与石油的分馏、裂化均属于化学变化 |
| D.在常见的营养物质中,葡萄糖可以在碱性、加热条件下与银氨溶液反应生成银单质,淀粉遇碘会变蓝,蛋白质和油脂都是高分子化合物 |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 工业上可用水蒸气蒸馏法从柠檬、橙子和柚子等水果的果皮中提取柠檬烯( ),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。

下列给出的柠檬烯的性质中,正确的是
①柠檬烯是一种芳香烃
②柠檬烯的一氯代物有8种
③柠檬烯分子中所有的碳原子可能在同一平面上
④在一定条件下,柠檬烯可以发生取代、加成、氧化等反应
 ),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
下列给出的柠檬烯的性质中,正确的是
①柠檬烯是一种芳香烃
②柠檬烯的一氯代物有8种
③柠檬烯分子中所有的碳原子可能在同一平面上
④在一定条件下,柠檬烯可以发生取代、加成、氧化等反应
| A.①④ | B.②③ | C.②④ | D.③④ |
您最近一年使用:0次
单选题
|
适中(0.65)
5. 工业上可用水蒸气蒸馏法从柠檬、橙子和柚子等水果的果皮中提取柠檬烯( ),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。

下列关于柠檬烯提取实验的说法中,错误的是
 ),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
),其实验装置如图所示,具体的实验步骤为①将1∼2个橙子皮剪成细碎的碎片,投入乙装置中,加入约30ml水;②松开活塞K,加热甲装置(水蒸气发生器)至水沸腾,当活塞K的支管口有大量水蒸气冒出时将K旋紧,并打开冷凝水,一段时间后,可观察到丙装置中馏出液的水面上有一层很薄的油层。
下列关于柠檬烯提取实验的说法中,错误的是
| A.当牛角管中滴落的馏出液澄清透明、无明显油珠时,说明蒸馏完成 |
| B.装置中的冷凝管需从a口注入冷凝水,且可以用球形冷凝管代替 |
| C.当长导管中液面持续升高时,应立刻打开活塞K放出水蒸气 |
| D.实验结束后,可以通过分液、蒸馏的方法得到高纯度的精油 |
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
6. 元素W、X、Y、Z组成的一种新型漂白剂结构如图,其中W、Y、Z为不同周期、不同主族的短周期元素,三者的最外层电子数之和等于X的最外层电子数,且W、X对应的简单离子核外电子排布相同,则


| A.非金属性:X>W>Y |
| B.简单离子半径:W>X>Z |
| C.元素Y最高价氧化物对应水化物为弱酸 |
| D.该漂白剂中所有原子最外层都满足8电子稳定结构 |
您最近一年使用:0次
单选题
|
适中(0.65)
7. 离子都是造成水体污染的因素,可以利用沉淀法除去,图中a、b分别是物质Mg3(AsO4)2和Mg3(PO4)2的沉淀溶解平衡曲线,下列说法错误的是


| A.Ksp[Mg3(AsO4)2]=10-19.68 |
B.向浓度相等的AsO 、PO 、PO 的水中同时滴加相同浓度的Mg(NO3)2溶液,PO 的水中同时滴加相同浓度的Mg(NO3)2溶液,PO 先沉淀 先沉淀 |
| C.要使水中浓度均不大于10-6mol/L,则Mg2+浓度至少为10-2.56mol/L |
D.反应Mg3(AsO4)2(s)+2PO (aq) (aq) Mg3(PO4)2(s)+2AsO Mg3(PO4)2(s)+2AsO (aq)的平衡常数K=102.76 (aq)的平衡常数K=102.76 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
解题方法
8. 锌是第四“常见”的金属,在现代工业中有不可磨灭的贡献。回答下列问题:
I.硫酸锌被广泛应用于医药领域和工农业生产。工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图:

(1)滤渣A的主要成分是____ 。
(2)为提高步骤I的效率,可以采取的措施为____ (写两点)。
(3)步骤II中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO2两种沉淀,该反应的离子方程式为____ 。
(4)步骤III中,加入锌粉的作用是____ (用离子方程式表示)。
(5)步骤IV中得到的ZnSO4•7H2O晶体需在低温、减压条件下烘干,不采用常压高温烘干的原因是____ 。
(6)取28.70gZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示,分析数据可知680 ℃时所得固体的化学式为____ 。

a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O
II.酸性锌锰干电池是应用最普遍的电池之一,其标称电压为1.5V。
(7)锌锰电池中锌为____ (选填“正极”或“负极)材料。
(8)已知1mol电子所带的电荷量约为96500C,若电池在放电过程中锌消耗了1.3g时,理论上输出的电能约为____ J。
I.硫酸锌被广泛应用于医药领域和工农业生产。工业上由氧化锌矿(主要成分为ZnO,另含ZnSiO3、FeCO3、CuO等)生产ZnSO4•7H2O的一种流程如图:

(1)滤渣A的主要成分是
(2)为提高步骤I的效率,可以采取的措施为
(3)步骤II中,在pH约为5.1的滤液中加入高锰酸钾,生成Fe(OH)3和MnO2两种沉淀,该反应的离子方程式为
(4)步骤III中,加入锌粉的作用是
(5)步骤IV中得到的ZnSO4•7H2O晶体需在低温、减压条件下烘干,不采用常压高温烘干的原因是
(6)取28.70gZnSO4•7H2O加热至不同温度,剩余固体的质量变化如图所示,分析数据可知680 ℃时所得固体的化学式为

a.ZnO b.Zn3O(SO4)2 c.ZnSO4 d.ZnSO4•H2O
II.酸性锌锰干电池是应用最普遍的电池之一,其标称电压为1.5V。
(7)锌锰电池中锌为
(8)已知1mol电子所带的电荷量约为96500C,若电池在放电过程中锌消耗了1.3g时,理论上输出的电能约为
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
9. 酸碱中和滴定是一种重要的化学分析手段,回答下列问题:
I.某班学生通过实验测定酸碱滴定曲线,实验用品包括0.1mol/LHCl溶液、0.1mol/LNaOH溶液、蒸馏水、pH计、酸式滴定管、碱式滴定管、滴定管架(铁架台和蝴蝶夹)、锥形瓶。甲、乙、丙3组同学用锥形瓶取体积为20.00mL的溶液,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示。
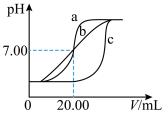
(1)滴定时选用的滴定管为____ (选填“酸式”或“碱式”)滴定管,在装入标准溶液前需要对滴定管进行的操作为____ 。
(2)在图中的三条滴定曲线中,较为准确的是____ 。
II.在实际操作过程中,由于甲基橙指示剂的变色不敏锐,难以判断滴定终点,需在其中加入少量的“惰性染料”靛蓝二磺酸钠,其固定颜色与甲基橙的可变颜色进行叠加(变色范围不变),形成“酸色”为紫色、过渡色为浅灰色、“碱色”为绿色的混合指示剂。已知室温下0.10mol/LNH4Cl溶液的,若以甲基橙-靛蓝二磺酸钠为指示剂,用0.20mol/L盐酸滴定20.00mL同浓度的氨水,则:
(3)NH4Cl溶液显酸性的原因是____ (用离子方程式表示)。
(4)判断滴定终点的现象是____ 。
(5)若多组实验中所用盐酸的体积均略大于20.00mL,原因是____ 。
I.某班学生通过实验测定酸碱滴定曲线,实验用品包括0.1mol/LHCl溶液、0.1mol/LNaOH溶液、蒸馏水、pH计、酸式滴定管、碱式滴定管、滴定管架(铁架台和蝴蝶夹)、锥形瓶。甲、乙、丙3组同学用锥形瓶取体积为20.00mL的溶液,且所用的试剂完全相同,根据实验所得的数据绘制的曲线分别如图中a、b、c所示。

(1)滴定时选用的滴定管为
(2)在图中的三条滴定曲线中,较为准确的是
II.在实际操作过程中,由于甲基橙指示剂的变色不敏锐,难以判断滴定终点,需在其中加入少量的“惰性染料”靛蓝二磺酸钠,其固定颜色与甲基橙的可变颜色进行叠加(变色范围不变),形成“酸色”为紫色、过渡色为浅灰色、“碱色”为绿色的混合指示剂。已知室温下0.10mol/LNH4Cl溶液的,若以甲基橙-靛蓝二磺酸钠为指示剂,用0.20mol/L盐酸滴定20.00mL同浓度的氨水,则:
(3)NH4Cl溶液显酸性的原因是
(4)判断滴定终点的现象是
(5)若多组实验中所用盐酸的体积均略大于20.00mL,原因是
您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
解题方法
10. 氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。回答下列问题:
I.氨热分解法制氢气:在一定温度下,利用催化剂将NH3分解为N2和H2,相关化学键的键能数据如表:
(1)计算反应2NH3(g) N2(g)+3H2(g)的焓变为
N2(g)+3H2(g)的焓变为____ kJ/mol,已知该反应的熵变198.9J/(mol•K),则该反应能自发进行的临界温度为____ K(保留一位小数)。
(2)某兴趣小组对(1)中的反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH3通入初始容积为2L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示,已知t1=5min时反应达到平衡。

①用H2的浓度变化表示时间内的反应速率v(H2)=____ 。
②该温度下的平衡常数为____ 。
③若在t2=6min时将容器体积迅速缩小至原来的一半后保持不变,在图中的a、b、c、d四条曲线中能正确表示此后N2分压变化趋势的是____ ,理由是____ 。
II.氨电解法制氢气:利用电解原理,将氦转化为高纯氢气,其装置如图所示:

(3)电解过程中OH-的移动方向为____ (选填“从左往右”或“从右往左”)。
(4)阳极的电极反应式为____ 。
I.氨热分解法制氢气:在一定温度下,利用催化剂将NH3分解为N2和H2,相关化学键的键能数据如表:
| 化学键 | N≡N | H-H | N-H |
| 键能E/(kJ/mol) | 946 | 436.0 | 390.8 |
 N2(g)+3H2(g)的焓变为
N2(g)+3H2(g)的焓变为(2)某兴趣小组对(1)中的反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH3通入初始容积为2L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示,已知t1=5min时反应达到平衡。

①用H2的浓度变化表示时间内的反应速率v(H2)=
②该温度下的平衡常数为
③若在t2=6min时将容器体积迅速缩小至原来的一半后保持不变,在图中的a、b、c、d四条曲线中能正确表示此后N2分压变化趋势的是
II.氨电解法制氢气:利用电解原理,将氦转化为高纯氢气,其装置如图所示:

(3)电解过程中OH-的移动方向为
(4)阳极的电极反应式为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. Li是最轻的固体金属,采用Li作为负极材料的电池具有小而轻、能量密度大等优良性能,得到广泛应用。回答下列问题:
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为____ 。
A. B.
B.
C.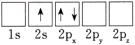 D.
D.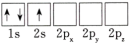
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是____ 。
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是____ ,中心原子的杂化形式为____ 。LiAlH4中,存在下列给出的____ 。
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为____ kJ/mol,O=O键能为____ kJ/mol,Li2O晶格能为____ kJ/mol。
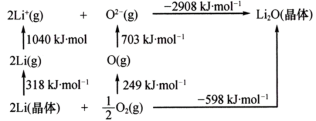
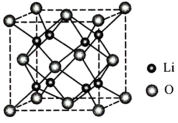
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为____ g•cm-3(列出计算式即可)。
(1)下列Li原子电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)Li+与H-具有相同的电子构型,但r(Li+)小于r(H-),原因是
(3)LiAlH4是有机合成中常用的还原剂,LiAlH4中的阴离子空间构型是
A.离子键 B.σ键 C.π键 D.氢键
(4)Li2O是离子晶体,其晶格能可通过图中的循环计算得到,由数据可知Li原子的第一电离能为
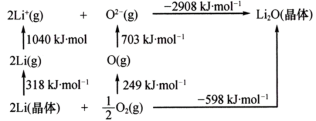
(5)Li2O具有反萤石结构,晶胞如图所示。已知晶胞参数为anm,阿伏加德罗常数的值为NA,则Li2O的密度为

您最近一年使用:0次
2022-09-19更新
|
158次组卷
|
2卷引用:内蒙古达拉特旗第一中学2022-2023学年高三上学期开学考试理综化学试题
解答题-有机推断题
|
较难(0.4)
解题方法
12. 化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如图,回答下列问题:

已知:①RCHO+CH3CHO RCH=CHCHO+H2O
RCH=CHCHO+H2O
② +
+


(1)A的化学名称为____ ,E的结构简式为____ 。
(2)由D生成E的过程中,1)的反应类型为____ 。
(3)由B生成C的过程中,1)的化学方程式为____ 。
(4)已知G为甲苯的同分异构体,则由F生成H的化学方程式为____ 。
(5)芳香化合物X是F的同分异构体,能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,符合要求的X的结构简式为____ (写出2种即可)。
(6)写出用环戊烷和2-丁炔为原料制备化合物 的合成路线(其他试剂任选)
的合成路线(其他试剂任选)____ 。

已知:①RCHO+CH3CHO
 RCH=CHCHO+H2O
RCH=CHCHO+H2O②
 +
+


(1)A的化学名称为
(2)由D生成E的过程中,1)的反应类型为
(3)由B生成C的过程中,1)的化学方程式为
(4)已知G为甲苯的同分异构体,则由F生成H的化学方程式为
(5)芳香化合物X是F的同分异构体,能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6:2:1:1,符合要求的X的结构简式为
(6)写出用环戊烷和2-丁炔为原料制备化合物
 的合成路线(其他试剂任选)
的合成路线(其他试剂任选)
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、化学与STSE、认识化学科学、化学反应原理、有机化学基础、化学实验基础、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 电解法制取铝 常见金属的冶炼 | |
| 2 | 0.65 | 离子方程式的正误判断 Fe2+的还原性 | |
| 3 | 0.65 | 焰色试验 金属的电化学腐蚀与防护 油脂在碱性条件下水解 石油裂化、裂解 | |
| 4 | 0.65 | 同分异构体的数目的确定 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 | |
| 5 | 0.65 | 蒸馏与分馏 萃取和分液 常见有机物的制备 | |
| 6 | 0.65 | 元素非金属性强弱的比较方法 微粒半径大小的比较方法 根据原子结构进行元素种类推断 | |
| 7 | 0.65 | 沉淀转化 溶度积规则及其应用 溶度积常数相关计算 | |
| 二、解答题 | |||
| 8 | 0.4 | 氧化还原反应方程式的配平 Fe2+的还原性 一次电池 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 酸碱中和滴定实验基本操作及步骤 酸碱中和滴定指示剂选择 酸碱中和滴定的误差分析 水解的离子方程式书写 | 实验探究题 |
| 10 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 压强对化学平衡移动的影响 化学平衡常数的有关计算 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 11 | 0.65 | 能量最低原理 利用杂化轨道理论判断分子的空间构型 晶胞的有关计算 晶格能 | 结构与性质 |
| 12 | 0.4 | 根据要求书写同分异构体 卤代烃的消去反应 乙醛与新制氢氧化铜悬浊液的反应 根据题给物质选择合适合成路线 | 有机推断题 |



