NH3是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水形成[Ni(NH3)6]SO4。工业上常采用氨氧化法制硝酸,其流程是将氨和空气混合后通入灼热的铂铑合金网,反应生成NO(g),生成的一氧化氮与残余的氧气继续反应生成二氧化氮:2NO(g)+O2(g)=2NO2(g) △H=−116.4 kJ∙mol−1。随后将二氧化氮通入水中制取硝酸。工业上一般用石灰乳吸收硝酸工业尾气(NO和NO2),由于NO不能被碱吸收,一般控制NO和NO2约为1:1通入石灰乳,净化尾气的同时又可制得混凝土添加剂Ca(NO2)2。电解法脱硝一般先用稀硝酸吸收氮氧化合物生成亚硝酸,再用电解法生成硝酸。对反应2NO(g)+O2(g) 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是
 2NO2(g),下列说法正确的是
2NO2(g),下列说法正确的是| A.该反应能够自发的原因△S>0 |
| B.工业上使用合适的催化剂可提高NO2的生产效率 |
| C.升高温度,该反应v(逆)减小,v(正)增大,平衡向逆反应方向移动 |
| D.2molNO(g)和1molO2(g)中所含化学键能总和比2molNO2(g)中大116.4 kJ∙mol−1 |
更新时间:2022-09-26 16:59:40
|
相似题推荐
【推荐1】化学反应常常伴随能量的变化,图是 与
与 反应的能量变化示意图,下列说法正确的是
反应的能量变化示意图,下列说法正确的是
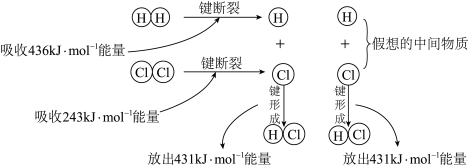
 与
与 反应的能量变化示意图,下列说法正确的是
反应的能量变化示意图,下列说法正确的是
A.氯化氢分子的电子式: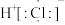 |
| B.该反应既是氧化还原反应又是放热反应 |
C.形成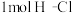 键要吸收 键要吸收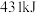 的能量 的能量 |
| D.反应物断键时吸收的能量大于产物形成化学键时释放的能量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】已知断裂下列化学键需要吸收的能量:H−H为436 kJ⋅mol-1,F−F为153 kJ⋅mol-1,H−F为565 kJ⋅mol-1。下列说法中正确的是
A. 与 与 反应的热化学方程式为 反应的热化学方程式为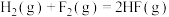 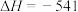 kJ kJ |
B.44.8 L HF气体分解成22.4 L  和22.4 L 和22.4 L  吸收541 kJ的热量 吸收541 kJ的热量 |
C.1 mol  与1 mol 与1 mol  反应生成2 mol液态HF放出的热量小于541 kJ 反应生成2 mol液态HF放出的热量小于541 kJ |
D.在相同条件下,1 mol  与1 mol 与1 mol  的能量总和大于2 mol HF气体的能量 的能量总和大于2 mol HF气体的能量 |
您最近一年使用:0次
【推荐1】挥发性有机物(VOCs)对环境易造成污染VOCs催化燃烧处理技术具有净化率高、燃烧温度低、无明火,不会有NOx等二次污染物产生等优点,图甲是VOCs处理过程中固体催化剂的催化原理,图乙是反应过程中的能量变化图,下列叙述正确的是( )
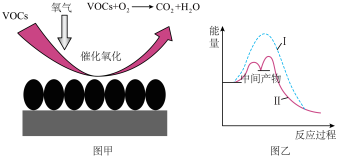

| A.图甲中固体催化剂表面既有化学键裂,也有化学键形成 |
| B.图甲中固体催化剂可提高该反应的焓变 |
| C.图乙中曲线1使用了固体催化剂,反应活化能降低 |
| D.VOCs催化氧化过程中所有反应均为放热反应 |
您最近一年使用:0次
【推荐2】已知反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在一定温度和压强下的密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0,在一定温度和压强下的密闭容器中,反应达到平衡。下列叙述正确的是
 CO2(g)+H2(g) ΔH<0,在一定温度和压强下的密闭容器中,反应达到平衡。下列叙述正确的是
CO2(g)+H2(g) ΔH<0,在一定温度和压强下的密闭容器中,反应达到平衡。下列叙述正确的是| A.降低温度,K增大 |
| B.更换高效催化剂,可增大CO的平衡转化率 |
| C.CO和H2O分子的每一次碰撞都能发生化学反应 |
| D.若该反应为非基元反应,其总反应速率由反应快的一步基元反应决定 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】某同学研究K2Cr2O7溶液中的化学平衡,并验证勒夏特列原理,设计如图所示实验。
已知:Cr2O (aq)(橙色)+H2O⇌2CrO
(aq)(橙色)+H2O⇌2CrO (aq)(黄色)+2H+ △H <0
(aq)(黄色)+2H+ △H <0
下列说法正确的是
已知:Cr2O
 (aq)(橙色)+H2O⇌2CrO
(aq)(橙色)+H2O⇌2CrO (aq)(黄色)+2H+ △H <0
(aq)(黄色)+2H+ △H <0| 实验过程 | 实验现象 |
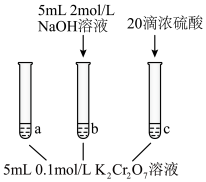 | 试管a中溶液为橙色; 试管b中溶液为黄色; 试管c中滴加浓硫酸后温度略有升高,溶液变为深橙色。 |
| A.该反应是一个氧化还原反应 |
B.b试管中只存在CrO ,不存在Cr2O ,不存在Cr2O |
| C.对比a、b可以证明减小生成物浓度,平衡正向移动 |
| D.对比a、c不可以证明升高温度,平衡正向移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】学习“化学平衡移动原理”后,以你的理解,下列叙述正确的是
| A.对于已达平衡的体系,改变影响化学平衡的条件,不可能出现v正增大,v逆减小的情况。 |
B.对2HI H2+I2(g),平衡体系增加压强使颜色变深,可用勒夏特列原理解释。 H2+I2(g),平衡体系增加压强使颜色变深,可用勒夏特列原理解释。 |
| C.升高温度,一定会使化学平衡发生移动。 |
| D.在盛有一定量NO2的注射器中,向外拉活塞,其中气体颜色先变浅再变深,甚至比原来深。 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】在常温常压下,下列属于自发过程的是
| A.2C(s) + O2(g) = 2CO(g) |
| B.NH4Cl(s) = NH3(g) + HCl(g) |
| C.CH3COOH(l) = CH3COOH(s) |
D.2Cr3+(aq) + 3Cl2(aq) + 7H2O(l) = Cr2O (aq) + 6Cl-(aq)+14H+(aq) (aq) + 6Cl-(aq)+14H+(aq) |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列有关说法正确的是
| A.SO2(g)+H2O(g)=H2SO3(l),该过程熵值增大 |
| B.SO2(g)= S(s)+O2(g); △H>0,△S<0,该反应能自发进行 |
| C.3S(s)+2H2O(1)= SO2(g)+2H2S(g),室温下能自发进行 |
| D.若某反应的△H<0,△S>0,则该反应一定能自发进行 |
您最近一年使用:0次

 2NH3(g),有关物质的化学键键能(拆开1mol化学键所需要的能量) 如下:
2NH3(g),有关物质的化学键键能(拆开1mol化学键所需要的能量) 如下:
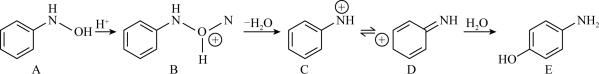
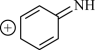 +H2O→
+H2O→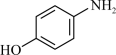 +H+
+H+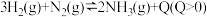 达到平衡后,升高温度,则
达到平衡后,升高温度,则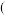

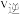 增大、
增大、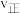 减小
减小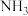 的含量增大
的含量增大

