反应Ⅰ、Ⅱ、Ⅲ均会在工业生产硝酸过程中发生,其中反应Ⅰ、Ⅱ发生在氧化炉中,反应Ⅲ发生在氧化塔中,不同温度下各反应的化学平衡常数如下表所示。下列说法正确的是
| 温度/K | 化学平衡常数 | |||
| 反应Ⅰ:4NH3+5O2=4NO+6H2O | 反应Ⅱ:4NH3+3O2=2N2+6H2O | 反应Ⅲ:2NO+O2=2NO2 | ||
| 500 | 1.1×1026 | 7.1×1034 | 1.3×102 | |
| 700 | 2.1×1019 | 2.6×1025 | 1.0 | |
| A.使用选择性催化反应Ⅰ的催化剂不能增大氧化炉中NO的含量 |
| B.通过改变氧化炉的温度可促进反应Ⅰ而抑制反应Ⅱ |
| C.通过改变氧化炉的压强可促进反应Ⅰ而抑制反应Ⅱ |
| D.氧化炉出气在进入氧化塔前应进一步降低温度 |
更新时间:2022-10-11 23:00:04
|
相似题推荐
【推荐1】下列各表述与示意图一致的是( )


| A.图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1KOH溶液,溶液的pH随加入酸体积的变化 |
B.图②中曲线表示反应N2(g)+3H2(g) 2NH3(g) ΔH< 0 正、逆反应的平衡常数K随温度的变化 2NH3(g) ΔH< 0 正、逆反应的平衡常数K随温度的变化 |
| C.图③表示用醋酸滴定NaOH和氨水混合溶液时,溶液的导电能力随醋酸体积变化的曲线 |
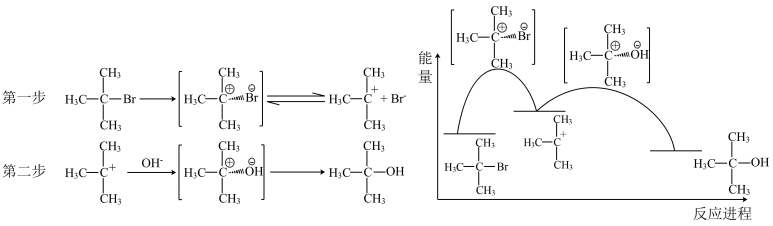
| D.图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g)→CH3CH3(g)ΔH< 0使用和未使用催化剂时,反应过程中的能量变化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列实验装置设计正确且能达到实验目的的是
| A. | B. | C. | D. |
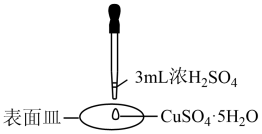 | 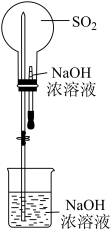 |  | 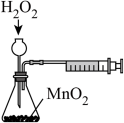 (含秒表) |
| 探究浓硫酸的脱水性 | 喷泉实验 | 制备 晶体 晶体 | 定量测定 的分解速率 的分解速率 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】“变化观念和平衡思想”是高中化学核心素养的重要组成部分,下列相关叙述正确的是
| A.可利用14C测定文物年代,14C会衰变为14N,该过程为化学变化 |
| B.高炉炼铁过程中,增加炉高并不能降低尾气中CO含量,说明化学反应是有限度的 |
C.恒容密闭容器中反应2NO2 N2O4达到平衡后,其它条件不变,升高温度,最终气体颜色比原平衡浅 N2O4达到平衡后,其它条件不变,升高温度,最终气体颜色比原平衡浅 |
D.密闭容器中反应H2(g)+I2(g) 2HI(g)达到平衡后,仅缩小容器体积,颜色加深,平衡逆向移动 2HI(g)达到平衡后,仅缩小容器体积,颜色加深,平衡逆向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列装置或操作能达到相应目的的是
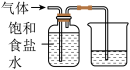 | 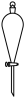 |
A.排饱和食盐水收集 | B.分离溴和四氯化碳 |
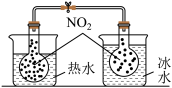 |  |
| C.探究温度对平衡的影响 | D.测定 溶液的pH 溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】液氨是一种很好的溶剂,液氨可以微弱的电离产生 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是
 和
和 。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有
。NH3中的一个H原子若被-NH2取代可形成N2H4(联氨),若被-OH取代可形成 NH2OH(羟胺)。在有 存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g)
存在时,Cu(OH)2能溶于氨水形成[Cu(NH3)4]2+。NH3经过一定的转化可以形成 N2、NO、NO2、N2O4(无色)、HNO3等。对于反应2NO2(g) N2O4(g),下列说法正确的是
N2O4(g),下列说法正确的是A.该反应的 H>0 H>0  S<0 S<0 |
B.该反应的平衡常数表达式为  |
C.升高温度, 该反应的  (正)增大, (正)增大,  (逆)减小 (逆)减小 |
| D.将容器体积压缩为原来一半,气体颜色比压缩前深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在一密闭容器中,充入一定量的反应物A,反应aA(g)⇌bB(?)达平衡后,保持温度不变,将容器体积缩到一半,当达到新的平衡时,B的浓度是原来的1.8倍,则
| A.B一定为气态 | B.平衡向正反应方向移动了 |
| C.物质B的体积分数增大 | D.混合气体的平均相对分子质量减小 |
您最近一年使用:0次

 B和②B
B和②B
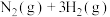
 ]。
]。 、3mol
、3mol