现有6种短周期元素X、Y、Z、W、M、Q,其原子序数依次增大,部分信息如下表:
请用相应的化学用语回答下列问题:
(1)中子数为8的一种Y原子常用于判断古生物化石年代,其原子符号是________ 。
(2)基态Q原子的核外电子排布中,电子占据的最高能级符号是________ ,其电子云轮廓图为________ 形。
(3)Z的电负性________ W的电负性(填“>”或“<”,下同),Z的第一电离能________ W的第一电离能,Z、W、M的简单离子半径由大到小的顺序是________ (用离子符号回答)。
(4)QW 的VSEPR模型是
的VSEPR模型是________ ,QW3分子中的键角是________ 。
(5)ZX 中的X—Z—X键角比ZX3中的X—Z—X键角大,原因是
中的X—Z—X键角比ZX3中的X—Z—X键角大,原因是________ 。
| X | 阴离子电子层结构与氦原子相同 |
| Y | 最高价氧化物在空气中增多会造成温室效应 |
| Z | 双原子单质分子中键与键的数目之比为1:2 |
| W | 基态原子的价电子排布式为nsnnpn+2 |
| M | 短周期元素中原子半径最大 |
| Q | 元素最高化合价与最低化合价的代数和等于4 |
(1)中子数为8的一种Y原子常用于判断古生物化石年代,其原子符号是
(2)基态Q原子的核外电子排布中,电子占据的最高能级符号是
(3)Z的电负性
(4)QW
 的VSEPR模型是
的VSEPR模型是(5)ZX
 中的X—Z—X键角比ZX3中的X—Z—X键角大,原因是
中的X—Z—X键角比ZX3中的X—Z—X键角大,原因是
21-22高二下·四川成都·期中 查看更多[2]
四川省成都崇州市怀远中学2021-2022学年高二下学期期中考试化学试题(已下线)专题02 分子结构与性质(知识串讲+专题过关)-2022-2023学年高二化学下学期期中期末考点大串讲(人教版2019)
更新时间:2022/10/01 17:08:13
|
相似题推荐
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐1】化合物YX2、ZX2中,X、Y、Z都是短周期元素,X与Y为同周期元素,Y与Z为同族元素,Y原子的最外层p能级电子数等于前一电子层电子总数。X原子最外层p能级中只有一个轨道填充了2个电子,则X的电子排布式为___________ ;Y的简化电子排布式为___________ ;Z的电子排布式为____________ ;YX2的化学式是________ ,电子式是________ ;ZX2的化学式是________ 。
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】短周期元素A、B、C、D、E、F六种元素,它们的原子序数由A到F依次增大。在周期表中,A的原子半径最小。B元素的原子最外层电子数是内层电子数的两倍,C为地壳中含量最多的元素,D是原子半径最大的短周期主族元素, D单质燃烧时呈现黄色火焰, D的单质在高温下与C的单质充分反应, 可以得到与E单质颜色相同的淡黄色固态化合物。D与F形成的离子化合物DF是常用的调味品。试根据以上叙述回答:
(1)元素名称: A_______ B_______ D _______
(2)E在周期表中的位置:_______
(3)F离子结构示意图:_______
(4)A、B组成的最简单化合物的名称是_______
(5)用电子式表示BC2的形成过程:_______
(6)C单质与D单质在常温下反应的产物的电子式_______
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为_______ ,将W溶于水的化学方程式_______ ,W的用途有_______ (填一种)
(8)能说明E的非金属性比F的非金属性_______ (填“强”或“弱”)的事实是: _______ (举一例)。
(1)元素名称: A
(2)E在周期表中的位置:
(3)F离子结构示意图:
(4)A、B组成的最简单化合物的名称是
(5)用电子式表示BC2的形成过程:
(6)C单质与D单质在常温下反应的产物的电子式
(7)C单质与D单质在点燃条件下反应的产物W中所含化学键类型为
(8)能说明E的非金属性比F的非金属性
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】有A、B、C、D四种元素,A元素是地壳中含量最多的金属元素;B元素的原子其M层电子数比L层少1个电子;C元素的原子得到2个电子,D元素的原子失去1个电子,所得到的微粒都具有与氩原子相同的电子数,回答下列问题:
(1)上述四种元素的名称分别是A___________ ,B___________ ,C____________ ,D____________ ,
(2)画出A离子、C原子的结构示意图_____________________ ,__________________ 。
(3)写出D与水反应离子方程式______________________________ 。
(1)上述四种元素的名称分别是A
(2)画出A离子、C原子的结构示意图
(3)写出D与水反应离子方程式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐1】如图是部分元素的第一电离能随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。
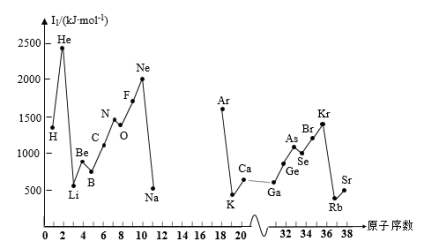
请回答下列问题
(1)分析图中同周期元素第一电离能的变化规律,推断 元素中,
元素中, 的第一电离能的最小范围为
的第一电离能的最小范围为_______ 
_______ (填元素符号)。
(2)同主族元素的第一电离能的变化规律是_______ 。
(3)图中第一电离能最小的元素在周期表中的位置是_______ 。
(4)根据对角线规则 、
、 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有_______ 性,其中 表现出这种性质的离子方程式是
表现出这种性质的离子方程式是_______ 。

请回答下列问题
(1)分析图中同周期元素第一电离能的变化规律,推断
 元素中,
元素中, 的第一电离能的最小范围为
的第一电离能的最小范围为
(2)同主族元素的第一电离能的变化规律是
(3)图中第一电离能最小的元素在周期表中的位置是
(4)根据对角线规则
 、
、 的最高价氧化物对应水化物的性质相似,它们都具有
的最高价氧化物对应水化物的性质相似,它们都具有 表现出这种性质的离子方程式是
表现出这种性质的离子方程式是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐2】氮、氧、硫、磷是与生命活动密切相关的元素。回答下列问题:
(1)SO2分子的VSEPR模型名称是___________
(2)N、O、P三种元素第一电离能由大到小的顺序是___________
(3)SCN-中C原子的杂化类型为___________ 杂化,1 mol SCN-中含π键的数目为___________ NA。
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为( ,
, ,0);D为(1,1,1)。则C的原子坐标参数为
,0);D为(1,1,1)。则C的原子坐标参数为___________

②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a cm,则磷化硼晶胞的边长为___________ cm。(用含a的代数式表示)
(1)SO2分子的VSEPR模型名称是
(2)N、O、P三种元素第一电离能由大到小的顺序是
(3)SCN-中C原子的杂化类型为
(4)晶胞有两个基本要素:
①原子坐标参数,表示晶胞内部各原子的相对位置。磷化硼是一种超硬耐磨的涂层材料,其晶胞结构如图所示,其中原子坐标参数A为(0,0,0);B为(
 ,
, ,0);D为(1,1,1)。则C的原子坐标参数为
,0);D为(1,1,1)。则C的原子坐标参数为
②晶胞参数,描述晶胞的大小和形状。P原子与B原子的最近距离为a cm,则磷化硼晶胞的边长为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】光催化是一种能耗低、效率高、无二次污染、反应条件温和的绿色化学法。我国科学家使用乙二胺和水混合溶剂,合成带状纳米光催化剂Zn2GeO4.这类光催化材料广泛应用于水污染治理、CO2还原、空气净化等领域。回答下列问题:
(1)基态Zn原子的核外电子排布式为________ 。
(2)利用CO(NH2)2(尿素)在Zn2GeO4表面沉积非金属N,能够有效提高Zn2GeO4的光催化性能。尿素分子中σ键与π键数目比为________ ,C、N、O元素第一电离能大小顺序为________ ,原因是________ 。
(3)乙二胺(H2NCH2CH2NH2)所含C、N原子的杂化轨道类型分别为________ 、________ 。它能与Zn2+形成环状离子,原因是________ 。
(4)钙钛矿也是一种光催化剂,它的一种立方晶体的晶胞结构如图。其组成元素电负性最小的是________ 。与Ti4+距离最近的O2-数目为________ ,若晶胞参数为apm,该晶体密度为________ g▪cm-3(写出表达式)。

(1)基态Zn原子的核外电子排布式为
(2)利用CO(NH2)2(尿素)在Zn2GeO4表面沉积非金属N,能够有效提高Zn2GeO4的光催化性能。尿素分子中σ键与π键数目比为
(3)乙二胺(H2NCH2CH2NH2)所含C、N原子的杂化轨道类型分别为
(4)钙钛矿也是一种光催化剂,它的一种立方晶体的晶胞结构如图。其组成元素电负性最小的是

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐1】W、X、Y、Z、M是原子序数依次增大的5种短周期元素,其元素性质或原子结构如下:
请完成下列空白:
(1)W的元素符号为________ 。
(2)写出Y的价层电子排布式:_________ 。
(3)下列状态的X中,电离最外层一个电子所需能量最小的是______ (填序号)。
a.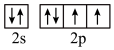 b.
b.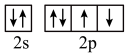 c.
c.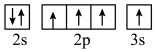
(4)基态M-占据的最高能级的电子云轮廓图的形状是_______ 。
(5)X、Z和M三种元素的电负性由大到小的顺序:_____ (请填元素符号)。
(6)X与同周期相邻的其它两种元素,它们的第一电离能由大到小的顺序:______ (请填元素符号)。
| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Z | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| M | 只有一个未成对电子 |
(1)W的元素符号为
(2)写出Y的价层电子排布式:
(3)下列状态的X中,电离最外层一个电子所需能量最小的是
a.
 b.
b. c.
c.
(4)基态M-占据的最高能级的电子云轮廓图的形状是
(5)X、Z和M三种元素的电负性由大到小的顺序:
(6)X与同周期相邻的其它两种元素,它们的第一电离能由大到小的顺序:
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】我国可燃冰资源一直被视为能源领域的宝藏,可燃冰被寄予厚望成为替代传统石油和天然气的清洁能源。回答下列问题:
(1)一定条件下, 、
、 都能与
都能与 形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。
形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。 与
与 形成的水合物晶体俗称“可燃冰”。
形成的水合物晶体俗称“可燃冰”。
 和
和 所含的三种元素电负性从大到小的顺序为
所含的三种元素电负性从大到小的顺序为___________ ;碳原子的最高能级的符号是___________ ,其电子云形状是___________ 。
(2) 分子的空间结构为
分子的空间结构为___________ 。相同条件下 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是 ,理由是
,理由是___________ 。
(3)“可燃冰”中分子间存在的两种作用力是___________ 。
(4)下列关于 和
和 的说法正确的是___________(填标号)。
的说法正确的是___________(填标号)。
(5)为开采深海海底的“可燃冰”,有科学家提出用 置换
置换 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是___________ 。
(1)一定条件下,
 、
、 都能与
都能与 形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。
形成笼状结构(如图所示)的水合物晶体,其相关参数见下表。 与
与 形成的水合物晶体俗称“可燃冰”。
形成的水合物晶体俗称“可燃冰”。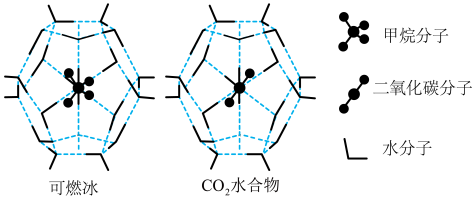
| 参数分子 | 分子直径/nm | 分子与 的结合能E/(kJ·mol 的结合能E/(kJ·mol ) ) |
 | 0.436 | 16.40 |
 | 0.512 | 29.91 |
 和
和 所含的三种元素电负性从大到小的顺序为
所含的三种元素电负性从大到小的顺序为(2)
 分子的空间结构为
分子的空间结构为 与
与 在水中的溶解度较大的是
在水中的溶解度较大的是 ,理由是
,理由是(3)“可燃冰”中分子间存在的两种作用力是
(4)下列关于
 和
和 的说法正确的是___________(填标号)。
的说法正确的是___________(填标号)。A. 分子中含有2个σ键和2个π键 分子中含有2个σ键和2个π键 |
B. 分子中含有极性共价键,是极性分子 分子中含有极性共价键,是极性分子 |
C.因为碳氢键键能小于碳氧键,所以 的熔点低于 的熔点低于 |
D. 和 和 分子中碳原子的杂化类型分别是 分子中碳原子的杂化类型分别是 和sp 和sp |
(5)为开采深海海底的“可燃冰”,有科学家提出用
 置换
置换 的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
的设想。已知上图中笼状结构的空腔直径为0.586nm,根据上述图表,从物质结构及性质的角度分析,该设想的依据是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】KZnF3被认为是良好的光学基质材料,可由K2CO3、ZnF2、NH4HF2制备。回答下列问题:
(1)基态F原子的价电子轨道表达式为_______ ;基态Zn原子核外占据最高能层电子的电子云轮廓图形状为_______ 。
(2)NH4HF2的组成元素的电负性由大到小的顺序为_______ (用元素符号表示);其中N原子的杂化方式为_______ ;HF能形成分子缔合体(HF)n的原因为_______ 。
(3)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为_______ ;
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为_______ g/cm3(用含a、c、NA的代数式表示)。
(1)基态F原子的价电子轨道表达式为
(2)NH4HF2的组成元素的电负性由大到小的顺序为
(3)ZnF2具有金红石型四方结构,KZnF3具有钙钛矿型立方结构,两种晶体的晶胞结构如图所示:

①ZnF2和KZnF3晶体(晶胞顶点为K+ )中,Zn的配位数之比为
②若NA表示阿伏加德罗常数的值,则ZnF2晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】砷化镓(GaAs)是当前最重要、技术成熟度最高的半导体材料之一,我国“玉兔二号”月球车就是通过砷化镓太阳能电池提供能量。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs___________ GaN(填“>”或“<”,下同),第一电离能Ga___________ As。
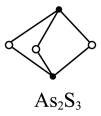
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为___________ 。
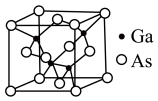
(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为______ 。
(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为___________ cm。
(1)GaAs、GaN结构相似,晶体类型都为共价晶体,沸点GaAs
(2)成语“信口雌黄”中雌黄的分子式为As2S3,分子结构如图,As原子的杂化方式为

(3)GaAs的晶胞结构如图,在GaAs晶体中,与As原子最近且等距离的As原子数为

(4)若砷化镓晶胞边长为apm,则Ga与最近As的核间距为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
【推荐2】治疗疟疾的有效药物青蒿素是白色针状晶体,受热不稳定,易溶于乙醇和乙醚;乙醚( )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。
(1)青蒿素的提取:
①萃取剂选用乙醚( )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是_____ 。
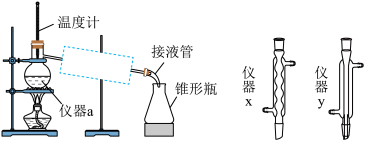
②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器_____ (填“x”或“y”)。
(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是_________ 。
②经测定得知其相对分子质量为282,所用物理方法名称是_________ 。
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其__________________ 信息。
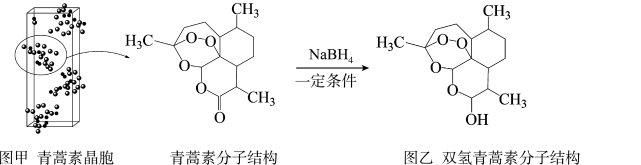
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如_________ 、_________ ,得出该分子的空间结构及其晶胞(长方体,棱长分别为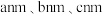 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
③晶体的密度为_________  (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。
(4)青蒿素结构的修饰:一定条件下,用 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
①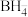 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为_________ 。
②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为_________ ,对应的官能团转变为_________ 。
 )的沸点小于乙醇的。按要求回答下列问题。
)的沸点小于乙醇的。按要求回答下列问题。(1)青蒿素的提取:
①萃取剂选用乙醚(
 )而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是
)而不用乙醇。这使蒸馏分离提纯青蒿素时效果更好的原因是②将粗品蒸馏所用装置如图所示,虚线框内应选用右侧的仪器

(2)青蒿素的分子式的确定
①经元素分析,得知其分子中含有C、H、O三种元素,其中电负性最最大的是
②经测定得知其相对分子质量为282,所用物理方法名称是
(3)青蒿素的分子结构的确定
①用红外光线照射青蒿素分子,是为获得其
②通过晶体X射线衍射实验,获得其晶胞的类型和大小、原子的种类和数目等信息,可计算出原子间的距离,判断出晶体中哪些原子间存在化学键,进而确定键参数如
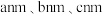 ,含4个青蒿素分子),如图甲所示。
,含4个青蒿素分子),如图甲所示。
③晶体的密度为
 (阿伏伽德罗常数的值设为
(阿伏伽德罗常数的值设为 ;列出表达式)。
;列出表达式)。(4)青蒿素结构的修饰:一定条件下,用
 将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。
将青蒿素选择性反应,结构修饰为双氢青蒿素(如图乙)。①
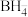 的中心原子的VSEPR模型名称为
的中心原子的VSEPR模型名称为②青蒿素结构修饰过程中,杂化轨道发生变化的碳原子的杂化方式变为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】锌是人体必需的微量元素,[Zn(NH3)4]CO3在生物活性等方面发挥重要的作用。
(1)Zn2+基态核外电子排布式为____________ 。
(2)[Zn(NH3)4]CO3中C、H、O、N四种元素的第一电离能由大到小的顺序为____________ ; 的空间构型为
的空间构型为____________ (用文字描述);1mol[Zn(NH3)4]CO3中内界所含有的σ键数目为____________ 。
(3)某含锌配合物可用于模拟碳酸酐酶的催化活性,该配合物中含有DMF分子。DMF分子的结构如图l所示。DMF分子中碳原子轨道的杂化类型是____________ 。

(4)闪锌矿可看作由Zn2+和S2-各自形成的面心立方结构相互穿插而成。其晶胞结构示意图如图2所示,则其中S2-的配位数是____________ 个。
(1)Zn2+基态核外电子排布式为
(2)[Zn(NH3)4]CO3中C、H、O、N四种元素的第一电离能由大到小的顺序为
 的空间构型为
的空间构型为(3)某含锌配合物可用于模拟碳酸酐酶的催化活性,该配合物中含有DMF分子。DMF分子的结构如图l所示。DMF分子中碳原子轨道的杂化类型是

(4)闪锌矿可看作由Zn2+和S2-各自形成的面心立方结构相互穿插而成。其晶胞结构示意图如图2所示,则其中S2-的配位数是
您最近一年使用:0次



