W、X、Y、Z、M是原子序数依次增大的5种短周期元素,其元素性质或原子结构如下:
请完成下列空白:
(1)W的元素符号为________ 。
(2)写出Y的价层电子排布式:_________ 。
(3)下列状态的X中,电离最外层一个电子所需能量最小的是______ (填序号)。
a.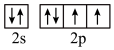 b.
b.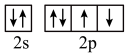 c.
c.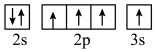
(4)基态M-占据的最高能级的电子云轮廓图的形状是_______ 。
(5)X、Z和M三种元素的电负性由大到小的顺序:_____ (请填元素符号)。
(6)X与同周期相邻的其它两种元素,它们的第一电离能由大到小的顺序:______ (请填元素符号)。
| 元素 | 元素性质或原子结构 |
| W | 电子只有一种自旋取向 |
| X | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Z | 其价电子中,在不同形状的原子轨道中运动的电子数相等 |
| M | 只有一个未成对电子 |
(1)W的元素符号为
(2)写出Y的价层电子排布式:
(3)下列状态的X中,电离最外层一个电子所需能量最小的是
a.
 b.
b. c.
c.
(4)基态M-占据的最高能级的电子云轮廓图的形状是
(5)X、Z和M三种元素的电负性由大到小的顺序:
(6)X与同周期相邻的其它两种元素,它们的第一电离能由大到小的顺序:
更新时间:2024-02-02 14:15:10
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E、F均为36号以前的元素,且原子序数依次增大。请完成下列空白:
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为_______ 。
(2)B元素的原子最外层电子排布式为 ,其元素符号为
,其元素符号为_________ 。
(3)C元素基态的正三价离子的3d轨道为半充满(即有5个电子),其元素符号为______ ,其基态原子的电子排布式为_______ 。
(4)D元素基态原子的M层全充满;N层没有成对电子,只有一个未成对电子。D的元素符号为___________ ,其基态原子的价层电子的轨道表示式为___________ 。
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用形成的离子的电子层结构相同,并且最高能级的电子对数等于其最高能层的电子层数。E、F的元素符号分别为___________ 。
(1)A元素基态原子的最外层有2个未成对电子,次外层有2个电子,其元素符号为
(2)B元素的原子最外层电子排布式为
 ,其元素符号为
,其元素符号为(3)C元素基态的正三价离子的3d轨道为半充满(即有5个电子),其元素符号为
(4)D元素基态原子的M层全充满;N层没有成对电子,只有一个未成对电子。D的元素符号为
(5)E、F元素的基态原子都只有一个未成对电子;它们相互作用形成的离子的电子层结构相同,并且最高能级的电子对数等于其最高能层的电子层数。E、F的元素符号分别为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】元素周期表是元素周期律的具体表现,是学习和研究化学的重要工具.下图是元素周期表的一部分:
请完成下列填空:
(1)元素①的简单气态氢化物的空间构型是_____________ 。
(2)元素②、③、④的简单离子半径由大到小的顺序为_____________ (用离子符号表示)。
(3) 元素在周期表中的位置是
元素在周期表中的位置是____ ,最后一行元素的基态原子中只有1个未成对电子的是_____ (填元素名称)。
(4)元素④、⑤非金属性更强的是________ (填元素符号),请从原子结构的角度解释:_________ 。并写出一个证明它们非金属性强弱的化学反应方程式________________________ 。
(5)表中第一电离能最大的元素是_____________ ,理由是__________________________ 。
| ① | ② | ||||
| ③ | ④ | ⑤ | ⑥ | ||
 |  |  |  |  |
(1)元素①的简单气态氢化物的空间构型是
(2)元素②、③、④的简单离子半径由大到小的顺序为
(3)
 元素在周期表中的位置是
元素在周期表中的位置是(4)元素④、⑤非金属性更强的是
(5)表中第一电离能最大的元素是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐3】前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题:
(1)D2+的价层电子排布图为_____ 。
(2)四种元素中第一电离最小的是____ ,电负性最大的是____ 。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。
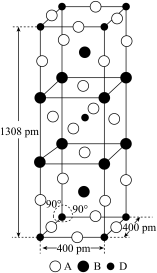
①该化合物的化学式为_____________ ;D的配位数为_______ ;
②列式计算该晶体的密度为___________ g·cm-3。(列式并计算)
(1)D2+的价层电子排布图为
(2)四种元素中第一电离最小的是
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。

①该化合物的化学式为
②列式计算该晶体的密度为
您最近一年使用:0次
【推荐1】明矾 是一种常用的净水剂。
是一种常用的净水剂。
(1)明矾中所含非金属元素的电负性由大到小的顺序为___________ (用元素符号表示)。
(2)下列状态的铝中,电离最外层的一个电子所需能量最小的是___________ (填序号)。
A.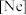 B.
B.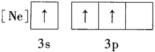 C.
C.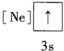 D.
D.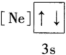
(3)基态 和
和 具有相同的核外电子排布,其核外电子占据的原子轨道数是
具有相同的核外电子排布,其核外电子占据的原子轨道数是___________ 。
(4) 中S原子的杂化方式为
中S原子的杂化方式为___________ ,其空间构型为___________ 。
 是一种常用的净水剂。
是一种常用的净水剂。(1)明矾中所含非金属元素的电负性由大到小的顺序为
(2)下列状态的铝中,电离最外层的一个电子所需能量最小的是
A.
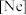 B.
B. C.
C.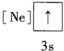 D.
D.
(3)基态
 和
和 具有相同的核外电子排布,其核外电子占据的原子轨道数是
具有相同的核外电子排布,其核外电子占据的原子轨道数是(4)
 中S原子的杂化方式为
中S原子的杂化方式为
您最近一年使用:0次
解答题-原理综合题
|
较易
(0.85)
名校
解题方法
【推荐2】完成下列问题。
(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是_______ 。
a. b.
b.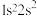 c.
c. d.
d.
(2)已知下图均与第三周期的主族元素有关。
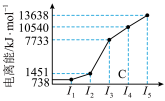
图甲
图甲表示第一至第五电离能数据,则该元素的原子有_______ 种不同运动状态的电子,基态原子未成对电子数为_______ 。
(3)以 燃料电池为电源电解法制取
燃料电池为电源电解法制取 ,二氧化氯(
,二氧化氯( )为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
)为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
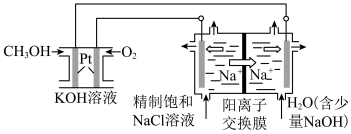
①图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ,阳极产生
,阳极产生 的反应式为
的反应式为_______ 。
②电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为_______ mol(精确到小数点后两位)。
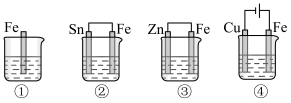
(4)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。
(1)下列状态的N原子或离子在跃迁时;用光谱仪可捕捉到发射光谱的是
a.
 b.
b.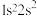 c.
c. d.
d.
(2)已知下图均与第三周期的主族元素有关。

图甲
图甲表示第一至第五电离能数据,则该元素的原子有
(3)以
 燃料电池为电源电解法制取
燃料电池为电源电解法制取 ,二氧化氯(
,二氧化氯( )为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
)为一稀黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
①图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取
 ,阳极产生
,阳极产生 的反应式为
的反应式为②电解一段时间,从阴极处收集到的气体比阳极处收集到气体多1.12L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
(4)下图所示的各容器中均盛有海水,铁在其中被腐蚀时由快到慢的顺序是_______。

| A.④>②>③>① | B.②>①>③>④ | C.④>②>①>③ | D.③>②>④>① |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】宋代《开宝本草》记载“取钢煅作叶如笏或团,平面磨错令光净,以盐水洒之,于醋瓮中阴处埋之一百日,铁上衣生,铁华成矣。”“铁华”是醋酸亚铁,其熔点约为195°C。请回答下列问题:
(1)基态Fe3+的电子排布式为__________ 。
(2)醋酸亚铁中碳原子的杂化轨道类型有__________ ,其晶体类型最可能是__________ 。
(3)盐水若洒在煤火上会产生黄色火焰,此过程中相应原子中电子跃迁方式为__________ 。
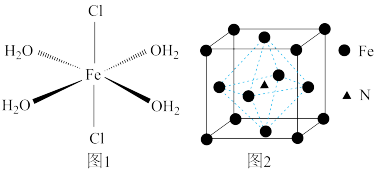
(4)FeCl2•4H2O是一种配合物,其结构如图l所示,则FeCl2•4H2O是__________ (填“极性”或“非极性”)分子。
(1)基态Fe3+的电子排布式为
(2)醋酸亚铁中碳原子的杂化轨道类型有
(3)盐水若洒在煤火上会产生黄色火焰,此过程中相应原子中电子跃迁方式为
(4)FeCl2•4H2O是一种配合物,其结构如图l所示,则FeCl2•4H2O是

您最近一年使用:0次
【推荐1】硼酸( )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
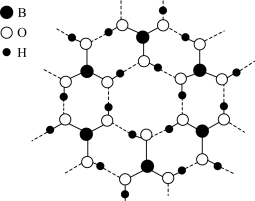
(1)关于 ,下列说法错误的是_______。
,下列说法错误的是_______。
(2)硼有两种天然同位素 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为_______ (用元素符号表示)。
(4) 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于_______ 元弱酸。B和 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:_______ 。
 )为白色晶体,晶体结构为层状,其二维平面结构如图所示。
)为白色晶体,晶体结构为层状,其二维平面结构如图所示。
(1)关于
 ,下列说法错误的是_______。
,下列说法错误的是_______。A.分子中B原子采用 杂化 杂化 | B.硼酸晶体中层与层之间存在范德华力 |
C.1  晶体中含有6 晶体中含有6 氢键 氢键 | D. 水溶性较好 水溶性较好 |
(2)硼有两种天然同位素
 和
和 ,硼元素的近似相对原子质量为10.80,则硼元素中
,硼元素的近似相对原子质量为10.80,则硼元素中 的质量分数为_______。
的质量分数为_______。| A.80% | B.20% | C.略大于20% | D.略小于20% |
(3)B与其同周期的相邻元素,第一电离能由大到小的顺序为
(4)
 与足量的
与足量的 反应,生成
反应,生成 ,则
,则 属于
属于 的某些性质相似,类比
的某些性质相似,类比 的酸式电离写出硼酸的电离方程式:
的酸式电离写出硼酸的电离方程式:
您最近一年使用:0次
【推荐2】明代宋应星所著《天工开物》中已经记载了我国古代用炉甘石(主要成分为ZnCO3)和煤冶锌工艺,锌的主要用途是制造锌合金和作为其他金属的保护层。回答下列问题:
(1)Zn基态原子核外电子排布式为_______ ,基态Zn原子电子占据最高能级的电子云轮廓图为_______ 形。
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①与SO 互为等电子体的阴离子化学式为
互为等电子体的阴离子化学式为_______ (写出一种)。
②氨是_______ 分子(“极性”或“非极性”),氨的热稳定性强于膦(PH3),原因是_______ 。
(3)黄铜是铜和锌组成的合金,元素铜与锌的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu<IZn的原因是_______ 。
(4)《本草纲目》中记载炉甘石(主要成分为ZnCO3)可止血、消肿毒、生肌、明目等。Zn、C、O的电负性由大至小的顺序是_______ 。
(1)Zn基态原子核外电子排布式为
(2)硫酸锌溶于氨水形成[Zn(NH3)4]SO4溶液。
①与SO
 互为等电子体的阴离子化学式为
互为等电子体的阴离子化学式为②氨是
(3)黄铜是铜和锌组成的合金,元素铜与锌的第一电离能分别为ICu=746 kJ·mol-1,IZn=906 kJ·mol-1,ICu<IZn的原因是
(4)《本草纲目》中记载炉甘石(主要成分为ZnCO3)可止血、消肿毒、生肌、明目等。Zn、C、O的电负性由大至小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】教材插图具有简洁而又内涵丰富的特点。请回答以下问题:
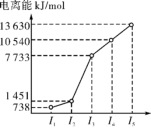
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有__________ 种不同空间运动状态的电子。
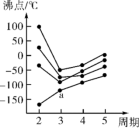
(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是___________ 。判断依据是_____________________ 。
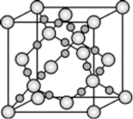
(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于___________ 晶体。
(4)第一电离能介于 Al、P 之间的第三周期元素有___________ 种。 GaCl3 中中心原子的杂化方式为___________ ,写出与 GaCl3 结构相同的一种离子___________ 。
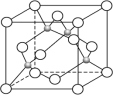
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为___________ g/cm3.(列出计算式即可)
(1)第三周期的某主族元素,其第一至第五电离能数据如图所示,则该元素对应的原子有

(2)如图所示,每条折线表示周期表ⅣA ~ⅦA 中的某一族元素氢化物的沸点变化。每个小黑点代表一种氢化物,其中 a 点代表的是

(3)CO2 在高温高压下所形成的晶体其晶胞如图所示。则该晶体的类型属于

(4)第一电离能介于 Al、P 之间的第三周期元素有
(5)下图是碳化硅的晶胞结构 。若碳化硅晶胞边长为 apm,阿伏加德罗常数为 NA ,则碳化硅晶体的密度为

您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】I.回答下列问题:
(1)下列原子或离子的核外电子排布正确的是___________ ,违反能量最低原理的是___________ ,违反洪特规则的是___________ ,违反泡利不相容原理的是___________ 。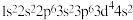 ⑤K:
⑤K: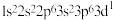 ⑥Mg:
⑥Mg:
(2)《中华本草》等中医典籍中,记载了炉甘石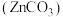 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是___________ ,其阴离子的空间结构为___________ ,Zn位于元素周期表的___________ 区。
(3)基态锰原子有___________ 种空间运动状态的电子,锰有多种化合价,在+2、+3、+4、+5和+6中,最稳定的化合价是___________ 。
(4) 已知无水 固态时具有链状结构
固态时具有链状结构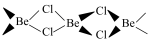 ,在二聚体分子(
,在二聚体分子(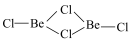 ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为___________ 。
(1)下列原子或离子的核外电子排布正确的是
① :
: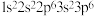 ②
② :
: ③P:
③P: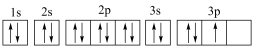
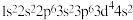 ⑤K:
⑤K: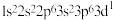 ⑥Mg:
⑥Mg:
⑦C: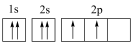
(2)《中华本草》等中医典籍中,记载了炉甘石
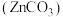 入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是
入药,可用于治疗皮肤炎症或表面创伤。Zn、C、O电负性由大至小的顺序是(3)基态锰原子有
(4) 已知无水
 固态时具有链状结构
固态时具有链状结构 ,在二聚体分子(
,在二聚体分子( ),其中铍原子的杂化类型为
),其中铍原子的杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】硼的化合物在生产、生活和科研中应用广泛。回答下列问题:
(1)基态硼原子的电子排布图为:_____ ;B、N、H的电负性由大到小的顺序为_____ 。
(2)科学家合成了一种含硼阴离子[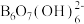 ],其结构如图1所示。其中硼原子的杂化方式为
],其结构如图1所示。其中硼原子的杂化方式为_______ ,该结构中共有_______ 种不同化学环境的氧原子。

图1
(3) 与
与 结合形成固态化合物
结合形成固态化合物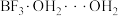 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出 和一种含硼阴离子
和一种含硼阴离子_______ (填离子符号); 空间构型为
空间构型为_______ 。
(1)基态硼原子的电子排布图为:
(2)科学家合成了一种含硼阴离子[
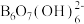 ],其结构如图1所示。其中硼原子的杂化方式为
],其结构如图1所示。其中硼原子的杂化方式为
图1
(3)
 与
与 结合形成固态化合物
结合形成固态化合物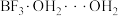 ,该物质在6.2℃时熔化电离出
,该物质在6.2℃时熔化电离出 和一种含硼阴离子
和一种含硼阴离子 空间构型为
空间构型为
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
【推荐3】“防晒霜”能有效地减轻紫外光对皮肤的伤害,其原因是其有效成分的分子中含有π键。研究表明,有效成分分子中的π键电子可在吸收紫外光后被激发,可以阻挡部分紫外光对皮肤的伤害,如对甲氧基肉桂酸辛酯、水杨酸辛酯均为“防晒霜”的主要成分。
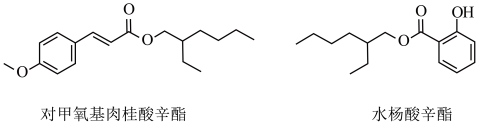
(1)对甲氧基肉桂酸辛酯和水杨酸辛酯均由H、C、O三种元素组成,按要求回答问题:
①基态O原子的核外电子排布式为_______ ,其中电子占据最高能级的电子云轮廓图为_____ 形。
其同周期元素中,第一电离能最大的是___________ (写元素符号)。
②在基态C原子中,核外存在___________ 对自旋相反的电子。
③三种元素电负性大小顺序为____________ 。
④水杨酸辛酯分子中碳原子的杂化方式有___________ 。
(2)早在公元前3000年,人们发现柳树皮具有解热镇痛功效。1838年意大利化学家拉菲勒·皮里亚以柳树皮为原料制得水杨酸,此后科学家对水杨酸的分子结构进行一系列修饰,合成出疗效更佳的长效缓释阿司匹林。

①已知苯酚(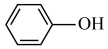 )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子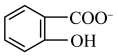 可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2
可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2___________ Ka(苯酚)(填“>”、“<”或“=”),其原因是___________ 。
②对羟基苯甲酸(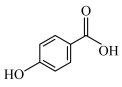 )是水杨酸的同分异构体,其沸点比水杨酸沸点
)是水杨酸的同分异构体,其沸点比水杨酸沸点___________ 。(填“高”、“低”或“相同”),原因是___________ 。
③用于合成阿司匹林的有机物A的结构简式为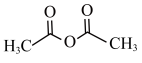 ,A分子中π键和σ键的个数之比为
,A分子中π键和σ键的个数之比为___________ 。

(1)对甲氧基肉桂酸辛酯和水杨酸辛酯均由H、C、O三种元素组成,按要求回答问题:
①基态O原子的核外电子排布式为
其同周期元素中,第一电离能最大的是
②在基态C原子中,核外存在
③三种元素电负性大小顺序为
④水杨酸辛酯分子中碳原子的杂化方式有
(2)早在公元前3000年,人们发现柳树皮具有解热镇痛功效。1838年意大利化学家拉菲勒·皮里亚以柳树皮为原料制得水杨酸,此后科学家对水杨酸的分子结构进行一系列修饰,合成出疗效更佳的长效缓释阿司匹林。

①已知苯酚(
 )具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子
)具有弱酸性,其Ka=1.1×10-10,水杨酸第一级电离形成离子 可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2
可以形成分子内氢键。在相同温度下,水杨酸的二级电离平衡常数Ka2②对羟基苯甲酸(
 )是水杨酸的同分异构体,其沸点比水杨酸沸点
)是水杨酸的同分异构体,其沸点比水杨酸沸点③用于合成阿司匹林的有机物A的结构简式为
 ,A分子中π键和σ键的个数之比为
,A分子中π键和σ键的个数之比为
您最近一年使用:0次



