周期表中VIIA族元素及其化合物应用广泛。Cl2是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等;ClO2用作自来水消毒剂;NaClO、Ca(ClO)2既可用作漂白棉麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂;氯可形成多种含氧酸HClO、HClO2、HClO3、HClO4;AgBr可用作感光材料;AgI可用于人工降雨;KIO3常用作食盐中的补碘剂。
已知下列离子反应自发进行:
①CO2+Ca2++2ClO-+H2O=CaCO3↓+2HClO
②CO +HClO=HCO
+HClO=HCO +ClO-
+ClO-
下列说法正确的是
已知下列离子反应自发进行:
①CO2+Ca2++2ClO-+H2O=CaCO3↓+2HClO
②CO
 +HClO=HCO
+HClO=HCO +ClO-
+ClO-下列说法正确的是
| A.由反应①可推断:Ka2(H2CO3)>Ka(HClO) |
| B.向新制饱和氯水中加入少量碳酸钙,固体不会溶解 |
| C.向等物质的量浓度NaHCO3和NaClO混合液中加入CaCl2(s),可生成HClO |
| D.将CO2通入NaClO溶液中,发生反应:CO2+2NaClO+H2O=Na2CO3+HClO |
更新时间:2022-10-18 16:35:25
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】相同温度下,根据三种酸的电离常数,下列判断正确的是
| 酸 |  |  | 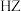 |
电离常数 | 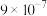 | 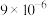 | 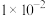 |
A.三种酸的强弱关系: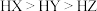 |
B.反应 能够发生 能够发生 |
C.相同温度下, 的 的 、 、 、 、 溶液, 溶液, 溶液 溶液 最大 最大 |
D.相同温度下,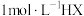 溶液的电离常数大于 溶液的电离常数大于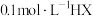 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】以下物理量与温度无关的是( )
| A.化学反应的平衡常数 | B.醋酸钠的浓度 |
| C.水的离子积 | D.CO2在水中溶解度 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】室温下,向100mL某浓度的二元弱酸H2A溶液中逐滴加入0.1mol/LNaOH溶液,溶液的pH随NaOH溶液体积的变化曲线如图所示。下列有关说法错误的是


| A.Ka1(H2A)数量级为10-3 |
| B.b点时:c(Na+)>c(HA—)>c(H+)>c(A2—)>c(OH—) |
| C.水的电离程度:d>c>b>a |
| D.b→c段,反应的离子方程式为HA—+OH—=A2—+H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如下图所示。下列说法正确的是
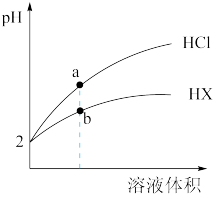

| A.稀释前,c(HX)=0.01mol/L | B.稀释10倍,HX溶液的pH=3 |
| C.a、b两点:c(X-)>c(Cl-) | D.溶液的导电性:a>b |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】浓度均为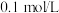 、体积均为
、体积均为 的
的 和
和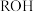 溶液,分别加水稀释至体积为V,
溶液,分别加水稀释至体积为V, 随
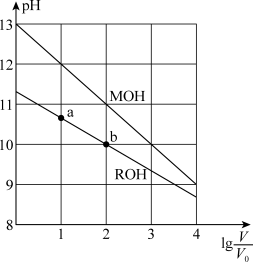
随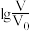 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
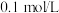 、体积均为
、体积均为 的
的 和
和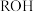 溶液,分别加水稀释至体积为V,
溶液,分别加水稀释至体积为V, 随
随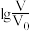 的变化如图所示。下列叙述正确的是
的变化如图所示。下列叙述正确的是
A. 的碱性弱于 的碱性弱于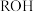 的碱性 的碱性 |
B.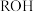 的电离程度:b点小于a点 的电离程度:b点小于a点 |
C.若两溶液无限稀释,则它们的 相等 相等 |
D.当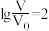 时,若两溶液同时升高温度,则 时,若两溶液同时升高温度,则 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】一种酸碱指示剂在水中存在电离平衡:HA(红色) (黄色)
(黄色) 。已知当
。已知当 时,溶液显红色;10≥
时,溶液显红色;10≥ ≥0.1时,溶液显橙色;
≥0.1时,溶液显橙色; 时,溶液显黄色。常温下,关于HA溶液和NaA溶液的下列说法正确的是
时,溶液显黄色。常温下,关于HA溶液和NaA溶液的下列说法正确的是
 (黄色)
(黄色) 。已知当
。已知当 时,溶液显红色;10≥
时,溶液显红色;10≥ ≥0.1时,溶液显橙色;
≥0.1时,溶液显橙色; 时,溶液显黄色。常温下,关于HA溶液和NaA溶液的下列说法正确的是
时,溶液显黄色。常温下,关于HA溶液和NaA溶液的下列说法正确的是| A.在NaOH溶液滴定盐酸的实验中,使用该指示剂,终点颜色变化为黄色变橙色 |
| B.调节HA溶液的pH为7,溶液颜色为黄色 |
C.NaA的溶液中, |
D.NaA和HA的混合溶液中: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在298K下,“H2A-HA--A2-”的水溶液体系中,H2A、HA-、A2-三种微粒的物质的量分数随溶液pH变化(仅用H2A和NaOH调节pH)的关系如图所示。下列说法正确的是
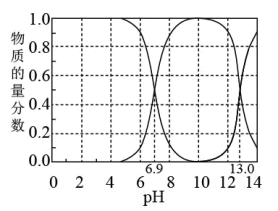

| A.Ka1(H2A)的数量级为10-6 |
| B.在pH=13.0的上述溶液中存在三个平衡 |
C.当体系呈中性时,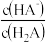 > >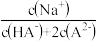 |
| D.NaHA溶液中,c(Na+)>c(HA-)>c(A2-)>c(H2A) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】向浓度为0.1 mol/L NaF溶液中不断加水稀释,下列各量增大的是
| A.c(OH-) | B.Ka(HF) | C.c(F-) | D. |
您最近一年使用:0次

 的值保持不变
的值保持不变 的值减小
的值减小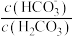 >
>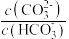
 始终增大
始终增大

