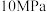下列叙述与图对应的是
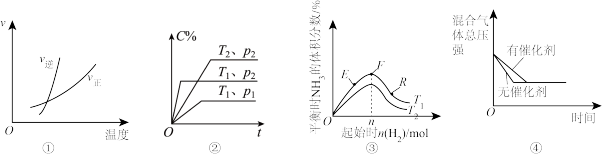
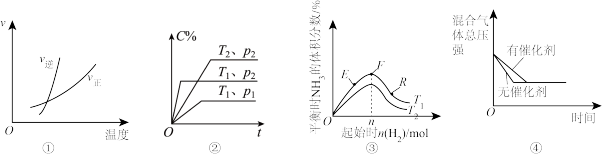
A.由图①可知,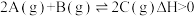 |
B.由图②可知,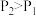 、 、 满足反应: 满足反应: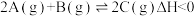 |
C.图③表示的在其他条件不变的情况下,改变初始 的物质的量对合成氨( 的物质的量对合成氨( )反应平衡的影响,其中,E,F,R三点中, )反应平衡的影响,其中,E,F,R三点中, 转化率最高的是F点 转化率最高的是F点 |
D.图④可以表示反应 加入催化剂的影响 加入催化剂的影响 |
更新时间:2022-10-28 16:47:38
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】北京化工大学研究了过渡金属 簇催化乙炔氢化的反应机理,
簇催化乙炔氢化的反应机理, 簇上的反应中间体亚乙烯基吸附物R,多步连续加氢反应路径的能量变化示意图如下(TS为过渡态,IM为中间体)。下列说法错误的是
簇上的反应中间体亚乙烯基吸附物R,多步连续加氢反应路径的能量变化示意图如下(TS为过渡态,IM为中间体)。下列说法错误的是

 簇催化乙炔氢化的反应机理,
簇催化乙炔氢化的反应机理, 簇上的反应中间体亚乙烯基吸附物R,多步连续加氢反应路径的能量变化示意图如下(TS为过渡态,IM为中间体)。下列说法错误的是
簇上的反应中间体亚乙烯基吸附物R,多步连续加氢反应路径的能量变化示意图如下(TS为过渡态,IM为中间体)。下列说法错误的是
| A.乙炔与氢气加成生成乙烷的反应为放热反应 |
| B.生产中将催化剂处理成纳米级颗粒可提高乙炔的平衡转化率 |
| C.图示反应历程中,最大能垒的反应过程为IM1到TS2 |
| D.乙炔氢化历程中涉及非极性键的断裂 |
您最近一年使用:0次
【推荐2】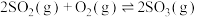
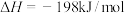 ,在V2O5存在时,该反应机理为:①
,在V2O5存在时,该反应机理为:①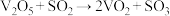 (快);②
(快);②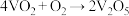 (慢)。下列说法正确的是
(慢)。下列说法正确的是
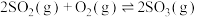
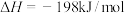 ,在V2O5存在时,该反应机理为:①
,在V2O5存在时,该反应机理为:①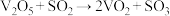 (快);②
(快);②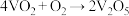 (慢)。下列说法正确的是
(慢)。下列说法正确的是| A.该反应速率主要由第①步基元反应决定 |
| B.增大SO2的浓度可显著提高反应速率 |
| C. V2O5的存在提高该反应活化分子百分数,使有效碰撞次数增加,反应速率加快 |
| D.该反应的逆反应的活化能为198kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】氯化碘(ICl)是一种卤素互化物,与氢气存在如下反应:2ICl(s)+ H2(g)=2HCl(g)+ I2(s) ΔH=-218 kJ·mol-1,该反应实际上分两步进行:
①H2(g)+ ICl(g)=HI(g)十HCl(g)(慢反应)
②HI(g)+ ICl(s)=I2(s)+ HCl( g)(快反应)
下列说法中正确的是
①H2(g)+ ICl(g)=HI(g)十HCl(g)(慢反应)
②HI(g)+ ICl(s)=I2(s)+ HCl( g)(快反应)
下列说法中正确的是
| A.ICl与水发生非氧化还原反应生成HI |
| B.两步反应的活化能之和等于-218 kJ·mol‑1 |
| C.总反应速率的快慢由反应①决定 |
| D.加入催化剂将影响最终总反应的反应热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】NH3与O2作用分别生成N2、NO、N2O的反应均为放热反应。工业尾气中的 可通过催化氧化为
可通过催化氧化为 除去。将一定比例的
除去。将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性
的选择性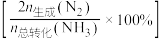 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 可通过催化氧化为
可通过催化氧化为 除去。将一定比例的
除去。将一定比例的 、
、 和
和 的混合气体以一定流速通过装有催化剂的反应管,
的混合气体以一定流速通过装有催化剂的反应管, 的转化率、生成
的转化率、生成 的选择性
的选择性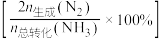 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是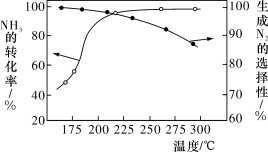
A.其他条件不变,升高温度, 的平衡转化率增大 的平衡转化率增大 |
B.其他条件不变,在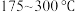 范围,随温度的升高,出口处 范围,随温度的升高,出口处 浓度不断增大 浓度不断增大 |
C.催化氧化除去尾气中的 应选择反应温度高于 应选择反应温度高于 |
D.高效除去尾气中的 ,需研发低温下 ,需研发低温下 转化率高和生成 转化率高和生成 选择性高的催化剂 选择性高的催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】对于密闭容器中的反应:N2(g)+3H2(g) 2NH3(g),该反应温度越高,反应物转化率越低,673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )
2NH3(g),该反应温度越高,反应物转化率越低,673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )

 2NH3(g),该反应温度越高,反应物转化率越低,673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )
2NH3(g),该反应温度越高,反应物转化率越低,673K、30MPa下n(NH3)和n(H2)随时间变化的关系如图所示。下列叙述正确的是( )
| A.点a的正反应速率比点b的小 |
| B.点c处反应达到平衡 |
| C.点d(t1时刻)和点e(t2时刻)处n(N2)不一样 |
| D.其他条件不变,773K下反应至t1时刻,n(H2)比图中d点的值大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】工业制备硫酸的生产过程及相关信息如下。下列有关说法正确的是
温度/℃ | 不同压强下接触室中 | |
|
| |
450 | 99.2 | 99.7 |
550 | 94.9 | 97.7 |
工艺流程 |
| |
A.循环利用的物质是 |
B. 为放热反应 为放热反应 |
C.吸收塔中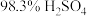 表现强氧化性 表现强氧化性 |
D.实际生产中,接触室中应采用温度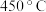 ,压强 ,压强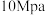 |
您最近一年使用:0次
单选题
|
适中
(0.65)
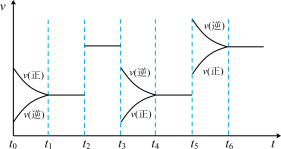
【推荐2】体积不变的密闭容器中发生反应: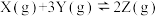
 ,下图表示该反应的速率(v)随时间(t)变化的关系,
,下图表示该反应的速率(v)随时间(t)变化的关系, 、
、 、
、 时刻外界条件有所改变。下列说法中正确的是
时刻外界条件有所改变。下列说法中正确的是
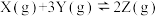
 ,下图表示该反应的速率(v)随时间(t)变化的关系,
,下图表示该反应的速率(v)随时间(t)变化的关系, 、
、 、
、 时刻外界条件有所改变。下列说法中正确的是
时刻外界条件有所改变。下列说法中正确的是
A. 时间内平衡转化率最低 时间内平衡转化率最低 | B. 时降低了温度 时降低了温度 |
C. 时只增加了气体物质Z 时只增加了气体物质Z | D. 时加入了催化剂 时加入了催化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
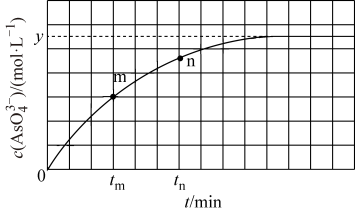
【推荐1】25°C,将Na3AsO3溶液、碘水和NaOH溶液混合,发生反应:AsO (aq)+ I2(aq)+ 2OH-
(aq)+ I2(aq)+ 2OH- AsO
AsO (aq)+2I- (aq)+ H2O(l)。溶液中c(AsO
(aq)+2I- (aq)+ H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。下列判断正确的是
)与反应时间(t)的关系如图所示。下列判断正确的是
 (aq)+ I2(aq)+ 2OH-
(aq)+ I2(aq)+ 2OH- AsO
AsO (aq)+2I- (aq)+ H2O(l)。溶液中c(AsO
(aq)+2I- (aq)+ H2O(l)。溶液中c(AsO )与反应时间(t)的关系如图所示。下列判断正确的是
)与反应时间(t)的关系如图所示。下列判断正确的是
A.c(AsO )/c(I-)= 1:2时不一定是平衡状态 )/c(I-)= 1:2时不一定是平衡状态 |
| B.平衡时c(I-)=y mol·L-1 |
C.tm时, 正< 正< 逆 逆 |
D.tm时 逆> tn时 逆> tn时 逆 逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】容积均为2L的甲乙丙三个恒容密闭容器中均加入0.10mol/L的N2、0.26mol/L的H2,进行合成氨反应:N2(g)+3H2(g)  2NH3(g) △H=-92.4kJ/mol。图1表示不同反应条件下N2的浓度随时间的变化,图2表示其它条件相同,温度分别为T1、T2、T3且恒定不变,达到平衡时NH3的质量分数。
2NH3(g) △H=-92.4kJ/mol。图1表示不同反应条件下N2的浓度随时间的变化,图2表示其它条件相同,温度分别为T1、T2、T3且恒定不变,达到平衡时NH3的质量分数。
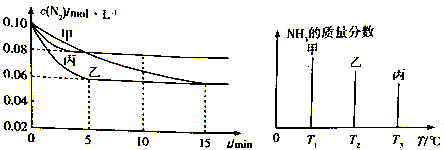
下列判断不正确的是
 2NH3(g) △H=-92.4kJ/mol。图1表示不同反应条件下N2的浓度随时间的变化,图2表示其它条件相同,温度分别为T1、T2、T3且恒定不变,达到平衡时NH3的质量分数。
2NH3(g) △H=-92.4kJ/mol。图1表示不同反应条件下N2的浓度随时间的变化,图2表示其它条件相同,温度分别为T1、T2、T3且恒定不变,达到平衡时NH3的质量分数。
下列判断不正确的是
| A.图2 中反应速率最快的是容器丙 |
| B.图1 中容器乙的反应可能使用了催化剂 |
| C.图l 中容器乙0~5 min时间内v(N2) = 0.012mol/(L·min) |
| D.图1 中容器丙内反应的平衡常数为2.5 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】在500℃、60.0MPa条件下合成氨,原料气投料比与平衡时 体积分数的关系如图所示。
体积分数的关系如图所示。
 体积分数的关系如图所示。
体积分数的关系如图所示。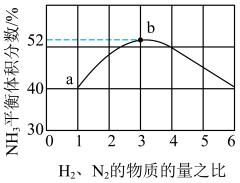
A.按a点的投料比进行反应,当 的体积分数不变时达到平衡状态 的体积分数不变时达到平衡状态 |
B.a点的平衡体系中, |
C.b点的平衡体系中, 的体积分数为36% 的体积分数为36% |
| D.b点混合气体的平均相对分子质量约为11.33 |
您最近一年使用:0次

 的恒容密闭容器中盛有一定量
的恒容密闭容器中盛有一定量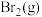 发生反应:
发生反应: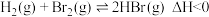 。当温度分别为
。当温度分别为 平衡时,
平衡时,


 的平衡转化率/
的平衡转化率/