回答下列问题
(1)已知:2Zn(s)+O2(g)=2ZnO(s) ΔH=-701.0 kJ/mol
2Hg(l)+O2(g)= 2HgO(s) ΔH=-181.6 kJ/mol
则Zn和HgO反应生成ZnO和Hg的热化学方程式为_______
(2)某温度时,在一密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示。
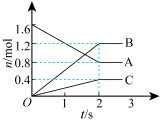
则该反应的化学方程式为_______ (用A、B、C表示)
(3)温度一定时, 于密闭容器中发生可逆反应: mA(g) + nB(g) pC(g), 达到平衡, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍, 则 m + n
pC(g), 达到平衡, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍, 则 m + n _______ p(填“>、<、=” )。
(1)已知:2Zn(s)+O2(g)=2ZnO(s) ΔH=-701.0 kJ/mol
2Hg(l)+O2(g)= 2HgO(s) ΔH=-181.6 kJ/mol
则Zn和HgO反应生成ZnO和Hg的热化学方程式为
(2)某温度时,在一密闭容器中,A、B、C三种物质的物质的量随时间的变化曲线如图所示。

则该反应的化学方程式为
(3)温度一定时, 于密闭容器中发生可逆反应: mA(g) + nB(g)
 pC(g), 达到平衡, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍, 则 m + n
pC(g), 达到平衡, 若将混合气体的体积压缩到原来的 1/2, 当再次达到平衡时, C的浓度为原平衡时C的浓度的 1.9 倍, 则 m + n
更新时间:2022-10-26 10:58:11
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气是一种常用的化工原料,如合成氨和尿素[CO(NH2)2]等。
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)=2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+ CO2(g)=
CO2(g)= NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为__________ 。
(2)电解制H2的原理为C(s)+2H2O(l)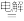 CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
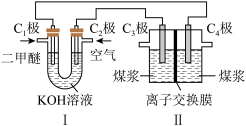
①分别写出电极C1和C3的电极反应式__________________ ;___________________ 。
②离子交换膜可能是________ (填字母)。
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=________ 。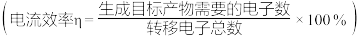
(1)以H2合成CO(NH2)2的有关热化学方程式有:
①N2(g)+3H2(g)=2NH3(g)ΔH1=-92.4 kJ·mol-1
②NH3(g)+
 CO2(g)=
CO2(g)= NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1
NH2CO2NH4(s)ΔH2=-79.7 kJ·mol-1③NH2CO2NH4(s)=CO(NH2)2(s)+H2O(l)ΔH3=+72.5 kJ·mol-1
则N2(g)、H2(g)与CO2(g)反应生成CO(NH2)2(s)和H2O(l)的热化学方程式为
(2)电解制H2的原理为C(s)+2H2O(l)
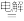 CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
CO2(g)+2H2(g)。某学习小组拟以二甲醚(CH3OCH3)-空气碱性燃料电池为电源,电解煤浆液(由煤粉与稀硫酸组成)探究上述原理,装置如图所示。
①分别写出电极C1和C3的电极反应式
②离子交换膜可能是
a.阳离子交换膜 b.阴离子交换膜 c.质子交换膜
③已知4.6 g二甲醚参与反应,假设装置Ⅰ的能量转化率为100%,C4极收集到11.2L(标准状况)气体,装置Ⅱ的电流效率η=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】异丁烯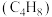 是一种重要的化工原料,可由异丁烷
是一种重要的化工原料,可由异丁烷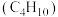 直接催化脱氢制备:
直接催化脱氢制备:
(1)已知: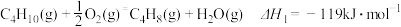
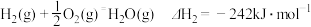
写出由异丁烷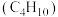 催化脱氢制备异丁烯
催化脱氢制备异丁烯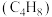 的热化学方程式。
的热化学方程式。_________ 。
(2)一定条件下,以异丁烷为原料催化脱氢生产异丁烯。温度、压强的改变对异丁烷平衡转化率的影响如图所示。
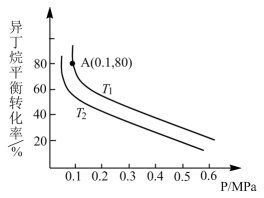
①判断 、
、 的大小关系:
的大小关系:
_____________  (填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是
(填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是____________ (填标号)。
a.升高温度 b.降低温度 c.增大压强 d.降低压强 e.使用催化剂
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即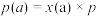 (总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数
(总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数
_____________ (保留两位有效数字)。
(3)温度对催化剂的活性和目标产物的选择性都有一定的影响。下表是以 为催化剂,在反应时间相同时,测得的不同温度下的数据。
为催化剂,在反应时间相同时,测得的不同温度下的数据。
已知①选择性 ;②异丁烷高温下裂解生成短碳链烃类化合物
;②异丁烷高温下裂解生成短碳链烃类化合物
①590℃时异丁烯的产率
_____________ ×100%。
②在590℃之前异丁烯的产率随温度升高而增大的原因可能是____________ 、_____________ 。
③590℃之后,异丁烯产率降低的主要原因可能是_____________ 。
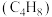 是一种重要的化工原料,可由异丁烷
是一种重要的化工原料,可由异丁烷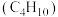 直接催化脱氢制备:
直接催化脱氢制备:(1)已知:
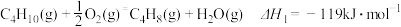
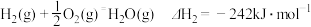
写出由异丁烷
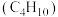 催化脱氢制备异丁烯
催化脱氢制备异丁烯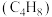 的热化学方程式。
的热化学方程式。(2)一定条件下,以异丁烷为原料催化脱氢生产异丁烯。温度、压强的改变对异丁烷平衡转化率的影响如图所示。

①判断
 、
、 的大小关系:
的大小关系:
 (填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是
(填“>”或“<”);能使单位时间内异丁烯的产量提高,又能使异丁烷平衡产率提高,应采取的措施是a.升高温度 b.降低温度 c.增大压强 d.降低压强 e.使用催化剂
②平衡常数的表达式中的平衡浓度可以用平衡时各气体的分压代替(气体a的分压=气体a的物质的量分数×总压强,即
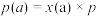 (总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数
(总)。求图中的A点状态下的异丁烷脱氢反应的平衡常数
(3)温度对催化剂的活性和目标产物的选择性都有一定的影响。下表是以
 为催化剂,在反应时间相同时,测得的不同温度下的数据。
为催化剂,在反应时间相同时,测得的不同温度下的数据。| 温度/℃ | 550 | 570 | 590 | 610 | 630 |
| 异丁烷转化率/% | 13.8 | 24.5 | 25.6 | 30.0 | 33.3 |
| 异丁烯选择性/% | 93.9 | 88.3 | 95.0 | 80.4 | 71.2 |
| 异丁烯的产率/% | 12.9 | 21.6 | w | 24.1 | 23.7 |
已知①选择性
 ;②异丁烷高温下裂解生成短碳链烃类化合物
;②异丁烷高温下裂解生成短碳链烃类化合物①590℃时异丁烯的产率

②在590℃之前异丁烯的产率随温度升高而增大的原因可能是
③590℃之后,异丁烯产率降低的主要原因可能是
您最近一年使用:0次
【推荐3】国家实施“青山绿水工程”,大力研究脱硝和脱硫技术。
(1)H2在催化剂作用下可将NO还原为N2。如图是该反应生成1 mol水蒸气的能量变化示意图。写出该反应的热化学方程式__________ 。

(2)2NO(g)+O2(g) 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
反应Ⅰ:2NO(g) N2O2(g)(快) ΔH1<0,v1正=k1正·c2(NO)、v1逆=k1逆·c(N2O2);
N2O2(g)(快) ΔH1<0,v1正=k1正·c2(NO)、v1逆=k1逆·c(N2O2);
反应Ⅱ:N2O2(g)+O2(g) 2NO2(g)(慢)ΔH2<0,v2正=k2正·c(N2O2)·c(O2)、v2逆=k2逆·c2(NO2)。
2NO2(g)(慢)ΔH2<0,v2正=k2正·c(N2O2)·c(O2)、v2逆=k2逆·c2(NO2)。
①一定条件下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,平衡常数K=
2NO2(g)达到平衡状态,平衡常数K=___________ (用含k1正、k1逆、k2正、k2逆的代数式表示)。反应Ⅰ的活化能EⅠ___________ (填“>”“<”或“=”)反应Ⅱ的活化能EⅡ。
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数__________ (填“大于”“小于”或“等于”)k2逆增大的倍数。
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。
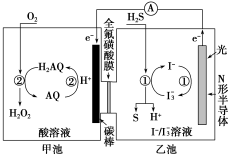
①装置中H+向_______ 池迁移。
②乙池溶液中发生反应的离子方程式:_______ 。
(4)废水处理时,通H2S(或加S2-)能使某些金属离子生成极难溶的硫化物而除去。25 ℃,某废液中c(Mn2+)=0.02 mol·L-1,调节废液的pH使Mn2+开始沉淀为MnS时,废液中c(H2S)=0.1 mol·L-1,此时pH约为_______ (已知:Ksp(MnS)=5.0×10-14,H2S的电离常数:Ka1=1.5×10-7,Ka2=6.0×10-15,lg 6=0.8)。
(1)H2在催化剂作用下可将NO还原为N2。如图是该反应生成1 mol水蒸气的能量变化示意图。写出该反应的热化学方程式

(2)2NO(g)+O2(g)
 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:反应Ⅰ:2NO(g)
 N2O2(g)(快) ΔH1<0,v1正=k1正·c2(NO)、v1逆=k1逆·c(N2O2);
N2O2(g)(快) ΔH1<0,v1正=k1正·c2(NO)、v1逆=k1逆·c(N2O2);反应Ⅱ:N2O2(g)+O2(g)
 2NO2(g)(慢)ΔH2<0,v2正=k2正·c(N2O2)·c(O2)、v2逆=k2逆·c2(NO2)。
2NO2(g)(慢)ΔH2<0,v2正=k2正·c(N2O2)·c(O2)、v2逆=k2逆·c2(NO2)。①一定条件下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,平衡常数K=
2NO2(g)达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(3)我国科学家在天然气脱硫研究方面取得了新进展,利用如图装置可发生反应:H2S+O2=H2O2+S↓。

①装置中H+向
②乙池溶液中发生反应的离子方程式:
(4)废水处理时,通H2S(或加S2-)能使某些金属离子生成极难溶的硫化物而除去。25 ℃,某废液中c(Mn2+)=0.02 mol·L-1,调节废液的pH使Mn2+开始沉淀为MnS时,废液中c(H2S)=0.1 mol·L-1,此时pH约为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】有效除去大气中的SO2和氮氧化物,是打赢蓝天保卫战的重中之重。
(1)某温度下,N2O5气体在一体积固定的容器中发生如下反应:
2N2O5=4NO2+O2(g)(慢反应) ΔH<0
2NO2 N2O4(快反应) ΔH<0
N2O4(快反应) ΔH<0
体系的总压强p总和pO2随时间的变化如图所示:

①图乙中表示O2压强变化的曲线是___ (填“A”或“B”)。
②已知N2O5分解的反应速率v=0.12pN2O5(kPa·h-1),t=10h时,pN2O5=___ kPa,v=____ kPa•h‑1(结果保留两位小数)。
(2)亚硝酸盐广泛存在于各种水体和腌制品中,可用电吸附装置去除。去除量跟电压、初始浓度、共存阴离子等因素有关。某科研机构的实验结果如图所示:

①据图丙可知,待处理液中NO 与NO
与NO 的C0=
的C0=____ mg·L-1时,装置对NO 的吸附量高于NO
的吸附量高于NO 。
。
②据图丙分析,为提高离子去除量可采取的措施有__ (写出一条即可)。
(1)某温度下,N2O5气体在一体积固定的容器中发生如下反应:
2N2O5=4NO2+O2(g)(慢反应) ΔH<0
2NO2
 N2O4(快反应) ΔH<0
N2O4(快反应) ΔH<0体系的总压强p总和pO2随时间的变化如图所示:

①图乙中表示O2压强变化的曲线是
②已知N2O5分解的反应速率v=0.12pN2O5(kPa·h-1),t=10h时,pN2O5=
(2)亚硝酸盐广泛存在于各种水体和腌制品中,可用电吸附装置去除。去除量跟电压、初始浓度、共存阴离子等因素有关。某科研机构的实验结果如图所示:

①据图丙可知,待处理液中NO
 与NO
与NO 的C0=
的C0= 的吸附量高于NO
的吸附量高于NO 。
。②据图丙分析,为提高离子去除量可采取的措施有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】Ⅰ.利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:①CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g)
CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g) CH3OH(g) △H2 ③CO2(g)+H2(g)
CH3OH(g) △H2 ③CO2(g)+H2(g) CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;
回答下列问题:
(1)已知△H2=-99 kJ·mol-1,则根据上表相关的化学键键能(“C O”表示CO的化学键)计算X=
O”表示CO的化学键)计算X=_______ kJ·mol-1。
(2)反应①、②、③对应的平衡常数K1、K2、K3之间的关系式为___________ 。
(3)根据化学反应原理,分析增大压强对反应③的影响为_______________ 。(提示:从对反应速率、平衡状态、转化率角度回答)
Ⅱ.清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g) CH3OH(g)△H=-99kJ•mol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
CH3OH(g)△H=-99kJ•mol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:

①Ⅱ和Ⅰ相比,改变的反应条件是_________ ;
②反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=_________ ;
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=_________ ;
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1_____ T3(填“>”“<”“=”),判断的理由是_________ 。
 CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g)
CH3OH(g)+H2O(g) △H1;②CO(g)+2H2(g) CH3OH(g) △H2 ③CO2(g)+H2(g)
CH3OH(g) △H2 ③CO2(g)+H2(g) CO(g)+H2O(g) △H3;
CO(g)+H2O(g) △H3;| 化学键 | H-H | C-O | C O O | H-O | C-H |
| E/(kJ·mol-1) | 436 | 343 | 1076 | 465 | X |
回答下列问题:
(1)已知△H2=-99 kJ·mol-1,则根据上表相关的化学键键能(“C
 O”表示CO的化学键)计算X=
O”表示CO的化学键)计算X=(2)反应①、②、③对应的平衡常数K1、K2、K3之间的关系式为
(3)根据化学反应原理,分析增大压强对反应③的影响为
Ⅱ.清洁能源具有广阔的开发和应用前景,可减小污染解决雾霾问题,其中甲醇、甲烷是优质的清洁燃料,可制作燃料电池。一定条件下用CO和H2合成CH3OH:CO(g)+2H2(g)
 CH3OH(g)△H=-99kJ•mol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
CH3OH(g)△H=-99kJ•mol-1。向体积为2L的密闭容器中充入2molCO和4molH2,测得不同温度下容器内的压强(P:kPa)随时间(min)的变化关系如图中Ⅰ、Ⅱ、Ⅲ曲线所示:
①Ⅱ和Ⅰ相比,改变的反应条件是
②反应Ⅰ在6min时达到平衡,在此条件下从反应开始到达到平衡时v(CH3OH)=
③反应Ⅱ在2min时达到平衡,平衡常数K(Ⅱ)=
④比较反应Ⅰ的温度(T1)和反应Ⅲ的温度(T3)的高低:T1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】氮是空气中含量最多的元素,在自然界中存在十分广泛,在生物体内亦有较大作用,是组成氨基酸的基本元素之一。请回答下列问题。
(1)用CO可将汽车尾气中的NO还原为N2,反应为2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g)
N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g) 2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+
2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+ O2(g)
O2(g) CO2(g) ΔH2=
CO2(g) ΔH2=____ kJ·mol-1(用含a、b的代数式表示),K2=____ (用含m、n的代数式表示)。
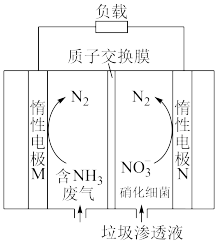
(2)“绿水青山就是金山银山”。现利用如图所示装置对工业废气、垃圾渗透液进行综合治理并实现发电。M极是____ 极,正极的电极反应式为____ 。
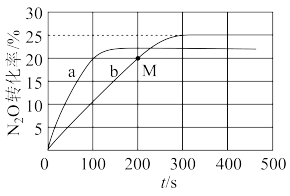
(3)N2O可以被CO还原:N2O(g)+CO(g) N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正____ v逆(填“>”“<”或“=”),A中反应的平衡常数为____ (用分数表示),平衡常数:B____ A(填“大于”“小于”或“等于”)。
(4)实验室中可用NaOH溶液吸收多余的NO2:2NO2+2NaOH=NaNO3+NaNO2+H2O。常温下,用含0.14molNaOH的水溶液吸收NO2,恰好完全反应得1L溶液,测得该溶液的pH=8,则HNO2的电离常数为____ 。
(1)用CO可将汽车尾气中的NO还原为N2,反应为2NO(g)+2CO(g)
 N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g)
N2(g)+2CO2(g) ΔH=-akJ·mol-1,K=m。已知:N2(g)+O2(g) 2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+
2NO(g) ΔH1=+bkJ·mol-1,K1=n,则CO(g)+ O2(g)
O2(g) CO2(g) ΔH2=
CO2(g) ΔH2=(2)“绿水青山就是金山银山”。现利用如图所示装置对工业废气、垃圾渗透液进行综合治理并实现发电。M极是

(3)N2O可以被CO还原:N2O(g)+CO(g)
 N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
N2(g)+CO2(g)。在体积均为1L的恒容密闭容器A(500℃,恒温)、B(起始500℃,绝热)中分别加入0.1molN2O、0.4molCO和相同的催化剂。实验测得A、B中N2O的转化率随时间的变化关系如图所示。A中N2O的转化率随时间的变化关系是图中的b曲线,M点:v正
(4)实验室中可用NaOH溶液吸收多余的NO2:2NO2+2NaOH=NaNO3+NaNO2+H2O。常温下,用含0.14molNaOH的水溶液吸收NO2,恰好完全反应得1L溶液,测得该溶液的pH=8,则HNO2的电离常数为
您最近一年使用:0次



