二甲醚( )是重要的化工原料,也是一种清洁的能源,可用
)是重要的化工原料,也是一种清洁的能源,可用 和
和 制得,由合成气制备二甲醚的主要原理如下:
制得,由合成气制备二甲醚的主要原理如下:
①
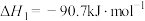

②
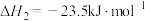

③
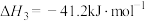

(1)反应 的
的
_______  ;该反应的平衡常数
;该反应的平衡常数
_______ (用 、
、 、
、 表示)。
表示)。
(2)下列措施中,能提高①中 产率的有_______。
产率的有_______。
(3)将合成气以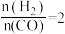 通入
通入 的反应器中,一定条件下发生反应:
的反应器中,一定条件下发生反应:
 ,其中
,其中 的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是
的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是_______ (填字母)。

A.
B.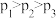
C. 若在 和316℃时,起始时
和316℃时,起始时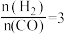 ,则平衡时,
,则平衡时,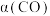 小于50%
小于50%
(4)采用一种新型的催化剂(主要成分是 的合金),利用
的合金),利用 和
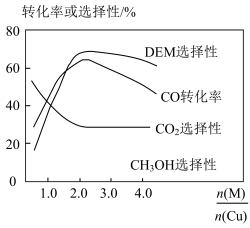
和 制备二甲醚(DME)。观察图,当
制备二甲醚(DME)。观察图,当 约为
约为_______ 时最有利于二甲醚的合成。
(5)下图为绿色电源“二甲醚燃料电池”的工作原理示意图,a极生成的气体是_______ ,b电极的电极反应式为_______ 。

(6)甲醇液相脱水法制二甲醚的原理是: ,
, 。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是
。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是_______ 。
 )是重要的化工原料,也是一种清洁的能源,可用
)是重要的化工原料,也是一种清洁的能源,可用 和
和 制得,由合成气制备二甲醚的主要原理如下:
制得,由合成气制备二甲醚的主要原理如下:①

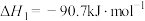

②

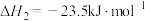

③

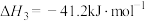

(1)反应
 的
的
 ;该反应的平衡常数
;该反应的平衡常数
 、
、 、
、 表示)。
表示)。(2)下列措施中,能提高①中
 产率的有_______。
产率的有_______。A.使用过量的 | B.升高温度 | C.增大压强 | D.使用催化剂 |
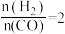 通入
通入 的反应器中,一定条件下发生反应:
的反应器中,一定条件下发生反应:
 ,其中
,其中 的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是
的平衡转化率随温度、压强的变化关系如图所示,下列说法正确的是
A.

B.
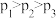
C. 若在
 和316℃时,起始时
和316℃时,起始时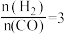 ,则平衡时,
,则平衡时,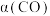 小于50%
小于50%(4)采用一种新型的催化剂(主要成分是
 的合金),利用
的合金),利用 和
和 制备二甲醚(DME)。观察图,当
制备二甲醚(DME)。观察图,当 约为
约为
(5)下图为绿色电源“二甲醚燃料电池”的工作原理示意图,a极生成的气体是

(6)甲醇液相脱水法制二甲醚的原理是:
 ,
, 。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是
。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是
更新时间:2022-10-27 20:30:30
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】氮的氧化物是严重的大气污染物,可以通过以下方法处理:
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)⇌N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)⇌2NO(g) △H=+180kJ/mol
则反应:2NO(g)+2CO(g) ⇌N2(g)+2CO2(g) △H=_____ kJ/mol。
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:
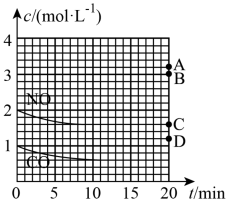
①该反应的平衡常数 K 的计算式为_____ ;前 10 分钟内用氮气表示的反应速率为_____ 。
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正______ ν逆(填“>”、“=”或“<”)。
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的_____ (填字母)。
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是__________________

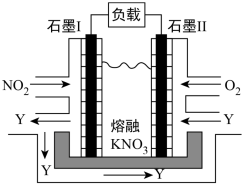
Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为_____ 相同条件下,消耗的 O2和 NO2的体积比为_____
Ⅰ.催化还原法:如在汽车排气管上安装一个催化转化器,发生如下反应: 2NO(g)+2CO(g)⇌N2(g)+2CO2(g)
(1)已知N2(g)+O2(g)⇌2NO(g) △H=+180kJ/mol
| 化学键 | O=O | C=O | C≡O |
| 键能(kJ/mol) | 497 | 803 | 1072 |
则反应:2NO(g)+2CO(g) ⇌N2(g)+2CO2(g) △H=
(2)在一定温度下,向体积为1L的密闭容器中充入2molNO、1molCO,10分钟时反应2NO(g)+2CO(g)⇌N2(g)+2CO2(g)达到平衡状态,反应过程中反应物浓度随时间变化情况如图所示:

①该反应的平衡常数 K 的计算式为
②若保持温度不变,15 分钟时再向该容器中充入1.6molNO、0.4molCO2,则此时反应的ν正
③若保持其他条件不变,15min 时压缩容器的体积至 0.5L,20 分钟时反应重新达到平衡,NO 的浓度对应的点应是图中的
④某科研小组研究发现以 Ag-ZSM-5 为催化剂,NO 转化为 N2的转化率随温度变化情况如图所示。若不使用 CO,温度超过775K,发现NO的分解率降低,其可能的原因是

Ⅱ.利用电化学原理,将 NO2、O2和熔融 KNO3制成燃料电池,其原理如图,该电池在工作过程中NO2转变成绿色硝化剂Y,Y是一种氧化物,可循环使用,石墨Ⅰ附近发生的反应电极反应式为

您最近一年使用:0次
【推荐2】节能减排措施是我国“十一五”期间提出的政策措施。
(1)煤的燃烧,会产生大量有害气体。将煤转化为水煤气,可有效降低排放。
C(s)+O2(g)=CO2(g)△H=-393.5 kJ·mol-1
H2(g)+ O2(g)=H2O(g)△H=-242.0kJ·mol-1
O2(g)=H2O(g)△H=-242.0kJ·mol-1
CO(g)+ O2(g)=CO2(g)△H=-283.0kJ·mol-1
O2(g)=CO2(g)△H=-283.0kJ·mol-1
根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式____________ 。
(2)汽车尾气的排放是大气污染物的重要来源,其中含有NO气体。根据资料显示用活性炭还原法可以处理氮氧化物,某研究小组向固定容积的密闭容器中加入一定量的活性炭和NO发生反应C(s)+2NO(g) CO2(g)+N2(g)△H=-574kJ·mol-1,并在温度T时将所测反应数据制成下表:
CO2(g)+N2(g)△H=-574kJ·mol-1,并在温度T时将所测反应数据制成下表:
①0到10min内,NO的平均反应速率v(NO)=___________ mol·L-1·min-1。
②下列数据不再变化可表示该反应达到平衡的是________________________ 。
a.容器内压强b.混合气体的平均摩尔质量c.混合气体的密度
③若容器改为可变容积容器,达平衡后,再充入少量NO气体,再次达到平衡时N2的浓度____________ (填“增大”,“减小”,或“不变”)
(3)在某温度T时能同时发生反应:
2N2O5(g)
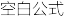 2N2O4(g)+O2(g) K1
2N2O4(g)+O2(g) K1
N2O4(g) 2NO2(g) K2
2NO2(g) K2
若向一体积固定为2L的密闭容器内加入N2O52mol,一段时间后,容器内的反应达到平衡,此时n(NO2)=0.4mol,已知K2=0.1,请计算出K1=___________ 。
(1)煤的燃烧,会产生大量有害气体。将煤转化为水煤气,可有效降低排放。
C(s)+O2(g)=CO2(g)△H=-393.5 kJ·mol-1
H2(g)+
 O2(g)=H2O(g)△H=-242.0kJ·mol-1
O2(g)=H2O(g)△H=-242.0kJ·mol-1CO(g)+
 O2(g)=CO2(g)△H=-283.0kJ·mol-1
O2(g)=CO2(g)△H=-283.0kJ·mol-1根据以上数据,写出C(s)与水蒸气反应生成CO和H2的热化学方程式
(2)汽车尾气的排放是大气污染物的重要来源,其中含有NO气体。根据资料显示用活性炭还原法可以处理氮氧化物,某研究小组向固定容积的密闭容器中加入一定量的活性炭和NO发生反应C(s)+2NO(g)
 CO2(g)+N2(g)△H=-574kJ·mol-1,并在温度T时将所测反应数据制成下表:
CO2(g)+N2(g)△H=-574kJ·mol-1,并在温度T时将所测反应数据制成下表:| 时间(min) 浓度( 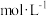 ) ) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.52 | 0.36 | 0.36 | 0.54 | 0.54 |
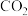 | 0 | 0.24 | 0.32 | 0.32 | 0.48 | 0.48 |
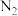 | 0 | 0.24 | 0.32 | 0.32 | 0.48 | 0.48 |
①0到10min内,NO的平均反应速率v(NO)=
②下列数据不再变化可表示该反应达到平衡的是
a.容器内压强b.混合气体的平均摩尔质量c.混合气体的密度
③若容器改为可变容积容器,达平衡后,再充入少量NO气体,再次达到平衡时N2的浓度
(3)在某温度T时能同时发生反应:
2N2O5(g)

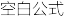 2N2O4(g)+O2(g) K1
2N2O4(g)+O2(g) K1N2O4(g)
 2NO2(g) K2
2NO2(g) K2若向一体积固定为2L的密闭容器内加入N2O52mol,一段时间后,容器内的反应达到平衡,此时n(NO2)=0.4mol,已知K2=0.1,请计算出K1=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐3】废气中的含氮氧化物是主要的大气污染物,因此脱出废气中的含氮氧化物对于保护大气环境具有重要的意义。
(1)汽车的大量使用是城市大气中含氮氧化物的主要来源。
①汽车燃油中一般不含有氮元素,汽车尾气中的NO是如何产生的?___________ (用化学方程式表示)。
②NO易被O2氧化为NO2。其他条件不变时,NO的氧化率[α(NO)%]与温度、压强的关系如图所示。则p1________ p2(填“>”、“<”或“=”);温度高于800℃时,α(NO)几乎为0的原因是_____ 。

(2)利用氨气脱除NO是大气污染防治研究的热点,过程中涉及的反应为:
主反应:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)
副反应:
①4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.5kJ/mol
4NO(g)+6H2O(g) ΔH=-905.5kJ/mol
②4NH3(g)+4O2(g) 2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol
2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol
③4NH3(g)+3O2(g) 2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol
2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol
回答下列问题:
主反应的ΔH为____________________ ;保持其它条件相同,使用两种不同的催化剂,主反应NO的转化率与温度关系如图所示,选用催化剂I的优势有_________________ (写出一点即可);R点对应的温度为210℃,低于210℃,NO的转化率是不是对应温度下的平衡转化率,请作出判断并写出理由__________________ 。

(3)碱液吸收法:用Na2CO3溶液吸收NO2生成CO2.若每4.6gNO2和Na2CO3溶液反应时转移电子数为0.05mol,则反应的离子方程式是__________ 。
(4)常温下,在通入O2的条件下用0.1mol/L的NaOH溶液吸收NO,产物为NaNO3 和NaNO2。已知反应后溶液的pH=12,溶液中NO2-浓度为5.6×10-2mol/L(忽略反应过程中溶液体积变化,HNO2的电离平衡常数Ka=5.1×10-4),则:
① =
=________ mol/L
②反应后溶液中NO3-的浓度约为___________ mol/L
③某溶液中c(NO2-)=1.0×10-6mol/L,取该溶液5mL,加入一滴0.1mol/L硝酸银溶液(一滴为0.05mL),通过计算说明能否产生沉淀______________ 。【Ksp(AgNO2)=2×10-8】
(1)汽车的大量使用是城市大气中含氮氧化物的主要来源。
①汽车燃油中一般不含有氮元素,汽车尾气中的NO是如何产生的?
②NO易被O2氧化为NO2。其他条件不变时,NO的氧化率[α(NO)%]与温度、压强的关系如图所示。则p1

(2)利用氨气脱除NO是大气污染防治研究的热点,过程中涉及的反应为:
主反应:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g)
4N2(g)+6H2O(g)副反应:
①4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) ΔH=-905.5kJ/mol
4NO(g)+6H2O(g) ΔH=-905.5kJ/mol②4NH3(g)+4O2(g)
 2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol
2N2O(g)+6H2O(g) ΔH=-1104.9kJ/mol③4NH3(g)+3O2(g)
 2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol
2N2(g)+6H2O(g) ΔH=-1269.0kJ/mol回答下列问题:
主反应的ΔH为

(3)碱液吸收法:用Na2CO3溶液吸收NO2生成CO2.若每4.6gNO2和Na2CO3溶液反应时转移电子数为0.05mol,则反应的离子方程式是
(4)常温下,在通入O2的条件下用0.1mol/L的NaOH溶液吸收NO,产物为NaNO3 和NaNO2。已知反应后溶液的pH=12,溶液中NO2-浓度为5.6×10-2mol/L(忽略反应过程中溶液体积变化,HNO2的电离平衡常数Ka=5.1×10-4),则:
①
 =
=②反应后溶液中NO3-的浓度约为
③某溶液中c(NO2-)=1.0×10-6mol/L,取该溶液5mL,加入一滴0.1mol/L硝酸银溶液(一滴为0.05mL),通过计算说明能否产生沉淀
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】CO是大气污染气体,可利用化学反应进行治理或转化。
(1)甲醇是重要的溶剂和燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g) CH3OH(g) ΔH<0
CH3OH(g) ΔH<0
①T℃时,向容积为2 L的恒容密闭容器中充入1 mol CO和1.2 mol H2,一段时间后达到平衡,此时H2与CH3OH的体积分数之比为2∶5,该反应的平衡常数K=____ ;此时若向容器中再通入0.4 mol CO和0.2 mol CH3OH(g),则平衡将____ 移动。(填“向正反应方向”、“不”或“向逆反应方向”)
②在一容积可变的密闭容器中充入一定物质的量的CO和H2,测得CO在不同温度下的平衡转化率与压强的关系如图所示。a、b、c三点平衡常数K(a)、K(b)、K(c)的大小关系是____ 。b、d两点的正反应速率vb(CO)____ vd(CO)。

(2)沥青混凝土可作为2CO(g)+O2(g) 2CO2(g)反应的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、反应相同的时间,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)反应的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、反应相同的时间,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。

①a、b、c、d四点中表示平衡状态的是____ ;
②相同条件下,____ 型沥青混凝土催化效果更佳;
③e点转化率出现突变的原因可能是____ 。
(1)甲醇是重要的溶剂和燃料,工业上用CO和H2在一定条件下制备CH3OH的反应为:CO(g)+2H2(g)
 CH3OH(g) ΔH<0
CH3OH(g) ΔH<0 ①T℃时,向容积为2 L的恒容密闭容器中充入1 mol CO和1.2 mol H2,一段时间后达到平衡,此时H2与CH3OH的体积分数之比为2∶5,该反应的平衡常数K=
②在一容积可变的密闭容器中充入一定物质的量的CO和H2,测得CO在不同温度下的平衡转化率与压强的关系如图所示。a、b、c三点平衡常数K(a)、K(b)、K(c)的大小关系是

(2)沥青混凝土可作为2CO(g)+O2(g)
 2CO2(g)反应的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、反应相同的时间,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
2CO2(g)反应的催化剂。如图表示在相同的恒容密闭容器、相同起始浓度、反应相同的时间,使用同质量的不同沥青混凝土(α型、β型)催化时,CO的转化率与温度的关系。
①a、b、c、d四点中表示平衡状态的是
②相同条件下,
③e点转化率出现突变的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】Ⅰ.CO和H2的混合气体俗称合成气,是一种重要的工业原料气,工业上利用天然气(主要成分为CH4)与水进行高温重整制备合成气。
(1)用甲烷与水蒸气制备合成气,每生成1mol合成气,需要供给51.5 kJ热量。该反应的热化学方程式为_____________________________________________________ 。
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),发生反应: CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g)。测得CH4和H2的物质的量浓度随时间变化如下表所示:
①该反应第一次达平衡时的平衡常数K=_______________ 。
②3min时改变的反应条件是__________________ (只填一种条件的改变即可)。
(3)已知一定压强下,温度、投料比X[n(CH4)/n(H2O)]对该反应的影响如图所示。图1中的两条曲线所示投料比的关系X1______ X2(填“=”、“>”或“<”)。

Ⅱ.(4)已知常温下HCOOH的电离常数为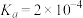 ,则HCOO—的水解反应HCOO- + H2O ⇌HCOOH + OH-的平衡常数K h =
,则HCOO—的水解反应HCOO- + H2O ⇌HCOOH + OH-的平衡常数K h =__________________ 。
(5)常温下,将a mol/L的HCOOH溶液与a/2mol/L的NaOH溶液等体积混合后,溶液中各离子浓度由大到小的顺序是______________________________ 。
(6)常温下,在a mol/L的HCOOH溶液中加入等体积的bmol/L的NaOH溶液至溶液呈中性,此时溶液中HCOOH的物质的量浓度为______________________ 。
(1)用甲烷与水蒸气制备合成气,每生成1mol合成气,需要供给51.5 kJ热量。该反应的热化学方程式为
(2)在一定温度下,向体积为2L的密闭容器中充入0.40mol CH4和0.60mol H2O(g),发生反应: CH4(g) + H2O(g) ⇌ CO(g) + 3H2(g)。测得CH4和H2的物质的量浓度随时间变化如下表所示:
| 时间/min 物质的浓度(mol/L) | 0 | 1 | 2 | 3 | 4 |
| CH4 | 0.2 | 0.13 | 0.1 | 0.1 | 0.09 |
| H2 | 0 | 0.21 | 0.3 | 0.3 | 0.33 |
①该反应第一次达平衡时的平衡常数K=
②3min时改变的反应条件是
(3)已知一定压强下,温度、投料比X[n(CH4)/n(H2O)]对该反应的影响如图所示。图1中的两条曲线所示投料比的关系X1

Ⅱ.(4)已知常温下HCOOH的电离常数为
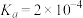 ,则HCOO—的水解反应HCOO- + H2O ⇌HCOOH + OH-的平衡常数K h =
,则HCOO—的水解反应HCOO- + H2O ⇌HCOOH + OH-的平衡常数K h =(5)常温下,将a mol/L的HCOOH溶液与a/2mol/L的NaOH溶液等体积混合后,溶液中各离子浓度由大到小的顺序是
(6)常温下,在a mol/L的HCOOH溶液中加入等体积的bmol/L的NaOH溶液至溶液呈中性,此时溶液中HCOOH的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】能源的合理开发和利用,低碳减排是人类正在努力解决的大问题。2023年2月21日,中国气候变化特使谢振华获得首届诺贝尔可持续发展特别贡献奖,以表彰他在全球生态保护中做出的贡献。
I.在 、
、 时,已知:
时,已知:
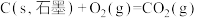
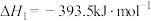 ;
;
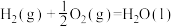
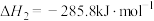 ;
;

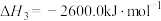
 时写出
时写出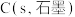 和
和 反应生成
反应生成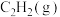 的热化学方程式:_______。
的热化学方程式:_______。
II.向密闭容器中充入一定量的 和
和 ,保持总压为
,保持总压为 ,发生反应:
,发生反应: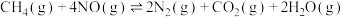
 。
。
(1)能表示此反应已经达到平衡的是_______(填字母)。
(2)当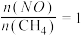 时,
时, 的平衡转化率
的平衡转化率 ;
; 时
时 平衡转化率
平衡转化率 的关系如图:
的关系如图:
_______  (填“>”或“<”)
(填“>”或“<”)
②表示当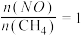 时,
时, 的平衡转化率
的平衡转化率 的关系是
的关系是_______ (填“I”或“II”),根据所选曲线写出判断依据_______ 。
③当 、
、 时,反应达平衡时,
时,反应达平衡时, 的分压为
的分压为_______ ,此温度下该反应的分压平衡常数
_______ (保留2位有效数字)(分压=总压×物质的量分数)。
I.在
 、
、 时,已知:
时,已知: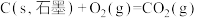
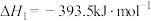 ;
;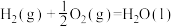
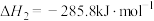 ;
;
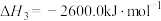
 时写出
时写出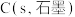 和
和 反应生成
反应生成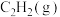 的热化学方程式:_______。
的热化学方程式:_______。II.向密闭容器中充入一定量的
 和
和 ,保持总压为
,保持总压为 ,发生反应:
,发生反应: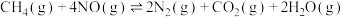
 。
。(1)能表示此反应已经达到平衡的是_______(填字母)。
| A.气体总体积保持不变 | B.混合气体的平均相对分子质量保持不变 |
C. 不再变化 不再变化 | D.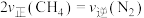 |
(2)当
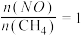 时,
时, 的平衡转化率
的平衡转化率 ;
; 时
时 平衡转化率
平衡转化率 的关系如图:
的关系如图:

 (填“>”或“<”)
(填“>”或“<”)②表示当
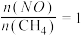 时,
时, 的平衡转化率
的平衡转化率 的关系是
的关系是③当
 、
、 时,反应达平衡时,
时,反应达平衡时, 的分压为
的分压为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】二甲醚 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:
I.

Ⅱ.
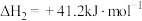
回答下列问题:
(1)已知反应: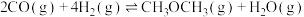
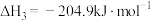 ,则
,则
______ ;
(2)在恒温恒容密闭容器中充入一定量的 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是______ 。
a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.
d.容器内气体平均相对分子质量不再变化
(3)在压强、 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性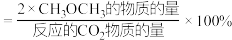 )
)

其中表示平衡时 的选择性的曲线是
的选择性的曲线是______ (填“①”或“②”);温度高于300℃时,曲线②随温度升高而升高的原因是______ 。
(4)对于反应Ⅱ的反应速率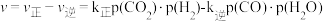 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。
a.达到平衡后,降低温度,
______ (填“增大”、“减小”或”不变”);
b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为______ 。
 是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用
是无色气体,可作为一种新型能源,同时也是重要的化工原料,采用 催化加氢可合成二甲醚,发生的反应如下:
催化加氢可合成二甲醚,发生的反应如下:I.


Ⅱ.

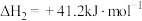
回答下列问题:
(1)已知反应:
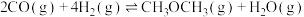
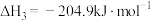 ,则
,则
(2)在恒温恒容密闭容器中充入一定量的
 和
和 ,发生上述反应。下列能说明反应I达到平衡状态的是
,发生上述反应。下列能说明反应I达到平衡状态的是a.容器内气体的密度不再发生变化
b.容器内的压强不再发生变化
c.

d.容器内气体平均相对分子质量不再变化
(3)在压强、
 和
和 的起始投料一定的条件下,发生反应I、Ⅱ,实验测得(
的起始投料一定的条件下,发生反应I、Ⅱ,实验测得( 平衡转化率和平衡时
平衡转化率和平衡时 的选择性随温度的变化如图所示。(已知:
的选择性随温度的变化如图所示。(已知: 的选择性
的选择性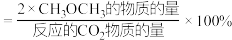 )
)
其中表示平衡时
 的选择性的曲线是
的选择性的曲线是(4)对于反应Ⅱ的反应速率
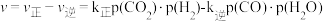 其中
其中 、
、 分别为正、逆反应速率常数,p为气体的分压(分压
分别为正、逆反应速率常数,p为气体的分压(分压 总压
总压 物质的量分数)。
物质的量分数)。a.达到平衡后,降低温度,

b.在一定温度和压强下的反应Ⅱ,按照n(CO2):n(H2)=6:7投料,当CO2转化率为50%时,用气体分压表示的平衡常数
(5)二甲醚—氧气燃料电池具有启动快,效率高等优点,若电解质溶液为NaOH溶液时,燃料电池的负极反应式为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】“低碳经济”备受关注,CO2的捕集、利用与封存成为科学家研究的重要课题。将一定量的CO2(B)和CH4(g)通入一恒容密闭容器中发生反应CO2(g)+CH4(g) 2CO(g)+2H2(g)。回答下列问题:
2CO(g)+2H2(g)。回答下列问题:
(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=-802 kJ·mol-1
CO(g)+ O2(g)=CO2(g) △H2=-283kJ·mol-1
O2(g)=CO2(g) △H2=-283kJ·mol-1
CO(g)+H2O(g)=CO2(g)+H2(g) △H3=-41 kJ·mol-1
则反应CO2(g)+CH4(g) 2CO(g) +2H2(g)的△H =
2CO(g) +2H2(g)的△H =___________ 。
(2)其他条件相同,在不同催化剂(Ⅰ、Ⅱ)作用下,反应经过相同时间时,体系中CO含量随反应温度的变化如图1所示。
①在a点与c点对应的反应条件下,反应继续进行一段时间后达到平衡,平衡常数K(a 点)________ K(c点 )( 填“>”“ <”或“=”)。
②b点CO含量低于c点的原因是____________________ 。
(3)为了探究反应:CO2(g) +CH4(g) 2CO(g)+2H2(g)的反应速率与浓度的关系,起始时向恒容密闭容器中通入CO2与CH4,使其物质的量浓度均为1.0 mol·L-1,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线(如图2):v正~c(CH4)和v逆~c(CO)。则与曲线v正~c(CH4)相对应的是图中曲线
2CO(g)+2H2(g)的反应速率与浓度的关系,起始时向恒容密闭容器中通入CO2与CH4,使其物质的量浓度均为1.0 mol·L-1,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线(如图2):v正~c(CH4)和v逆~c(CO)。则与曲线v正~c(CH4)相对应的是图中曲线____________ (填“甲”或“乙”);该反应达到平衡后,某一时刻降低温度,反应重新达到平衡,则此时曲线甲对应的平衡点可能为____________ (填字母)。

(4)将足量CO2通入饱和氨水中可得氮肥NH4HCO3。在NH4HCO3溶液中,反应NH4++HCO3-+H2O NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=_________ (已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka2=4×10-11)。
(5)科学家用氮化镓材料与铜组装成如图3所示的人工光合系统,利用该装置成功地实现了用CO2和H2O合成CH4。。氮化镓(GaN)表面发生__________ (填“氧化”或“还 原”)反应,铜电极上的电极反应式为______________________ 。
 2CO(g)+2H2(g)。回答下列问题:
2CO(g)+2H2(g)。回答下列问题:(1)已知:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H1=-802 kJ·mol-1
CO(g)+
 O2(g)=CO2(g) △H2=-283kJ·mol-1
O2(g)=CO2(g) △H2=-283kJ·mol-1CO(g)+H2O(g)=CO2(g)+H2(g) △H3=-41 kJ·mol-1
则反应CO2(g)+CH4(g)
 2CO(g) +2H2(g)的△H =
2CO(g) +2H2(g)的△H =(2)其他条件相同,在不同催化剂(Ⅰ、Ⅱ)作用下,反应经过相同时间时,体系中CO含量随反应温度的变化如图1所示。
①在a点与c点对应的反应条件下,反应继续进行一段时间后达到平衡,平衡常数K(a 点)
②b点CO含量低于c点的原因是
(3)为了探究反应:CO2(g) +CH4(g)
 2CO(g)+2H2(g)的反应速率与浓度的关系,起始时向恒容密闭容器中通入CO2与CH4,使其物质的量浓度均为1.0 mol·L-1,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线(如图2):v正~c(CH4)和v逆~c(CO)。则与曲线v正~c(CH4)相对应的是图中曲线
2CO(g)+2H2(g)的反应速率与浓度的关系,起始时向恒容密闭容器中通入CO2与CH4,使其物质的量浓度均为1.0 mol·L-1,平衡时,根据相关数据绘制出两条反应速率与浓度关系曲线(如图2):v正~c(CH4)和v逆~c(CO)。则与曲线v正~c(CH4)相对应的是图中曲线
(4)将足量CO2通入饱和氨水中可得氮肥NH4HCO3。在NH4HCO3溶液中,反应NH4++HCO3-+H2O
 NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=(5)科学家用氮化镓材料与铜组装成如图3所示的人工光合系统,利用该装置成功地实现了用CO2和H2O合成CH4。。氮化镓(GaN)表面发生
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】 的资源化可以推动经济高质量发展和生态环境质量的持续改善。
的资源化可以推动经济高质量发展和生态环境质量的持续改善。
Ⅰ. 和
和 都是主要的温室气体。已知25℃时,相关物质的燃烧热数据如下表:
都是主要的温室气体。已知25℃时,相关物质的燃烧热数据如下表:
(1)25℃时, 和
和 反应生成水煤气的热化学方程式为
反应生成水煤气的热化学方程式为_______ 。
(2)在恒温恒容装置中通入等体积的 和
和 ,发生反应
,发生反应 ,起始压强为p,
,起始压强为p, 的平衡转化率为
的平衡转化率为 。反应达到平衡时,容器内的总压强为
。反应达到平衡时,容器内的总压强为_______ (用含 、p的代数式表示,下同),该反应的平衡常数
、p的代数式表示,下同),该反应的平衡常数
_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅱ. 制取甲醇的反应为
制取甲醇的反应为
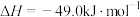 。起始投料比
。起始投料比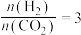 不变,研究不同温度、压强下,平衡时甲醇的物质的量分数
不变,研究不同温度、压强下,平衡时甲醇的物质的量分数 的变化规律,如图所示。其中,
的变化规律,如图所示。其中,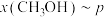 图在
图在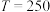 ℃下测得,
℃下测得,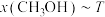 图在
图在 下测得。
下测得。

(3)图中等压过程的曲线是_______ (填“a”或“b”)。
(4)当 时,反应条件可能为
时,反应条件可能为_______ 或_______ 。
Ⅲ.运用电化学原理可以很好利用 资源
资源
(5)火星大气由96%的二氧化碳气体组成,火星探测器采用 电池供电,其反应机理如图:
电池供电,其反应机理如图:

电池中的“交换膜”应为_______ (填“阳离子”或“阴离子”)交换膜,写出 电极上的电极反应式:
电极上的电极反应式:_______ 。
 的资源化可以推动经济高质量发展和生态环境质量的持续改善。
的资源化可以推动经济高质量发展和生态环境质量的持续改善。Ⅰ.
 和
和 都是主要的温室气体。已知25℃时,相关物质的燃烧热数据如下表:
都是主要的温室气体。已知25℃时,相关物质的燃烧热数据如下表:| 物质 |  |  |  |
燃烧热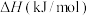 |  |  |  |
 和
和 反应生成水煤气的热化学方程式为
反应生成水煤气的热化学方程式为(2)在恒温恒容装置中通入等体积的
 和
和 ,发生反应
,发生反应 ,起始压强为p,
,起始压强为p, 的平衡转化率为
的平衡转化率为 。反应达到平衡时,容器内的总压强为
。反应达到平衡时,容器内的总压强为 、p的代数式表示,下同),该反应的平衡常数
、p的代数式表示,下同),该反应的平衡常数
Ⅱ.
 制取甲醇的反应为
制取甲醇的反应为
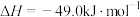 。起始投料比
。起始投料比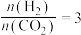 不变,研究不同温度、压强下,平衡时甲醇的物质的量分数
不变,研究不同温度、压强下,平衡时甲醇的物质的量分数 的变化规律,如图所示。其中,
的变化规律,如图所示。其中,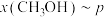 图在
图在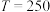 ℃下测得,
℃下测得,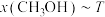 图在
图在 下测得。
下测得。
(3)图中等压过程的曲线是
(4)当
 时,反应条件可能为
时,反应条件可能为Ⅲ.运用电化学原理可以很好利用
 资源
资源(5)火星大气由96%的二氧化碳气体组成,火星探测器采用
 电池供电,其反应机理如图:
电池供电,其反应机理如图:
电池中的“交换膜”应为
 电极上的电极反应式:
电极上的电极反应式:
您最近一年使用:0次



