我国科学家研发的全球首套千吨级太阳能燃料合成项目,为实现“碳中和”目标作出了重大贡献。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。
(1)钙钛矿( )型化合物是一类可用于生产太阳能电池的功能材料,
)型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。
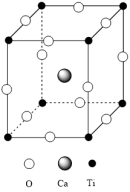
①基态 原子的核外电子排布式为
原子的核外电子排布式为_______ 。
② 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是_______ ;一个晶胞中含_______ O2-。
(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是_______ 。
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为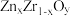 ,则y=
,则y=_______ (用含x的表达式)。
(1)钙钛矿(
 )型化合物是一类可用于生产太阳能电池的功能材料,
)型化合物是一类可用于生产太阳能电池的功能材料, 的晶胞如图所示。
的晶胞如图所示。
①基态
 原子的核外电子排布式为
原子的核外电子排布式为②
 组成元素的电负性大小顺序是
组成元素的电负性大小顺序是(2)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(3)我国科学家发明了高选择性的二氧化碳加氢合成甲醇的催化剂,其组成为
 固溶体。在
固溶体。在 中掺杂少量
中掺杂少量 后形成的催化剂,化学式可表示为
后形成的催化剂,化学式可表示为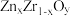 ,则y=
,则y=
更新时间:2022-10-07 20:14:16
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】雄黄(As4S4)、雌黄(As2S3)均可入药,具有解毒、杀菌、去燥湿的功效,也是中国画主要的黄色矿物质颜料。回答下列问题:
(1)基态硫原子核外电子的空间运动状态有___________ 种;其核外电子运动最高能级的电子云轮廓图的形状为___________ 。
(2)基态砷原子的价层电子的轨道表示式为___________ 。
(3)第一电离能As___________ Se(填“>”或“<”)。
(4)基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是___________ (填元素符号,下同),其价层电子排布式为___________ 。该元素处于周期表的___________ 区。
(1)基态硫原子核外电子的空间运动状态有
(2)基态砷原子的价层电子的轨道表示式为
(3)第一电离能As
(4)基态原子的N能层有1个未成对电子,M能层未成对电子数最多的元素是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】氮(N)、磷(P)、砷(As)等VA族元素化合物在研究和生产中有重要用途。如我国科研人员研究发现As2O3(或写成As4O6,俗称砒霜)对白血病有明显的治疗作用回答下列问题:
(1)As原子的核外电子排布式为_________________ ;P的第一电离能比S大的原因为_______________
(2)写出一种与CNˉ互为等电子体的粒子________ (用化学式表示);(SCN)2分子中σ键和π键个数比为___________
(3)砒霜剧毒,可用石灰消毒生成AsO33-和少量AsO43-,其中AsO33-中As的杂化方式为__________ ,AsO43-的空间构型为___________
(4)NH4+中H一N一H的键角比NH3中H 一N一H的键角大的原因是__________ ;NH3和水分子与铜离子形成的化合物中阳离子呈轴向狭长的八面体结构(如下图I),该化合物加热时首先失去水,请从原子结构角度加以分析:__________
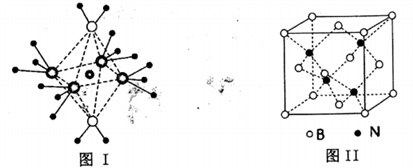
(5)BN的熔点为3000℃,密度为2.25g·cm-3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有__________ 个;若原子半径分别为rNpm和rBpm,阿伏伽德罗常数值为NA,则BN晶胞中原子的体积占晶胞体积的百分率为__________
(1)As原子的核外电子排布式为
(2)写出一种与CNˉ互为等电子体的粒子
(3)砒霜剧毒,可用石灰消毒生成AsO33-和少量AsO43-,其中AsO33-中As的杂化方式为
(4)NH4+中H一N一H的键角比NH3中H 一N一H的键角大的原因是

(5)BN的熔点为3000℃,密度为2.25g·cm-3,其晶胞结构如上图Ⅱ所示,晶体中一个B原子周围距离最近的N原子有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)铁的一种配合物的化学式为[Fe(Htrz)3](ClO4)2,其中Htrz为1,2,4-三氮唑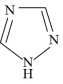 ,配合物中阴离子空间构型为
,配合物中阴离子空间构型为_______ ,阴离子的中心原子的杂化方式是_______ 。
(2)下图表示一些晶体中的某些结构,请回答下列问题:
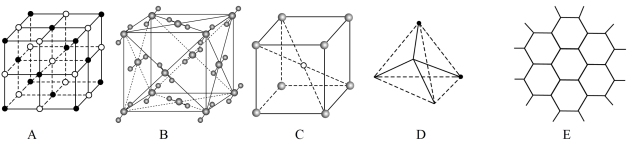
①代表金刚石的是_______ (填编号字母,下同),其中每个碳原子与_______ 个碳原子最近且距离相等,金刚石属于_______ 晶体。
②代表石墨的是_______ ,每个正六边形占有的碳原子数平均为_______ 个。
(3)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有I、II、III、IV4种类型,苏丹红I的分子结构如图1所示。
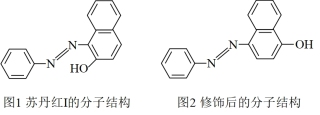
苏丹红I在水中溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会_______ (填“增大”或“减小”),原因是_______ 。
(1)铁的一种配合物的化学式为[Fe(Htrz)3](ClO4)2,其中Htrz为1,2,4-三氮唑
 ,配合物中阴离子空间构型为
,配合物中阴离子空间构型为(2)下图表示一些晶体中的某些结构,请回答下列问题:

①代表金刚石的是
②代表石墨的是
(3)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有I、II、III、IV4种类型,苏丹红I的分子结构如图1所示。

苏丹红I在水中溶解度很小,微溶于乙醇,有人把羟基取代在对位形成图2所示的结构,则其在水中的溶解度会
您最近一年使用:0次
【推荐1】含硫、氮物质的使用在为人类带来益处的同时,也给人们带来了一些困扰。利用化学原理处理含硫、氮的废气、废液等具有重要意义。二氧化氯(ClO2)可用于烟气中SO2和NO的脱除。研究发现ClO2氧化SO2和NO时涉及以下基元反应。
脱硝:
ⅰ
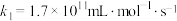
ⅱ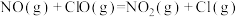
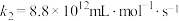
脱硫:
ⅲ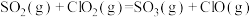

ⅳ
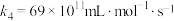
其中k为速率常数。对于基元反应: ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。_______ 。
2.脱硝反应和脱硫反应哪个活化能更大?说明理由_______ 。
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由_______ 。
CO也可以与NO反应生成无污染物: 。
。
已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数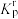 。
。
ⅱ 气体的相对分压等于其分压(单位为kPa)除以 (
(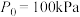 )。
)。
4.在某温度下,原料组成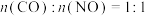 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
_______ 。
5.该反应中,如果在恒压密闭容器中,仍保持原料组成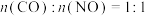 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。
脱硝:
ⅰ

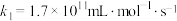
ⅱ
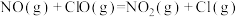
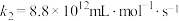
脱硫:
ⅲ
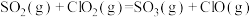

ⅳ

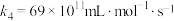
其中k为速率常数。对于基元反应:
 ,其速率方程表达式为
,其速率方程表达式为
实验测得:ClO2分别单独氧化纯SO2、纯NO以及同时氧化二者混合物的氧化率随时间(t)的变化情况如图所示。
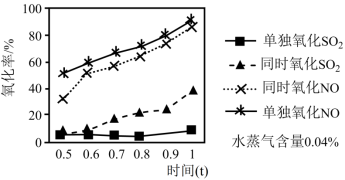
2.脱硝反应和脱硫反应哪个活化能更大?说明理由
3.请结合ⅰ、ⅲ、ⅳ的速率常数,判断NO的存在是否会影响ClO2氧化SO2的速率并说明理由
CO也可以与NO反应生成无污染物:
 。
。已知:
ⅰ 在浓度平衡常数表达式中,用相对分压代替浓度,可得到相对压力平衡常数
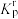 。
。ⅱ 气体的相对分压等于其分压(单位为kPa)除以
 (
(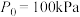 )。
)。4.在某温度下,原料组成
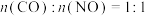 ,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
,初始总压为100 kPa的恒容容器中进行上述反应,达到平衡时CO2的分压为40 kPa,则该反应的相对压力平衡常数
5.该反应中,如果在恒压密闭容器中,仍保持原料组成
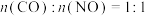 ,以下哪些条件可以判断反应达到平衡_______。
,以下哪些条件可以判断反应达到平衡_______。| A.CO的消耗速率等于NO的消耗速率 | B.容器内气体密度保持不变 |
| C.容器内平均相对分子质量保持不变 | D.CO的转化率保持不变 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】(I)氧化还原滴定是中学化学常用的定量分析方法。 是常见的氧化剂,在实验室利用
是常见的氧化剂,在实验室利用 和乙二酸(
和乙二酸( )的反应进行滴定实验。
)的反应进行滴定实验。
①配制250mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,加入少量硫酸酸化,用
 溶液滴定至乙二酸恰好全部氧化成二氧化碳,共消耗
溶液滴定至乙二酸恰好全部氧化成二氧化碳,共消耗 溶液20.00mL。
溶液20.00mL。
回答下列问题:
(1)配制样品溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、______ , 标准液装入
标准液装入______ (填“酸式”或“碱式”)滴定管。
(2) 溶液滴定乙二酸过程中发生反应的离子方程式为
溶液滴定乙二酸过程中发生反应的离子方程式为______ 。
(3)滴定终点的现象为______ 。
(4)计算此样品的纯度为______ (保留4位有效数字)。
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有______。
(II)锰元素、溴元素的化合物在高中实验中应用广泛。
(6)写出基态Mn原子的电子排布式:______ 。
(7)基态溴原子中有______ 个未成对电子;
(8)在元素周期表中,介于Mn与Br之间的主族元素有四种,请按照电负性由大到小排序:______ (用元素符号表示)。
 是常见的氧化剂,在实验室利用
是常见的氧化剂,在实验室利用 和乙二酸(
和乙二酸( )的反应进行滴定实验。
)的反应进行滴定实验。①配制250mL溶液:准确称量5.000g乙二酸样品,配成250mL溶液。
②取所配溶液25.00mL于锥形瓶中,加入少量硫酸酸化,用

 溶液滴定至乙二酸恰好全部氧化成二氧化碳,共消耗
溶液滴定至乙二酸恰好全部氧化成二氧化碳,共消耗 溶液20.00mL。
溶液20.00mL。回答下列问题:
(1)配制样品溶液,需要用到的玻璃仪器有烧杯、量筒、玻璃棒、胶头滴管、
 标准液装入
标准液装入(2)
 溶液滴定乙二酸过程中发生反应的离子方程式为
溶液滴定乙二酸过程中发生反应的离子方程式为(3)滴定终点的现象为
(4)计算此样品的纯度为
(5)在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有______。
| A.滴定终点读数时俯视读数 | B.滴定管使用前,水洗后未用标准溶液润洗 |
| C.锥形瓶水洗后未干燥 | D.滴定管尖嘴部分有气泡,滴定后消失 |
(II)锰元素、溴元素的化合物在高中实验中应用广泛。
(6)写出基态Mn原子的电子排布式:
(7)基态溴原子中有
(8)在元素周期表中,介于Mn与Br之间的主族元素有四种,请按照电负性由大到小排序:
您最近一年使用:0次
【推荐3】X、Y、Z、W为周期表中前四周期元素,它们的原子序数依次增大。X的基态原子有3个不同的能级,各能级中电子数相等;Y与X同周期,其第一电离能高于同周期与 之相邻的元素;Z的基态原子2p能级上的未成对电子数与X原子相同;W元素原子最外层只有未成对电子,其内层所有轨道全部充满,但并不是第IA族元素。
(1)请写出W原子基态的电子排布式___ 。
(2)写出X原子价电子的轨道表示式___ 。
(3)X、Y、Z三种元素第一电离能从大到小的顺序是__ (填元素符号,下同),三种元素的电负性由大到小的顺序是___ 。
(1)请写出W原子基态的电子排布式
(2)写出X原子价电子的轨道表示式
(3)X、Y、Z三种元素第一电离能从大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe-Sm-As-F-O组成的化合物。回答下列问题:
(1)元素As与N同族。预测As的氢化物分子的立体结构为__________________ ,其沸点比NH3的____________ (填“高”或“低”),其判断理由是________________________ 。
(2)Fe成为阳离子时首先失去_____________ 轨道电子。
(3)比较离子半径:F-______ O2-(填“大于”“等于”或“小于”)。
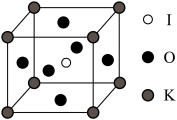
(4)晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的O个数为________ 。在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于__________ 位置,O处于_________________ 位置。
(1)元素As与N同族。预测As的氢化物分子的立体结构为
(2)Fe成为阳离子时首先失去
(3)比较离子半径:F-
(4)晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。与K紧邻的O个数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】回答下列问题:
(1)某二价金属离子有9个价电子,价电子的能级为3d。该元素位于周期表中的第四周期、第_______ 族。
(2)在氰酸钾(KOCN)的组成元素中,第一电离能最大的是________ (填元素符号、下同)、电负性最小的是__________ ;其中阴离子的空间结构是_________ ,C的杂化方式为_______ 。
(3)乙二胺能与Mg2+离子形成稳定环状离子:[Mg(C2H8N2)2]2+,其结构如图所示:
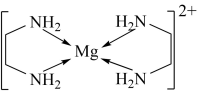
则该环状离子中镁离子的配位数为________ 。
(4)金属A的原子只有3个电子层,其第一至第四电离能如下:
则A原子的价电子排布式为________ 。
(5)用锌还原TiCl4的盐酸溶液,经后续处理可制得绿色的晶体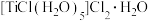 。1mol该配合物中含有
。1mol该配合物中含有 键数目为
键数目为_____ 。
(1)某二价金属离子有9个价电子,价电子的能级为3d。该元素位于周期表中的第四周期、第
(2)在氰酸钾(KOCN)的组成元素中,第一电离能最大的是
(3)乙二胺能与Mg2+离子形成稳定环状离子:[Mg(C2H8N2)2]2+,其结构如图所示:

则该环状离子中镁离子的配位数为
(4)金属A的原子只有3个电子层,其第一至第四电离能如下:
| 电离能(kJ/mol) |  | 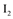 |  |  |
| A | 932 | 1821 | 15390 | 21771 |
则A原子的价电子排布式为
(5)用锌还原TiCl4的盐酸溶液,经后续处理可制得绿色的晶体
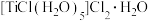 。1mol该配合物中含有
。1mol该配合物中含有 键数目为
键数目为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有五种短周期元素,它们的结构、性质等信息如下表所示:
请根据表中信息回答下列问题。
(1)A元素原子的核外电子排布式为___ 。
(2)B元素在元素周期表中的位置为___ ;离子半径:B___ (填“>”或“<”)A。
(3)C元素原子的轨道表示式为___ ,其原子核外有___ 个未成对电子,能量最高的电子排布在轨道上,该轨道呈___ 形。
(4)D元素原子的核外电子排布式为___ ,D-的结构示意图为___ 。
(5)C、E元素的第一电离能的大小关系是___ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3___ (用元素符号表示),CD3与水反应后的产物是___ (填化学式)。
| 元素 | 结构、性质等信息 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素原子的轨道表示式为
(4)D元素原子的核外电子排布式为
(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是CD3
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】含氮化合物具有非常广泛的应用.
(1)基态氮原子的电子有__________ 种空间运动状态.
(2)很多有机化合物中含有氮元素.
① 组成物质A的4种元素的电负性由大到小的顺序是_____________
②A的熔点高于B的原因是__________ .
(3)氮元素可以与短周期金属元素形成化合物. 是离子化合物,比较两种微粒的半径:
是离子化合物,比较两种微粒的半径:
_________  (填“>”、“<”或“=”).
(填“>”、“<”或“=”).
(4)氮元素可以与过渡金属元素形成化合物,其具备高硬度、高化学稳定性和优越的催化活性等性质.某三元氮化物是良好的超导材料,其晶胞结构如图所示.
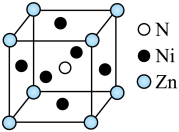
① 基态Ni原子价层电子的轨道表示式为___________ .
②与Zn原子距离最近且相等的Ni原子有___________ 个.
③ 表示阿伏加德罗常数的值.若此晶体的密度为
表示阿伏加德罗常数的值.若此晶体的密度为 ,则晶胞的边长为
,则晶胞的边长为________ nm.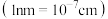
(1)基态氮原子的电子有
(2)很多有机化合物中含有氮元素.
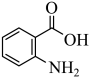
物质 | A(对氨基苯甲酸) | B(邻氨基苯甲酸) |
结构简式 |
|
|
熔点 | 188℃ | 145℃ |
作用 | 防晒剂 | 制造药物及香料 |
②A的熔点高于B的原因是
(3)氮元素可以与短周期金属元素形成化合物.
 是离子化合物,比较两种微粒的半径:
是离子化合物,比较两种微粒的半径:
 (填“>”、“<”或“=”).
(填“>”、“<”或“=”).(4)氮元素可以与过渡金属元素形成化合物,其具备高硬度、高化学稳定性和优越的催化活性等性质.某三元氮化物是良好的超导材料,其晶胞结构如图所示.

① 基态Ni原子价层电子的轨道表示式为
②与Zn原子距离最近且相等的Ni原子有
③
 表示阿伏加德罗常数的值.若此晶体的密度为
表示阿伏加德罗常数的值.若此晶体的密度为 ,则晶胞的边长为
,则晶胞的边长为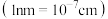
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
真题
【推荐2】[选修3—物质结构与性质( )
Ⅰ下列物质的结构或性质与氢键无关的是
Ⅱ钒(23V)是我国的丰产元素,广泛用于催化及钢铁工业。
回答下列问题:
(1)钒在元素周期表中的位置为_________ ,其价层电子排布图为______________ 。
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为____ 、 _____ 。
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是__ 对,分子的立体构型为___ ;SO3气态为单分子,该分子中S原子的杂化轨道类型为__ ;SO3的三聚体环状结构如图2所示,该结构中S原子的杂化轨道类型为__ ;该结构中S—O键长由两类,一类键长约140pm,另一类键长约为160pm,较短的键为__ (填图2中字母),该分子中含有_______ 个σ键。

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为___ ;也可以得到偏钒酸钠,其阴离子呈如图3所示的无限链状结构,则偏钒酸钠的化学式为___ 。
Ⅰ下列物质的结构或性质与氢键无关的是
| A.乙醚的沸点 | B.乙醇在水中的溶解度 |
| C.氢化镁的晶格能 | D.DNA的双螺旋结构 |
回答下列问题:
(1)钒在元素周期表中的位置为
(2) 钒的某种氧化物的晶胞结构如图1所示。晶胞中实际拥有的阴、阳离子个数分别为
(3)V2O5常用作SO2转化为SO3的催化剂。SO2分子中S原子价层电子对数是

(4)V2O5溶解在NaOH溶液中,可得到钒酸钠(Na3VO4),该盐阴离子的立体构型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】有机物中的C―H键较难断裂,活化C―H键是有机反应研究的热点之一。由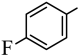 经两步反应合成
经两步反应合成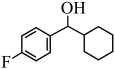 ,均需使C―H键活化,步骤如下:
,均需使C―H键活化,步骤如下:
a.s区 b.d区 c.p区 d.ds区
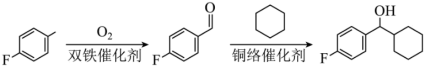
(2)
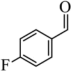 转化为
转化为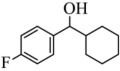 的过程中,断裂的化学键为
的过程中,断裂的化学键为(3)利用有机金属框架(MOF)构筑双铁催化剂,制备过程的核心结构变化如下。
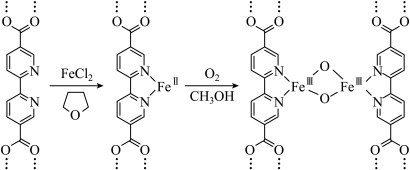
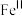 代表+2价铁,
代表+2价铁,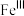 代表+3价铁。
代表+3价铁。① 的相对分子质量比
的相对分子质量比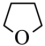 小的多,但二者的沸点却极为接近(相差1℃左右),原因有:
小的多,但二者的沸点却极为接近(相差1℃左右),原因有:
i. 的极性强于
的极性强于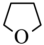 ;
;
②
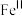 易被氧化为
易被氧化为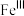 ,结合价层电子排布解释原因:
,结合价层电子排布解释原因:(4)铜铬催化剂的主要成分是CuCl、
 和
和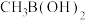 (甲基硼酸)等,
(甲基硼酸)等,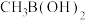 能有效抑制副产物的生成。
能有效抑制副产物的生成。①
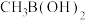 中B的杂化轨道类型是
中B的杂化轨道类型是②已知:
 和
和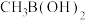 均为一元弱酸,推测
均为一元弱酸,推测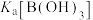
 (填“>”或“<”)。
(填“>”或“<”)。
您最近一年使用:0次