尿素 是目前使用量较大的一种化学氮肥。
是目前使用量较大的一种化学氮肥。
I.以 、
、 为原料生产尿素
为原料生产尿素 的反应历程与能量变化示意图如下:
的反应历程与能量变化示意图如下:
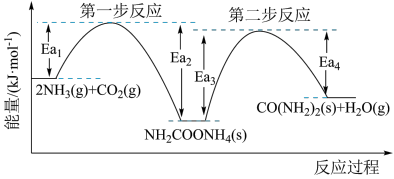
(1)图中的两步反应属于放热反应的
_______  。(用
。(用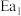 、
、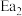 、
、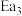 、
、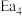 表示,下同)
表示,下同)
(2)根据图像写出以 、
、 为原料生产尿素
为原料生产尿素 的热化学方程式:
的热化学方程式:_______ 。
(3)根据上述反应历程与能量变化示意图,过程_______ (填“第一步反应”或“第二步反应”)为决速步。
II.氨基甲酸铵为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:①
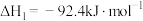
②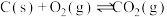
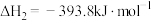
③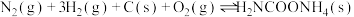
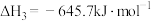
(4)请写出 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:_______ 。
 是目前使用量较大的一种化学氮肥。
是目前使用量较大的一种化学氮肥。I.以
 、
、 为原料生产尿素
为原料生产尿素 的反应历程与能量变化示意图如下:
的反应历程与能量变化示意图如下:
(1)图中的两步反应属于放热反应的

 。(用
。(用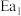 、
、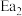 、
、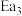 、
、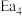 表示,下同)
表示,下同)(2)根据图像写出以
 、
、 为原料生产尿素
为原料生产尿素 的热化学方程式:
的热化学方程式:(3)根据上述反应历程与能量变化示意图,过程
II.氨基甲酸铵为尿素生产过程的中间产物,易分解。某小组对氨基甲酸铵的分解实验进行探究。
已知:①

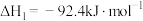
②
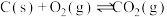
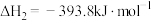
③
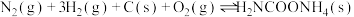
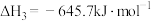
(4)请写出
 分解生成
分解生成 与
与 气体的热化学方程式:
气体的热化学方程式:
更新时间:2022-12-06 10:47:34
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】A、B、C、D、E、W均为短周期元素,原子序数依次增大。回答下列问题:
(1)E单质为双原子分子,气体E的密度3.17g.L-1(标准状况),写出用石灰水吸收E反应的离子方程式:_________________________________________ 。
(2)由A、B、D元素原子组成的化合物CH4和H2O在一定条件下发生反应:CH4(g)+H2O(g) CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如右图。
CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如右图。
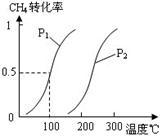
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为_______________ 。
②图中的P1___ P2(填“<”、“>”或“=”),100℃时平衡常数为________ 。
③在其它条件不变的情况下降低温度,逆反应速率将______ (填“增大”、“减小”或“不变”)。
(3)由A、C、D元素原子组成的化合物N2H4和H2O2 有广泛的用途。
①N2H4(肼)一空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的氢氧化钾溶液。电池放电时,负极的电极反应式为________________________ 。
②已知:16 g液态N2H4(肼)与足量过氧化氢反应生成氮气和水蒸气,放出320.75 KJ的热量。
H2O(l)=H2O(g) △H=+44 kJ·mol-1
2H2O2(1)=2H2O(1)+O2(g) △H= -196.4 kJ·mol-1
写出N2H4(肼)与氧气反应的热化学方程式为________________________ 。
(1)E单质为双原子分子,气体E的密度3.17g.L-1(标准状况),写出用石灰水吸收E反应的离子方程式:
(2)由A、B、D元素原子组成的化合物CH4和H2O在一定条件下发生反应:CH4(g)+H2O(g)
 CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如右图。
CO(g)+3H2(g) 。将1.0mol CH4和2.0mol H2O(g)通入反应室(容积为100L),达到平衡时,CH4的转化率与温度、压强的关系如右图。
①已知100℃时达到平衡所需的时间为5min,则用H2表示的平均反应速率为
②图中的P1
③在其它条件不变的情况下降低温度,逆反应速率将
(3)由A、C、D元素原子组成的化合物N2H4和H2O2 有广泛的用途。
①N2H4(肼)一空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的氢氧化钾溶液。电池放电时,负极的电极反应式为
②已知:16 g液态N2H4(肼)与足量过氧化氢反应生成氮气和水蒸气,放出320.75 KJ的热量。
H2O(l)=H2O(g) △H=+44 kJ·mol-1
2H2O2(1)=2H2O(1)+O2(g) △H= -196.4 kJ·mol-1
写出N2H4(肼)与氧气反应的热化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)在25℃、1.01×105Pa时,16g S粉在足量的氧气中充分燃烧生成二氧化硫气体,放出148.5kJ的热量,则S的燃烧热的热化学方程式为:___ 。
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:___ 。
(3)已知如图所示的可逆反应:
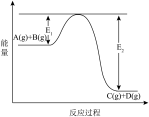
①A(g)+B(g) 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q___ 0(填“>”、“<”或“=”)
②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1___ ,ΔH的变化是:ΔH___ (填“增大”“减小”“不变”)。
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=___ kJ/mol。
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1___ △H2
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=___ kJ/mol;
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为___ (填序号)
(2)1L1mol/L稀盐酸跟1L1mol/LNaOH溶液起中和反应放出57.3kJ热量,其热化学方程式为:
(3)已知如图所示的可逆反应:

①A(g)+B(g)
 2C(g) +D(g);ΔH=QkJ/mol则Q
2C(g) +D(g);ΔH=QkJ/mol则Q②反应体系中加入催化剂,反应速率增大,则E1的变化是:E1
(4)发射卫星用N2H4作燃料,NO2作氧化剂,两者反应生成N2和水蒸气,
已知:N2(g)+2O2(g)=2NO2(g) △H1=+67.7kJ/mol
N2H4(g)+O2(g)=N2(g)+2H2O(g) △H2=-534kJ/mol
则1mol气体肼和NO2完全反应时的反应热△H=
(5)已知反应A放出热量Q1kJ,焓变为△H1,反应B放出热量Q2kJ,焓变为△H2,若Q1>Q2,则△H1
(6)1molC与1molH2O(g)反应生成1molCO(g)和1molH2(g),需吸收131.5kJ的热量,该反应的反应热为△H=
(7)反应A+3B=2C+2D在四种不同情况下的反应速率分别为:
①v(A)=0.15mol/(L・s) ②v(B)=0.6mol/(L・s)
③v(C)=0.4mol/(L・s) ④v(D)=0.45mol(L・s)
则该反应进行最快的为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲醇既是重要的化工原料,又可作为燃料。利用合成气(主要成分为CO、CO2和H2 )在催化剂作用下合成甲醇,发生的主要反应如下:
①CO(g)+2H2(g) CH3OH(g) △H1
CH3OH(g) △H1
②CO2(g)+3H2(g) CH 3OH(g)+H2O(g) △H2
CH 3OH(g)+H2O(g) △H2
③CO2(g)+H2(g) CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3
已知反应①中相关的化学键键能数据如下:
回答下列问题:
(1)CH3OH中氧在周期表中位于___ ,属于___ 区元素,与其同周期相邻两种元素原子的第一电离能由大到小的顺序为___ (用元素符号表示),其原因是___ 。
(2)写出CH3OH的结构式___ ;反应①的热化学方程式(热量用具体数值表示)___ 。
(3)当△H2=-58kJ mol-1,则△H3=__ kJ mol-1。
(4)CO和H2的混合气体又称水煤气,可由水和煤在一定条件下产生,写出该反应的化学方程式___ 。
①CO(g)+2H2(g)
 CH3OH(g) △H1
CH3OH(g) △H1②CO2(g)+3H2(g)
 CH 3OH(g)+H2O(g) △H2
CH 3OH(g)+H2O(g) △H2③CO2(g)+H2(g)
 CO(g)+H2O(g) △H3
CO(g)+H2O(g) △H3已知反应①中相关的化学键键能数据如下:
| 化学键 | H—H | C—O |  | H—O | C—H |
| E/(kJ mol-1) | 436 | 343 | 1076 | 465 | 413 |
回答下列问题:
(1)CH3OH中氧在周期表中位于
(2)写出CH3OH的结构式
(3)当△H2=-58kJ mol-1,则△H3=
(4)CO和H2的混合气体又称水煤气,可由水和煤在一定条件下产生,写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)以下反应:①木炭与水制备水煤气,②氯酸钾分解,③炸药爆炸,④酸与碱的中和反应,⑤生石灰与水作用制熟石灰,⑥Ba(OH)2•H2O 与 NH4Cl ,⑦浓硫酸溶于水, 属于放热反应__________ .(填序号)
(2)Mg-Al-NaOH 电池中的负极反应:___________ .
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为___________ ,当线路中转移 0.2mol 电 子时,则被腐蚀铜的质量为___________ g.
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出___________ 的热量。
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是___________ ,存在非极性键的是___________ 。
(2)Mg-Al-NaOH 电池中的负极反应:
(3)FeCl3 溶液常用于腐蚀印刷电路铜板,发生 2FeCl3+Cu=2FeCl2+CuCl2,若将 此反应设计成原电池,则负极所用电极材料为
(4)已知拆开 1mol H-H 键、1mol N≡N、1mol N-H 键分别需要吸收的能量为 436kJ、946k J、391k J.则由 N2 和 H2 反应生成 1mol NH3 需要放出
(5)用序号回答:①HCl ②NaOH ③Cl2 ④H2O ⑤NH4Cl ⑥P4 ⑦NH3•H2O ⑧Na2O2 ⑨HClO⑩CaO⑪HF⑫MgCl2
属于共价化合物的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
I.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出_______ kJ热量。
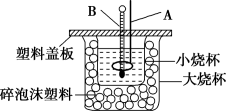
(2)如图装置中仪器A的名称_______ ,作用是_______ ;仪器B的名称_______ ,作用是_______ ;碎泡沫塑料的作用是_______ 。若通过实验测定中和热的ΔH,其结果常常大于-57.3kJ/mol,其原因可能是_______ 。
II.已知某反应A(g)+B(g)⇌C(g)+D(g),反应过程中的能量变化如图所示。
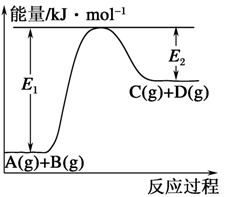
(3)该反应是_______ 反应(填“吸热”或“放热”),该反应的ΔH=_______ kJ·mol-1(用含E1、E2的代数式表示),1mol气体A和1mol气体B具有的总能量比1mol气体C和1mol气体D具有的总能量_______ (填“高”、“低”或“高低不一定”)。
I.已知H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3kJ/mol。回答有关中和反应的问题。
(1)用0.1molBa(OH)2配成稀溶液与足量稀硝酸反应,能放出
(2)如图装置中仪器A的名称

II.已知某反应A(g)+B(g)⇌C(g)+D(g),反应过程中的能量变化如图所示。

(3)该反应是
您最近一年使用:0次
【推荐3】生产生活中的化学反应都伴随着能量的变化,请根据有关知识回答下列问题:
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用_______ (填“放热”或“吸热”)的化学变化或物理变化。
(2)“即热饭盒”给人们生活带来方便,它可利用下面_______ (填字母)反应释放的热量加热食物。
A.生石灰和水 B.浓硫酸和水
(3)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是 和
和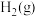 反应生成
反应生成 过程中能量变化示意图。请写出
过程中能量变化示意图。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:_______ ;

(4)温度在150℃以上时, 便迅速分解为
便迅速分解为 和
和 ,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
a.
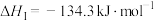
b.
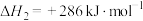
则反应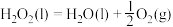 的
的
_______ 。
(1)冷敷袋在日常生活中有降温、保鲜和镇痛等用途。制作冷敷袋可以利用
(2)“即热饭盒”给人们生活带来方便,它可利用下面
A.生石灰和水 B.浓硫酸和水
(3)氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用,下图是
 和
和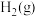 反应生成
反应生成 过程中能量变化示意图。请写出
过程中能量变化示意图。请写出 和
和 反应的热化学方程式:
反应的热化学方程式:
(4)温度在150℃以上时,
 便迅速分解为
便迅速分解为 和
和 ,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:
,发射火箭时用过氧化氢作强氧化剂就是利用这个原理,已知:a.

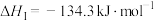
b.

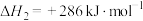
则反应
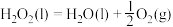 的
的
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】天然气中伴随有H2S等合硫化合物,脱硫方法有多种:
(1)一种湿法脱硫是用碳酸钾溶液吸收其中的H2S,同时生成两种酸式盐,该反应的化学方程为___________ 。
(2)一种于法脱硫,其涉及反应:H2(g)+CO(g)+SO2(g) H2O(g)+CO2(g)+S(s)
H2O(g)+CO2(g)+S(s) ,高脱硫率可采取的措施是
,高脱硫率可采取的措施是_____________ 。
a.高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出硫
(3)用脱硫剂ZDE—01的海绵铁法脱硫,可实现常温脱硫
①脱硫:Fe2O3·H2O(s)+3H2S(g)=Fe2S3·H2O(s)+3H2O(g)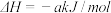
②再生:2Fe2S3·H2O(s)+3O2(g)=2Fe2O3·H2O(s)+6S(s)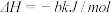
则2H2S(g)+O2(g)=2H2O(g)+2S(s) =
=_______ (用a、b表示)
(4)一种改进的克劳斯法脱硫的工艺,化学反应如下:
H3S+1.5O2=H2O+SO2 SO2+0.5O2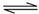 SO3
SO3
SO3(g)+H2O(g)=H2SO4(g) H2SO4(g)+0.17H2O(g) H2SO4(aq)
H2SO4(aq)
该法最终得到的硫酸溶液的质量分数为________ 。
(1)一种湿法脱硫是用碳酸钾溶液吸收其中的H2S,同时生成两种酸式盐,该反应的化学方程为
(2)一种于法脱硫,其涉及反应:H2(g)+CO(g)+SO2(g)
 H2O(g)+CO2(g)+S(s)
H2O(g)+CO2(g)+S(s) ,高脱硫率可采取的措施是
,高脱硫率可采取的措施是a.高压 b.加入催化剂 c.减少CO2的浓度 d.增加CO的浓度 e.分离出硫
(3)用脱硫剂ZDE—01的海绵铁法脱硫,可实现常温脱硫
①脱硫:Fe2O3·H2O(s)+3H2S(g)=Fe2S3·H2O(s)+3H2O(g)
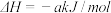
②再生:2Fe2S3·H2O(s)+3O2(g)=2Fe2O3·H2O(s)+6S(s)
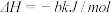
则2H2S(g)+O2(g)=2H2O(g)+2S(s)
 =
=(4)一种改进的克劳斯法脱硫的工艺,化学反应如下:
H3S+1.5O2=H2O+SO2 SO2+0.5O2
 SO3
SO3SO3(g)+H2O(g)=H2SO4(g) H2SO4(g)+0.17H2O(g)
 H2SO4(aq)
H2SO4(aq)该法最终得到的硫酸溶液的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)Ⅰ.已知:①CO燃烧热为283.0kJ·mol-l,②N2(g)+O2(g) =2NO(g)△H=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应,能消除污染,写出该反应的热化学方程式___________ 。
Ⅱ.水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(2)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192.根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO___________ H2(填“大于”或“小于”)。
(3)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为___________(填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
(1)Ⅰ.已知:①CO燃烧热为283.0kJ·mol-l,②N2(g)+O2(g) =2NO(g)△H=+180.5kJ·mol-1,汽车尾气中的NO(g)和CO(g)在一定温度和催化剂条件下可发生反应,能消除污染,写出该反应的热化学方程式
Ⅱ.水煤气变换[CO(g)+H2O(g)=CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(2)Shibata曾做过下列实验:①使纯H2缓慢地通过处于721 ℃下的过量氧化钴CoO(s),氧化钴部分被还原为金属钴(Co),平衡后气体中H2的物质的量分数为0.0250。
②在同一温度下用CO还原CoO(s),平衡后气体中CO的物质的量分数为0.0192.根据上述实验结果判断,还原CoO(s)为Co(s)的倾向是CO
(3)721 ℃时,在密闭容器中将等物质的量的CO(g)和H2O(g)混合,采用适当的催化剂进行反应,则平衡时体系中H2的物质的量分数为___________(填标号)。
A.<0.25 B.0.25 C.0.25~0.50 D.0.50 E.>0.50
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】请回答以下问题:
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.

Ⅱ.
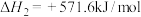
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式__________ 。
(2)在 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(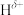 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(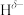 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是__________ 。
(3)100mLpH=10.00的 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为__________ mol。
(4)已知:25℃时碳酸的 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式__________ 。
(5)据文献报道, 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是__________ 。
(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是__________ 。
(7)乙醇的挥发性比水的强,原因是__________ 。
(1)在载人航天器中,通过以下两个反应实现氧的循环:
Ⅰ.


Ⅱ.

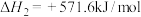
写出甲烷与氧气反应生成二氧化碳和液态水的热化学方程式
(2)在
 分子中,与N原子相连的H呈正电性(
分子中,与N原子相连的H呈正电性(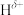 ),与B原子相连的H呈负电性(
),与B原子相连的H呈负电性(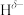 ),这三种元素电负性从大到小的顺序是
),这三种元素电负性从大到小的顺序是(3)100mLpH=10.00的
 溶液中水电离出
溶液中水电离出 的物质的量为
的物质的量为(4)已知:25℃时碳酸的
 、
、 ,次氯酸的
,次氯酸的 。写出在NaClO溶液中通入
。写出在NaClO溶液中通入 气体的离子方程式
气体的离子方程式(5)据文献报道,
 可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是
可以在碱性水溶液中电解生成甲烷,生成甲烷的电极反应式是(6)锗(Ge)与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(7)乙醇的挥发性比水的强,原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】(1)如图为某实验小组依据氧化还原反应(用离子方程式表示)________ 设计的原电池装置。反应前,电极质量相等,一段时间后,两电极质量相差12 g,导线中通过________ mol电子。
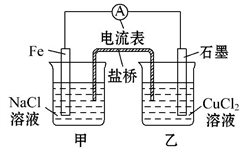
(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:__________ 。
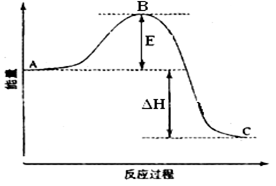
(3)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点_________ (填“升高”还是“降低”),△H______ (填“变大”、“变小”或“不变”)。

(2)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H= - 24.8kJ/mol
3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H= - 47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H= +640.5kJ/mol
写出CO气体还原FeO固体得到Fe 固体和CO2气体的热化学反应方程式:
(3)2SO2(g)+O2(g) =2SO3(g)反应过程的能量变化如图所示。该反应通常用V2O5作催化剂,加V2O5会使图中B点

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
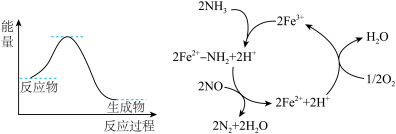
【推荐2】氮的氧化物是造成大气污染的主要物质。研究氮氧化物的反应机理对于消除环境污染有重要意义。
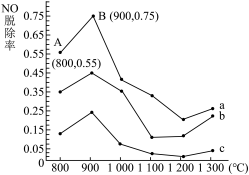
(1)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示。
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示。
①n(NH3)∶n(NO)的物质的量之比为1:3时,对应的是曲线______ (填“a”“b”或“c”)。
②由图可知,无论以何种比例反应,在温度超过900 ℃时NO脱除率都会骤然下降的原因可能是______ 。 2NO2(g)分两步进行,其反应过程能量变化示意图如图。
2NO2(g)分两步进行,其反应过程能量变化示意图如图。
①化学反应速率由速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是______ (填“I”或“II”)。
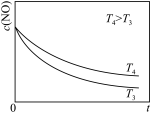
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度______ (填“T3”或“T4”)下消耗的时间较长,试结合反应过程能量图(图)分析其原因:___________ 。________ 。
(1)催化氧化法去除NO是在一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO
 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示。
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4:1、3:1、1:3时,得到NO脱除率曲线如图所示。①n(NH3)∶n(NO)的物质的量之比为1:3时,对应的是曲线
②由图可知,无论以何种比例反应,在温度超过900 ℃时NO脱除率都会骤然下降的原因可能是
 2NO2(g)分两步进行,其反应过程能量变化示意图如图。
2NO2(g)分两步进行,其反应过程能量变化示意图如图。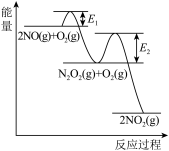
①化学反应速率由速率较慢的反应步骤决定。以上反应决定NO氧化反应速率的步骤是
②在恒容的密闭容器中充入一定量的NO和O2气体,保持其他条件不变,控制反应温度分别为T3和T4(T4>T3),测得c(NO)随t(时间)的变化曲线如图。转化相同量的NO,在温度
您最近一年使用:0次
【推荐3】回答下列问题
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:
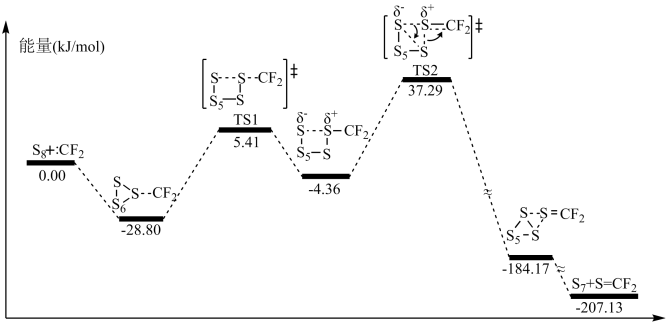
①由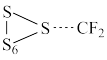 生成
生成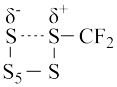 的活化能为
的活化能为__________________ ;
②决定反应速率的基元反应的活化能为______________________ 。
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g) 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
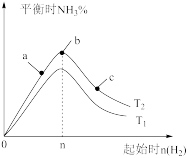
①图象中T2和T1的关系是:T2___________ T1(填“高于”、“低于”、 “等于”或“无法确定”)。
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是_______________ (填字母)。
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=__________________ 。
(1)二氟卡宾(:CF2)作为一种活性中间体,一直受到有机氟化学研究工作者的高度关注。硫单质与二氟卡宾可以形成S=CF2,反应历程如图所示:

①由
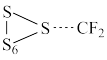 生成
生成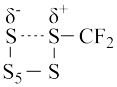 的活化能为
的活化能为②决定反应速率的基元反应的活化能为
(2)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对N2(g)+3H2(g)
 2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量)
2NH3(g)反应的影响。实验结果如图所示:(图中T表示温度,n表示物质的量) 
①图象中T2和T1的关系是:T2
②比较在a、b、c三点所处的平衡状态中,反应物N 2的转化率最高的是
③在起始体系中n(N2):n(H2)= 1:3时,反应后氨的百分含量最大;若容器容积为1 L, n=3 mol反应达到平衡时H2的转化率为60%,则此条件下(T2),反应的平衡常数K=
您最近一年使用:0次



