全球大气 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
(1)已知25℃时,大气中的 溶于水存在以下过程:
溶于水存在以下过程:
①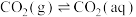
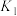
②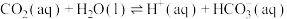

过程①的混合平衡常数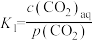 ,其中
,其中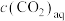 表示溶液中的
表示溶液中的 浓度,
浓度,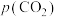 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
______ (填“增大”或“减小”);当大气压强为akPa,溶液中的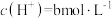 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为______ 。
(2)由 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应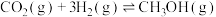
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
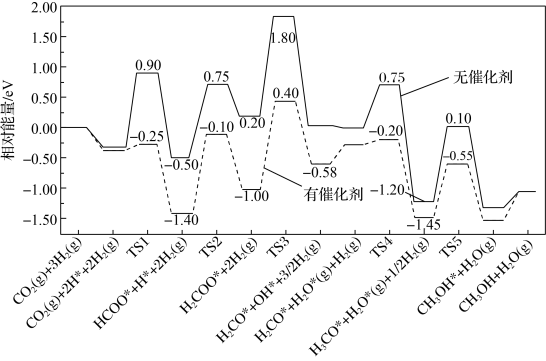
该反应历程中决速步骤的化学方程式为______ ,有催化剂时决速步骤的活化能为______ eV。
(3)一种脱除和利用工厂废气中 方法的示意图如下:
方法的示意图如下:
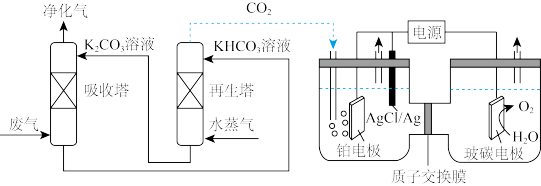
①某温度下,吸收塔中 溶液吸收一定量的
溶液吸收一定量的 后,溶液的
后,溶液的 ,则
,则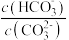 =
=______ (该温度下 的
的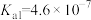 ,
,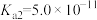 );
);
②再生塔中产生 的离子方程式为
的离子方程式为______ 。
③利用电化学原理将 同时转化为多种燃料(
同时转化为多种燃料( 、
、 、
、 及CO),将
及CO),将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为______ 。若铂电极上只生成6.4g ,则正极区产生气体标准状况下的体积为
,则正极区产生气体标准状况下的体积为______ L。
 浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:
浓度升高对人类生产、生活产生影响,碳及其化合物的资源化利用成为研究热点。回答下列问题:(1)已知25℃时,大气中的
 溶于水存在以下过程:
溶于水存在以下过程:①
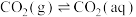
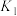
②
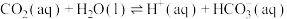

过程①的混合平衡常数
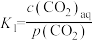 ,其中
,其中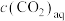 表示溶液中的
表示溶液中的 浓度,
浓度,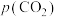 表示大气中
表示大气中 的分压(单位:kPa)。温度升高,
的分压(单位:kPa)。温度升高,
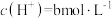 (忽略
(忽略 和水的电离)时,大气中
和水的电离)时,大气中 的体积分数为
的体积分数为(2)由
 转化制甲醇具有重要的经济效益。反应
转化制甲醇具有重要的经济效益。反应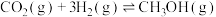
 ,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
,在有、无催化剂条件下的反应机理和相对能量的变化如图所示(吸附在催化剂表面上的粒子用*标注,TS为过渡态)。
该反应历程中决速步骤的化学方程式为
(3)一种脱除和利用工厂废气中
 方法的示意图如下:
方法的示意图如下:
①某温度下,吸收塔中
 溶液吸收一定量的
溶液吸收一定量的 后,溶液的
后,溶液的 ,则
,则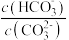 =
= 的
的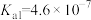 ,
,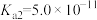 );
);②再生塔中产生
 的离子方程式为
的离子方程式为③利用电化学原理将
 同时转化为多种燃料(
同时转化为多种燃料( 、
、 、
、 及CO),将
及CO),将 电催化还原为
电催化还原为 ,阴极反应式为
,阴极反应式为 ,则正极区产生气体标准状况下的体积为
,则正极区产生气体标准状况下的体积为
更新时间:2022/12/08 10:39:39
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】控制和治理CO2是解决温室效应及能源问题的有效途径。
已知:H2(g)和CH3OH(l)的标准燃烧热分别为△H=akJ•mol-1和△H=bkJ•mol-1
(1)研究表明,在Cu/ZnO催化剂存在下,CO2和H2反应生成液态甲醇和液态水,该反应的热化学方程式为_________ 。
(2)已知:2CO2(g)+ 6H2(g)⇌C2H4(g)+4H2O(g)△H,在两个固定容积均为1L的密闭容器中以不同的氢碳比[ ]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。
]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。_______________ (填“>”“<”或“=”)2.0;
②若起始加入的CO2、H2的物质的量分别为1mol和2mol,计算P点时的化学平衡常数K=____________ 。
③比较P点和Q点的化学平衡常数:KP_________ KQ(填“>”“<”或“=”),理由是__________________ 。
④一定温度下在体积为VL的容器中进行该反应,下列一定能说明反应达到平衡状态的是_______________ (填字母序号)。
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(CO2)=v逆(C2H4)
D.容器内混合气体的密度不再变化
(3)以CH3OH作燃料,以NaOH溶液作电解质溶液形成的燃料电池,电池工作时,溶液中的阴离子向电池的哪一极定向移动(填写电极名称)________ ;写出负极的电极反应式_________ .
(4)常温下,若在 硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的 时,
时,
____  。
。
已知:H2(g)和CH3OH(l)的标准燃烧热分别为△H=akJ•mol-1和△H=bkJ•mol-1
(1)研究表明,在Cu/ZnO催化剂存在下,CO2和H2反应生成液态甲醇和液态水,该反应的热化学方程式为
(2)已知:2CO2(g)+ 6H2(g)⇌C2H4(g)+4H2O(g)△H,在两个固定容积均为1L的密闭容器中以不同的氢碳比[
 ]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。
]充入H2和CO2,CO2的平衡转化率a(CO2)与温度的关系如图所示。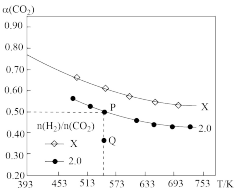
②若起始加入的CO2、H2的物质的量分别为1mol和2mol,计算P点时的化学平衡常数K=
③比较P点和Q点的化学平衡常数:KP
④一定温度下在体积为VL的容器中进行该反应,下列一定能说明反应达到平衡状态的是
A.混合气体的平均相对分子质量不再变化
B.容器内气体总压强不再变化
C.2v正(CO2)=v逆(C2H4)
D.容器内混合气体的密度不再变化
(3)以CH3OH作燃料,以NaOH溶液作电解质溶液形成的燃料电池,电池工作时,溶液中的阴离子向电池的哪一极定向移动(填写电极名称)
(4)常温下,若在
 硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的
硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的 时,
时,
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮及其化合物在工业生产和国防建设中有广泛应用。回答下列问题:
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程:______ 。
(2)联氨(N2H4)是一种还原剂,能与氧气反应生成氮气和水蒸气。试结合下表数据,写出在该反应的热化学方程式:____________________________ 。
(3)氨的催化氧化用于工业生产硝酸。该反应可设计成新型电池,试写出碱性环境下,该电池的负极电极反应式:__________________________ 。
(4)常温下用氨水吸收CO2可得(NH4)2CO3溶液,在(NH4)2CO3溶液中,c(OH-)_________ c(H+)(填“>”“<”或“=”);反应NH +CO
+CO +H2O
+H2O NH3·H2O+HCO
NH3·H2O+HCO 的平衡常数K=
的平衡常数K=______ (已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数Ka1=4×10-7,Ka2=4×10-11)
(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2 N2O4其相关图象如下。
N2O4其相关图象如下。

①0~3s时v(NO2)增大的原因是_________ 。
②5s时NO2转化率为__________ 。
(1)氮气性质稳定,可用作保护气。请用电子式表示氮气的形成过程:
(2)联氨(N2H4)是一种还原剂,能与氧气反应生成氮气和水蒸气。试结合下表数据,写出在该反应的热化学方程式:
| 化学键 | N—H | N—N | N=N | N≡N | O=O | O—H |
| 键能(kJ/mol) | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
(4)常温下用氨水吸收CO2可得(NH4)2CO3溶液,在(NH4)2CO3溶液中,c(OH-)
 +CO
+CO +H2O
+H2O NH3·H2O+HCO
NH3·H2O+HCO 的平衡常数K=
的平衡常数K=(5)将某浓度的NO2气体充入一恒容绝热容器中,发生反应2NO2
 N2O4其相关图象如下。
N2O4其相关图象如下。
①0~3s时v(NO2)增大的原因是
②5s时NO2转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】工业上利用N2和H2可以合成氨气,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产。请回答下列有关问题:
(1)已知:N2(g)+O2(g) 2NO(g) ΔH=akJ·mol-1
2NO(g) ΔH=akJ·mol-1
N2(g)+3H2(g) 2NH3(g) ΔH=bkJ·mol-1
2NH3(g) ΔH=bkJ·mol-1
2H2(g)+O2(g) 2H2O(g) ΔH=ckJ·mol-1
2H2O(g) ΔH=ckJ·mol-1
写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式____ 。
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+O2(g) 2NO(g) ΔH<0。
2NO(g) ΔH<0。
其化学平衡常数K与温度t的关系如表:
完成下列问题:
①比较K1、K2的大小:K1____ K2(填“>”“=”或“<”);
②在恒温恒容条件下判断该反应达到化学平衡状态的依据是____ (填序号)。
A.2v正(N2)=v逆(H2) B.2v正(H2)=3v逆(NH3)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)工业上生产尿素的化学方程式为2NH3(g)+CO2(g) CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,10s反应达到平衡,此时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。10s内v(NH3)为
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,10s反应达到平衡,此时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。10s内v(NH3)为____ 。若此时保持T℃和平衡时容器的压强不变,再向体积可变的容器中充入3molNH3,则此时反应的v正____ v逆(填“>”“<”或“=”)。再次平衡后,平衡常数为____ 。
(1)已知:N2(g)+O2(g)
 2NO(g) ΔH=akJ·mol-1
2NO(g) ΔH=akJ·mol-1N2(g)+3H2(g)
 2NH3(g) ΔH=bkJ·mol-1
2NH3(g) ΔH=bkJ·mol-12H2(g)+O2(g)
 2H2O(g) ΔH=ckJ·mol-1
2H2O(g) ΔH=ckJ·mol-1写出氨气经催化氧化完全生成一氧化氮和水蒸气的热化学方程式
(2)在一定体积的密闭容器中,进行如下化学反应:N2(g)+O2(g)
 2NO(g) ΔH<0。
2NO(g) ΔH<0。其化学平衡常数K与温度t的关系如表:
| t/K | 298 | 398 | 498 | …… |
| K/(mol·L-1) | 4.1×106 | K1 | K2 | …… |
①比较K1、K2的大小:K1
②在恒温恒容条件下判断该反应达到化学平衡状态的依据是
A.2v正(N2)=v逆(H2) B.2v正(H2)=3v逆(NH3)
C.容器内压强保持不变 D.混合气体的密度保持不变
(3)工业上生产尿素的化学方程式为2NH3(g)+CO2(g)
 CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,10s反应达到平衡,此时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。10s内v(NH3)为
CO(NH2)2(s)+H2O(l)。在T℃,体积为4L的密闭容器中,通入6molNH3和3molCO2,10s反应达到平衡,此时,c(NH3)=0.5mol·L-1,c(CO2)=0.25mol·L-1。10s内v(NH3)为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】2-丁烯有顺反异构,是有机合成的重要原料,可由正丁烷催化脱氢得到2-丁烯,其转化关系如下:
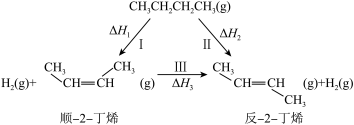
若用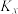 表示反应的体积分数平衡常数(即浓度平衡常数中的浓度用体积分数代替)。上述三个反应的体积分数平衡常数的对数
表示反应的体积分数平衡常数(即浓度平衡常数中的浓度用体积分数代替)。上述三个反应的体积分数平衡常数的对数 与温度的变化关系如图所示:
与温度的变化关系如图所示:

回答下列问题:
(1)
______ (填“>”或“<”)0,理由是________________________ 。
(2)图中b=______ (用含a、c的代数式表示)。
(3)在 K时,向某密闭容器中加入2mol正丁烷,测得生成的顺-2-丁烯为0.15mol。
K时,向某密闭容器中加入2mol正丁烷,测得生成的顺-2-丁烯为0.15mol。
①平衡体系中正丁烷为______ mol, 与顺-2-丁烯的浓度比为
与顺-2-丁烯的浓度比为______ 。
②反应I的体积分数平衡常数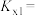
______ (列出计算式)。
③保持恒温恒压下,再向该容器中充入一定量惰性气体He,则反-2-丁烯的体积分数将会______ (填“增大”“减小”或“不变”),理由是________________________ 。

若用
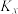 表示反应的体积分数平衡常数(即浓度平衡常数中的浓度用体积分数代替)。上述三个反应的体积分数平衡常数的对数
表示反应的体积分数平衡常数(即浓度平衡常数中的浓度用体积分数代替)。上述三个反应的体积分数平衡常数的对数 与温度的变化关系如图所示:
与温度的变化关系如图所示:
回答下列问题:
(1)

(2)图中b=
(3)在
 K时,向某密闭容器中加入2mol正丁烷,测得生成的顺-2-丁烯为0.15mol。
K时,向某密闭容器中加入2mol正丁烷,测得生成的顺-2-丁烯为0.15mol。①平衡体系中正丁烷为
 与顺-2-丁烯的浓度比为
与顺-2-丁烯的浓度比为②反应I的体积分数平衡常数
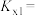
③保持恒温恒压下,再向该容器中充入一定量惰性气体He,则反-2-丁烯的体积分数将会
您最近一年使用:0次
【推荐2】有效利用 对实现“碳中和”意义重大。请回答下列问题:
对实现“碳中和”意义重大。请回答下列问题:
(1) 加氢制甲醇的总反应为:
加氢制甲醇的总反应为:
 ,该总反应可认为通过如下两个反应步骤来实现,能量变化如图所示。
,该总反应可认为通过如下两个反应步骤来实现,能量变化如图所示。
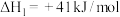
Ⅱ.
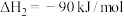
则 =
=___________ kJ/mol,反应步骤___________ (填“I”或“Ⅱ”)是总反应的决速步。
(2)一定温度下,在体积为1L的恒容密闭容器中,充入1mol (g)和3mol
(g)和3mol  (g),发生反应:
(g),发生反应: 。测得
。测得 (g)和
(g)和 (g)的浓度随时间变化如图所示。
(g)的浓度随时间变化如图所示。___________ (选填字母编号)。
A.容器内气体密度不变 B.
C.容器内气体压强不变 D.
②从理论上分析,为了使 尽可能多地转化为甲醇,应选择的条件是
尽可能多地转化为甲醇,应选择的条件是___________ (选填字母编号)。
A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
③3min~9min时间内, 的化学反应速率
的化学反应速率
___________  (结果保留到小数点后3位)。该温度下,化学平衡常数K=
(结果保留到小数点后3位)。该温度下,化学平衡常数K=___________ (结果保留到小数点后1位)。
(3)使用惰性电极电解 制取甲醇的反应装置如图所示:
制取甲醇的反应装置如图所示:___________ (填“正”或“负”)极。
②生成甲醇的电极反应式为:___________ 。
 对实现“碳中和”意义重大。请回答下列问题:
对实现“碳中和”意义重大。请回答下列问题:(1)
 加氢制甲醇的总反应为:
加氢制甲醇的总反应为:
 ,该总反应可认为通过如下两个反应步骤来实现,能量变化如图所示。
,该总反应可认为通过如下两个反应步骤来实现,能量变化如图所示。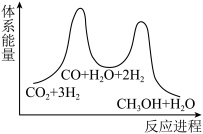

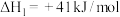
Ⅱ.

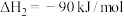
则
 =
=(2)一定温度下,在体积为1L的恒容密闭容器中,充入1mol
 (g)和3mol
(g)和3mol  (g),发生反应:
(g),发生反应: 。测得
。测得 (g)和
(g)和 (g)的浓度随时间变化如图所示。
(g)的浓度随时间变化如图所示。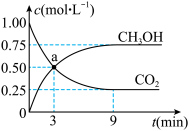
A.容器内气体密度不变 B.

C.容器内气体压强不变 D.
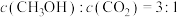
②从理论上分析,为了使
 尽可能多地转化为甲醇,应选择的条件是
尽可能多地转化为甲醇,应选择的条件是A.高温、高压 B.高温、低压 C.低温、低压 D.低温、高压
③3min~9min时间内,
 的化学反应速率
的化学反应速率
 (结果保留到小数点后3位)。该温度下,化学平衡常数K=
(结果保留到小数点后3位)。该温度下,化学平衡常数K=(3)使用惰性电极电解
 制取甲醇的反应装置如图所示:
制取甲醇的反应装置如图所示: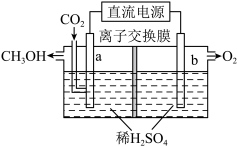
②生成甲醇的电极反应式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】甲醇是一种重要的有机化工原料。在工业生产中可以通过乙烯和水蒸气化合生成甲醇已知:
①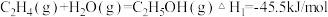
②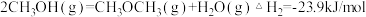
③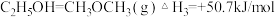
(1)请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:______ 。
(2)也可以将 与
与  混合,在恒容密闭容器中发生反应来制备:
混合,在恒容密闭容器中发生反应来制备: ,图1是在两种投料比
,图1是在两种投料比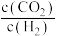 分别为1:4和1:6时,
分别为1:4和1:6时, 平衡转化率随温度变化的曲线,图2是生成的甲醇
平衡转化率随温度变化的曲线,图2是生成的甲醇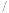 过氧化氢燃料电池的工作原理示意图:
过氧化氢燃料电池的工作原理示意图:
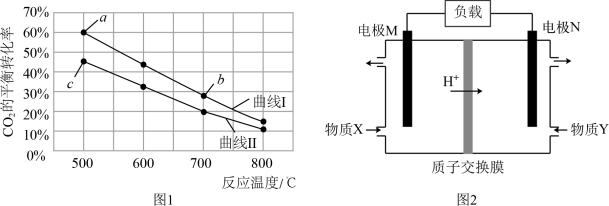
①图1中b点对应的平衡常数K值______ c点对应的平衡常数K值 填“
填“ ”“
”“ ”或“
”或“ ”
” ,理由是
,理由是______ 。
②图1中a点对应的 的转化率
的转化率______ c点对应的 的转化率。
的转化率。  填“
填“ ”“
”“ ”或“
”或“ ”
” ,
,
③图2中电极N是______  填负极或正极
填负极或正极
④图2中电极M的电极反应式:______ 。
(3) 时,
时,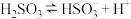 的电离常数
的电离常数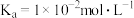 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
______ ,若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将______  填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。
(4)常温下,用NaOH溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡______  填“向左”、“向右”或“不”
填“向左”、“向右”或“不” 移动。试计算溶液中
移动。试计算溶液中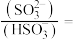
______ 。 常温下
常温下 的电离平衡常数
的电离平衡常数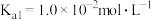 ,
,
①
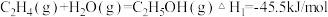
②
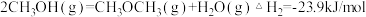
③
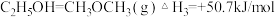
(1)请写出乙烯和水蒸气化合生成甲醇气体的热化学方程式:
(2)也可以将
 与
与  混合,在恒容密闭容器中发生反应来制备:
混合,在恒容密闭容器中发生反应来制备: ,图1是在两种投料比
,图1是在两种投料比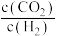 分别为1:4和1:6时,
分别为1:4和1:6时, 平衡转化率随温度变化的曲线,图2是生成的甲醇
平衡转化率随温度变化的曲线,图2是生成的甲醇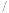 过氧化氢燃料电池的工作原理示意图:
过氧化氢燃料电池的工作原理示意图:
①图1中b点对应的平衡常数K值
 填“
填“ ”“
”“ ”或“
”或“ ”
” ,理由是
,理由是②图1中a点对应的
 的转化率
的转化率 的转化率。
的转化率。  填“
填“ ”“
”“ ”或“
”或“ ”
” ,
,③图2中电极N是
 填负极或正极
填负极或正极
④图2中电极M的电极反应式:
(3)
 时,
时,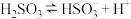 的电离常数
的电离常数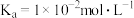 ,则该温度下
,则该温度下 水解反应的平衡常数
水解反应的平衡常数
 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将 填“增大”、“减小”或“不变”
填“增大”、“减小”或“不变” 。
。(4)常温下,用NaOH溶液吸收
 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡 填“向左”、“向右”或“不”
填“向左”、“向右”或“不” 移动。试计算溶液中
移动。试计算溶液中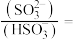
 常温下
常温下 的电离平衡常数
的电离平衡常数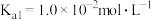 ,
,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】电镀在工业生产中具有重要作用,某电镀厂生产的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
若废水中还含有Cd2+,pH=4时Cd2+的浓度为_______ mol·L-1,用该结果说明Cd2+影响上述流程进行分离的原因是_______ (设H2S平衡浓度为1.0× 10-6mol·L-1。已知:H2S的K1=1.0×10-7,K2=7.0×10-15,Ksp(CdS)=7.0×10-27)
 和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。
和少量的Cu2+、Ni2+,能够采用如图流程进行逐一分离, 实现资源再利用。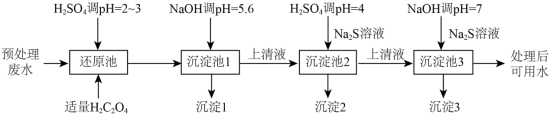
若废水中还含有Cd2+,pH=4时Cd2+的浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)某温度时,醋酸的电离平衡常数Ka=1.6×10-5,则物质的量浓度为1mol∙L-1的醋酸溶液中,达到电离平衡时,CH3COOH的电离度α=_______ 。
(2)某温度时,纯水的pH=6,将此温度下pH=11的NaOH溶液a L与pH=2的H2SO4溶液b L混合,若所得溶液为中性,则a∶b=_______ 。
某同学欲用0.1000 mol∙L-1的盐酸滴定某未知浓度的NH3∙H2O溶液。操作步骤可分为以下几步:
A.移取20.00 mL 待测氨水溶液注入洁净的锥形瓶中,并滴加 2~3滴指示剂。
B.用标准溶液润洗滴定管 2~3次。
C.取标准盐酸注入酸式滴定管至“0”刻度以上2~3 mL处
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液。
E.调节液面至“0”或“0”以下刻度,记下读数。
F.把锥形瓶放在滴定管下,用标准盐酸溶液滴定至终点,并记下滴定管液面的刻度。
(3)正确操作步骤的顺序是_______ (填字母)。
(4)盛装待测液后排气泡的正确操作是_______ 。(填序号)

(5)本实验该选择的指示剂为_______ (填字母),达到滴定终点的现象为_______ 。
a.甲基橙 b.酚酞 c.石蕊
(6)某同学的三次实验数据如下表所示。根据表中数据计算出的待测NH3∙H2O溶液的平均浓度是_______ mol∙L-1(保留4位有效数字)
(7)下列操作可能使测定结果比实际值偏高的是_______(填字母)。
(1)某温度时,醋酸的电离平衡常数Ka=1.6×10-5,则物质的量浓度为1mol∙L-1的醋酸溶液中,达到电离平衡时,CH3COOH的电离度α=
(2)某温度时,纯水的pH=6,将此温度下pH=11的NaOH溶液a L与pH=2的H2SO4溶液b L混合,若所得溶液为中性,则a∶b=
某同学欲用0.1000 mol∙L-1的盐酸滴定某未知浓度的NH3∙H2O溶液。操作步骤可分为以下几步:
A.移取20.00 mL 待测氨水溶液注入洁净的锥形瓶中,并滴加 2~3滴指示剂。
B.用标准溶液润洗滴定管 2~3次。
C.取标准盐酸注入酸式滴定管至“0”刻度以上2~3 mL处
D.把盛有标准溶液的酸式滴定管固定好,调节滴定管尖嘴使之充满溶液。
E.调节液面至“0”或“0”以下刻度,记下读数。
F.把锥形瓶放在滴定管下,用标准盐酸溶液滴定至终点,并记下滴定管液面的刻度。
(3)正确操作步骤的顺序是
(4)盛装待测液后排气泡的正确操作是

(5)本实验该选择的指示剂为
a.甲基橙 b.酚酞 c.石蕊
(6)某同学的三次实验数据如下表所示。根据表中数据计算出的待测NH3∙H2O溶液的平均浓度是
| 实验编号 | 待测NH3∙H2O溶液的体积/mL | 滴定前盐酸的体积读数/mL | 滴定后盐酸的体积读数/mL |
| 1 | 20.00 | 1.20 | 23.22 |
| 2 | 20.00 | 1.21 | 29.21 |
| 3 | 20.00 | 1.50 | 23.48 |
| A.读取NH3∙H2O溶液体积时,开始时仰视读数,取液结束时俯视读数 |
| B.滴定前锥形瓶未用待测液润洗 |
| C.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出 |
| D.酸式滴定管滴定前有气泡,滴定后气泡消失 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】硒(34Se)与氧同主族,硒元素及其化合物与人体健康、工业生产密切相关。某科研小组以阳极泥(主要成分是Se,含有CuSe、Ag2Se等杂质)为原料,提炼硒的流程如下:
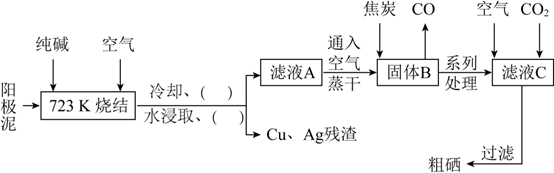
请回答下列问题:
(1)硒原子的次外层电子数_______ ,与硒同周期相邻元素是________ (填元素名称)。
(2)已知A是Na2SeO3,可用于治疗克山病,则A的化学名称为______ ;C是Na2Se,则Na2Se的电子式为_______ 。
(3)上述流程图中的括号内“( )”,按操作先后顺序依次填写的内容是_____ 、_____ 。
(4)写出高温下用焦炭还原B的化学方程式___________________ 。
(5)溶液C中析出硒的离子方程式____________________ 。
(6)向Na2SeO3溶液中滴加稍过量的乙酸,其离子方程式为__________________ 。已知:Ka1(H2SeO3)=2.7×10-3、Ka2(H2SeO3)=2.5×10-8、Ka(CH3COOH)=1.8×10-5。
(7)粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:
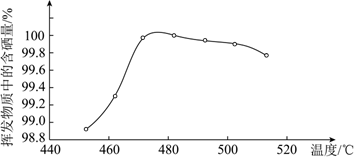
蒸馏操作中控制的最佳温度是________ (填标号)。
A.455℃ B.462℃ C.475℃ D.515℃

请回答下列问题:
(1)硒原子的次外层电子数
(2)已知A是Na2SeO3,可用于治疗克山病,则A的化学名称为
(3)上述流程图中的括号内“( )”,按操作先后顺序依次填写的内容是
(4)写出高温下用焦炭还原B的化学方程式
(5)溶液C中析出硒的离子方程式
(6)向Na2SeO3溶液中滴加稍过量的乙酸,其离子方程式为
(7)粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:

蒸馏操作中控制的最佳温度是
A.455℃ B.462℃ C.475℃ D.515℃
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】某工业生产上用铜镍矿石(主要成分为CuS、NiS、FeS、SiO2及不溶于酸的杂质)制备胆矾CuSO4•5H2O的流程如图。
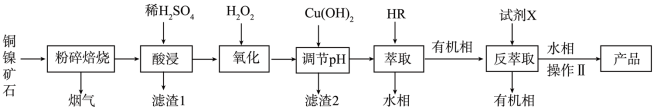
已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相); Cu2+(aq)+2HR(org)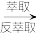 CuR2(org)+2H+(aq)。
CuR2(org)+2H+(aq)。
(1)焙烧前粉碎的目的是_______ 。
(2)调节pH时,加入Cu(OH)2生成氢氧化铁沉淀的离子方程式为_______ ,试剂X的最佳选择是_______ (填标号)。
a.HCl b.NaOH c.H2SO4 d.NH3•H2O
(3)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反应的离子方程式为_______ 。
(4)“操作II”包括洗涤,洗涤该沉淀的操作为_______ 。
(5)上述流程中获取金属铜的方法是电解硫酸铜溶液。若电解200 mL 0.5 mol/L CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是_______ 。

已知:有机萃取剂HR可以萃取Cu2+,其萃取原理(org为有机相); Cu2+(aq)+2HR(org)
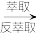 CuR2(org)+2H+(aq)。
CuR2(org)+2H+(aq)。(1)焙烧前粉碎的目的是
(2)调节pH时,加入Cu(OH)2生成氢氧化铁沉淀的离子方程式为
a.HCl b.NaOH c.H2SO4 d.NH3•H2O
(3)向“萃取”后的水相中加入一定量的NaClO和NaOH,能制得黑色不溶物NiOOH,该反应的离子方程式为
(4)“操作II”包括洗涤,洗涤该沉淀的操作为
(5)上述流程中获取金属铜的方法是电解硫酸铜溶液。若电解200 mL 0.5 mol/L CuSO4溶液,生成铜3.2 g,此时溶液中离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求回答下列问题:
I.已知:N2(g)和O2(g)反应生成NO((g)过程中的能量变化情况如下

则气体NO分解为氮气和氧气的热化学方程式为____________________ >
Ⅱ.根据下图填空:

(1)图1为含有少量Zn杂质的粗银电解精炼银的示意图,则
①_______ (填“a”或“b")极为含有杂质的粗银。
②电解一段时间后电解液中c(Ag+)浓度______ (填“偏大”、“偏小”或“不变”)。
③若b极有少量红棕色气体生成,则生成该气体的电极反应式为_______________ 。
(2)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图2所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是_______________ 。
A.铁被氧化的电极反应式为Fe-2e-=Fe2+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工作原理如图3所示,则b极是_________ 极。当电路中转移4×10-4mol电子时,传感.器内参加反应的甲醛(HCHO)质量为_______________ 。
I.已知:N2(g)和O2(g)反应生成NO((g)过程中的能量变化情况如下

则气体NO分解为氮气和氧气的热化学方程式为
Ⅱ.根据下图填空:

(1)图1为含有少量Zn杂质的粗银电解精炼银的示意图,则
①
②电解一段时间后电解液中c(Ag+)浓度
③若b极有少量红棕色气体生成,则生成该气体的电极反应式为
(2)将铁粉和活性炭的混合物用NaCl溶液湿润后,置于如图2所示装置中,进行铁的电化学腐蚀实验。下列有关该实验的说法正确的是
A.铁被氧化的电极反应式为Fe-2e-=Fe2+
B.铁腐蚀过程中化学能全部转化为电能
C.活性炭的存在会加速铁的腐蚀
D.以水代替NaCl溶液,铁不能发生吸氧腐蚀
(3)甲醛超标会危害人体健康,需对甲醛进行含量检测及污染处理。某甲醛气体传感器的工作原理如图3所示,则b极是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯碱工厂按下面的流程生产:

(1)电解饱和食盐水的化学方程式是_______ ,氯气在_______ 极产生,检验氯气的方法是_______ 。若产生了71g氯气,则阴极产生气体的物质的量为_______ ,同时生成的氢氧化钠的质量为_______ 。
(2)该流程中合成氯化氢的化学方程式为_______ ,燃烧时火焰呈_______ 色。生成的氯化氢溶于水即得盐酸,写出氯化氢的电离方程式_______ 。
某化学兴趣小组欲用下图装置制备氯水并探究其性质。
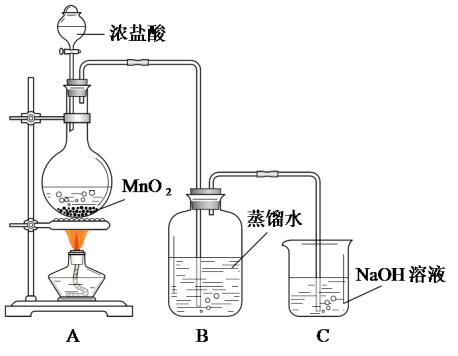
(3)烧瓶内发生的化学反应是_______ (书写化学方程式)。
(4)C装置的作用是_______ ,其中发生的化学反应是_______ (书写化学方程式)。
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:_______ ;化学性质变化:_______ 。
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
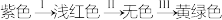
导致变色的微粒I、II、III依次为_______。
(7)某同学从B中取出少量样品,滴在NaHCO3粉末上,有无色气泡产生,由此他认为氯气与水反应产生了酸性强于碳酸的物质。请评价他的观点是否正确并说明理由_______ 。

(1)电解饱和食盐水的化学方程式是
(2)该流程中合成氯化氢的化学方程式为
某化学兴趣小组欲用下图装置制备氯水并探究其性质。

(3)烧瓶内发生的化学反应是
(4)C装置的作用是
(5)B装置中取出一定量的样品置于日光下照射一段时间,发现样品某些性质发生了明显的变化,请各列举一项:物理性质变化:
(6)若将氯气持续通入紫色石蕊试液中,可以观察到溶液的颜色变化过程为:
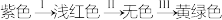
导致变色的微粒I、II、III依次为_______。
| A.H+、HClO、Cl2 | B.H+、ClO-、Cl- | C.HCl、ClO-、Cl- | D.HCl、HClO、Cl2 |
您最近一年使用:0次



