回答下列问题:
(1)①25℃时,三种弱电解质的电离平衡常数如表:
下列方法中,可以使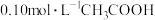 溶液中
溶液中 电离程度增大的是
电离程度增大的是_______ 。
a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
(2)常温下, 的
的 溶液加水稀释过程,下列表达式的数据一定变小的是
溶液加水稀释过程,下列表达式的数据一定变小的是_______ 。
a. b.
b. c.
c. d.
d.
(3)常温下,有pH相同、体积相同的a. 溶液和b.HCl溶液,现采取以下措施:
溶液和b.HCl溶液,现采取以下措施:
①分别加适量醋酸钠晶体后, 溶液中
溶液中
_______ HCl溶液中 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)
②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积: 溶液
溶液_______ (填“>”“<”或“=”)HCl溶液。
③温度都升高20℃, 溶液中
溶液中
_______ (填“>”“<”或“=”)HCl溶液中 。
。
④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是_______ (填字母)。(①表示盐酸,②表示醋酸)
a. b.
b. 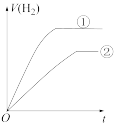 c.
c.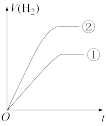 d.
d.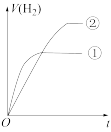
(4)常温下,等体积等物质的量浓度的 和
和 溶液混合后,溶液的
溶液混合后,溶液的
_______ ,等物质的量浓度的① ②
② ③
③ ④
④ 溶液的pH大小顺序是
溶液的pH大小顺序是_______ (填序号); 溶液滴入
溶液滴入 中的离子方程式
中的离子方程式_______ 。
(1)①25℃时,三种弱电解质的电离平衡常数如表:
| 化学式 | HCOOH |  |  |  |
| 电离平衡常数 | 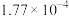 | 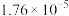 | 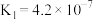  | 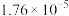 |
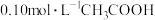 溶液中
溶液中 电离程度增大的是
电离程度增大的是a.通入少量HCl气体 b.加入少量冰醋酸 c.加入少量醋酸钠固体 d.加入少量水
(2)常温下,
 的
的 溶液加水稀释过程,下列表达式的数据一定变小的是
溶液加水稀释过程,下列表达式的数据一定变小的是a.
 b.
b. c.
c. d.
d.
(3)常温下,有pH相同、体积相同的a.
 溶液和b.HCl溶液,现采取以下措施:
溶液和b.HCl溶液,现采取以下措施:①分别加适量醋酸钠晶体后,
 溶液中
溶液中
 。(填“>”“<”或“=”)
。(填“>”“<”或“=”)②分别加等浓度的NaOH溶液至恰好反应,所需NaOH溶液的体积:
 溶液
溶液③温度都升高20℃,
 溶液中
溶液中
 。
。④分别与足量的锌粉发生反应,下列关于氢气体积(V)随时间(t)变化的示意图正确的是
a.
 b.
b.  c.
c. d.
d.
(4)常温下,等体积等物质的量浓度的
 和
和 溶液混合后,溶液的
溶液混合后,溶液的
 ②
② ③
③ ④
④ 溶液的pH大小顺序是
溶液的pH大小顺序是 溶液滴入
溶液滴入 中的离子方程式
中的离子方程式
更新时间:2022-12-22 16:20:26
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】完成下列各题.
(1)常温下,浓度均为 0.1mol•L﹣1 的下列五种钠盐溶液的 pH如表;
上述盐溶液中的阴离子,结合H+能力最强的是_________ ,根据表中数据,浓度均为0.01mol•L﹣1 的下列四种酸的溶液分别稀释 100倍,pH变化最大的是_________ (填编号)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL 0.1mol/L NaHCO3②100mL 0.1mol/L Na2CO3 两种溶液:溶液中水电离出的OH-个数:①_________ ②(填“>”、“=”或“<”,下同)。溶液中阴离子的物质的量浓度之和:①__________ ②。
(3)NaCN遇水可产生易燃的HCN气体,浓度均为0.1mol/L的NaCN和HCN的混合液中滴加酚酞,溶液变红,则混合液中各离子的浓度大小关系为______ 。
(4)研究证实,CO2可在酸性水溶液中通过电解生成甲醇(CH3OH),则生成甲醇的反应发生在_______ (填阴极或阳极),该电极反应式是______ 。
(5)已知Ksp(CuS)=1.3×10-36,Ksp(NiS)=1.0×10-24;在含Cu2+,Ni2+的溶液中,当Ni2+恰好完全沉淀[此时溶液中c(Ni2+)=1.0×10-5 mol·L-1],溶液中Cu2+的浓度是___ mol·L-1。
(1)常温下,浓度均为 0.1mol•L﹣1 的下列五种钠盐溶液的 pH如表;
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述盐溶液中的阴离子,结合H+能力最强的是
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)有①100mL 0.1mol/L NaHCO3②100mL 0.1mol/L Na2CO3 两种溶液:溶液中水电离出的OH-个数:①
(3)NaCN遇水可产生易燃的HCN气体,浓度均为0.1mol/L的NaCN和HCN的混合液中滴加酚酞,溶液变红,则混合液中各离子的浓度大小关系为
(4)研究证实,CO2可在酸性水溶液中通过电解生成甲醇(CH3OH),则生成甲醇的反应发生在
(5)已知Ksp(CuS)=1.3×10-36,Ksp(NiS)=1.0×10-24;在含Cu2+,Ni2+的溶液中,当Ni2+恰好完全沉淀[此时溶液中c(Ni2+)=1.0×10-5 mol·L-1],溶液中Cu2+的浓度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氨是合成硝酸、铵盐和氮肥的基本原料,回答下列问题:
(1)写出实验室制备氨气的化学方程式:______________________________ ;氨的水溶液显弱碱性,其原因为__________________________ (用离子方程式表示),0.1 mol·L-1的氨水中加入少量的NH4Cl固体,溶液的pH________ (填“升高”或“降低”) ;若加入少量的明矾,溶液中的NH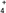 的浓度
的浓度________ (填“增大”或“减小”) 。
(2)硝酸铵加热分解可得到N2O和H2O。250 ℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为________________________________ ,平衡常数表达式为________ ;若有1 mol硝酸铵完全分解,转移的电子数为________ mol。
(3)将pH=12的氨水和pH=2的盐酸等体积混合后溶液呈______ 性。
(4)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=________ kJ·mol-1。
(1)写出实验室制备氨气的化学方程式:
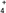 的浓度
的浓度(2)硝酸铵加热分解可得到N2O和H2O。250 ℃时,硝酸铵在密闭容器中分解达到平衡,该分解反应的化学方程式为
(3)将pH=12的氨水和pH=2的盐酸等体积混合后溶液呈
(4)由N2O和NO反应生成N2和NO2的能量变化如图所示,若生成1 mol N2,其ΔH=

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】A、B、C、D、E五种溶液分别是NaOH、NH3·H2O、CH3COOH、HCl、NH4HSO4中的一种。常温下进行下列实验:
①相同温度下,同浓度的5中溶液中,水的电离程度的大小顺序为:E=B>C>A=D
②B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
③浓度均为0.1mol·L-1 C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是___________ ,E是___________ ;
(2)用水稀释0.1mol·L-1 B溶液时,溶液中随着水量的增加而减小的是_________ (填写序号)
a. b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)
(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是_____________ (填写序号)。
a.反应所需要的时间E>A b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E d.E溶液里有镁粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中________ 曲线(填写序号)。
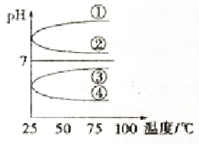
①相同温度下,同浓度的5中溶液中,水的电离程度的大小顺序为:E=B>C>A=D
②B、D均能与pH=3的A溶液反应,当它们以等物质的量混合时均能恰好反应,反应后得到的溶液前者呈酸性,后者呈中性;
③浓度均为0.1mol·L-1 C与D溶液等体积混合,溶液呈酸性。
回答下列问题:
(1)D是
(2)用水稀释0.1mol·L-1 B溶液时,溶液中随着水量的增加而减小的是
a.
 b.
b. c.c(H+)·c(OH-) d.n(OH-)
c.c(H+)·c(OH-) d.n(OH-)(3)pH相同的等体积的两份溶液A和E,分别与镁粉反应,若最后仅有一份溶液中存在镁粉,且放出氢气的质量相同,则下列说法正确的是
a.反应所需要的时间E>A b.开始反应时的速率A>E
c.参加反应的镁粉物质的量A=E d.E溶液里有镁粉剩余
(4)将等体积、等物质的量浓度B和C混合后溶液,升高温度(溶质不会分解)溶液pH随温度变化如图中

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_______ 。
(2)已知:25℃时,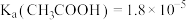 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
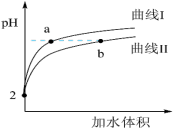
①曲线I代表_______ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a_______ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=_______ 。
(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
①三种酸的酸性由强到弱的顺序为_______ (填标号)。
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是_______ (填标号)。
A.通入氨气 B.加入Na C.加入苯甲酸钠 固体 D.加热至90℃
固体 D.加热至90℃
(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
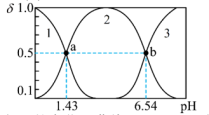
①写出亚磷酸H3PO3的第一步电离方程式_______ 。
② 随溶液pH的变化用曲线
随溶液pH的变化用曲线_______ (填“1”、“2”或“3”)表示。
③反应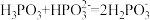 的平衡常数K=
的平衡常数K=_______ 。
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
(2)已知:25℃时,
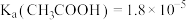 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
 ”、“
”、“ ”或“
”或“ ”)。
”)。③向上述
 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。④酸度(
 )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
| 化学式 | 苯甲酸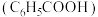 | 碳酸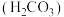 | 柠檬酸 |
| 电离常数 | 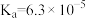 | 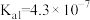  | 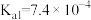 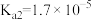 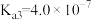 |
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是
A.通入氨气 B.加入Na C.加入苯甲酸钠
 固体 D.加热至90℃
固体 D.加热至90℃(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①写出亚磷酸H3PO3的第一步电离方程式
②
 随溶液pH的变化用曲线
随溶液pH的变化用曲线③反应
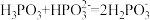 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】平衡常数是分析平衡问题的重要依据。回答下列问题:
(1)高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大,但在冰醋酸中却有一定的差异,以下是某温度下这四种酸在冰醋酸中的电离常数:
从表格中的数据判断以下说法不正确的是_______________ (填字母)。
a.在冰醋酸中这四种酸都没有完全电离
b.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
c.在冰醋酸中硫酸的电离方程式为
d.水对于这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
(2)已知: 时,
时, 的
的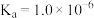 ,则
,则 的
的 溶液的
溶液的
__________ 。
(3)在温度为t时,某研究人员测定 的电离常数
的电离常数 为
为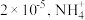 的水解常数
的水解常数 为
为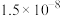 ,则该温度下水的离子积常数
,则该温度下水的离子积常数 为
为__________ ,请判断t__________ (填“>”“<”或“=”) 。
。
(4)化工生产中常用 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的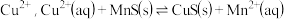 ;该反应的平衡常数K为
;该反应的平衡常数K为_______________ (保留两位有效数字, 和
和 的
的 分别为
分别为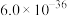 、
、 )。
)。
(5) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中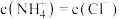 ,则溶液显
,则溶液显_______________ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离常数
的电离常数
_______________ 。
(1)高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大,但在冰醋酸中却有一定的差异,以下是某温度下这四种酸在冰醋酸中的电离常数:
| 酸 |  |  |  |  |
 |  | 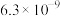 |  | 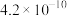 |
a.在冰醋酸中这四种酸都没有完全电离
b.在冰醋酸中高氯酸是这四种酸中酸性最强的酸
c.在冰醋酸中硫酸的电离方程式为

d.水对于这四种酸的强弱没有区分能力,但冰醋酸可以区分这四种酸的强弱
(2)已知:
 时,
时, 的
的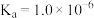 ,则
,则 的
的 溶液的
溶液的
(3)在温度为t时,某研究人员测定
 的电离常数
的电离常数 为
为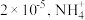 的水解常数
的水解常数 为
为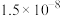 ,则该温度下水的离子积常数
,则该温度下水的离子积常数 为
为 。
。(4)化工生产中常用
 作沉淀剂除去工业废水中的
作沉淀剂除去工业废水中的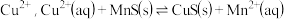 ;该反应的平衡常数K为
;该反应的平衡常数K为 和
和 的
的 分别为
分别为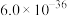 、
、 )。
)。(5)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中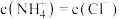 ,则溶液显
,则溶液显 的电离常数
的电离常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示:

(1)A点水的离子积为1×10-14,B点水的离子积为__________ 。造成水的离子积变化的原因是__________________________________________________ 。
(2)25℃时,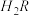 在水溶液中的电离方程式为:
在水溶液中的电离方程式为:
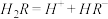 ,
,

 。
。
① 0.1 mol/L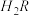 溶液的pH
溶液的pH________ 1(填“>”、“<”或“=”)。
②在0.1 mol/L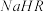 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:______________ 。
(3)100℃时,0.01 mol/L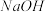 溶液的pH =
溶液的pH =____________ 。
(4)100℃时,将pH =8的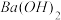 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则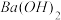 溶液与盐酸的体积比为
溶液与盐酸的体积比为___________ 。

(1)A点水的离子积为1×10-14,B点水的离子积为
(2)25℃时,
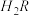 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: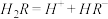 ,
,

 。
。① 0.1 mol/L
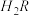 溶液的pH
溶液的pH②在0.1 mol/L
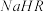 溶液中,各离子浓度由大到小的顺序是:
溶液中,各离子浓度由大到小的顺序是:(3)100℃时,0.01 mol/L
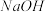 溶液的pH =
溶液的pH =(4)100℃时,将pH =8的
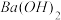 溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则
溶液与pH =5的稀盐酸混合,并保持100℃恒温,欲使混合溶液的pH =7,则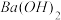 溶液与盐酸的体积比为
溶液与盐酸的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】(1)常温下, 的
的 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是__________  填序号
填序号 。
。
A.

C.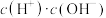
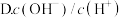
(2)体积均为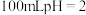 的
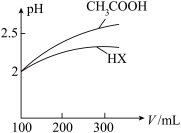
的 与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则
与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则
________  填”大于”、”小于”或“等于”
填”大于”、”小于”或“等于”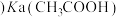 。
。
(3)23℃时,在 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中离子浓度大小关系是
,则溶液中离子浓度大小关系是________________ ,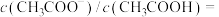
__________ (已知醋酸的电离平衡常数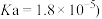
 的
的 溶液加水稀释过程中,下列表达式的数据变大的是
溶液加水稀释过程中,下列表达式的数据变大的是 填序号
填序号 。
。A.


C.
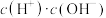
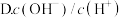
(2)体积均为
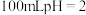 的
的 与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则
与一元酸HX,加水稀释过程中pH与溶液体积的关系如图所示,则
 填”大于”、”小于”或“等于”
填”大于”、”小于”或“等于”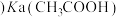 。
。
(3)23℃时,在
 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中离子浓度大小关系是
,则溶液中离子浓度大小关系是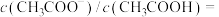
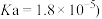
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)海洋是地球上碳元素的最大吸收池。

①溶于海水中的CO2主要以四种无机碳形式存在,即:CO2、H2CO3、___________ 、___________ 。
②在海洋碳循环中,可通过如上图所示的途径固碳。写出钙化作用的离子方程式___________ 。
(2)过量CO2溶解于海水将使许多海洋生物面临巨大威胁。研究者提出,用下图所示方法从海水中提取CO2,可以降低环境温室气体CO2的含量。

① a室的电极反应式是__________ ;
② 利用该装置产生的物质X可处理b室排出的海水,获得可排回大海的合格海水,X的化学式是__________ 。
(3)已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。所得溶液的pH___________ 7(填“>”、“=”或“<”)。烟气需冷却至15.5℃~26.5℃的可能原因是____________ 。
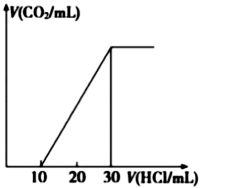
(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收。往吸收液中滴加1.0mol/L盐酸,生成的V(CO2)随V(盐酸)变化关系如图所示,则原吸收液中离子浓度由大到小的顺序为__________ 。
(1)海洋是地球上碳元素的最大吸收池。

①溶于海水中的CO2主要以四种无机碳形式存在,即:CO2、H2CO3、
②在海洋碳循环中,可通过如上图所示的途径固碳。写出钙化作用的离子方程式
(2)过量CO2溶解于海水将使许多海洋生物面临巨大威胁。研究者提出,用下图所示方法从海水中提取CO2,可以降低环境温室气体CO2的含量。

① a室的电极反应式是
② 利用该装置产生的物质X可处理b室排出的海水,获得可排回大海的合格海水,X的化学式是
(3)已知:NH3·H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7、Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至15.5℃~26.5℃后用氨水吸收过量的CO2。所得溶液的pH
(4)为了测量某湖水中无机碳含量,量取100mL湖水,酸化后用N2吹出CO2,再用NaOH溶液吸收。往吸收液中滴加1.0mol/L盐酸,生成的V(CO2)随V(盐酸)变化关系如图所示,则原吸收液中离子浓度由大到小的顺序为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】已知常温下部分弱电解质的电离平衡常数如表:
(1)25℃时,用离子方程式说明 溶液呈酸性的原因:
溶液呈酸性的原因:_____ , 的
的 溶液中各离子浓度的大小关系为
溶液中各离子浓度的大小关系为_____ 。
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_____ 。
(3)室温下,经测定0.1mol⋅L
 溶液
溶液 ,则
,则
_____  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4)25℃时,若氨水的浓度为2.0mol⋅L ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 mol⋅L
mol⋅L 时,溶液中
时,溶液中
_____ 。
| 化学式 | HF | HClO |  |  |  |
| 电离常数 | 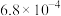 | 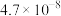 | 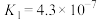 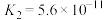 |   | 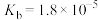 |
 溶液呈酸性的原因:
溶液呈酸性的原因: 的
的 溶液中各离子浓度的大小关系为
溶液中各离子浓度的大小关系为(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定0.1mol⋅L

 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)25℃时,若氨水的浓度为2.0mol⋅L
 ,将
,将 通入该氨水中,当
通入该氨水中,当 降至
降至 mol⋅L
mol⋅L 时,溶液中
时,溶液中
您最近一年使用:0次



