回答下列问题:
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_______ 。
(2)已知:25℃时,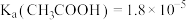 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
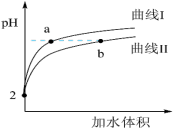
①曲线I代表_______ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a_______ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=_______ 。
(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
①三种酸的酸性由强到弱的顺序为_______ (填标号)。
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是_______ (填标号)。
A.通入氨气 B.加入Na C.加入苯甲酸钠 固体 D.加热至90℃
固体 D.加热至90℃
(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
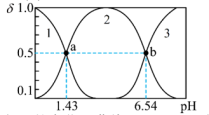
①写出亚磷酸H3PO3的第一步电离方程式_______ 。
② 随溶液pH的变化用曲线
随溶液pH的变化用曲线_______ (填“1”、“2”或“3”)表示。
③反应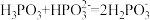 的平衡常数K=
的平衡常数K=_______ 。
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
(2)已知:25℃时,
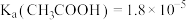 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
 ”、“
”、“ ”或“
”或“ ”)。
”)。③向上述
 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。④酸度(
 )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
| 化学式 | 苯甲酸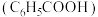 | 碳酸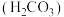 | 柠檬酸 |
| 电离常数 | 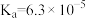 | 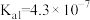  | 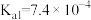 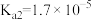 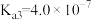 |
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是
A.通入氨气 B.加入Na C.加入苯甲酸钠
 固体 D.加热至90℃
固体 D.加热至90℃(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①写出亚磷酸H3PO3的第一步电离方程式
②
 随溶液pH的变化用曲线
随溶液pH的变化用曲线③反应
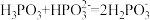 的平衡常数K=
的平衡常数K=
更新时间:2024-04-04 02:41:35
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.随着碳中和目标的提出,CO2回收技术已成为科学研究热点问题,其中逆水煤气变换反应引起了广泛关注。该反应是将CO2加氢转化为CH3OH等高附加值化学品的关键步骤。
在催化剂作用下,逆水煤气变换体系中存在以下反应:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g);∆H1= ‒ 49.5 kJ∙mol-1;K1
CH3OH(g)+H2O(g);∆H1= ‒ 49.5 kJ∙mol-1;K1
②CO2(g)+H2(g) CO(g)+H2O(g);∆H2= 41.2 kJ∙mol-1;K2
CO(g)+H2O(g);∆H2= 41.2 kJ∙mol-1;K2
③CO(g)+2H2(g) CH3OH(g);∆H3= ‒ 90.7 kJ∙mol-1;K3
CH3OH(g);∆H3= ‒ 90.7 kJ∙mol-1;K3
(1)K1=___________ (用K2、K3表示)。
Ⅱ.将6 mol CO2和8 mol H2充入容积为2L的密闭容器中,分别在T1、T2温度下发生反应①,H2的物质的量变化如表所示:
(2)T1温度下,5~10min内以CO2表示该反应速率v(CO2)=___________ 。该温度下,若各物质的起始量n(CO2) = n(H2) = n(CH3OH) = n(H2O) = 2 mol,则v(正)___________ v(逆)。
A.> B.= C.<
(3)下列说法正确的是___________。
Ⅲ.一定条件下,将原料气n(CO2)∶n(H2)=1∶3进行投料,在恒容密闭容器中模拟上述三个反应,CO和CH3OH在含碳产物(CH3OH和CO)中物质的量分数及CO2的平衡转化率随温度变化的情况如图所示___________ 。曲线___________ 代表CH3OH在含碳产物中物质的量分数。
A.m B.n
(5)有利于提高CO2转化为CH3OH的平衡转化率的措施有___________。
Ⅳ.光催化CO2也可以制备甲醇、甲烷等燃料,反应原理示意图如下图所示:
(7)写出a区的电极反应式___________ 。
在催化剂作用下,逆水煤气变换体系中存在以下反应:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g);∆H1= ‒ 49.5 kJ∙mol-1;K1
CH3OH(g)+H2O(g);∆H1= ‒ 49.5 kJ∙mol-1;K1②CO2(g)+H2(g)
 CO(g)+H2O(g);∆H2= 41.2 kJ∙mol-1;K2
CO(g)+H2O(g);∆H2= 41.2 kJ∙mol-1;K2③CO(g)+2H2(g)
 CH3OH(g);∆H3= ‒ 90.7 kJ∙mol-1;K3
CH3OH(g);∆H3= ‒ 90.7 kJ∙mol-1;K3(1)K1=
Ⅱ.将6 mol CO2和8 mol H2充入容积为2L的密闭容器中,分别在T1、T2温度下发生反应①,H2的物质的量变化如表所示:
| 物质的量/mol | T1/℃ | T2/℃ | |||||
| 0 | 5min | 10min | 15min | 20min | 25min | 30min | |
| H2 | 8.0 | 3.5 | 2.0 | 2.0 | 1.7 | 1.5 | 1.5 |
(2)T1温度下,5~10min内以CO2表示该反应速率v(CO2)=
A.> B.= C.<
(3)下列说法正确的是___________。
| A.T1 < T2 |
| B.混合气体的密度保持不变时,反应已达到平衡 |
| C.平衡后向容器中充入稀有气体,平衡不发生移动 |
| D.加入合适的催化剂可以降低反应的活化能,∆H减小 |
Ⅲ.一定条件下,将原料气n(CO2)∶n(H2)=1∶3进行投料,在恒容密闭容器中模拟上述三个反应,CO和CH3OH在含碳产物(CH3OH和CO)中物质的量分数及CO2的平衡转化率随温度变化的情况如图所示
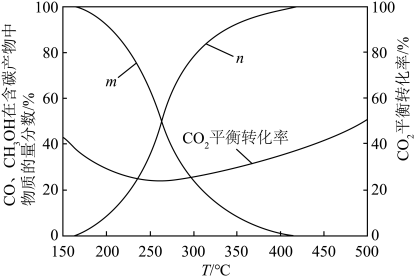
A.m B.n
(5)有利于提高CO2转化为CH3OH的平衡转化率的措施有___________。
| A.使用催化性能好的催化剂 | B.降低反应温度 |
| C.投料比不变,增加反应物的浓度 | D.增大CO2和H2的初始投料比 |
Ⅳ.光催化CO2也可以制备甲醇、甲烷等燃料,反应原理示意图如下图所示:
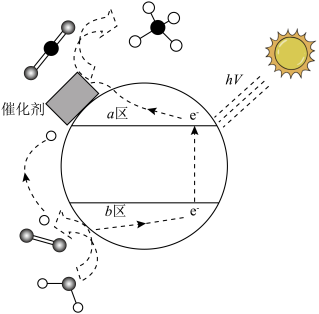
| A.H+由a区向b区移动 |
| B.b区电极反应为2H2O-4e-=O2↑+4H+ |
| C.CH4是氧化产物 |
| D.该装置实现了电能转化为化学能 |
(7)写出a区的电极反应式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】按要求回答下列问题
Ⅰ.以下是生产、生活中常见的物质:①冰醋酸 ②MgO ③NaOH ④盐酸 ⑤H2SO3 ⑥Al(OH)3 ⑦Cu ⑧C2H5OH ⑨NH3 ⑩BaCO3
(1)属于强电解质的有_______ (用序号填空,下同),属于非电解质的有_______ ,常温下能导电的物质有_______
(2)写出⑤溶于水中发生的电离方程式:_______ 。
(3)在火箭推进器中装有强还原剂肼 和强氧化剂
和强氧化剂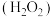 ,当它们混合时,即产生大量的
,当它们混合时,即产生大量的 和水蒸气,并放出大量热。已知
和水蒸气,并放出大量热。已知 液态肼和足量液态
液态肼和足量液态 反应,生成氮气和水蒸气,放出
反应,生成氮气和水蒸气,放出 的热量。写出该反应的热化学方程式
的热量。写出该反应的热化学方程式_______ ( 数值保留到小数点后一位)。已知
数值保留到小数点后一位)。已知 ,则
,则 液态肼与液态
液态肼与液态 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是_______  。
。
Ⅱ.已知,常温下几种酸的电离平衡常数如表:
(4)常温下, 的
的 溶液中,
溶液中, 约为
约为_______  。
。
(5)根据电离平衡常数判断,以下说法正确的是_______。
Ⅰ.以下是生产、生活中常见的物质:①冰醋酸 ②MgO ③NaOH ④盐酸 ⑤H2SO3 ⑥Al(OH)3 ⑦Cu ⑧C2H5OH ⑨NH3 ⑩BaCO3
(1)属于强电解质的有
(2)写出⑤溶于水中发生的电离方程式:
(3)在火箭推进器中装有强还原剂肼
 和强氧化剂
和强氧化剂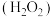 ,当它们混合时,即产生大量的
,当它们混合时,即产生大量的 和水蒸气,并放出大量热。已知
和水蒸气,并放出大量热。已知 液态肼和足量液态
液态肼和足量液态 反应,生成氮气和水蒸气,放出
反应,生成氮气和水蒸气,放出 的热量。写出该反应的热化学方程式
的热量。写出该反应的热化学方程式 数值保留到小数点后一位)。已知
数值保留到小数点后一位)。已知 ,则
,则 液态肼与液态
液态肼与液态 反应生成氮气和液态水时,放出的热量是
反应生成氮气和液态水时,放出的热量是 。
。Ⅱ.已知,常温下几种酸的电离平衡常数如表:
| 化学式 |  |  |  |
| 电离平衡常数 | 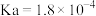 | 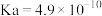 | 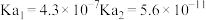 |
 的
的 溶液中,
溶液中, 约为
约为 。
。(5)根据电离平衡常数判断,以下说法正确的是_______。
A.电离 的能力: 的能力: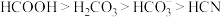 |
B.可发生反应 |
C.可发生反应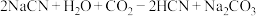 |
D.给饱和碳酸钠溶液中滴入少量的甲酸溶液,离子反应为 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氢气是一种清洁高效的新型能源,如何经济实用的制取氢气成为重要课题。
(1)硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
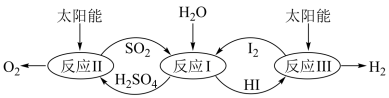
已知:
反应II:H2SO4(aq)=SO2(g)+H2O(l)+ O2(g) ΔH2=+327kJ·mol-1
O2(g) ΔH2=+327kJ·mol-1
反应III:2HI(aq)=H2(g)+I2(g) ΔH3=+172kJ·mol-1
反应2H2O(l)=2H2(g)+O2(g) ΔH=+572kJ·mol-1
则反应I的热化学方程式为_______ 。
(2)H2S可用于高效制取氢气,发生的反应为2H2S(g)=S2(g)+2H2(g)。

I.若起始时容器中只有H2S,平衡时三种物质的物质的量与裂解温度的关系如图1。
①图中曲线Z表示的物质是_______ (填化学式)。
②C点时H2S的转化率为_______ %(保留一位小数)。
③A点时,设容器内的总压为pPa,则平衡常数Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压x物质的量分数)。
II.若在两个等体积的恒容容器中分别加入2.0mol H2S、1.0mol H2S,测得不同温度下H2S的平衡转化率如图2所示。
①M点、O点和N点的逆反应速率 (M)、
(M)、 (O)和
(O)和 (N)的大小关系为
(N)的大小关系为_______ (用“>”“<”或“=”表示,下同);
②M、N两点容器内的压强2p(M)_______ p(N),平衡常数K(M)、K(N)、K(O)三者的大小关系为_______ 。
(1)硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:

已知:
反应II:H2SO4(aq)=SO2(g)+H2O(l)+
 O2(g) ΔH2=+327kJ·mol-1
O2(g) ΔH2=+327kJ·mol-1反应III:2HI(aq)=H2(g)+I2(g) ΔH3=+172kJ·mol-1
反应2H2O(l)=2H2(g)+O2(g) ΔH=+572kJ·mol-1
则反应I的热化学方程式为
(2)H2S可用于高效制取氢气,发生的反应为2H2S(g)=S2(g)+2H2(g)。

I.若起始时容器中只有H2S,平衡时三种物质的物质的量与裂解温度的关系如图1。
①图中曲线Z表示的物质是
②C点时H2S的转化率为
③A点时,设容器内的总压为pPa,则平衡常数Kp=
II.若在两个等体积的恒容容器中分别加入2.0mol H2S、1.0mol H2S,测得不同温度下H2S的平衡转化率如图2所示。
①M点、O点和N点的逆反应速率
 (M)、
(M)、 (O)和
(O)和 (N)的大小关系为
(N)的大小关系为②M、N两点容器内的压强2p(M)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】25℃时,部分物质的电离平衡常数如下表所示:
请回答下列问题。
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是___________ (用离子方程式表示),再将此溶液加热,溶液颜色___________ 。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:___________ 。
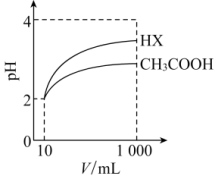
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___________ (填“大于”“等于”或“小于”)醋酸的电离平衡常数,理由是___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 4.7×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】请回答下列问题:
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)=_______ mol/L。
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)__________ pH(B) (填“>”、“=”或“<”);现用上述稀释溶液中和等浓度等体积的NaOH溶液,则需稀释溶液的体积V(A)_________ V(B)(填“>”、“=”或“<”)。
(3)已知:二元酸H2R 的电离方程式是: ,
,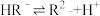 ,若0.1mol•L﹣1NaHR溶液的c(H+)="a"
,若0.1mol•L﹣1NaHR溶液的c(H+)="a" 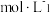 ,则0.1
,则0.1 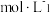 H2R溶液中c(H+)
H2R溶液中c(H+)___________ (0.1+a) 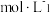 (填“<”、“>”或“=”),理由是
(填“<”、“>”或“=”),理由是______________ 。
(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为________ (用化学式表示)。
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为__________________ 。
(1)纯水在T ℃时pH=6,该温度下1 mol/L的NaOH溶液中,由水电离出的c(OH-)=
(2)某一元弱酸溶液(A)与二元强酸(B)的pH相等。若将两溶液稀释相同的倍数后,pH(A)
(3)已知:二元酸H2R 的电离方程式是:
 ,
,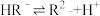 ,若0.1mol•L﹣1NaHR溶液的c(H+)="a"
,若0.1mol•L﹣1NaHR溶液的c(H+)="a" 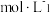 ,则0.1
,则0.1 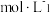 H2R溶液中c(H+)
H2R溶液中c(H+)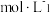 (填“<”、“>”或“=”),理由是
(填“<”、“>”或“=”),理由是(4)电离平衡常数是衡量弱电解质电离程度的物理量。已知:
| 化学式 | 电离常数(25 ℃) |
| HCN | K=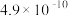 |
| CH3COOH[] | K=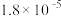 |
| H2CO3 | K1=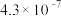 、K2= 、K2=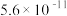 |
①25 ℃时,有等浓度的HCN溶液、H2CO3溶液和CH3COOH溶液,三溶液的pH由大到小的顺序为
②向NaCN溶液中通入少量的CO2,发生反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】根据所学的知识回答以下问题。
(1)在常温下,有下列4种溶液:
①取这四种溶液各 稀释至
稀释至 ,所得溶液的
,所得溶液的 由大到小的顺序是
由大到小的顺序是_______ (用编号表示)
②恰好中和一定量的B溶液,消耗的C溶液和D溶液的体积的大小关系是C_______ D(填“ ”,“
”,“ ”或“
”或“ ”)
”)
③将A溶液和D溶液等体积混合,混合后溶液中离子浓度的大小关系是_______ ;
④将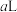 溶液B与
溶液B与 溶液D混合后,若所得溶液的
溶液D混合后,若所得溶液的 ,则
,则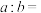
_______ (忽略混合后溶液体积的变化)
(2)已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。
A是宇宙中含量最多的元素;
B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
C元素原子的价层电子排布是 ;
;
D元素是金属性最强的短周期元素;
E与D的最高能层数相同,但其价层电子数等于其电子层数;
F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
请根据以上信息回答以下问题。
①写出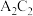 的电子式
的电子式_______
②写出元素F的核外电子排布式_______
③B、C、D、E四种元素第一电离能由小到大的顺序是_______ (用元素符号表示)
(1)在常温下,有下列4种溶液:
| 编号 | A | B | C | D |
| 溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
 | 11 | 11 | 3 | 3 |
①取这四种溶液各
 稀释至
稀释至 ,所得溶液的
,所得溶液的 由大到小的顺序是
由大到小的顺序是②恰好中和一定量的B溶液,消耗的C溶液和D溶液的体积的大小关系是C
 ”,“
”,“ ”或“
”或“ ”)
”)③将A溶液和D溶液等体积混合,混合后溶液中离子浓度的大小关系是
④将
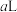 溶液B与
溶液B与 溶液D混合后,若所得溶液的
溶液D混合后,若所得溶液的 ,则
,则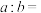
(2)已知A、B、C、D、E、F是原子序数依次增大的前四周期元素。
A是宇宙中含量最多的元素;
B元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
C元素原子的价层电子排布是
 ;
;D元素是金属性最强的短周期元素;
E与D的最高能层数相同,但其价层电子数等于其电子层数;
F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。
请根据以上信息回答以下问题。
①写出
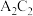 的电子式
的电子式②写出元素F的核外电子排布式
③B、C、D、E四种元素第一电离能由小到大的顺序是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】草酸是化工上常用的还原剂,实验空中可以用浓硝酸在Hg(NO3)2催化F氧化C2H2气体来制备,可能用到的仪器如图所示。
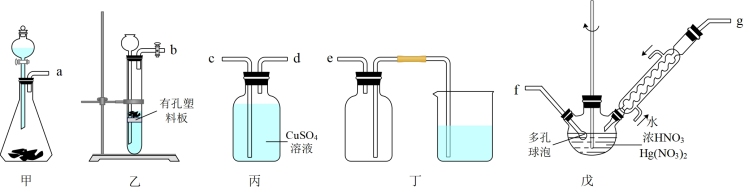
已知电石(主要成分为CaC2,含少量CaS和Ca3P2等杂质)遇水可以迅速生成C2H2,CuSO4浴液能够吸收PH3气体,浓硝酸氧化C2H2时会被还原为NO2。问答下列问题:
(1)CaC2的电子式为______ ;CaC2与H2O反应制备C2H2的化学反应方程式为______ 。
(2)选择所需的仪器,接口正确的连接顺序为______ →e。
(3)为便于控制电石与水反应制备C2H2,有同学认为宜选取仪器乙,不宜选取甲,该观点是否正确?请说明原因______ 。
(4)制备C2H2气体时,常用饱和食盐水代替水的原因是______ 。
(5)装置戊中生成草酸的反应方程式为______ ,反应一般控制在50℃左右,若高于50℃,则生成草酸的速率会减慢,原因是______ 。
(6)三颈烧瓶中液体经过蒸发浓缩。冷却结晶、过滤等操作可得到草酸晶体(H2C2O4·2H2O),设计一个实验证明草酸属于二元弱酸:______ 。

已知电石(主要成分为CaC2,含少量CaS和Ca3P2等杂质)遇水可以迅速生成C2H2,CuSO4浴液能够吸收PH3气体,浓硝酸氧化C2H2时会被还原为NO2。问答下列问题:
(1)CaC2的电子式为
(2)选择所需的仪器,接口正确的连接顺序为
(3)为便于控制电石与水反应制备C2H2,有同学认为宜选取仪器乙,不宜选取甲,该观点是否正确?请说明原因
(4)制备C2H2气体时,常用饱和食盐水代替水的原因是
(5)装置戊中生成草酸的反应方程式为
(6)三颈烧瓶中液体经过蒸发浓缩。冷却结晶、过滤等操作可得到草酸晶体(H2C2O4·2H2O),设计一个实验证明草酸属于二元弱酸:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】下表是25℃时某些弱酸的电离常数,其中多元弱酸分步电离。
(1)等浓度的HCOOH、 和
和 溶液中,水电离出的氢离子浓度:
溶液中,水电离出的氢离子浓度:_______ >_______ >_______ 。
(2)根据表中数据判断下述反应可以发生的是_______ 。(填编号)
①
②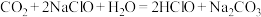
③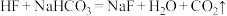
④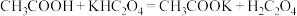
(3)少量 通入NaCN溶液中发生反应的离子方程式为
通入NaCN溶液中发生反应的离子方程式为_______ 。
(4)常温下在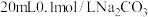 溶液中逐滴滴加
溶液中逐滴滴加 盐酸溶液40mL,溶液中含碳元素的三种微粒
盐酸溶液40mL,溶液中含碳元素的三种微粒 、
、 、
、 (
( 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。回答下列问题:
因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。回答下列问题:
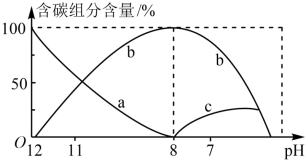
①各字母代表的粒子为b_______ ,c_______ 。
②在同一溶液中, 、
、 、
、
_______ (填“能”或“不能”)大量共存。
③当 时,溶液中含碳元素的主要微粒为
时,溶液中含碳元素的主要微粒为_______ 。
(5)若以熔融 作为电解质,写出
作为电解质,写出 燃料电池负极的电极反应式
燃料电池负极的电极反应式_______ 。
(6)等浓度等体积的 溶液和
溶液和 溶液混合,写出离子浓度由大到小的排序:
溶液混合,写出离子浓度由大到小的排序:_______ 。
| 弱酸 | K | 弱酸 | K |
| HF | 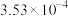 |  |   |
| HCN |  | ||
| HCOOH | 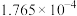 |  |  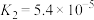 |
 | 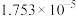 |
 和
和 溶液中,水电离出的氢离子浓度:
溶液中,水电离出的氢离子浓度:(2)根据表中数据判断下述反应可以发生的是
①

②
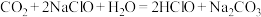
③
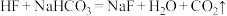
④
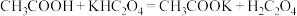
(3)少量
 通入NaCN溶液中发生反应的离子方程式为
通入NaCN溶液中发生反应的离子方程式为(4)常温下在
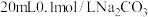 溶液中逐滴滴加
溶液中逐滴滴加 盐酸溶液40mL,溶液中含碳元素的三种微粒
盐酸溶液40mL,溶液中含碳元素的三种微粒 、
、 、
、 (
( 因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。回答下列问题:
因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如图所示。回答下列问题:
①各字母代表的粒子为b
②在同一溶液中,
 、
、 、
、
③当
 时,溶液中含碳元素的主要微粒为
时,溶液中含碳元素的主要微粒为(5)若以熔融
 作为电解质,写出
作为电解质,写出 燃料电池负极的电极反应式
燃料电池负极的电极反应式(6)等浓度等体积的
 溶液和
溶液和 溶液混合,写出离子浓度由大到小的排序:
溶液混合,写出离子浓度由大到小的排序:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、___ 和____ 。
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
则该醋酸溶液的准确浓度为________ 。(保留小数点后四位)
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸溶液的pH,结果如下:
回答下列问题:
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是_________
(2)从表中的数据,还可以得出另一结论:随着醋酸溶液浓度的减小,醋酸的电离程度________ (填“增大”“减小”或“不变”)。
实验一 配制并标定醋酸溶液的浓度
取冰醋酸配制250 mL 0.2 mol·L-1的醋酸溶液,用0.2 mol·L-1的醋酸溶液稀释成所需浓度的溶液,再用NaOH标准溶液对所配醋酸溶液的浓度进行标定。回答下列问题:
(1)配制250 mL 0.2 mol·L-1醋酸溶液时需要用到的玻璃仪器有量筒、烧杯、玻璃棒、
(2)为标定某醋酸溶液的准确浓度,用0.200 0 mol·L-1的NaOH溶液对20.00 mL醋酸溶液进行滴定,几次滴定消耗NaOH溶液的体积如下:
| 实验序号 | 1 | 2 | 3 | 4 |
| 消耗NaOH溶液的体积(mL) | 20.05 | 20.00 | 18.80 | 19.95 |
实验二 探究浓度对醋酸电离程度的影响
用pH计测定25℃时不同浓度的醋酸溶液的pH,结果如下:
| 醋酸溶液浓度(mol·L-1) | 0.001 0 | 0.010 0 | 0.020 0 | 0.100 0 | 0.200 0 |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
(1)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是
(2)从表中的数据,还可以得出另一结论:随着醋酸溶液浓度的减小,醋酸的电离程度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】化学反应原理在科研和工农业生产中有广泛应用。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g) 2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
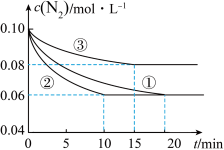
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=__________________ ;与实验①相比,实验②和实验③所改变的实验条件分别为下列选项中的__________ 、__________ (填字母编号)。
a.增大压强
b.减小压强
c.升高温度
d.降低温度
e.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g) N2O4(g)。
N2O4(g)。
①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)=0.05mol/L,则该反应的平衡常数K=__________ ;
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将__________ (填“增大”、“减小”或“不变”)。
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时间的变化如图所示。下列说法正确的是__________ (填字母编号)。
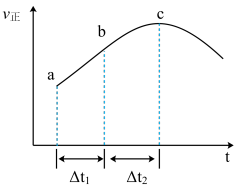
A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a______ b。 (填“>”、“<”或“=”);用a、b表示NH3 H2O的电离平衡常数Kb=
H2O的电离平衡常数Kb=________________ 。
(1)某化学兴趣小组进行工业合成氨的模拟研究,反应的方程式为N2(g)+3H2(g)
 2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
2NH3(g) ΔH<0。在lL密闭容器中加入0.1 mol N2和0.3mol H2,实验①、②、③中c(N2)随时间(t)的变化如下图所示:
实验②从初始到平衡的过程中,该反应的平均反应速率v(NH3)=
a.增大压强
b.减小压强
c.升高温度
d.降低温度
e.使用催化剂
(2)已知NO2与N2O4可以相互转化:2NO2(g)
 N2O4(g)。
N2O4(g)。①T℃时,将0.40 mol NO2气体充入容积为2L的密闭容器中,达到平衡后,测得容器中c(N2O4)=0.05mol/L,则该反应的平衡常数K=
②已知N2O4在较高温度下难以稳定存在,易转化为NO2,若升高温度,上述反应的平衡常数K将
③向绝热密闭容器中通入一定量的NO2,某时间段内正反应速率随时间的变化如图所示。下列说法正确的是

A.反应在c点达到平衡状态
B.反应物浓度:a点小于b点
C.Δt1=Δt2时,NO2的转化率:a~b段小于 b~c段
(3)25℃时,将amol/L的氨水与b mol/L盐酸等体积混合,反应后溶液恰好显中性,则a
 H2O的电离平衡常数Kb=
H2O的电离平衡常数Kb=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】已知在25℃时,醋酸、次氯酸、碳酸、亚硫酸和氢氰酸的电离平衡常数分别为
醋酸: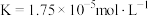
次氯酸: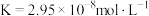
碳酸: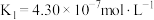 ;
;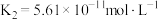
亚硫酸: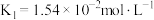 ;
;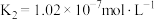
氢氰酸: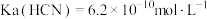
(1)写出碳酸的第一级电离平衡常数表达式:
_______ 。
(2)在相同条件下,等浓度的 、
、 、
、 和
和 溶液中碱性最强的是
溶液中碱性最强的是_______ 。
 溶液中各离子浓度大小顺序为
溶液中各离子浓度大小顺序为_______ 。
(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是_________ 。
a.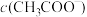 b.
b.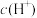 c.醋酸的电离平衡常数
c.醋酸的电离平衡常数
(4)下列离子方程式中错误的是___________ 。
a.少量 通入次氯酸钠溶液中:
通入次氯酸钠溶液中: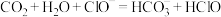
b.少量 通入次氯酸钙溶液中:
通入次氯酸钙溶液中: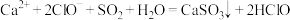
c.过量 通入澄清石灰水中:
通入澄清石灰水中:
(5)等物质的量浓度的NaCN和HCN的混合溶液中粒子浓度大小顺序_______ 。
醋酸:
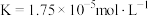
次氯酸:
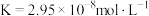
碳酸:
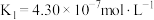 ;
;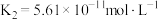
亚硫酸:
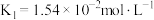 ;
;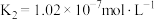
氢氰酸:
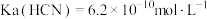
(1)写出碳酸的第一级电离平衡常数表达式:

(2)在相同条件下,等浓度的
 、
、 、
、 和
和 溶液中碱性最强的是
溶液中碱性最强的是
 溶液中各离子浓度大小顺序为
溶液中各离子浓度大小顺序为(3)若保持温度不变,在醋酸溶液中通入少量HCl,下列量会变小的是
a.
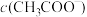 b.
b.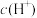 c.醋酸的电离平衡常数
c.醋酸的电离平衡常数(4)下列离子方程式中错误的是
a.少量
 通入次氯酸钠溶液中:
通入次氯酸钠溶液中: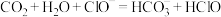
b.少量
 通入次氯酸钙溶液中:
通入次氯酸钙溶液中: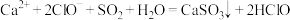
c.过量
 通入澄清石灰水中:
通入澄清石灰水中:
(5)等物质的量浓度的NaCN和HCN的混合溶液中粒子浓度大小顺序
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】碲及其化合物具有许多优良性能,被广泛用于冶金、化工、医药卫生等工业领域。工业上用铜阳极泥(主要成分除含Cu、Te外,还有少量Ag和Au)经如下工艺流程得到粗碲。
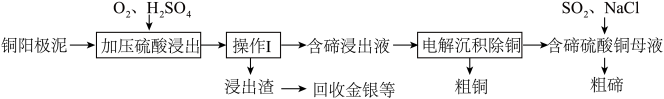
已知: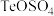 为正盐。
为正盐。
(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应: ;
; 。“含碲浸出液”的溶质成分除了
。“含碲浸出液”的溶质成分除了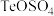 外,主要是
外,主要是_______ (填化学式)。
(2)操作Ⅰ的分离方法是_______ 。
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应是_______ 。
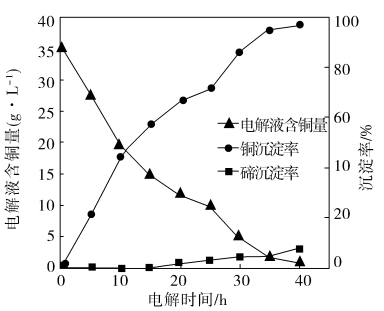
(4)通过图像分析,你认为工业上该过程持续的时段最好是_______(填标号)。
(5)向“含碲硫酸铜母液”中通入 并加入NaCl反应一段时间后,Te(Ⅳ)浓度从
并加入NaCl反应一段时间后,Te(Ⅳ)浓度从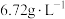 下降到
下降到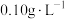 ,该过程生成粗碲的离子方程式:
,该过程生成粗碲的离子方程式:_______ 。
(6)25℃时,亚碲酸 的
的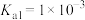 ,
,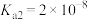 。
。
①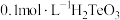 的pH约为
的pH约为_______ 。
② 的
的 溶液中,下列粒子的物质的量浓度关系正确的是
溶液中,下列粒子的物质的量浓度关系正确的是_______ (填标号)。
A.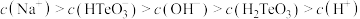
B.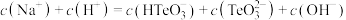
C.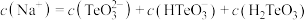
D.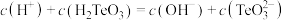

已知:
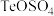 为正盐。
为正盐。(1)已知此工艺中“加压硫酸浸出”过程中会发生以下化学反应:
 ;
; 。“含碲浸出液”的溶质成分除了
。“含碲浸出液”的溶质成分除了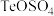 外,主要是
外,主要是(2)操作Ⅰ的分离方法是
(3)“电解沉积除铜”时,将“含碲浸出液”置于电解槽中,铜、碲沉淀的关系如下图。电解初级阶段阴极的主要电极反应是

(4)通过图像分析,你认为工业上该过程持续的时段最好是_______(填标号)。
| A.20h | B.30h | C.35h | D.40h |
 并加入NaCl反应一段时间后,Te(Ⅳ)浓度从
并加入NaCl反应一段时间后,Te(Ⅳ)浓度从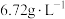 下降到
下降到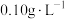 ,该过程生成粗碲的离子方程式:
,该过程生成粗碲的离子方程式:(6)25℃时,亚碲酸
 的
的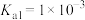 ,
,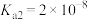 。
。①
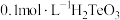 的pH约为
的pH约为②
 的
的 溶液中,下列粒子的物质的量浓度关系正确的是
溶液中,下列粒子的物质的量浓度关系正确的是A.
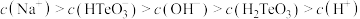
B.
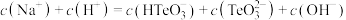
C.
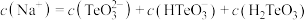
D.
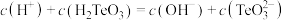
您最近一年使用:0次



