氨硼烷(NH3BH3)因其高含氢量,且性质稳定,被认为是一种极具应用前景的储氢材料。
(1)氮原子中有_____ 个未成对电子。其中具有未成对电子所处能级轨道电子云轮廓图的形状为_____ (填字母)。
a.球形 b.哑铃形
(2)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),组成元素的电负性大小顺序是______ (请填元素符号),其中B的化合价为_____ 。
(3)依据对角线规则,B的化学性质与第三周期______ (请填元素符号)性质相似,原因是______ 。
(4)第一电离能I1(N)______ I1(B)(填“>”或“<”),原因是______ 。
(5)氨硼烷水解制氢可以通过催化剂进行可控放氢,Fe-Ni合金作为氨硼烷水解的催化剂,表现出很好的催化活性,写出基态Ni原子的价层电子排布式______ ,Ni属于元素周期表的______ 区。
(1)氮原子中有
a.球形 b.哑铃形
(2)NH3BH3分子中,与N原子相连的H呈正电性(Hδ+),与B原子相连的H呈负电性(Hδ-),组成元素的电负性大小顺序是
(3)依据对角线规则,B的化学性质与第三周期
(4)第一电离能I1(N)
(5)氨硼烷水解制氢可以通过催化剂进行可控放氢,Fe-Ni合金作为氨硼烷水解的催化剂,表现出很好的催化活性,写出基态Ni原子的价层电子排布式
更新时间:2023-01-06 08:58:02
|
相似题推荐
【推荐1】过波金属元素及其化合物的应用广泛,是科学家们进行前沿研究的方向之一。
(1)基态Cu原子核外K、L层电子的电子云有_____ 种不同的伸展方向。
(2)锌化铜是一种金属互化物,元素铜的第二电离能_____ (填“大于”、“小于”或“等于”)锌的第二电离能,理由是______ 。
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C-S-O的键角______ (填“大于”、“小于”或“等于”)CH3COCH3中C-C-O的键角,理由是_____ ;元素S、Cl、O的电负性由大到小的顺序为______ 。
(4)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成红色的Cu2O,其晶胞结构如图所示。
①该晶胞原子坐标参数A为(0,0,0);C为( ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为______ 。

②若Cu2O晶体密度为dg•cm-3,晶胞参数为apm,则阿伏加德罗常数值NA为______ (用含d和a的式子表示)。
(1)基态Cu原子核外K、L层电子的电子云有
(2)锌化铜是一种金属互化物,元素铜的第二电离能
(3)[Co(DMSO)6](ClO4)2是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为(CH3)2SO。(CH3)2SO中C-S-O的键角
(4)利用CuSO4和NaOH制备的Cu(OH)2悬浊液检验醛基时,生成红色的Cu2O,其晶胞结构如图所示。
①该晶胞原子坐标参数A为(0,0,0);C为(
 ,
, ,
, )。则D原子的坐标参数为
)。则D原子的坐标参数为
②若Cu2O晶体密度为dg•cm-3,晶胞参数为apm,则阿伏加德罗常数值NA为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】据《科学》报道,中国科学家首次实现超导体(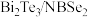 )中分段费米面。回答下列问题:
)中分段费米面。回答下列问题:
(1)Bi与P位于同主族,基态P原子的价层电子排布式为_______ 。基态Se原子核外电子云轮廓图呈哑铃形的能级上共有_______ 个电子
(2)二氯二茂铌的组成为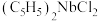 环戊二烯阴离子(
环戊二烯阴离子(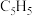 )的平面结构简式如图所示:
)的平面结构简式如图所示:
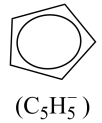
① 中C原子的杂化类型是
中C原子的杂化类型是_______ 。
②已知分子中的大π键可以用 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为_______ 。
(3) 的空间构型为
的空间构型为_______ 。
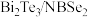 )中分段费米面。回答下列问题:
)中分段费米面。回答下列问题:(1)Bi与P位于同主族,基态P原子的价层电子排布式为
(2)二氯二茂铌的组成为
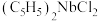 环戊二烯阴离子(
环戊二烯阴离子(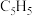 )的平面结构简式如图所示:
)的平面结构简式如图所示:
①
 中C原子的杂化类型是
中C原子的杂化类型是②已知分子中的大π键可以用
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数,则 中大π键可以表示为
中大π键可以表示为(3)
 的空间构型为
的空间构型为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如表为元素周期表的一部分,其中的编号代表对应的不同元素。
请回答下列问题:
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为___________ 。
(2)基态③原子中电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形。
(3)写出②的氧化物与NaOH溶液反应的化学方程式:___________ 。
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)___________
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式___________ 。
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是___________ 。
(7)⑨基态原子的简化电子排布式为___________ ,在周期表中的位置___________ 。
(8)⑩基态原子的价层电子轨道表示式为___________ 。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为
(2)基态③原子中电子占据最高能级的符号是
(3)写出②的氧化物与NaOH溶液反应的化学方程式:
(4)元素④⑤⑥的电负性:___________>___________>___________。(填元素符号)
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素的名称是
| 元素 | 电离能(kJ•mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
(8)⑩基态原子的价层电子轨道表示式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】铜阳极泥含有金属( 、
、 、
、 等)及它们的化合物,其中银在铜阳极泥中的存在状态有
等)及它们的化合物,其中银在铜阳极泥中的存在状态有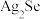 、
、 、
、 等。下图是从铜阳极泥提取银的一种工艺:
等。下图是从铜阳极泥提取银的一种工艺:

已知:Ag++2NH3 [Ag(NH3)2]+
[Ag(NH3)2]+
(1)基态Se原子的核外电子排布式是_______ 。
(2)炉气中的 可与
可与 、
、 反应生成硒单质。写出该反应方程式
反应生成硒单质。写出该反应方程式_______ 。
(3)溶液a的主要成分是_______ 。
(4)水氯化浸金过程中,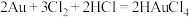 。
。 配离子中提供空轨道的是
配离子中提供空轨道的是_______ (填元素符号),配位数是_______ 。
(5)加入氨气后, 溶解,请写出氨浸分银的离子方程式
溶解,请写出氨浸分银的离子方程式_______ 。
(6)SO 的孤电子对数为
的孤电子对数为_______ 。
(7)Au的晶胞为面心立方体结构、如图所示棱长为apm(1pm=1×10-10cm)晶体金的密度
_______  。(NA为阿伏加德罗常数)
。(NA为阿伏加德罗常数)

 、
、 、
、 等)及它们的化合物,其中银在铜阳极泥中的存在状态有
等)及它们的化合物,其中银在铜阳极泥中的存在状态有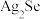 、
、 、
、 等。下图是从铜阳极泥提取银的一种工艺:
等。下图是从铜阳极泥提取银的一种工艺:
已知:Ag++2NH3
 [Ag(NH3)2]+
[Ag(NH3)2]+(1)基态Se原子的核外电子排布式是
(2)炉气中的
 可与
可与 、
、 反应生成硒单质。写出该反应方程式
反应生成硒单质。写出该反应方程式(3)溶液a的主要成分是
(4)水氯化浸金过程中,
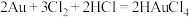 。
。 配离子中提供空轨道的是
配离子中提供空轨道的是(5)加入氨气后,
 溶解,请写出氨浸分银的离子方程式
溶解,请写出氨浸分银的离子方程式(6)SO
 的孤电子对数为
的孤电子对数为(7)Au的晶胞为面心立方体结构、如图所示棱长为apm(1pm=1×10-10cm)晶体金的密度

 。(NA为阿伏加德罗常数)
。(NA为阿伏加德罗常数)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】Al2O3可以从铝土矿中获得,铝土矿的主要成分为Al2O3,含Fe2O3、SiO2等杂质。经过“酸溶法”或“碱溶法”等都可以去掉杂质得到Al2O3。19世纪后期,美国的霍尔和法国的埃鲁先后独立发明了电解Al2O3法生产铝。2Al2O3 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
(1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是___________ ,Al3+电子排布式___________ ,O原子的未成对电子数___________ 。
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第___________ 周期第___________ 族。冰晶石(Na3AlF6)晶体中阴、阳离子各一种,阴离子符号___________ 。
(3)用“>”或“<”填空:
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因_________ 。
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s) 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJ
II.3 AlCl(g) 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ
①反应I中的还原产物是___________ ;若有0.6gC反应,电子转移数目为___________
②结合反应I、II分析,请说出这种提炼方法2条优点___________ ___________ 。
 4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点]
4Al+3O2↑[冰晶石(Na3AlF6)作助熔剂,降低氧化铝熔点](1)上述涉及到Al、Na、O、F、Si、Fe六种元素中,不是主族元素的是
(2)制造“中国芯”芯片的核心元素Si位于元素周期表第
(3)用“>”或“<”填空:
原子半径 | 非金属性 | 熔点 |
| Al | O | 二氧化硅 |
(4)用离子晶体的知识解释Al2O3比Na2O熔点高的原因
(5)其实电解法生产铝有很多弊端,科技工作者不断创新。下面一种新型直接从铝土矿中提取铝的方法
I.Al2O3(s)+AlCl3(g)+3C(s)
 3 AlCl(g)+ 3CO(g) -1486kJ
3 AlCl(g)+ 3CO(g) -1486kJII.3 AlCl(g)
 2 Al(l)+ AlCl3(g) +140 kJ
2 Al(l)+ AlCl3(g) +140 kJ①反应I中的还原产物是
②结合反应I、II分析,请说出这种提炼方法2条优点
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】元素X是地壳中含量最多的元素;元素Y基态原子的3p轨道上有4个电子;元素Z位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2。
(1)X基态原子的电子排布式为_______ 。
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是_______ 。
(3)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是_______ 。
(4)Y与X可形成YX 。
。
①YX 的立体构型为
的立体构型为_______ (用文字描述)。
②写出一种与YX 互为等电子体的分子的化学式
互为等电子体的分子的化学式_______ 。
(5)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为_______ 。其晶胞边长为540.0 pm,密度为_______ g·cm-3(列式并计算),a位置Y与b位置Z之间的距离为_______ pm(列式表示)。

(6)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,2 mol 该配合物中含有σ键的数目为_______ 。
(1)X基态原子的电子排布式为
(2)X的氢化物(H2X)在乙醇中的溶解度大于H2Y,其原因是
(3)在Y的氢化物(H2Y)分子中,Y原子轨道的杂化类型是
(4)Y与X可形成YX
 。
。①YX
 的立体构型为
的立体构型为②写出一种与YX
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(5)Y与Z所形成化合物晶体的晶胞如图所示,该化合物的化学式为

(6)Z的氯化物与氨水反应可形成配合物[Z(NH3)4]Cl2,2 mol 该配合物中含有σ键的数目为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】硼、氮、磷、钴、镍等元素的化合物在现代农业、科技、国防建设中有着许多独特的用途。
(1)制备氮化硼(BN)的一种方法为:BCl3(g)+NH3(g)=BN(s)+3HCl(g)。立方氮化硼(BN)硬度大、熔点为3000℃,其晶体类型为_______ 。试用价层电子对互斥理论解释BCl3的键角比NH3大的原因_______ 。
(2)磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态磷原子的核外电子排布式_______ 。
(3)一种Ni2+配合物的结构如图所示:

①该配合物中第二周期元素的第一电离能由大到小的顺序是_______ (填元素符号)。
②该配合物中碳原子的杂化方式为_______ 。
③该配合物中存在的化学键类型有_______ (填标号)。
A.离子键 B.σ键 C.π键 D.氢键 E.配位键
(4)钴位于周期表的_______ 区,钴与NH3易形成正八面体形的[Co(NH3)6]3+配离子,试推测[CoCl2(NH3)4]+的空间结构有_______ 种。Co可以形成六方晶系的CoO(OH),晶胞结构如图所示,设NA为阿伏加德罗常数的值,该晶体的密度为_______ g/cm3(用代数式表示)。

(1)制备氮化硼(BN)的一种方法为:BCl3(g)+NH3(g)=BN(s)+3HCl(g)。立方氮化硼(BN)硬度大、熔点为3000℃,其晶体类型为
(2)磷原子在成键时,能将一个3s电子激发进入3d能级而参加成键,写出该激发态磷原子的核外电子排布式
(3)一种Ni2+配合物的结构如图所示:

①该配合物中第二周期元素的第一电离能由大到小的顺序是
②该配合物中碳原子的杂化方式为
③该配合物中存在的化学键类型有
A.离子键 B.σ键 C.π键 D.氢键 E.配位键
(4)钴位于周期表的

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】绿柱石被国际珠宝界公认为四大名贵宝石之一。主要成分为Be3Al2[Si6O18],因含适量的Cr2O3(0.15~0.6%),而形成祖母绿。试回答下列问题:
(1)基态Al原子中,电子填充的最高能级是_______ ,基态Cr原子的价电子排布式是_____ 。
(2)用“>”或“<”填空:
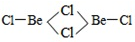
(3)BeCl2分子的空间构型是______ ,它的二聚体Be2Cl4结构如图所示,其中Be原子的杂化方式是_____ 。
(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式______ 。
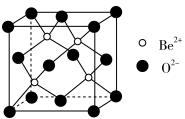
(5)Be的氧化物的立方晶胞结构如图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞边长为___ cm(设NA为阿伏加德罗常数的值,用含NA、ρ的代数式表示)。
(1)基态Al原子中,电子填充的最高能级是
(2)用“>”或“<”填空:
| 第一电离能 | 键能 | 沸点 | 离子半径 |
| Be | C—C | H2S | Al3+ |

(4)强还原剂LiAlH4能将SiCl4还原成SiH4,试写出SiH4在空气中自燃的化学方程式
(5)Be的氧化物的立方晶胞结构如图所示,已知氧化铍晶体的密度为ρg·cm-3,则晶胞边长为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】硅晶体常用作太阳能电池材料。
(1)硅在元素周期表中的位置为___________ ,硅的基态原子的电子排布式为___________ 。
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能___________ Se(ⅥA族)的第一电离能(填“>”“<”或“=”),原因是___________ 。基态Ga原子核外电子占据的最高能级为___________ 。
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有___________ 。
A.在Ⅰ中S原子采取 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大
C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是___________ 。
③化合物Ⅳ(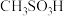 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式___________ 。
(1)硅在元素周期表中的位置为
(2)GaAlAs也可作太阳能电池材料,同周期元素As(ⅤA族)的第一电离能
(3)很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。

①化合物Ⅲ也是一种汞解毒剂,下列说法正确的有
A.在Ⅰ中S原子采取
 杂化 B.在Ⅱ中O元素的电负性最大
杂化 B.在Ⅱ中O元素的电负性最大C.在Ⅲ中C-C-C键角是180° D.在Ⅳ中硫氧键的键能均相等
②汞解毒剂的水溶性好,有利于体内重金属元素汞的解毒。化合物Ⅰ与化合物Ⅲ相比,水溶性较好的是
③化合物Ⅳ(
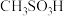 )是一种强酸,写出其电离方程式
)是一种强酸,写出其电离方程式
您最近一年使用:0次
【推荐1】元素a、b、c、d、e、f在元素周期表的前四周期。
(1)元素a位于第二周期,其最高能层只有1个电子,该电子占据最高能级的符号是___________ ,占据该能级电子的电子云轮廓图为___________ 形。其离子半径___________ H-离子(填“大于”、“小于”或“等于”)。
(2)元素b的价电子排布式为nsnnpn,它的轨道表示式为___________ 。
(3)元素c、d、e为从上至下的卤族元素,关于其元素及对应单质,随核电荷数的性质变化不正确的是___________。
(4)元素f在第三周期,其各级电离能数据如下表,结合数据说明判断该元素是___________ 。
(1)元素a位于第二周期,其最高能层只有1个电子,该电子占据最高能级的符号是
(2)元素b的价电子排布式为nsnnpn,它的轨道表示式为
(3)元素c、d、e为从上至下的卤族元素,关于其元素及对应单质,随核电荷数的性质变化不正确的是___________。
A.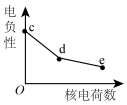 | B. | C. | D.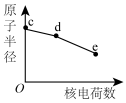 |
| 元素 | 电离能(kJ∙mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E是原子序数依次增大 的六种短周期元素,其元素性质或原子结构如下。
(1)写出B、D的元素名称:B_______ 、D_______ 。
(2)元素F位于周期表的_______ 区,其价电子的排布式为_______ 。
(3)A、C和E三种元素的电负性由大到小的顺序:_______ (请填元素符号)
(4)已知元素A、B形成的(AB)2链状分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键之比为_______ 。
(5)烯丙醇(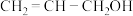 )分子中碳原子的杂化类型为
)分子中碳原子的杂化类型为_______ 。
(6)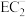 的空间构型为
的空间构型为_______ 。
(7)电解D与E形成的化合物的水溶液在工业上有着重要应用,请写出其电解的总化学方程式_______ 。
| 元素 | 元素性质或原子结构 |
| A | 原子核外有6种不同运动状态的电子 |
| B | 原子最高能级的不同轨道都有电子且自旋方向相同 |
| C | 原子核外s能级上的电子总数与p能级上的电子总数相等,但第一电离能都低于同周期相邻元素 |
| D | 在同周期元素中,原子半径最大、第一电离能最小 |
| E | 元素最高正价与最低负价代数和为6 |
| F | 基态原子的M层全充满,N层只有一个电子 |
(2)元素F位于周期表的
(3)A、C和E三种元素的电负性由大到小的顺序:
(4)已知元素A、B形成的(AB)2链状分子中所有原子都满足8电子稳定结构,则其分子中σ键与π键之比为
(5)烯丙醇(
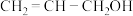 )分子中碳原子的杂化类型为
)分子中碳原子的杂化类型为(6)
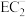 的空间构型为
的空间构型为(7)电解D与E形成的化合物的水溶液在工业上有着重要应用,请写出其电解的总化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铜及其化合物的用途非常广泛,回答下列问题:
(1)基态铜原子有种不同运动状态的电子,二价铜离子的电子排布式为________ 。
(2)铜能与类卤素(CN)2反应生成Cu(CN)2 1mol(CN)2分子中含有π键的数目为___________ 。
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),结构如图所示,

则Cu2+的配位数为_________ ,该配离子中所含的非金属元素的电负性由大到小的顺序是________ ;乙二胺分子中氮原子轨道的杂化类型为______ ,乙二胺和三甲胺[N(CH3)3]均属于胺,但相对分子质量相近,但乙二胺比三甲胺的沸点高的多,原因是__________ 。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子数目为________ 。
(5)某M原子的外围电子排布是为3s23p5,铜与M形成化合物的晶胞如图所示(黑球代表铜原子)。
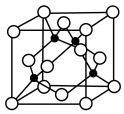
①已知铜和M的电负性分别为1.9和3.0,则铜与M形成的该种化合物属于________ (填“离子”或“共价”)化合物。
②已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为______ pm(只写计算式)。
(1)基态铜原子有种不同运动状态的电子,二价铜离子的电子排布式为
(2)铜能与类卤素(CN)2反应生成Cu(CN)2 1mol(CN)2分子中含有π键的数目为
(3)CuCl2溶液与乙二胺(H2N-CH2-CH2-NH2)可形成配离子[Cu(En)2]2+(En是乙二胺的简写),结构如图所示,

则Cu2+的配位数为
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子数目为
(5)某M原子的外围电子排布是为3s23p5,铜与M形成化合物的晶胞如图所示(黑球代表铜原子)。

①已知铜和M的电负性分别为1.9和3.0,则铜与M形成的该种化合物属于
②已知该晶体的密度为ρg·cm-3,阿伏伽德罗常数为NA,则该晶体中铜原子和M原子之间的最短距离为
您最近一年使用:0次



