已知:沉淀的 如下表:
如下表:
(1)除去 中混有的
中混有的 的方法
的方法
向混合溶液中加入_______ 、_______ 、_______ 其中之一,与 水解产生的
水解产生的 反应,促进
反应,促进 的水解,将
的水解,将 转化为
转化为 沉淀除去。
沉淀除去。
(2)除去 中混有的
中混有的 的方法
的方法
先加入氧化剂,如_______ ,将溶液中的 氧化成
氧化成 ,然后再按(1)的方法除去溶液中的
,然后再按(1)的方法除去溶液中的 。
。
(3)请设计实验方案:除去 溶液中混有的少量
溶液中混有的少量
_______ 。
 如下表:
如下表:| 化合物 |  |  |  |  |
| 沉淀范围 | 1.14~3.0 | 5.8~8.3 | 8.4~10.8 | 4.2~6.7 |
 中混有的
中混有的 的方法
的方法向混合溶液中加入
 水解产生的
水解产生的 反应,促进
反应,促进 的水解,将
的水解,将 转化为
转化为 沉淀除去。
沉淀除去。(2)除去
 中混有的
中混有的 的方法
的方法先加入氧化剂,如
 氧化成
氧化成 ,然后再按(1)的方法除去溶液中的
,然后再按(1)的方法除去溶液中的 。
。(3)请设计实验方案:除去
 溶液中混有的少量
溶液中混有的少量
更新时间:2023-02-08 20:42:48
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】软锰矿的主要成分为MnO2,还含有Fe2O3、MgO、Al2O3、CaO、SiO2等杂质,工业上用软锰矿制取MnSO4·H2O的流程如下:

(1)“浸出”时所加的X酸是_______ (填化学式),浸出渣的主要成分为_______ (填化学式)。为了提高浸出速率,可采取哪些措施_______ ?(回答两点)。
(2)浸出过程中MnO2转化为Mn2+的离子方程式为_______ 。
(3)第一步除杂,加过氧化氢的作用是_______ ,该反应的离子反应方程式为_______ ,第2步除杂,主要将Ca2+、Mg2+转化为相应氟化物沉淀除去,写出MnF2除去Mg2+的离子反应方程式:_______ 。(已知:MnF2的Ksp=5.6×10-3;MgF2的Ksp=8.0×10-11)。该反应的平衡常数K=_______ 。
(4)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是_______ (用离子方程式表示)。

(1)“浸出”时所加的X酸是
(2)浸出过程中MnO2转化为Mn2+的离子方程式为
(3)第一步除杂,加过氧化氢的作用是
(4)取少量MnSO4•H2O溶于水,配成溶液,测其pH发现该溶液显酸性,原因是
您最近半年使用:0次
【推荐2】某氯化铁样品含有少量 杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:

请根据上面流程,回答以下问题:
(1)“操作I”是配制溶液,所用到的玻璃仪器除烧杯玻璃棒、容量瓶外,还必须有______ (填仪器名称)。
(2)下列操作可能使所配溶液浓度偏小的是______ (填写序号)。
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子反应方程式______
(4)检验沉淀是否已经洗涤干净的操作是______
(5)若原样品质量a为100g,灼烧至固体质量不再变化时,最终得到6.0g红棕色固体,样品中铁元素的质量分数是______
(6)取红棕色固体溶于稀硫酸配成溶液甲,用于验证 与
与 发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
发生了氧化还原反应,使用的药品和装置如图所示,则下列说法不合理 的是______
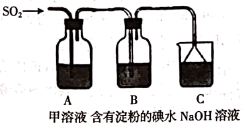
A.能表明 的还原性弱于
的还原性弱于 的现象是B中蓝色溶液褪色
的现象是B中蓝色溶液褪色
B.装置C中使用倒置的漏斗,其目的是防止倒吸
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的 溶液产生白色沉淀
溶液产生白色沉淀
D.为了验证A中的 全部被
全部被 还原了,可先加入氯水,再加KSCN溶液
还原了,可先加入氯水,再加KSCN溶液
 杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
杂质。现要测定其中铁元素的质量分数,实验按以下步骤进行:
请根据上面流程,回答以下问题:
(1)“操作I”是配制溶液,所用到的玻璃仪器除烧杯玻璃棒、容量瓶外,还必须有
(2)下列操作可能使所配溶液浓度偏小的是
①未洗涤烧杯和玻璃棒
②定容时俯视容量瓶的刻度线
③配溶液前容量瓶中有少量蒸馏水
④摇匀后,发现液面低于刻度线后继续加水至凹液面与刻度线相切
(3)请写出加入氯水发生的离子反应方程式
(4)检验沉淀是否已经洗涤干净的操作是
(5)若原样品质量a为100g,灼烧至固体质量不再变化时,最终得到6.0g红棕色固体,样品中铁元素的质量分数是
(6)取红棕色固体溶于稀硫酸配成溶液甲,用于验证
 与
与 发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
发生了氧化还原反应,使用的药品和装置如图所示,则下列说法
A.能表明
 的还原性弱于
的还原性弱于 的现象是B中蓝色溶液褪色
的现象是B中蓝色溶液褪色B.装置C中使用倒置的漏斗,其目的是防止倒吸
C.为了验证A中发生了氧化还原反应,加入用稀盐酸酸化的
 溶液产生白色沉淀
溶液产生白色沉淀D.为了验证A中的
 全部被
全部被 还原了,可先加入氯水,再加KSCN溶液
还原了,可先加入氯水,再加KSCN溶液
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
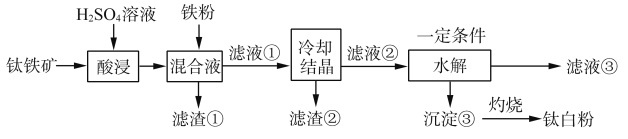
【推荐3】钛铁矿(FeTiO3)中往往含有Fe2O3、MgO、CaO、Al2O3、SiO2等杂质。一种硫酸法制取白色颜料钛白粉(TiO2)生产工艺如下:
 +
+
已知:①酸浸后,钛主要以TiOSO4形式存在;
②强电解质TiOSO4在溶液中仅能电离出 和一种阳离子。
和一种阳离子。
③H2TiO3不溶于水和稀酸。
(1)为提高酸浸速率,一般采取的措施是___________ 。(写两条)
(2)滤渣①的主要成分是___________ 。
(3)酸浸过程中,写出含钛化合物发生反应的化学方程式___________ 。
(4)加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。

①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:___________ 。
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是___________ 。
(5)水解过程中得到沉淀③的化学式为___________ 。
 +
+已知:①酸浸后,钛主要以TiOSO4形式存在;
②强电解质TiOSO4在溶液中仅能电离出
 和一种阳离子。
和一种阳离子。③H2TiO3不溶于水和稀酸。
(1)为提高酸浸速率,一般采取的措施是
(2)滤渣①的主要成分是
(3)酸浸过程中,写出含钛化合物发生反应的化学方程式
(4)加入铁粉的目的是还原体系中的Fe3+。为探究最佳反应条件,某实验室做如下尝试。

①在其它条件不变的情况下,体系中Fe(Ⅲ)含量随pH变化如图1,试分析在pH介于4~6之间时,Fe(Ⅲ)含量基本保持不变的原因:
②保持其它条件不变的情况下,体系中Fe(Ⅲ)含量随温度变化如图2,55℃后,Fe(Ⅲ)含量增大的原因是
(5)水解过程中得到沉淀③的化学式为
您最近半年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】Mg及其化合物可以发生如下转化(部分反应物、生成物或水已略去),已知X、Y、Z为气态单质,B常温下为液态,化合物D的焰色反应为黄色,C和G混合冒白烟并生成A,电解E的水溶液常用于某种工业生产。
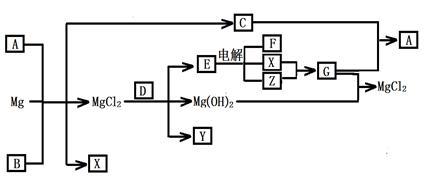
(1)写出下列物质的化学式:
A___________ ,Y__________ ;
(2)写出C的电子式____________ ;
(3)写出MgCl2与D反应的化学方程式_____________ ;
(4)请用水解平衡理论解释A+B+Mg→C+X+ MgCl2的原因______________ 。
(5)将0.1molCO2通入1L溶质为F的溶液中,充分反应后,再向混合液中逐滴滴加盐酸,所加盐酸的体积与生成的气体的关系如下图所示:则原F溶液的浓度为_______ mol/L。


(1)写出下列物质的化学式:
A
(2)写出C的电子式
(3)写出MgCl2与D反应的化学方程式
(4)请用水解平衡理论解释A+B+Mg→C+X+ MgCl2的原因
(5)将0.1molCO2通入1L溶质为F的溶液中,充分反应后,再向混合液中逐滴滴加盐酸,所加盐酸的体积与生成的气体的关系如下图所示:则原F溶液的浓度为

您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】研究碳及其化合物的相互转化对能源的充分利用、低碳经济有着重要的作用。
(1)已知:①CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1
②2H2(g)+CO(g) CH3OH(l) △H2=-128.3kJ·mol-1
CH3OH(l) △H2=-128.3kJ·mol-1
③2H2(g)+O2(g) 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-1
25℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为_________ 。
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
①实验2和实验3相比,其平衡常数关系是K2______ K3(填“>”、“<”或“=”)。
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为________ 。
(3)科学家提出由CO2制取C的太阳能工艺如图1所示。
①“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则FexOy的化学式为______________ 。
②“热分解系统”中每分解lmolFexOy,转移电子的物质的量为________ 。

(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。若某溶液中溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图2为25℃时H2CO3溶液的pC-pH图。请回答下列问题(若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-_____________ (填“能”或“不能”)大量共存。
②求H2CO3一级电离平衡常数的数值Ka1=________________ 。
③人体血液里主要通过碳酸氢盐缓冲体系c(H2CO3)/c(HCO3-)可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将_______ 。
A.变大 B.变小 C.基本不变 D.无法判断
(1)已知:①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+206.1kJ·mol-1
CO(g)+3H2(g) △H1=+206.1kJ·mol-1②2H2(g)+CO(g)
 CH3OH(l) △H2=-128.3kJ·mol-1
CH3OH(l) △H2=-128.3kJ·mol-1③2H2(g)+O2(g)
 2H2O(g) △H3=-483.6kJ·mol-1
2H2O(g) △H3=-483.6kJ·mol-125℃时,在合适的催化剂作用下,采用甲烷和氧气一步合成液态甲醇的热化学方程式为
(2)利用反应①来制备氢气,为了探究温度、压强对反应①速率、转化率的影响,某同学设计了以下三组对比实验(温度为400℃或500℃,压强为101kPa或404kPa)。
| 实验序号 | 温度℃ | 压强/kPa | CH4初始浓度/mol·L-1 | H2O初始浓度/mol·L-1 |
| 1 | 400 | P | 3.0 | 7.0 |
| 2 | T | 101 | 3.0 | 7.0 |
| 3 | 400 | 101 | 3.0 | 7.0 |
①实验2和实验3相比,其平衡常数关系是K2
②将等物质的量的CH4和水蒸气充入1L恒容密闭容器中,发生上述反应,在400℃下达到平衡,平衡常数K=27,此时容器中CO物质的量为0.10mol,则CH4的转化率为
(3)科学家提出由CO2制取C的太阳能工艺如图1所示。
①“重整系统”发生的反应中n(FeO):n(CO2)=6:1,则FexOy的化学式为
②“热分解系统”中每分解lmolFexOy,转移电子的物质的量为

(4)pC类似pH,是指极稀溶液中的溶质浓度的常用负对数值。若某溶液中溶质的浓度为1×10-3mol·L-1,则该溶液中溶质的pC=-lg(1×10-3)=3。如图2为25℃时H2CO3溶液的pC-pH图。请回答下列问题(若离子浓度小于10-5mol/L,可认为该离子不存在):
①在同一溶液中,H2CO3、HCO3-、CO32-
②求H2CO3一级电离平衡常数的数值Ka1=
③人体血液里主要通过碳酸氢盐缓冲体系c(H2CO3)/c(HCO3-)可以抵消少量酸或碱,维持pH=7.4。当过量的酸进入血液中时,血液缓冲体系中的c(H+)/c(H2CO3)最终将
A.变大 B.变小 C.基本不变 D.无法判断
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
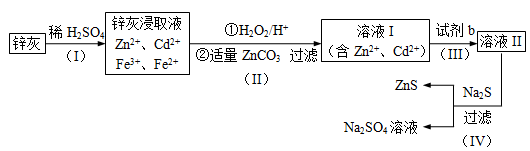
(1)为提高锌灰的浸取率,可采用的方法是______________ (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是_______________ 写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________ 。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是______________ ;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为_______________________________ ;
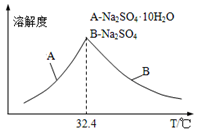
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是_______________________________ 。
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________ 。

(1)为提高锌灰的浸取率,可采用的方法是
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是

(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】氯化镍(NiCl2·6H2O)常用于电镀、陶瓷等工业,某实验室以单质Ni为原料制取氯化镍的实验步骤如下:

已知:①Fe(OH)3完全沉淀pH为3.2;Ni(OH)2开始沉淀pH为7.2,完全沉淀pH为9.2。
②NiCl2易水解,从溶液中获取NiCl2·6H2O须控制pH<2。
(1)在三颈烧瓶中(装置见图)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得NiSO4溶液。
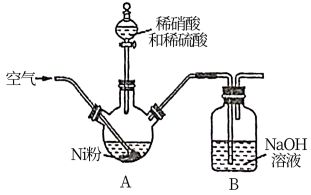
①反应过程中,为提高稀硝酸的利用率,在不改变投料比的情况下,可采取的合理措施有___________ 。
②向A装置中通入空气的作用是搅拌、___________ 。
③若镍粉过量,判断反应完成的现象是___________ 。
(2)将所得NiSO4溶液与NaHCO3溶液混合反应得到NiCO3·Ni(OH)2沉淀,过滤,洗涤。
①沉淀反应的离子方程式为___________ 。
②检验NiCO3·Ni(OH)2沉淀是否洗涤完全的方法是___________ 。
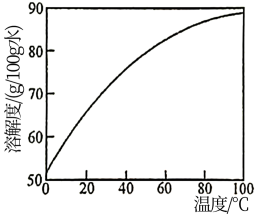
(3)在NiCO3·Ni(OH)2固体中混有少量Fe(OH)3,请补充完整由NiCO3·Ni(OH)2固体制备NiCl2·6H2O的实验方案:向NiCO3·Ni(OH)2固体中加入盐酸,边加边搅拌,___________ 。
[NiCl2的溶解度曲线如图所示。实验中须选用的仪器和试剂:pH计、盐酸、乙醇等]

已知:①Fe(OH)3完全沉淀pH为3.2;Ni(OH)2开始沉淀pH为7.2,完全沉淀pH为9.2。
②NiCl2易水解,从溶液中获取NiCl2·6H2O须控制pH<2。
(1)在三颈烧瓶中(装置见图)加入一定量Ni粉和水,通入空气,滴入稀硝酸和稀硫酸的混酸,至反应结束,过滤,制得NiSO4溶液。

①反应过程中,为提高稀硝酸的利用率,在不改变投料比的情况下,可采取的合理措施有
②向A装置中通入空气的作用是搅拌、
③若镍粉过量,判断反应完成的现象是
(2)将所得NiSO4溶液与NaHCO3溶液混合反应得到NiCO3·Ni(OH)2沉淀,过滤,洗涤。
①沉淀反应的离子方程式为
②检验NiCO3·Ni(OH)2沉淀是否洗涤完全的方法是
(3)在NiCO3·Ni(OH)2固体中混有少量Fe(OH)3,请补充完整由NiCO3·Ni(OH)2固体制备NiCl2·6H2O的实验方案:向NiCO3·Ni(OH)2固体中加入盐酸,边加边搅拌,
[NiCl2的溶解度曲线如图所示。实验中须选用的仪器和试剂:pH计、盐酸、乙醇等]

您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
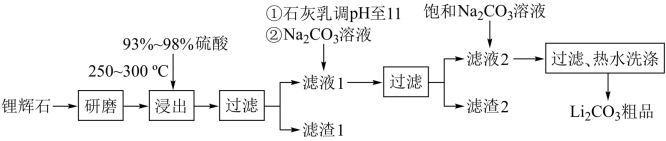
【推荐2】工业上以锂辉石为原料生产碳酸锂的部分工业流程如下:
已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓) Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O
③某些物质的溶解度(s)如下表所示。
(1)滤渣2的主要成分有___ 。
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)____ 。
(3)最后一个步骤中,用“热水洗涤”的目的是____ 。
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是__ 。
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加___ g,b中生成Li2CO3反应的化学方程式是___ 。
(5)磷酸亚铁锂电池总反应为:FePO4+Li LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:___ 。

已知:①锂辉石的主要成分为Li2O·Al2O3·4SiO2,其中含少量Ca、Mg元素。
②Li2O·Al2O3·4SiO2+H2SO4(浓)
 Li2SO4+Al2O3·4SiO2·H2O
Li2SO4+Al2O3·4SiO2·H2O③某些物质的溶解度(s)如下表所示。
| T/℃ | 20 | 40 | 60 | 80 |
| s(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| s(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)向滤液1中加入石灰乳的作用是(运用化学平衡原理简述)
(3)最后一个步骤中,用“热水洗涤”的目的是
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下:
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液做阴极液,两者用阳离子选择透过膜隔开,用惰性电极电解。
b.电解后向LiOH溶液中加入少量NH4HCO3溶液并共热沉锂,过滤、烘干可得高纯Li2CO3。
①a中,阳极的电极反应式是
②电解一段时间后,当外电路转移2mol电子,LiOH溶液质量增加
(5)磷酸亚铁锂电池总反应为:FePO4+Li
 LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
LiFePO4,电池中的固体电解质可传导Li+,试写出该电池放电时的正极反应:
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锑(Sb)是第五周期VA族元素,三氧化二锑是一种两性氧化物,俗称锑白,不溶于水,可用作白色颜料、油漆和塑料阻燃剂。以脆硫铅锑矿(主要成分为Pb4FeSb6S14)为原料制备锑白的工艺流程如图所示。
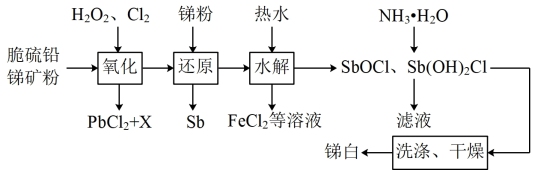
已知常温下,溶液中金属阳离子开始沉淀、完全沉淀的pH如表所示:
回答下列问题:
(1)Pb4FeSb6S14中各元素的化合价均为整数,已知铅元素为+2价,则铁元素的化合价为___ ,X的成分是___ 。
(2)氧化过程中,反应后锑为最高价态,则参加反应的n(Pb4FeSb6S14):n(Cl2)=___ ;还原过程中发生多个反应,其中之一是Fe3+被还原为Fe2+,将Fe3+还原为Fe2+的目的是___ 。
(3)常温下,Fe(OH)2的Ksp为___ (当溶液中某离子浓度c≤1×10-5mol•L-1时,可认为该离子沉淀完全)。
(4)水解过程中加入热水的原因是___ ,写出生成Sb(OH)2Cl的离子方程式___ 。
(5)写出加入氨水后SbOCl发生反应的化学方程式___ 。

已知常温下,溶液中金属阳离子开始沉淀、完全沉淀的pH如表所示:
| 金属离子 | Pb2+ | Sb3+ | Fe2+ | Fe3+ |
| 开始沉淀的pH | 7.04 | 0.53 | 7.0 | 1.9 |
| 完全沉淀的pH | 9.04 | 2.05 | 9.0 | 3.2 |
(1)Pb4FeSb6S14中各元素的化合价均为整数,已知铅元素为+2价,则铁元素的化合价为
(2)氧化过程中,反应后锑为最高价态,则参加反应的n(Pb4FeSb6S14):n(Cl2)=
(3)常温下,Fe(OH)2的Ksp为
(4)水解过程中加入热水的原因是
(5)写出加入氨水后SbOCl发生反应的化学方程式
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】利用某油脂厂制硬化油废弃的镍催化剂(主要含有Ni,还含有Fe、Cu)为原料制备电池材料Ni(OH)2及Cu2S的工艺流程如下:

已知:①Ni2++6NH3·H2O⇌[Ni(NH3)6]2++6H2O
②制备过程中,降低Ni(OH)2沉淀速率,可以避免沉淀团聚,提升电池性能
③25℃时相关物质的Ksp见下表
回答下列问题:
(1)反应器I中加入NaOH溶液的主要目的是_______ 。
(2)保持其它条件不变,在不同温度下进行稀H2SO4溶浸,镍浸出率随时间变化如图。酸浸的最佳温度和时间分别为_______ ℃、_______ min。
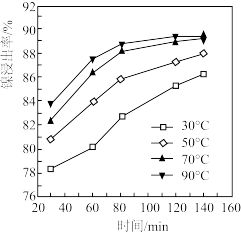
(3)25℃时加入NiCO3调节溶液的pH,则pH的理论最小值为_______ (溶液中离子浓度≤1.0×10-5mol·L-1时,认为该离子沉淀完全)。滤渣II中含有少量FeOOH,写出由Fe3+生成FeOOH的离子方程式_______ 。
(4)反应器IV中,需先加氨水,再加过量NaOH。先加氨水的目的是_______ 。
(5)反应器V中,加入稀硫酸制取Cu2S的化学方程式为_______ 。Cu2S可溶于FeCl3溶液,有研究指出CuCl2是该反应的催化剂,该过程的反应原理可用化学方程式表示为①Cu2S+2CuCl2=4CuCl+S;②_______ 。

已知:①Ni2++6NH3·H2O⇌[Ni(NH3)6]2++6H2O
②制备过程中,降低Ni(OH)2沉淀速率,可以避免沉淀团聚,提升电池性能
③25℃时相关物质的Ksp见下表
| 物质 | Fe(OH)2 | Fe(OH)3 | Ni(OH)2 | NiCO3 |
| Ksp | 1.0×10-17 | 1.0×10-38 | 1.0×10-15 | 1.0×10-5 |
(1)反应器I中加入NaOH溶液的主要目的是
(2)保持其它条件不变,在不同温度下进行稀H2SO4溶浸,镍浸出率随时间变化如图。酸浸的最佳温度和时间分别为

(3)25℃时加入NiCO3调节溶液的pH,则pH的理论最小值为
(4)反应器IV中,需先加氨水,再加过量NaOH。先加氨水的目的是
(5)反应器V中,加入稀硫酸制取Cu2S的化学方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】碘化亚铜(CuI)是阳极射线管覆盖物,不溶于水和乙醇。下图是工业上由冰铜制取无水碘化亚铜的流程。回答下列问题:

(1)步骤①中 被转化为
被转化为 ,同时有大气污染物A生成,相关反应的化学方程式为
,同时有大气污染物A生成,相关反应的化学方程式为_____ 。
(2)熔渣B主要成分为黑色磁性物质,其化学式为_____ 。
(3)步骤②中当温度高于40℃时,反应速率减慢,原因是_____ 。
(4)步骤③中加入过量 涉及的主要反应的离子方程式为
涉及的主要反应的离子方程式为_____ 。
(5)步骤④用乙醇洗涤的优点是_____ 。
(6)准确称取mgCuI样品,加入足量的Fe2(SO4)3溶液,发生反应为2CuⅠ+4Fe3+=2Cu2++4Fe2++I2,待样品完全反应后,用amol/L酸性KMnO4溶液滴定Fe(Ⅱ),消耗标准液的体积平均值为VmL。样品中CuI的质量分数的计算表达式为_____ 。如果滴定前,滴定管未用标准液润洗,CuI的质量分数_____ (填“偏低”、“偏高”或“无影响”)。

(1)步骤①中
 被转化为
被转化为 ,同时有大气污染物A生成,相关反应的化学方程式为
,同时有大气污染物A生成,相关反应的化学方程式为(2)熔渣B主要成分为黑色磁性物质,其化学式为
(3)步骤②中当温度高于40℃时,反应速率减慢,原因是
(4)步骤③中加入过量
 涉及的主要反应的离子方程式为
涉及的主要反应的离子方程式为(5)步骤④用乙醇洗涤的优点是
(6)准确称取mgCuI样品,加入足量的Fe2(SO4)3溶液,发生反应为2CuⅠ+4Fe3+=2Cu2++4Fe2++I2,待样品完全反应后,用amol/L酸性KMnO4溶液滴定Fe(Ⅱ),消耗标准液的体积平均值为VmL。样品中CuI的质量分数的计算表达式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】锂被誉为“高能金属”,废旧锂离子电池的正极材料主要含有LiCoO2及少量Al、Fe等,处理该废料的一种工艺流程如图所示:
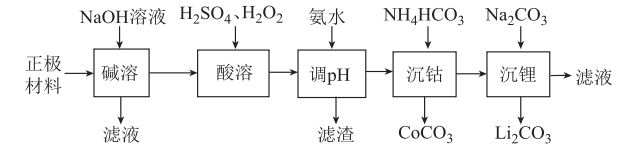
已知:① ,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);
,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);
②相关金属离子形成氢氧化物沉淀的pH值如表所示:
回答下列问题::
(1)写出“碱溶”时发生主要反应的化学方程式:___________ 。
(2)为提高“酸溶”的浸出速率,可采取的措施有___________ (任写一种)。
(3)“酸溶”时,LiCoO2能将H2O2氧化,其离子方程式为___________ ;若用浓盐酸代替H2SO4和H2O2的混合液,缺点是___________ 。
(4)用氨水调节pH的范围为___________ 。
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为___________ 。
(6)写出“沉钴”过程中发生反应的离子方程式:___________ 。

已知:①
 ,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);
,LiCoO2难溶于水,具有强氧化性(且氧化性强于KMnO4);②相关金属离子形成氢氧化物沉淀的pH值如表所示:
| 金属离子 | Al3+ | Fe3+ | Fe2+ | Co2+ |
| 开始沉淀的pH | 4.0 | 2.7 | 7.6 | 7.0 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.6 | 9.0 |
回答下列问题::
(1)写出“碱溶”时发生主要反应的化学方程式:
(2)为提高“酸溶”的浸出速率,可采取的措施有
(3)“酸溶”时,LiCoO2能将H2O2氧化,其离子方程式为
(4)用氨水调节pH的范围为
(5)该流程涉及多次过滤,实验室中过滤后洗涤沉淀的操作为
(6)写出“沉钴”过程中发生反应的离子方程式:
您最近半年使用:0次



