室温下,取四根打磨后形状大小相同的镁条,通过下列实验探究镁在溶液中的反应。
实验1 将镁条放入滴有酚酞的蒸馏水中,无明显现象,加热溶液,镁条表面产生气泡,溶液逐渐变红
实验2 将镁条放入滴有酚酞的1
 溶液中,产生气泡,溶液逐渐变红
溶液中,产生气泡,溶液逐渐变红
实验3 将镁条放入滴有酚酞的1
 溶液(pH≈7),产生气泡,溶液逐渐变红
溶液(pH≈7),产生气泡,溶液逐渐变红
实验4 将镁条放入滴有酚酞的1 NaCl溶液中,产生气泡,溶液逐渐变红
NaCl溶液中,产生气泡,溶液逐渐变红
下列基于相应实验现象得出的结论不正确的是
实验1 将镁条放入滴有酚酞的蒸馏水中,无明显现象,加热溶液,镁条表面产生气泡,溶液逐渐变红
实验2 将镁条放入滴有酚酞的1

 溶液中,产生气泡,溶液逐渐变红
溶液中,产生气泡,溶液逐渐变红实验3 将镁条放入滴有酚酞的1

 溶液(pH≈7),产生气泡,溶液逐渐变红
溶液(pH≈7),产生气泡,溶液逐渐变红实验4 将镁条放入滴有酚酞的1
 NaCl溶液中,产生气泡,溶液逐渐变红
NaCl溶液中,产生气泡,溶液逐渐变红下列基于相应实验现象得出的结论不正确的是
A.实验1加热时发生反应的化学方程式为 |
B.实验2反应后的溶液中存在: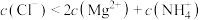 |
C.实验3产生的气体中可能含 |
D.实验1和实验4表明 对Mg与 对Mg与 反应有催化作用 反应有催化作用 |
2023·江苏南通·一模 查看更多[5]
(已下线)FHgkyldyjhx13江苏省无锡市第一中学2023-2024学年高三上学期综合练习(二)化学试题河北省部分学校2023届高三下学期二模联考化学试题(已下线)专题13 化学实验方案的设计与评价江苏省南通市2023届高三第一次调研测试(一模)化学试题
更新时间:2023-02-14 22:02:25
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,通过下列实验探究NaHS溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| 1 | 向0.1mol·L-1NaHS溶液中滴加几滴酚酞试剂,溶液变红 |
| 2 | 向0.1mol·L-1NaHS溶液中加入等体积0.1mol·L-1NaOH溶液充分混合 |
| 3 | 向0.1mol·L-1NaHS溶液中滴加过量CuCl2溶液,产生黑色沉淀 |
| 4 | 向0.1mol·L-1NaHS溶液中通入过量氯气,无淡黄色沉淀产生 |
| A.0.1mol·L-1NaHS溶液中:c(H+)·c(S2-)>c(H2S)·c(OH-) |
| B.实验2所得溶液中:c(Na+)=c(S2-)+c(HS-)+c(H2S) |
| C.实验3反应静置后的上层清液中有c(Cu2+)·c(S2-)=Ksp(CuS) |
| D.实验4说明HS-不能被氯气氧化 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】室温下,通过下列实验探究0.1mol·L-1 NaHS溶液的性质。
下列有关说法正确的是
| 实验 | 实验操作和现象 |
| ① | 滴加几滴酚酞试液,溶液变红 |
| ② | 加入等体积0.1mol⋅L-1 NaOH溶液充分混合,无明显现象 |
| ③ | 加入少量CuSO4溶液,产生黑色沉淀 |
| ④ | 通入少量氯气,有淡黄色沉淀产生 |
| A.实验①溶液中:c(S2-)>c(H2S) |
| B.实验②所得溶液中:c(OH-)=c(H+)+c(HS-)+2c(H2S) |
| C.实验③可以证明:H2S和H2SO4均为强电解质 |
| D.实验④中反应的离子方程式:S2-+Cl2=2S↓+2Cl- |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】如图模拟“侯氏制碱法”的部分过程。下列说法不正确的是
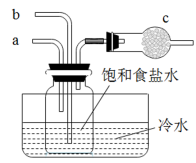

A. 中通入 中通入 , , 中通入 中通入 |
B. 中放入蘸有稀硫酸的棉花团用于 中放入蘸有稀硫酸的棉花团用于 的尾气吸收 的尾气吸收 |
| C.工业上常以海水为原料,经过净化、浓缩得到饱和食盐水 |
D.先通 ,再通 ,再通 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法错误的是
| A.将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色,可证明氧化性H2O2比Fe3+强 |
| B.酸性高锰酸钾溶液具有强的氧化性,配制时不能用盐酸酸化 |
| C.向某溶液中加入KSCN溶液,无明显现象,再加入氯水,溶液变红,说明原溶液中含有Fe2+ |
| D.某未知液中加入浓NaOH溶液,加热,没有产生使湿润的红色石蕊试纸变蓝的气体,则该未知液中不含NH4+ |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】类比(比较)是研究物质性质的常用方法之一,可预测许多物质的性质。但类比是相对的,不能违背客观实际。下列各说法中正确的是( )
| A.根据化合价Fe3O4可表示为FeO·Fe2O3,则Pb3O4也可表示为PbO·Pb2O3 |
| B.CaC2能水解:CaC2+2H2O→Ca(OH)2 + C2H2↑ ,则Al4C3也能水解:Al4C3+ 12H2O→4Al(OH)3↓+ 3CH4↑ |
| C.O2与Cu反应加热生成CuO,则S与Cu反应加热生成CuS |
| D.SO2通入BaCl2溶液中不产生沉淀,则SO2通入Ba(NO3)2溶液中也不产生沉淀 |
您最近半年使用:0次

 溶液的导电性相同
溶液的导电性相同 溶液中:
溶液中: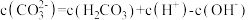
 的溶液:
的溶液: 、
、 、
、 、
、 可能大量共存
可能大量共存

