海洋元素“溴”的单质及其化合物的用途广泛。
(1)Br原子的最外层电子排布式为_______ ,其中未成对电子的电子云形状为_______ 。
(2)能作为溴、碘元素原子得电子能力递变规律的判断依据是_______ (填序号)。
a.IBr中溴为﹣1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)从原子结构角度解释氯的非金属性强于溴的原因:_______ 。
(4)Br2和碱金属单质形成的MBr熔点如表:
NaBr的电子式_______ ,MBr熔点呈现表中趋势的原因是_______ 。
(5)海水提溴过程中,先向酸化的浓缩海水中通入_______ ,将其中的Br—氧化,再用“空气吹出法”吹出Br2,并用纯碱吸收:Br2+Na2CO3+H2O→NaBr+NaBrO3+NaHCO3(未配平),则吸收1mol Br2,转移电子_______ mol,反应中氧化产物为_______ 。
(6)随后用硫酸酸化吸收液,得到Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得Br2的质量减少,可能原因是_______ 。
(1)Br原子的最外层电子排布式为
(2)能作为溴、碘元素原子得电子能力递变规律的判断依据是
a.IBr中溴为﹣1价 b.HBr、HI的酸性
c.HBr、HI的热稳定性 d.Br2、I2的熔点
(3)从原子结构角度解释氯的非金属性强于溴的原因:
(4)Br2和碱金属单质形成的MBr熔点如表:
| MBr | NaBr | KBr | RbBr | CsBr |
| 熔点/℃ | 747 | 734 | 693 | 636 |
(5)海水提溴过程中,先向酸化的浓缩海水中通入
(6)随后用硫酸酸化吸收液,得到Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得Br2的质量减少,可能原因是
2023·上海黄浦·一模 查看更多[2]
更新时间:2023-02-17 15:28:03
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】Ⅰ.某废水中可能含有下列离子中的若干种:Fe3+、Al3+、Fe2+、Cu2+、Cl-、CO 、NO
、NO 、SO
、SO 、SiO
、SiO 。现进行如下实验:
。现进行如下实验:
Ⅰ.取少量溶液,加入KSCN溶液,无明显变化
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得溶液中加入BaCl2溶液,有白色沉淀生成
Ⅳ.向Ⅱ中所得溶液中加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成
请回答下列问题:
(1)该废水一定含有的离子是_______ ;
(2)实验Ⅱ中加入盐酸生成无色气体的离子方程式是_______ ;
(3)过滤除去Ⅳ中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO +OH-
+OH- AlO
AlO +NH3+N2+H2O(未配平)。若除去0.2molNO
+NH3+N2+H2O(未配平)。若除去0.2molNO ,消耗铝
,消耗铝_______ g。
Ⅱ.某混合液中,可能大量含有的离子如下:
阳离子:H+、K+、Al3+、NH 、Mg2+阴离子:Cl-、Br-、OH-、CO
、Mg2+阴离子:Cl-、Br-、OH-、CO 、AlO
、AlO
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示:
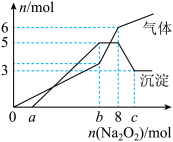
(4)该溶液中一定含有的阳离子是_______ ,其对应物质的量浓度之比为_______ ,溶液中一定不存在的阴离子是_______ 。
(5)请写出沉淀减少的离子方程式_______ 。
 、NO
、NO 、SO
、SO 、SiO
、SiO 。现进行如下实验:
。现进行如下实验:Ⅰ.取少量溶液,加入KSCN溶液,无明显变化
Ⅱ.另取溶液加入少量盐酸,有无色气体生成,该无色气体遇空气变成红棕色
Ⅲ.向Ⅱ中所得溶液中加入BaCl2溶液,有白色沉淀生成
Ⅳ.向Ⅱ中所得溶液中加入过量浓氨水,仅有红褐色沉淀生成,过滤,在所得溶液中加入盐酸至酸性时,再加入氢氧化钠溶液,有蓝色沉淀生成
请回答下列问题:
(1)该废水一定含有的离子是
(2)实验Ⅱ中加入盐酸生成无色气体的离子方程式是
(3)过滤除去Ⅳ中的蓝色沉淀,调整溶液的pH为10.7左右时,加入铝粉,反应产生氨气和氮气的体积比为1:4,其离子方程式为Al+NO
 +OH-
+OH- AlO
AlO +NH3+N2+H2O(未配平)。若除去0.2molNO
+NH3+N2+H2O(未配平)。若除去0.2molNO ,消耗铝
,消耗铝Ⅱ.某混合液中,可能大量含有的离子如下:
阳离子:H+、K+、Al3+、NH
 、Mg2+阴离子:Cl-、Br-、OH-、CO
、Mg2+阴离子:Cl-、Br-、OH-、CO 、AlO
、AlO
为探究其成分,某同学将Na2O2逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入Na2O2的物质的量的关系分别如图所示:

(4)该溶液中一定含有的阳离子是
(5)请写出沉淀减少的离子方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】氧化钪( )可用作半导体镀层的蒸镀材料,是一种重要的工业材料。以钪锰矿石(主要含
)可用作半导体镀层的蒸镀材料,是一种重要的工业材料。以钪锰矿石(主要含 、
、 及少量
及少量 、
、 、CaO、FeO)为原料制备
、CaO、FeO)为原料制备 的工艺流程如图,其中TBP和P507均为有机萃取剂。
的工艺流程如图,其中TBP和P507均为有机萃取剂。
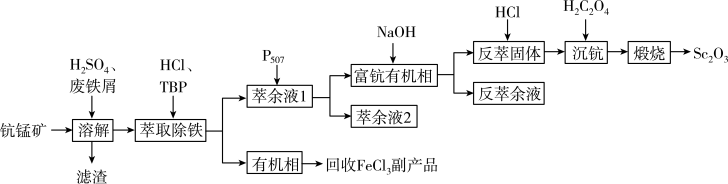
回答下列问题:
(1)“溶解”时 被
被 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是_______ 。
(2)“滤渣”的主要成分是_______ 。
(3)“萃取除铁”时铁和的萃取率与O/A比(有机溶剂与水溶液的体积比)的关系如图所示。该工艺中最佳O/A比为_______ 。
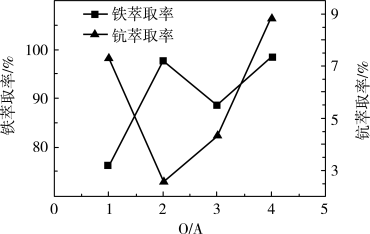
(4)有机萃取剂P507萃取 的反应原理为阳离子交换:
的反应原理为阳离子交换: (HR代表P507)。在“富钪有机相”中反应生成
(HR代表P507)。在“富钪有机相”中反应生成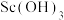 的化学方程式是
的化学方程式是_______ 。
(5)“萃余液2”中的金属阳离子除 、
、 外,还有
外,还有_______ 。
(6) 在空气中“煅烧”生成
在空气中“煅烧”生成 的化学方程式是
的化学方程式是_______ 。
(7)某厂用100kg的钪锰矿制备 ,最终得到
,最终得到 276g,该矿中钪的质量分数为
276g,该矿中钪的质量分数为_______ 。
 )可用作半导体镀层的蒸镀材料,是一种重要的工业材料。以钪锰矿石(主要含
)可用作半导体镀层的蒸镀材料,是一种重要的工业材料。以钪锰矿石(主要含 、
、 及少量
及少量 、
、 、CaO、FeO)为原料制备
、CaO、FeO)为原料制备 的工艺流程如图,其中TBP和P507均为有机萃取剂。
的工艺流程如图,其中TBP和P507均为有机萃取剂。
回答下列问题:
(1)“溶解”时
 被
被 氧化为
氧化为 ,该反应的离子方程式是
,该反应的离子方程式是(2)“滤渣”的主要成分是
(3)“萃取除铁”时铁和的萃取率与O/A比(有机溶剂与水溶液的体积比)的关系如图所示。该工艺中最佳O/A比为

(4)有机萃取剂P507萃取
 的反应原理为阳离子交换:
的反应原理为阳离子交换: (HR代表P507)。在“富钪有机相”中反应生成
(HR代表P507)。在“富钪有机相”中反应生成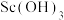 的化学方程式是
的化学方程式是(5)“萃余液2”中的金属阳离子除
 、
、 外,还有
外,还有(6)
 在空气中“煅烧”生成
在空气中“煅烧”生成 的化学方程式是
的化学方程式是(7)某厂用100kg的钪锰矿制备
 ,最终得到
,最终得到 276g,该矿中钪的质量分数为
276g,该矿中钪的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】含氮的化合物在化学反应中变化复杂。
Ⅰ.现用下图所示仪器(夹持装置已省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①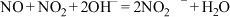 ;
;
②气体液化的温度: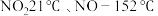 。
。___________ 。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:___________ 。
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%硫酸的仪器名称是___________ ;
②实验确认有NO的现象是___________ 。
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是___________ 。
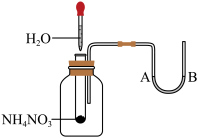
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇。
b.在230℃以上时,同时有弱光: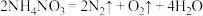
c.在400℃以上时,剧烈分解发生爆炸:
(5)如图将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因___________ 。___________ ,___________ (填“能”或“不能”)用硝酸铵代替氯化铵。
(7)完成离子反应Ⅳ:________ 。
 。
。
Ⅰ.现用下图所示仪器(夹持装置已省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分。
已知:①
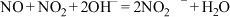 ;
;②气体液化的温度:
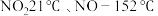 。
。
(2)反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
(3)在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体。
①盛装70%硫酸的仪器名称是
②实验确认有NO的现象是
(4)通过上述实验探究过程,可得出装置A中反应的化学方程式是
Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
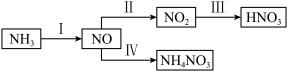
a.NH4NO3是一种白色晶体,易溶于水,微溶于乙醇。
b.在230℃以上时,同时有弱光:
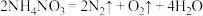
c.在400℃以上时,剧烈分解发生爆炸:

(5)如图将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因
(7)完成离子反应Ⅳ:
 。
。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】[Cu(NH3)4]SO4是一 种深蓝色的配位化合物。
(1)Cu2+可被还原成Cu+,Cu+基态核外的外围电子排布式为_________________________ 。
(2)H元素与N元素可形成分子式为N2H2的化合物,该物质的分子具有平面结构,则该分子中N原子的杂化轨道类型为______________________ 。
(3)与CS2分子互为等电子体的SCN-离子的电子式为_________________ 。
(4) Cu可形成多种配合物,且各种配合物有广乏的用途。某Cu的配合物结构如图1所示,则该配合物中心原子Cu的配体数为____ ; 其分子内含有的作用力有________ (填序号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键


(5)Cu元素与S元素形成的一种化合物品跑如图2所示,其中S的配位数为______________ 。
(1)Cu2+可被还原成Cu+,Cu+基态核外的外围电子排布式为
(2)H元素与N元素可形成分子式为N2H2的化合物,该物质的分子具有平面结构,则该分子中N原子的杂化轨道类型为
(3)与CS2分子互为等电子体的SCN-离子的电子式为
(4) Cu可形成多种配合物,且各种配合物有广乏的用途。某Cu的配合物结构如图1所示,则该配合物中心原子Cu的配体数为
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键


(5)Cu元素与S元素形成的一种化合物品跑如图2所示,其中S的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】钛被称为继铁、铝之后的“第三金属”。一种制备金属钛的工艺流程如下所示:___________ 。
(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点___________ 136℃(填“>”“<”或“=”)并阐述推测理由___________ 。
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:___________ 。
(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为___________ 。___________ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。

(2)已知TiCl4在通常情况下是无色液体,熔点为-37℃,沸点为136℃,结构与CCl4相似。试预测CCl4的沸点
(3)纳米TiO2是一种应用广泛的催化剂,其催化作用的一个实例如下所示:

(4)硫酸氧钛晶体中阳离子为链状聚合形式的离子,该阳离子的结构片段如图所示。该阳离子中Ti与O的原子数之比为


您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】元素是构成我们生活的世界中一切物质的“原材料”。
(1)自18世纪以来,科学家们不断探索元素之谜。通过从局部到系统 的研究过程,逐渐发现了元素之间的内在联系。下面列出了几位杰出科学家的研究工作。
上述科学家的研究按照时间先后排序合理的是_________ (填数字序号)。
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
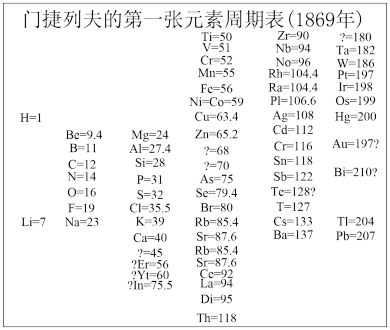
①门捷列夫将已有元素按照相对原子质量排序,同一___________ (填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是_______________ ,第5列方框中“Te=128?”的问号表达的含义是_______________ 。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量 递增呈现周期性变化,而是随着原子序数 (核电荷数)递增呈现周期性变化。其本质原因是_______________ (填字母序号)。
A. 随着核电荷数递增,原子核外电子排布呈现周期性变化
B. 随着核电荷数递增,原子半径呈现周期性变化
C. 随着核电荷数递增,元素主要化合价呈现周期性变化
(3)短周期元素A、B、D、E、G、J在周期表中的位置如下:
根据上表回答问题:
①D在周期表中的位置是_______________ 。
②A、B、E、G的原子半径由大到小的顺序是_______________ (填元素符号)。
③B、D的气态氢化物的稳定性大小关系为_______________ (填化学式)。
④E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i. H++OH-=H2O、ii._______________ 、iii_______________ 。
⑤用电子式表示E的最高价氧化物的形成过程_______________ 。
(1)自18世纪以来,科学家们不断探索元素之谜。通过
| 序号 | ① | ② | ③ | ④ |
| 科学 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
| 工作 | 发现“ | 创立 | 发现了5组性质相似的“ | 认为 |
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。

①门捷列夫将已有元素按照相对原子质量排序,同一
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着
A. 随着核电荷数递增,原子核外电子排布呈现周期性变化
B. 随着核电荷数递增,原子半径呈现周期性变化
C. 随着核电荷数递增,元素主要化合价呈现周期性变化
(3)短周期元素A、B、D、E、G、J在周期表中的位置如下:
| A | |||||||
| B | D | ||||||
| E | G | J |
①D在周期表中的位置是
②A、B、E、G的原子半径由大到小的顺序是
③B、D的气态氢化物的稳定性大小关系为
④E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i. H++OH-=H2O、ii.
⑤用电子式表示E的最高价氧化物的形成过程
您最近一年使用:0次
【推荐1】前四周期元素A、B、C、D、E、F原子序数依次增大,其相关性质如表所示:
请根据以上情况,回答下列问题:
(1)E元素基态原子核外有___________ 种能量不同的电子,电子排布式为___________ ,F位于元素周期表第___________ 周期第___________ 族,写出F元素基态原子的价电子排布式___________ 。
(2)A、B、C、D四种元素第一电离能由大到小的顺序为___________ (用元素符号表示)。B、C、D三种元素的简单离子的半径由大到小的顺序为___________ (用离子符号表示)。
(3)许多金属盐都可以发生焰色试验,如元素C,其原因是___________ 。
| A | 2p能级电子半充满 |
| B | 与A同周期,且原子核外有2个未成对电子 |
| C | 基态原子核外有6个原子轨道排有电子,且只有1个未成对电子 |
| D | 其基态原子价电子排布式为msnmpn+2 |
| E | 前四周期元素中,E元素基态原子未成对电子数最多 |
| F | 基态F+各能级电子全充满 |
(1)E元素基态原子核外有
(2)A、B、C、D四种元素第一电离能由大到小的顺序为
(3)许多金属盐都可以发生焰色试验,如元素C,其原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】表为周期表的一部分,其中的字母代表对应的元素
(1)元素A的元素符号_______ ,该原子的核外电子排布式________ ;
(2)表中元素第一电离能最小的是_______ (填元素符号,下同),电负性最大的是________ ,化学性质最稳定的是________ 。
(3)表中元素处于d区的是___________ (填元素符号)。
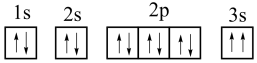
(4)某同学根据上述信息,推断D基态原子的核外电子排布图为(见图),该同学所画的电子排布图违背了________ 。
(5)已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的位置___________
(6)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
锰元素位于第四周期第Ⅶ B族。请写出基态Mn2+的价电子排布式:___________ 。比较两元素的I2、I3可知,气态Mn2+再失去1个电子比气态Fe2+再失去1个电子难,请用原子结构的角度进行解释___________ 。
| A | B | ||||||||||||||||
| C | D | E | |||||||||||||||
| F | G | H | I |
(2)表中元素第一电离能最小的是
(3)表中元素处于d区的是
(4)某同学根据上述信息,推断D基态原子的核外电子排布图为(见图),该同学所画的电子排布图违背了

(5)已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的位置
(6)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于表:
| 元素 | Mn | Fe | |
| 电离能/kJ·mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】东晋《华阳国志•南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的价电子排布式为________ 。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____________ 。
②1 mol [Ni(NH3)6]2+含有σ键为___ mol。
③氨的沸点高于膦(PH3),原因是________ 。
(3)某镍白铜合金的立方晶胞结构如图所示,该合金的化学式为________ 。

(1)镍元素基态原子的价电子排布式为
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②1 mol [Ni(NH3)6]2+含有σ键为
③氨的沸点高于膦(PH3),原因是
(3)某镍白铜合金的立方晶胞结构如图所示,该合金的化学式为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】已知海水中溴元素主要以Br-形式存在,工业上从海水中提取溴的流程如下:

(1)写出“氧化”反应的离子方程式:_______ 。
(2)将吹出后的含Br2的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:_______ 。
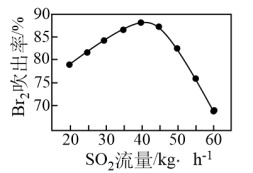
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。SO2流量过大,Br2吹出率反而下降的原因是_______ 。
(3)对于较低浓度的溴水,可采用萃取的方法提取Br2。四氯化碳可作为Br2的萃取剂,其原因除四氯化碳不与溴反应外,还有_______ 。
(4)除了四氯化碳,还可以选择下列_______ 试剂
A. 苯 B.酒精 C.氢氧化钠溶液

(1)写出“氧化”反应的离子方程式:
(2)将吹出后的含Br2的空气按一定速率通入吸收塔,用SO2和水进行吸收,吸收后的空气进行循环利用。
①写出吸收反应的离子方程式:
②吹出时,Br2吹出率与吸收塔中SO2流量的关系如图所示。SO2流量过大,Br2吹出率反而下降的原因是

(3)对于较低浓度的溴水,可采用萃取的方法提取Br2。四氯化碳可作为Br2的萃取剂,其原因除四氯化碳不与溴反应外,还有
(4)除了四氯化碳,还可以选择下列
A. 苯 B.酒精 C.氢氧化钠溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】海洋是一个巨大的化学资源宝库。海水资源综合利用的部分过程如下图所示:

回答下列问题:
(1)粗盐中含有 、
、 、
、 等可溶性杂质。根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期沉淀的离子。
等可溶性杂质。根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期沉淀的离子。
(2)操作X为___________ 。
(3)镁可从母液中提取。工业上由无水 制取
制取 的化学方程式为
的化学方程式为________ 。
(4)海水提溴工艺流程主要包括氧化、吹出、吸收、分离等环节。
①向母液中通入适量的 ,其目的是
,其目的是___________ (用离子方程式表示)。
②已知溴的沸点为59℃。上述流程中“操作Ⅰ”应为___________ 。
(5)下列有关说法正确的是___________。

回答下列问题:
(1)粗盐中含有
 、
、 、
、 等可溶性杂质。根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期沉淀的离子。
等可溶性杂质。根据除杂原理,在表中填写“除杂”时依次添加的试剂及其预期沉淀的离子。| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 |  溶液 溶液 |  |
| 步骤2 | ||
| 步骤3 |
(3)镁可从母液中提取。工业上由无水
 制取
制取 的化学方程式为
的化学方程式为(4)海水提溴工艺流程主要包括氧化、吹出、吸收、分离等环节。
①向母液中通入适量的
 ,其目的是
,其目的是②已知溴的沸点为59℃。上述流程中“操作Ⅰ”应为
(5)下列有关说法正确的是___________。
A.海水中含量最多的元素是 、 、 |
| B.海水淡化的主要方法有蒸馏法、电渗析法和离子交换法 |
| C.电解饱和食盐水过程中既发生氧化反应又发生还原反应 |
| D.海水提溴工艺中“吹出”和“吸收”两环节的目的是富集溴 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】从海水(含 )中提溴
)中提溴 ,常用
,常用 做吸收剂。
做吸收剂。
资料:ⅰ. 在碱性溶液中可转化为
在碱性溶液中可转化为 (有强氧化性)和
(有强氧化性)和 。
。
ⅱ. ,深红棕色液体,易挥发。
,深红棕色液体,易挥发。
(1)向 溶液中滴加酚酞,溶液变红,说明
溶液中滴加酚酞,溶液变红,说明 溶液呈
溶液呈_______ 性。
(2)从海水中提溴的流程示意如下:
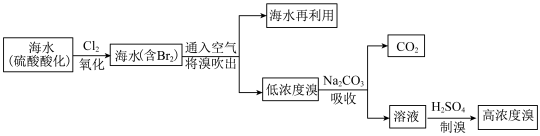
①海水中含大量 、
、 、
、 、
、 、
、 等离子,硫酸酸化能除去的离子是
等离子,硫酸酸化能除去的离子是_______ 。
②“氧化”过程体现出氧化性,
_______  (填“>”或“<”)。
(填“>”或“<”)。
③ 可用热空气吹出,原因是
可用热空气吹出,原因是_______ 。
④低浓度溴中含 、
、 ,吸收过程反应如下:
,吸收过程反应如下:
ⅰ.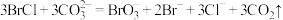
ⅱ._______
⑤“制溴”过程生成 的离子方程式是
的离子方程式是_______ 。
⑥“制溴”过程,用 而不用
而不用 ,可能的原因是
,可能的原因是_______ 。
 )中提溴
)中提溴 ,常用
,常用 做吸收剂。
做吸收剂。资料:ⅰ.
 在碱性溶液中可转化为
在碱性溶液中可转化为 (有强氧化性)和
(有强氧化性)和 。
。ⅱ.
 ,深红棕色液体,易挥发。
,深红棕色液体,易挥发。(1)向
 溶液中滴加酚酞,溶液变红,说明
溶液中滴加酚酞,溶液变红,说明 溶液呈
溶液呈(2)从海水中提溴的流程示意如下:

①海水中含大量
 、
、 、
、 、
、 、
、 等离子,硫酸酸化能除去的离子是
等离子,硫酸酸化能除去的离子是②“氧化”过程体现出氧化性,

 (填“>”或“<”)。
(填“>”或“<”)。③
 可用热空气吹出,原因是
可用热空气吹出,原因是④低浓度溴中含
 、
、 ,吸收过程反应如下:
,吸收过程反应如下:ⅰ.
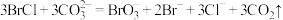
ⅱ.
⑤“制溴”过程生成
 的离子方程式是
的离子方程式是⑥“制溴”过程,用
 而不用
而不用 ,可能的原因是
,可能的原因是
您最近一年使用:0次



