在总压为 的恒容密闭容器中,充入一定量的
的恒容密闭容器中,充入一定量的 和
和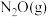 ,发生反应。
,发生反应。
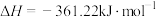 。
。 时
时 的平衡转化率与投料比
的平衡转化率与投料比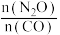 的变化曲线以及投料比
的变化曲线以及投料比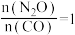 时
时 的平衡转化率与
的平衡转化率与 的变化曲线如图所示。
的变化曲线如图所示。
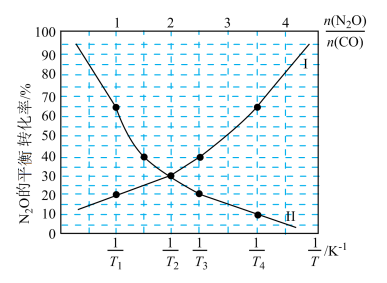
(1)表示 的平衡转化率随
的平衡转化率随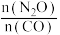 的变化曲线为曲线
的变化曲线为曲线________ (填“Ⅰ”或“Ⅱ”)。
(2)
________  (填“>”或“<”),判断的理由是
(填“>”或“<”),判断的理由是________________________ 。
(3)已知:该反应的标准平衡常数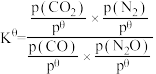 ,其中
,其中 为标准压强(
为标准压强( ),
),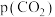 、
、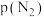 、
、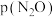 和
和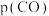 为各组分的平衡分压,则
为各组分的平衡分压,则 时,该反应的标准平衡常数
时,该反应的标准平衡常数
________ (计算结果保留两位有效数字,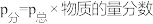 )。
)。
 的恒容密闭容器中,充入一定量的
的恒容密闭容器中,充入一定量的 和
和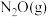 ,发生反应。
,发生反应。
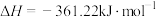 。
。 时
时 的平衡转化率与投料比
的平衡转化率与投料比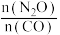 的变化曲线以及投料比
的变化曲线以及投料比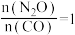 时
时 的平衡转化率与
的平衡转化率与 的变化曲线如图所示。
的变化曲线如图所示。
(1)表示
 的平衡转化率随
的平衡转化率随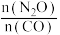 的变化曲线为曲线
的变化曲线为曲线(2)

 (填“>”或“<”),判断的理由是
(填“>”或“<”),判断的理由是(3)已知:该反应的标准平衡常数
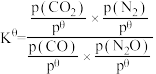 ,其中
,其中 为标准压强(
为标准压强( ),
),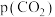 、
、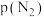 、
、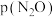 和
和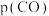 为各组分的平衡分压,则
为各组分的平衡分压,则 时,该反应的标准平衡常数
时,该反应的标准平衡常数
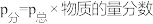 )。
)。
2023高三·全国·专题练习 查看更多[2]
更新时间:2023-02-19 11:28:14
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】硫酸是重要的化工原料,工业制取硫酸最重要的一步反应为: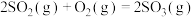

(1)为提高 的转化率,可通入过量
的转化率,可通入过量 ,用平衡移动原理解释其原因:
,用平衡移动原理解释其原因:___________ 。
(2)某兴趣小组在实验室对该反应进行研究,部分实验数据和图象(如图)如下。反应条件:催化剂、一定温度、容积10L。

①实验i中 的转化率为
的转化率为___________ 。
②
___________ 。
③ 、
、 、
、 中,达到化学平衡状态的是
中,达到化学平衡状态的是___________ 。
(3)已知 :
: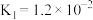 、
、 ,常温下,将
,常温下,将 通入氨水中,当溶液中的
通入氨水中,当溶液中的 时,此时使溶液的PH为
时,此时使溶液的PH为___________ 。
(4) 具有还原性,现用0.001
具有还原性,现用0.001 酸性
酸性 溶液滴定未知浓度的
溶液滴定未知浓度的 溶液,反应的离子方程式是
溶液,反应的离子方程式是 。实验时,应用
。实验时,应用___________ (填“酸式”或“碱式”)滴定管量取酸性高锰酸钾溶液,滴定达到终点的标志是___________ 。
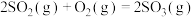

(1)为提高
 的转化率,可通入过量
的转化率,可通入过量 ,用平衡移动原理解释其原因:
,用平衡移动原理解释其原因:(2)某兴趣小组在实验室对该反应进行研究,部分实验数据和图象(如图)如下。反应条件:催化剂、一定温度、容积10L。
| 实验 | 起始物质的量/mol | 平衡时 物质的量/mol 物质的量/mol | ||
 |  |  | ||
| i | 0.2 | 0.1 | 0 | 0.14 |
| ii | 0 | 0 | 0.2 | a |

①实验i中
 的转化率为
的转化率为②

③
 、
、 、
、 中,达到化学平衡状态的是
中,达到化学平衡状态的是(3)已知
 :
: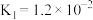 、
、 ,常温下,将
,常温下,将 通入氨水中,当溶液中的
通入氨水中,当溶液中的 时,此时使溶液的PH为
时,此时使溶液的PH为(4)
 具有还原性,现用0.001
具有还原性,现用0.001 酸性
酸性 溶液滴定未知浓度的
溶液滴定未知浓度的 溶液,反应的离子方程式是
溶液,反应的离子方程式是 。实验时,应用
。实验时,应用
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】党的二十大报告提出发展绿色低碳产业,力争在2030年前实现碳达峰、2035年基本实现美丽中国建设目标,下面是CO2转化为高附加值化学品的反应。相关反应的热化学方程式如下:
反应I:CO2(g)+H2(g) H2O(g)+CO(g) ΔH1=+41.0kJ•mol-1
H2O(g)+CO(g) ΔH1=+41.0kJ•mol-1
反应II:CO(g)+2H2(g) CH3OH(g) ΔH2=-90.0kJ•mol-1
CH3OH(g) ΔH2=-90.0kJ•mol-1
反应III:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3
反应IV:CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH4=-165.0kJ•mol-1
CH4(g)+2H2O(g) ΔH4=-165.0kJ•mol-1
反应V:CO2(g)+6H2(g) C2H4(g)+4H2O(g) ΔH5=-122.7kJ•mol-1
C2H4(g)+4H2O(g) ΔH5=-122.7kJ•mol-1
回答下列问题:
(1)反应III一般认为通过反应I、II来实现,则反应III的ΔH3=____ kJ•mol-1。
(2)已知:由实验测得反应I的v正=k正c(CO2)•c(H2),v逆=k逆c(H2O)•c(CO)(k正、k逆为速率常数,其与温度、催化剂有关)。若平衡后升高温度,则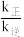
____ (填“增大”“减小”或“不变”)。
(3)CO2在一定条件下催化加氢生成CH3OH,主要发生三个竞争反应(即反应III、IV、V),为了弄清楚催化剂对反应的选择性,在1L恒容密闭容器中充入2.0molCO2和5.3molH2,若测得反应进行相同时间后,有关物质的物质的量随温度的变化如图所示:

①催化剂在较低温度时主要选择反应____ (填“III”、“IV”、“V”),研究发现,若温度过高,三种含碳产物的物质的量均会迅速降低,其主要原因可能是____ 。
②在一定温度下,反应III、IV、V达到平衡,此时测得容器中CH4、C2H4、CH3OH的物质的量分别为0.1mol、0.4mol、0.5mol,该温度下反应III的平衡常数K(III)=____ L2•mol-2(保留两位小数)。
反应I:CO2(g)+H2(g)
 H2O(g)+CO(g) ΔH1=+41.0kJ•mol-1
H2O(g)+CO(g) ΔH1=+41.0kJ•mol-1反应II:CO(g)+2H2(g)
 CH3OH(g) ΔH2=-90.0kJ•mol-1
CH3OH(g) ΔH2=-90.0kJ•mol-1反应III:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH3
CH3OH(g)+H2O(g) ΔH3反应IV:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH4=-165.0kJ•mol-1
CH4(g)+2H2O(g) ΔH4=-165.0kJ•mol-1反应V:CO2(g)+6H2(g)
 C2H4(g)+4H2O(g) ΔH5=-122.7kJ•mol-1
C2H4(g)+4H2O(g) ΔH5=-122.7kJ•mol-1回答下列问题:
(1)反应III一般认为通过反应I、II来实现,则反应III的ΔH3=
(2)已知:由实验测得反应I的v正=k正c(CO2)•c(H2),v逆=k逆c(H2O)•c(CO)(k正、k逆为速率常数,其与温度、催化剂有关)。若平衡后升高温度,则
(3)CO2在一定条件下催化加氢生成CH3OH,主要发生三个竞争反应(即反应III、IV、V),为了弄清楚催化剂对反应的选择性,在1L恒容密闭容器中充入2.0molCO2和5.3molH2,若测得反应进行相同时间后,有关物质的物质的量随温度的变化如图所示:

①催化剂在较低温度时主要选择反应
②在一定温度下,反应III、IV、V达到平衡,此时测得容器中CH4、C2H4、CH3OH的物质的量分别为0.1mol、0.4mol、0.5mol,该温度下反应III的平衡常数K(III)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】含硫化合物在自然界中广泛存在。请按要求回答下列问题:
(1)火山喷发产生 在大气中发生如下反应:
在大气中发生如下反应:
①

②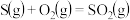
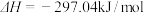 。
。
写出 与
与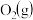 反应产生
反应产生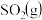 和
和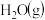 的热化学方程式:
的热化学方程式:_________________ 。
(2) 和
和 混合加热的反应是
混合加热的反应是
①某温度下,在 恒容密闭容器中,通入
恒容密闭容器中,通入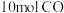 和
和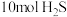 ,平衡时测得
,平衡时测得 的转化率为60%,则该温度下反应的平衡常数
的转化率为60%,则该温度下反应的平衡常数
__________ 。
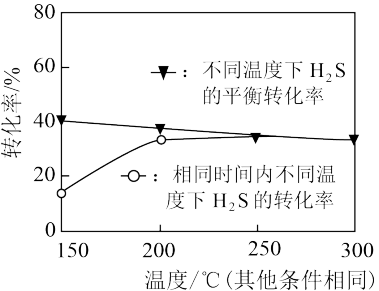
②由图分析该反应的
______ 0(填“<”“>”)。
③如图250℃以前,曲线 变化的可能原因:
变化的可能原因:_____________ 。
(3)工业上可用 碱性溶液脱硫,吸收大气污染物之一
碱性溶液脱硫,吸收大气污染物之一 。
。
①该反应的离子方程式为_______________________________ 。
②用 作催化剂,催化该反应的过程如图示:
作催化剂,催化该反应的过程如图示:
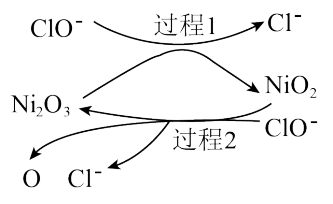
过程2中, 所起的作用是
所起的作用是______________________________ 。(填“氧化剂”“还原剂”或“既作氧化剂又作还原剂”)。
(4)不同温度下 溶液与
溶液与 酸性溶液反应速率的探究:均取
酸性溶液反应速率的探究:均取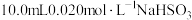 溶液(含少量淀粉)与
溶液(含少量淀粉)与 (过量)酸性溶液混合(已知:
(过量)酸性溶液混合(已知: ),做不同温度下系列实验,
),做不同温度下系列实验,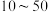 ℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
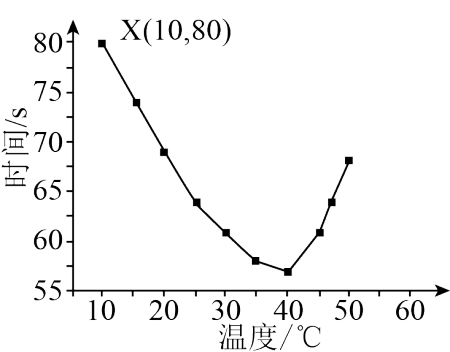
①X点 的反应速率为
的反应速率为______ 。
②40℃之前溶液由无色变蓝速率变快的主要因素是__________________ ;40℃之后溶液由无色变蓝的时间变长,且55℃未观察到溶液变蓝,可能的原因是__________________ 。
(1)火山喷发产生
 在大气中发生如下反应:
在大气中发生如下反应:①


②
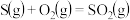
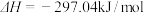 。
。写出
 与
与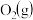 反应产生
反应产生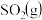 和
和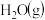 的热化学方程式:
的热化学方程式:(2)
 和
和 混合加热的反应是
混合加热的反应是
①某温度下,在
 恒容密闭容器中,通入
恒容密闭容器中,通入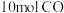 和
和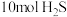 ,平衡时测得
,平衡时测得 的转化率为60%,则该温度下反应的平衡常数
的转化率为60%,则该温度下反应的平衡常数
②由图分析该反应的

③如图250℃以前,曲线
 变化的可能原因:
变化的可能原因:
(3)工业上可用
 碱性溶液脱硫,吸收大气污染物之一
碱性溶液脱硫,吸收大气污染物之一 。
。①该反应的离子方程式为
②用
 作催化剂,催化该反应的过程如图示:
作催化剂,催化该反应的过程如图示:
过程2中,
 所起的作用是
所起的作用是(4)不同温度下
 溶液与
溶液与 酸性溶液反应速率的探究:均取
酸性溶液反应速率的探究:均取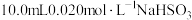 溶液(含少量淀粉)与
溶液(含少量淀粉)与 (过量)酸性溶液混合(已知:
(过量)酸性溶液混合(已知: ),做不同温度下系列实验,
),做不同温度下系列实验,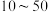 ℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
℃间溶液由无色变蓝的时间,55℃未观察到溶液变蓝,实验记录结果如图所示:
①X点
 的反应速率为
的反应速率为②40℃之前溶液由无色变蓝速率变快的主要因素是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】在恒容密闭容器中合成甲醇;CO(g)+2H2(g) CH3OH(g)。
CH3OH(g)。

(1)图1中t3时刻改变的条件是____ ,t5时刻改变的条件是____ .
(2)判断反应达到化学平衡状态的依据是____ (填序号)。
a.生成CH3OH的速率与消耗CO的速率相等
b.混合气体的密度不变
c.混合气体的总物质的量不变
d.CH3OH、CO、H2的浓度都不再发生变化
(3)如图2表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、B两点的反应速率:A____ B(填“>”“;”或“<”,下同),A、C两点的化学平衡常数:A____ C。
(4)恒容条件下,下列措施中能使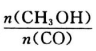 增大的有
增大的有_____ 。
A.升高温度 B.充入He气 C.使用催化剂 D.再充入1molCO和2molH2
(5)在某温度下,容积均为2L的三个密闭容器中-按不同方式投入反应物。初始投料与各容器达到平衡时的有关数据如下:
下列说法正确的是____ (填字母)。
A.在该温度下,甲容器中从反应开始到平衡所需时间为4min,则v(H2)为0.25 mol/(L·min)
B.转化率:α3 >α1,平衡时n(CH3OH):n3>1.0mol
C.丙容器中,平衡后将容器的容积压缩到原来的1/2,平衡常数K增大
D.体系的压强:p3<2p1=2P2
 CH3OH(g)。
CH3OH(g)。
(1)图1中t3时刻改变的条件是
(2)判断反应达到化学平衡状态的依据是
a.生成CH3OH的速率与消耗CO的速率相等
b.混合气体的密度不变
c.混合气体的总物质的量不变
d.CH3OH、CO、H2的浓度都不再发生变化
(3)如图2表示在温度分别为T1、T2时,平衡体系中H2的体积分数随压强变化曲线,A、B两点的反应速率:A
(4)恒容条件下,下列措施中能使
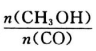 增大的有
增大的有A.升高温度 B.充入He气 C.使用催化剂 D.再充入1molCO和2molH2
(5)在某温度下,容积均为2L的三个密闭容器中-按不同方式投入反应物。初始投料与各容器达到平衡时的有关数据如下:
实验 | 甲 | 乙 | 丙 |
初始投料 | 2molH2、1molCO | 1molCH3OH | 4molH2、2molCO |
平衡时n(CH3OH) | 0.5mol | n2 | n3 |
体系的压强 | p1 | p2 | p3 |
反应物的转化率 | a1 | a2 | a3 |
A.在该温度下,甲容器中从反应开始到平衡所需时间为4min,则v(H2)为0.25 mol/(L·min)
B.转化率:α3 >α1,平衡时n(CH3OH):n3>1.0mol
C.丙容器中,平衡后将容器的容积压缩到原来的1/2,平衡常数K增大
D.体系的压强:p3<2p1=2P2
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①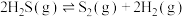
 kJ·mol
kJ·mol
②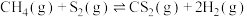
 kJ·mol
kJ·mol
计算反应③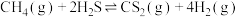 的
的
_______ kJ·mol ;反应③能够自发的条件是
;反应③能够自发的条件是_______ (填“低温”或“高温”或“任何温度”)。
(2)在1000℃时,反应①的 kJ·mol
kJ·mol ,反应③的
,反应③的 kJ·mol
kJ·mol 。已知
。已知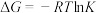 (R为常数,T为温度,K为平衡常数),据此分析反应③处理
(R为常数,T为温度,K为平衡常数),据此分析反应③处理 的工艺方法的优点是
的工艺方法的优点是_______ 。
(3)在不同温度、反应压强为100 kPa,进料比 分别为a、b、c的条件下,反应③
分别为a、b、c的条件下,反应③ 平衡转化率如下图所示,则a、b、c由大到小的顺序为
平衡转化率如下图所示,则a、b、c由大到小的顺序为_______ ;

温度越高,反应③ 平衡转化率越大的原因是
平衡转化率越大的原因是_______ 。
(4)在T℃、p kPa条件下,将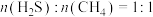 的混合气进行反应③,同时发生副反应
的混合气进行反应③,同时发生副反应 ,达到平衡时,
,达到平衡时, 的转化率为80%,
的转化率为80%, 的转化率为90%,则反应③的
的转化率为90%,则反应③的
_______  (列出计算式即可)。
(列出计算式即可)。
(1)已知下列反应的热化学方程式:
①
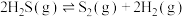
 kJ·mol
kJ·mol
②
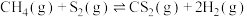
 kJ·mol
kJ·mol
计算反应③
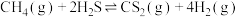 的
的
 ;反应③能够自发的条件是
;反应③能够自发的条件是(2)在1000℃时,反应①的
 kJ·mol
kJ·mol ,反应③的
,反应③的 kJ·mol
kJ·mol 。已知
。已知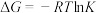 (R为常数,T为温度,K为平衡常数),据此分析反应③处理
(R为常数,T为温度,K为平衡常数),据此分析反应③处理 的工艺方法的优点是
的工艺方法的优点是(3)在不同温度、反应压强为100 kPa,进料比
 分别为a、b、c的条件下,反应③
分别为a、b、c的条件下,反应③ 平衡转化率如下图所示,则a、b、c由大到小的顺序为
平衡转化率如下图所示,则a、b、c由大到小的顺序为
温度越高,反应③
 平衡转化率越大的原因是
平衡转化率越大的原因是(4)在T℃、p kPa条件下,将
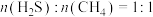 的混合气进行反应③,同时发生副反应
的混合气进行反应③,同时发生副反应 ,达到平衡时,
,达到平衡时, 的转化率为80%,
的转化率为80%, 的转化率为90%,则反应③的
的转化率为90%,则反应③的
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物是形成光化学烟雾和酸雨的重要原因。人们研究了诸多有关氮氧化物的性质,请回答下列问题:
(1)处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) K1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) K2
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) K3
K1、K2、K3依次为三个反应的平衡常数,则K3=__ (用K1、K2表示)。
(2)在恒容密闭容器中通入等物质的量的CO和NO,在一定条件下发生反应:2CO(g)+2NO(g) N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
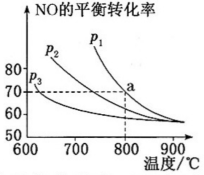
①对于气相反应,用某组分(B)的平衡分压强p(B)代替物质的量浓度c(B)也可表示平衡常数kp,如果p1=1.65MPa,求a点的平衡常数kp=__ (MPa)−1(结果保留3位有效数字,分压=总压×物质的量分数)。
②为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制了2条速率—浓度关系曲线:v正~c(NO)和v逆~c(CO2)则:与曲线v正~c(NO)相对应的是图中曲线__ (填“甲”或“乙”)。当降低反应体系的温度,反应一段时间后,重新达到平衡,v正和v逆相应的平衡点分别为___ (填字母)。

(3)利用电化学原理,将NO2、O2和熔融的KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72−的废水,如图所示;电解过程中溶液发生反应:Cr2O72−+6Fe2++14H+=2Cr3++6Fe3++7H2O。甲电池工作时,Y是气体,可循环使用。则石墨I附近发生的电极反应式为___ 。

(4)已知H3PO4为三元酸,Ka1=7.0×10−3mol·L−1,Ka2=6.2×10−8mol·L−1,Ka3=4.5×10−13mol·L−1。则Na2HPO4水溶液呈__ 。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) K1
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) K2
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) K3
K1、K2、K3依次为三个反应的平衡常数,则K3=
(2)在恒容密闭容器中通入等物质的量的CO和NO,在一定条件下发生反应:2CO(g)+2NO(g)
 N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
N2(g)+2CO2(g),测得NO的平衡转化率与温度及压强的关系如图所示:
①对于气相反应,用某组分(B)的平衡分压强p(B)代替物质的量浓度c(B)也可表示平衡常数kp,如果p1=1.65MPa,求a点的平衡常数kp=
②为探究速率与浓度的关系,该实验中,根据相关实验数据,粗略绘制了2条速率—浓度关系曲线:v正~c(NO)和v逆~c(CO2)则:与曲线v正~c(NO)相对应的是图中曲线

(3)利用电化学原理,将NO2、O2和熔融的KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72−的废水,如图所示;电解过程中溶液发生反应:Cr2O72−+6Fe2++14H+=2Cr3++6Fe3++7H2O。甲电池工作时,Y是气体,可循环使用。则石墨I附近发生的电极反应式为

(4)已知H3PO4为三元酸,Ka1=7.0×10−3mol·L−1,Ka2=6.2×10−8mol·L−1,Ka3=4.5×10−13mol·L−1。则Na2HPO4水溶液呈
您最近一年使用:0次



