某温度下,Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改变溶液pH,金属阳离子浓度的变化如图所示。据图分析,下列判断错误的是
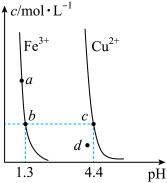

| A.Ksp[Fe(OH)3]<Ksp[Cu(OH)2] |
| B.c、d两点代表的溶液中c(H+)与c(OH-)乘积不相等 |
| C.加适量NH4Cl固体可使溶液由a点变到b点 |
| D.在b、c两点代表的溶液中Fe(OH)3、Cu(OH)2均达到饱和 |
更新时间:2023-03-01 20:14:15
|
相似题推荐
多选题
|
较难
(0.4)
解题方法
【推荐1】常温下,向25 mL0.12 mol/LAgNO3溶液中逐滴加入一定浓度的氨水,先出现沉淀,继续滴加沉淀溶解。该过程中加大氨水的体积V与溶液中lg[c(H+)/c(OH- )]的关系如图所示。已知e点对应的溶液迅速由浑浊变得澄清,且此时溶液中c(Ag+)与c(NH3)均约为2×10-3 mol/L。下列叙述错误的是


| A.a点对应溶液呈酸性的原因是AgNO3水解 |
B.b点对应溶液中:c(Ag+)+c{[Ag(NH3)2]+}> c(NO ) ) |
| C.cd段加入的氨水主要用于沉淀的生成和溶解 |
D.由e点可知,反应Ag++2NH3 [Ag(NH3)2]+的平衡常数的数量级为105 [Ag(NH3)2]+的平衡常数的数量级为105 |
您最近一年使用:0次
【推荐2】 时,
时, 的
的 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
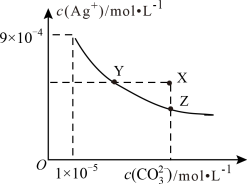
 时,
时, 的
的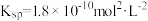 ,
, 在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是
在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是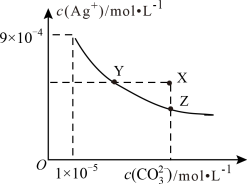
A. 的 的 为 为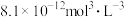 |
B.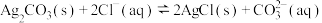 的平衡常数 的平衡常数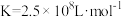 |
C.向 的饱和溶液中加入 的饱和溶液中加入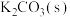 ,可使 ,可使 增大(由Y点到X点) 增大(由Y点到X点) |
D.向同浓度的 和 和 的混合溶液中滴入 的混合溶液中滴入 溶液, 溶液, 先沉淀 先沉淀 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐1】硫酸工业中用NaOH溶液吸收 尾气得到硫酸盐的过程如图。室温下,用
尾气得到硫酸盐的过程如图。室温下,用 溶液吸收
溶液吸收 (忽略溶液体积变化),所得溶液中含硫物种的浓度
(忽略溶液体积变化),所得溶液中含硫物种的浓度 。室温下,
。室温下,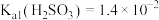 ,
,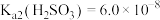 ,
,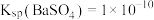 。
。
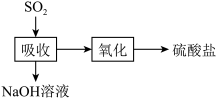
下列说法正确的是
 尾气得到硫酸盐的过程如图。室温下,用
尾气得到硫酸盐的过程如图。室温下,用 溶液吸收
溶液吸收 (忽略溶液体积变化),所得溶液中含硫物种的浓度
(忽略溶液体积变化),所得溶液中含硫物种的浓度 。室温下,
。室温下,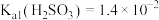 ,
,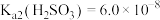 ,
,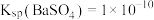 。
。
下列说法正确的是
A.若“吸收”所得溶液中含硫物种的浓度 ,则溶液呈酸性 ,则溶液呈酸性 |
B.若“吸收”所得溶液 ,则溶液中 ,则溶液中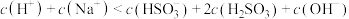 |
C.若“吸收”所得溶液 ,则“氧化”时主要反应的离子方程式为 ,则“氧化”时主要反应的离子方程式为 |
D.将“氧化”所得溶液用 溶液调节至 溶液调节至 ,再与 ,再与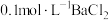 溶液等体积混合,最终溶液中 溶液等体积混合,最终溶液中 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】在“水质研学行动”中,科学兴趣小组对某地矿泉水进行了检测。室温下,测得该水中p(X)与pOH关系如图所示[已知:p(X)=-lgc(X),X为H2CO3、 、
、 或Ca2+]。下列说法错误的是
或Ca2+]。下列说法错误的是

 、
、 或Ca2+]。下列说法错误的是
或Ca2+]。下列说法错误的是
| A.曲线③代表p(Ca2+)随pOH的变化 | B.该温度下,pH+ p( p( )=10.8 )=10.8 |
| C.该温度下的Ksp(CaCO3)=1×10-9.2 | D.当p(Ca2+)=6.1时,p( )=1.8 )=1.8 |
您最近一年使用:0次

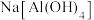 溶液中滴入
溶液中滴入 溶液
溶液 比
比 悬浊液中加入适量
悬浊液中加入适量 固体
固体 水解显酸性,溶解了
水解显酸性,溶解了 溶液和淀粉
溶液和淀粉 溶液
溶液 气体的容器
气体的容器 的方向移动
的方向移动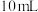 、浓度均为
、浓度均为 的
的 和
和 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液
溶液,滴加过程中溶液 和
和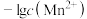 与滴入
与滴入 )的关系如图所示。[已知:
)的关系如图所示。[已知: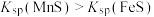 ,
, ,忽略溶液混合时温度和体积的变化],下列说法错误的是
,忽略溶液混合时温度和体积的变化],下列说法错误的是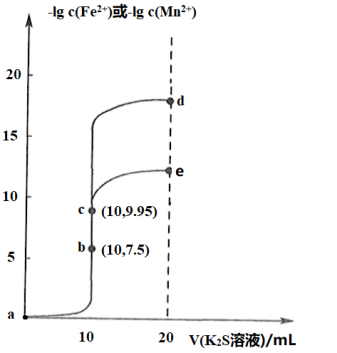
 可除去
可除去