如表为元素周期表的一部分,其中的编号代表对应的不同元素。
请回答下列问题:
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为______ 。
(2)基态③原子中电子占据最高能级的符号是______ ,占据该能级电子的电子云轮廓图为______ 形。
(3)写出②的氧化物与NaOH溶液反应的化学方程式:______ 。
(4)元素④⑤⑥的电负性:______>______>______(填元素符号)______ 。
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式______ 。
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素是______ 。
(7)⑨基态原子的简化电子排布式为______ ,在周期表中的位置______ 。
(8)⑩基态原子的价层电子轨道表示式为______ ,位于周期表的______ 区。
| ① | |||||||||||||||||
| ② | ③ | ④ | ⑤ | ⑥ | |||||||||||||
| ⑦ | ⑧ | ||||||||||||||||
| ⑨ | ⑩ | ||||||||||||||||
(1)某元素的价电子排布式为nsnnpn+1,该元素与元素①形成的最简单化合物的电子式为
(2)基态③原子中电子占据最高能级的符号是
(3)写出②的氧化物与NaOH溶液反应的化学方程式:
(4)元素④⑤⑥的电负性:______>______>______(填元素符号)
(5)元素⑤(设为字母X)和元素⑧(设为字母Y)形成的化合物XY3与水反应产生有漂白性的物质,写出该反应的化学方程式
(6)如表是第三周期元素中某种元素的部分电离能,由此可判断该元素是
| 元素 | 电离能(kJ•mol-1) | ||||
| I1 | I2 | I3 | I4 | I5 | |
| 某种元素 | 578 | 1817 | 2745 | 11575 | 14830 |
(8)⑩基态原子的价层电子轨道表示式为
更新时间:2023-03-05 17:42:23
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】已知:W、X、Y、Z、T 均为短周期元素,且原子半径依次增大。请填空:
(1)W、Z 是形成化合物种类最多的两种元素,写出 Z 的核外电子的轨道表示式______________ 。
(2)化合物 YW3 溶于水能使酚酞变红,用方程式表示酚酞变红的原因____ 。
(3)元素 T 的原子中电子占据 7 根轨道,则 T 在元素周期表____ 周期___ 族; T 的化合物 TY 熔融时不导电,常用作砂轮与耐高温材料,由此推知,它属于____ 。
a 离子晶体 b 原子晶体 c 分子晶体 d 无法判断
(4)YX3 与 YW3 具有相同的分子空间构型,YX3 属于______ (填“极性”、“非极性”)分子,其中 Y 的化合价为____ 。
(1)W、Z 是形成化合物种类最多的两种元素,写出 Z 的核外电子的轨道表示式
(2)化合物 YW3 溶于水能使酚酞变红,用方程式表示酚酞变红的原因
(3)元素 T 的原子中电子占据 7 根轨道,则 T 在元素周期表
a 离子晶体 b 原子晶体 c 分子晶体 d 无法判断
(4)YX3 与 YW3 具有相同的分子空间构型,YX3 属于
您最近一年使用:0次
【推荐2】现有原子序数小于20的A,B,C,D,E,F6种元素,它们的原子序数依次增大,已知B元素是地壳中含量最多的元素;A和C的价电子数相同,B和D的价电子数也相同,且A和C两元素原子核外电子数之和是B,D两元素原子核内质子数之和的1/2;C,D,E三种元素的基态原子具有相同的电子层数,且E原子的p轨道上电子数比D原子的p轨道上多一个电子;6种元素的基态原子中,F原子的电子层数最多且和A处于同一主族。回答下列问题。
(1)用电子式表示C和E形成化合物的过程________________ 。
(2)写出基态F原子核外电子排布式__________________ 。
(3)写出A2D的电子式________ ,其分子中________ (填“含”或“不含”)σ键,________ (填“含”或“不含”)π键。
(4)A,B,C共同形成的化合物化学式为________ ,其中化学键的类型有________ 。
(1)用电子式表示C和E形成化合物的过程
(2)写出基态F原子核外电子排布式
(3)写出A2D的电子式
(4)A,B,C共同形成的化合物化学式为
您最近一年使用:0次
【推荐3】有五种短周期元素,它们的结构或性质等信息如下表所示:
请根据表中信息回答下列问题:
(1)A元素基态原子的核外电子排布式为______________ 。
(2)B元素在元素周期表中的位置为_________ ;离子半径:B___________ (填“>”或“<”)A。
(3)C元素基态原子的核外电子轨道表示式为________ ,其原子核外有_______ 个未成对电子,能量最高的电子排布在_______ 轨道上。
(4)D元素基态原子的核外电子排布式为______  的结构示意图为
的结构示意图为__________ 。
(5)C、E元素的第一电离能的大小关系是_______ (用元素符号表示)。
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是______ (填元素符号),CD3与水反应后的产物是______ (填化学式)。
| 元素 | 结构或性质 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的杀菌消毒剂 |
| E | 元素原子的L电子层上有2对成对电子 |
(1)A元素基态原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素基态原子的核外电子轨道表示式为
(4)D元素基态原子的核外电子排布式为
 的结构示意图为
的结构示意图为(5)C、E元素的第一电离能的大小关系是
(6)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】第4周期的A、B、C、D四种元素,其最外层电子数依次为1、2、2、7。其原子序数按A、B、C、D顺序增大,已知A和B的次外层电子数均为8,而C与D的次外层电子数均为18,根据结构用元素符号或化学式填空:
(1)写出元素名称:A____ 、B_____ 、C _____ 、D ____ 。
(2)D的简单离子的电子排布式_______________ 。
(3)元素的氢氧化物碱性最强的是______________ 。
(4)B原子与D原子间形成化合物的电子式为____________ 。
(5)写出A、B的第一电离能大小____________________ 。
(6)写出C基态原子的外围电子排布图______________________ 。
(1)写出元素名称:A
(2)D的简单离子的电子排布式
(3)元素的氢氧化物碱性最强的是
(4)B原子与D原子间形成化合物的电子式为
(5)写出A、B的第一电离能大小
(6)写出C基态原子的外围电子排布图
您最近一年使用:0次
【推荐2】X、T、Y、Z为1-36号元素,且原子序数依次增大,四种元素的性质或结构信息如表。请根据信息回答下列问题。
(1)写出元素T原子外围电子的轨道表示式____ ;写出元素X的气态氢化物的电子式____ ;写出Z元素原子的外围电子排布式____ ;元素Y的原子核外共有____ 种形状不同的电子云。
(2)Y元素原子的第一电离能____ 镁(填“>”“<”“=”),从结构上分析,其理由是:___ 。
(3)元素T与氟元素相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ (填序号字母)。
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
| 元素 | T | X | Y | Z |
| 性质结构信息 | 人体内含量最多的 元素,且其单质是 最常见的助燃剂 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质性质稳定,但其原子较活泼 | 第3周期元素的简单离子中半径最小 | 第4周期元素,M电子层为全充满状态,最外层只有二个电子的原子 |
(2)Y元素原子的第一电离能
(3)元素T与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
【推荐3】治疗血栓的药物阿派沙班(VII)的合成路线如图所示,请回答下列问题:
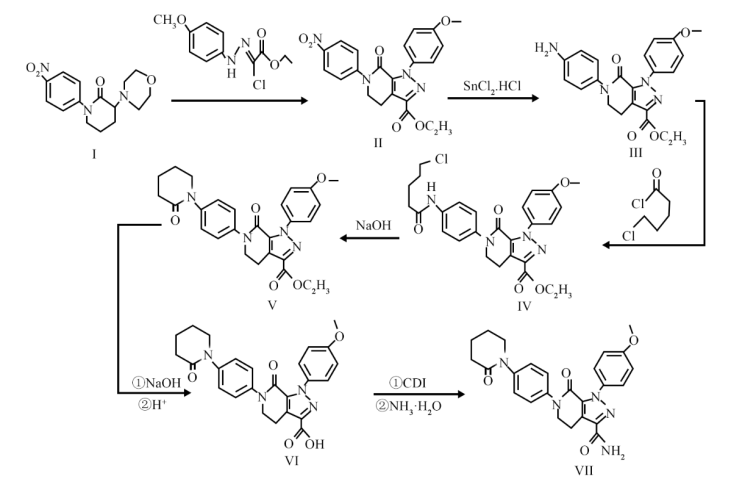
(1)已知:Sn与C同主族,则基态Sn原子的价层电子轨道表示式为_______ 。
(2) 具有较强的还原性,易被
具有较强的还原性,易被 氧化成
氧化成 ,
, 中Sn原子的杂化类型为
中Sn原子的杂化类型为_______ , 分子的空间结构为
分子的空间结构为_______ 。
(3)写出化合物I中所有含氧官能团的名称:_______ 。
(4)II→III的反应类型为____ 。将物质IV简记为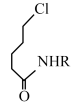 ,则IV→V的化学方程式为
,则IV→V的化学方程式为____ 。
(5)请写出以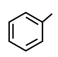 和
和 (
( )为原料合成
)为原料合成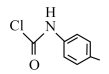 的路线
的路线____ (其他试剂任选)。

(1)已知:Sn与C同主族,则基态Sn原子的价层电子轨道表示式为
(2)
 具有较强的还原性,易被
具有较强的还原性,易被 氧化成
氧化成 ,
, 中Sn原子的杂化类型为
中Sn原子的杂化类型为 分子的空间结构为
分子的空间结构为(3)写出化合物I中所有含氧官能团的名称:
(4)II→III的反应类型为
 ,则IV→V的化学方程式为
,则IV→V的化学方程式为(5)请写出以
 和
和 (
( )为原料合成
)为原料合成 的路线
的路线
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐1】某钙钛型复合氧化物如图所示,以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应。

(1)用A,B,O表示这类特殊晶体的化学式:_______ 。
(2)已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁—铁磁、铁磁—顺磁及金属—半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为_______ 。
(3)Mn的外围电子排布式为_______ 。
(4)下列有关说法正确的是_______。


(1)用A,B,O表示这类特殊晶体的化学式:
(2)已知La为+3价,当被钙等二价元素A替代时,可形成复合钙钛矿化合物La1-xAxMnO3(x<0.1),此时一部分锰转变为+4价。导致材料在某一温度附近有反铁磁—铁磁、铁磁—顺磁及金属—半导体的转变,则La1-xAxMnO3中三价锰与四价锰的物质的量之比为
(3)Mn的外围电子排布式为
(4)下列有关说法正确的是_______。

| A.镧、锰、氧分别位于周期表f、d、p区 |
| B.氧的第一电离能比氮的第一电离能大 |
| C.锰的电负性为1.59,Cr的电负性为1.66,说明锰的金属性比铬强 |
| D.铬的堆积方式与钾相同,则其堆积方式如图所示 |
您最近一年使用:0次
【推荐2】X、T、Y、Z为1-36号元素,且原子序数依次增大,四种元素的性质或结构信息如表。请根据信息回答下列问题。
(1)写出元素T原子外围电子的轨道表示式____ ;写出元素X的气态氢化物的电子式____ ;写出Z元素原子的外围电子排布式____ ;元素Y的原子核外共有____ 种形状不同的电子云。
(2)Y元素原子的第一电离能____ 镁(填“>”“<”“=”),从结构上分析,其理由是:___ 。
(3)元素T与氟元素相比,非金属性较强的是____ (用元素符号表示),下列表述中能证明这一事实的是____ (填序号字母)。
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
| 元素 | T | X | Y | Z |
| 性质结构信息 | 人体内含量最多的 元素,且其单质是 最常见的助燃剂 | 单质为双原子分子,分子中含有3对共用电子对,常温下单质性质稳定,但其原子较活泼 | 第3周期元素的简单离子中半径最小 | 第4周期元素,M电子层为全充满状态,最外层只有二个电子的原子 |
(2)Y元素原子的第一电离能
(3)元素T与氟元素相比,非金属性较强的是
a.常温下氟气的颜色比T单质的颜色深
b.氟气与T的氢化物剧烈反应,产生T的单质
c.氟与T形成的化合物中T元素呈正价态
d.比较两元素的单质与氢气化合时得电子的数目
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】已知元素A、B、C、D、E、F均属前四周期且原子序数依次增大,A的p能级电子数是s能级的一半,C的基态原子2p轨道有2个未成对电子;C与D形成的化合物中C显正化合价;E的M层电子数是N层电子数的4倍,F的内部各能层均排满,且最外层电子数为1。请回答下列问题。
(1)C原子基态时电子排布式为______ 。
(2)B、C两种元素第一电离能为______ >______ (用元素符号表示)。试解释其原因: ______ 。
(3)任写一种与AB-离子互为等电子体的离子______ 。
(4)B与C形成的四原子阴离子的立体构型为______ ,其中B原子的杂化类型是______ 。
(5)F(OH)2难溶于水,易溶于氨水,写出其溶于氨水的离子方程式______ 。
(6)D和E形成的化合物的晶胞结构如图,其化学式为______ ;∠EDE= ______ ;E的配位数是______ ;已知晶体的密度为ρg·cm-3,阿伏加德罗常数为NA,则晶胞边长a=______ cm。(用ρ、NA的计算式表示)

(1)C原子基态时电子排布式为
(2)B、C两种元素第一电离能为
(3)任写一种与AB-离子互为等电子体的离子
(4)B与C形成的四原子阴离子的立体构型为
(5)F(OH)2难溶于水,易溶于氨水,写出其溶于氨水的离子方程式
(6)D和E形成的化合物的晶胞结构如图,其化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】我国科学家借助自主研制的新型钨钴铁合金催化剂攻克了单壁碳纳米管结构的可控制备难题。海底金属软泥是在海底覆盖着的一层红棕色沉积物,蕴藏着大量的金属资源, 含有钨、铁、锰、锌、钴等金属元素。
(1)基态钴原子的价电子排布图为___________ 。单壁碳纳米管可看作石墨烯沿一定方向卷曲而成的空心圆柱体,其碳原子的杂化方式为___________ 。
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲硫醛分子属___________ (填“极性”或“非极性”)分子,其中心原子的VSEPR模型名称为___________ 。
(3)六羰基钨[W(CO)6]的熔点为172 ℃,是一种重要的无机金属配合物,可溶于大多数有机溶剂。三种组成元素的电负性由大到小的顺序为___________ (用元素符号表示)。配体CO中与W形成配位键的原子是C而不是O,原因是___________ 。
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是___________(填字母)。
(1)基态钴原子的价电子排布图为
(2)纳米结构氧化钴可在室温下将甲硫醛(CH2S)完全催化氧化,甲硫醛分子属
(3)六羰基钨[W(CO)6]的熔点为172 ℃,是一种重要的无机金属配合物,可溶于大多数有机溶剂。三种组成元素的电负性由大到小的顺序为
(4)多原子分子中各原子若在同一平面内,且有相互平行的p轨道,则p电子可在多个原子间运动,形成“离域π键”。下列物质中存在“离域π键”的是___________(填字母)。
| A.苯 | B.二氧化硫 |
| C.四氯化碳 | D.环己烷 |
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】如图是元素周期表的一部分,根据元素在周期表中的位置,回答下列问题:

(1)由②③④形成的简单离子半径由小到大顺序是_________ (填化学用语)。
(2)元素④的最高价氧化物对应的水化物和元素⑤的最高价氧化物对应的水化物反应的离子方程式为_______ ,⑦的单质和⑨的单质反应的化学方程式为________ ,冶炼单质⑤的方法是_______ (用化学方程式表示)。
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式____ ,该分子中含有的共价键类型为_____ (填“极性共价键”或“非极性共价键”) 。
(4)下列有关性质的比较正确且能用元素周期律解释的是___ (填标号)
A.电负性:②>③ B.最高价氧化物对应的水化物的碱性:④>⑤
(5)③的简单氢化物的沸点高于⑦的简单氢化物的沸点的原因是_______ 。

(1)由②③④形成的简单离子半径由小到大顺序是
(2)元素④的最高价氧化物对应的水化物和元素⑤的最高价氧化物对应的水化物反应的离子方程式为
(3)元素⑦⑧可形成原子个数比为1:1的共价化合物,分子中各原子最外层均达到8电子的稳定结构,试写出其结构式
(4)下列有关性质的比较正确且能用元素周期律解释的是
A.电负性:②>③ B.最高价氧化物对应的水化物的碱性:④>⑤
(5)③的简单氢化物的沸点高于⑦的简单氢化物的沸点的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是_______ ;基态硫原子的价电子排布式是________ 。
(2)基态铁原子有____ 个未成对电子,基态 的价电子排布图为
的价电子排布图为______ 。
(3) 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是______ ,电负性最大的是______ 。
(4)下列说法错误的是_______。
(5)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。 的电子式为
的电子式为______ ,结构式为_______ 。
② 中存在
中存在_____ 键和______ 键,为_____ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)
 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是(4)下列说法错误的是_______。
A.元素的电负性: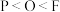 | B.元素的第一电离能: |
C.离子半径: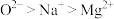 | D.原子的未成对电子数: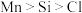 |
(5)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。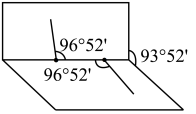
 的电子式为
的电子式为②
 中存在
中存在
您最近一年使用:0次



