依据原子结构知识回答下列问题。
(1)基态硅原子的电子排布式是_______ ;基态硫原子的价电子排布式是________ 。
(2)基态铁原子有____ 个未成对电子,基态 的价电子排布图为
的价电子排布图为______ 。
(3) 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是______ ,电负性最大的是______ 。
(4)下列说法错误的是_______。
(5)过氧化氢( )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。 的电子式为
的电子式为______ ,结构式为_______ 。
② 中存在
中存在_____ 键和______ 键,为_____ (填“极性”或“非极性”)分子。
(1)基态硅原子的电子排布式是
(2)基态铁原子有
 的价电子排布图为
的价电子排布图为(3)
 、K、O、F四种元素中第一电离能最小的是
、K、O、F四种元素中第一电离能最小的是(4)下列说法错误的是_______。
A.元素的电负性: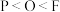 | B.元素的第一电离能: |
C.离子半径: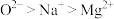 | D.原子的未成对电子数: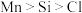 |
(5)过氧化氢(
 )是一种医用消毒杀菌剂。已知
)是一种医用消毒杀菌剂。已知 的结构如图所示。
的结构如图所示。 不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个
不是直线形的,两个氢原子犹如在半展开的书的两面纸上,书面角为93°52′,而两个 与
与 的夹角均为96°52′。
的夹角均为96°52′。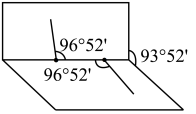
 的电子式为
的电子式为②
 中存在
中存在
更新时间:2024-05-04 21:18:46
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】金属镓有“电子工业脊梁”的美誉,它与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示:

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为____________ CO2的电子式为_____________________
(2)下列有关Al、Ga的说法不正确的是______
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序_____________
(4)步骤二中不能通入过量的CO2,理由_________________ (用离子方程式表示)
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是_______
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式__________________________________
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式__________________

(1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为
(2)下列有关Al、Ga的说法不正确的是
A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3
C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga
(3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序
(4)步骤二中不能通入过量的CO2,理由
(5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+)
①下列有关电解精炼说法正确的是
A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+
B.电解过程中,阳极质量的减少与阴极质量的增加相等
C.在阴极除了析出高纯度的镓之外,还有H2产生
D.电解后,电解槽底部的阳极泥中只有Cu和Fe
②阴极析出高纯度镓的电极反应式
(6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】 是一种重要的无机化合物,可作为食盐中的补碘剂。利用“
是一种重要的无机化合物,可作为食盐中的补碘剂。利用“ 氧化法”制备
氧化法”制备 工艺流程如图所示:
工艺流程如图所示:
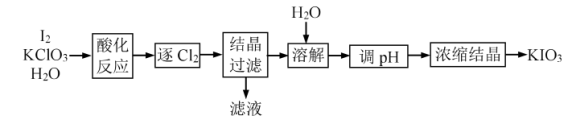
已知:“酸化反应”所得产物有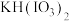 、
、 和
和 。
。
回答下列问题:
(1) 在元素周期表中的位置是
在元素周期表中的位置是_______ ; 的电子式为
的电子式为_______ ; 中两种离子的半径大小关系为
中两种离子的半径大小关系为_______ 。
(2)将“酸化反应”的化学方程式补充完整。
______
(3)“逐 ”采用的方法是
”采用的方法是_______ 。
(4)“滤液”中的溶质主要是_______ 。
(5)“调 ”时,加入的试剂为
”时,加入的试剂为_______ 溶液。
(6)“ 氧化法”的明显不足之处有
氧化法”的明显不足之处有_______ (任写一条)。
 是一种重要的无机化合物,可作为食盐中的补碘剂。利用“
是一种重要的无机化合物,可作为食盐中的补碘剂。利用“ 氧化法”制备
氧化法”制备 工艺流程如图所示:
工艺流程如图所示:
已知:“酸化反应”所得产物有
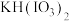 、
、 和
和 。
。回答下列问题:
(1)
 在元素周期表中的位置是
在元素周期表中的位置是 的电子式为
的电子式为 中两种离子的半径大小关系为
中两种离子的半径大小关系为(2)将“酸化反应”的化学方程式补充完整。

(3)“逐
 ”采用的方法是
”采用的方法是(4)“滤液”中的溶质主要是
(5)“调
 ”时,加入的试剂为
”时,加入的试剂为(6)“
 氧化法”的明显不足之处有
氧化法”的明显不足之处有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】五种短周期主族元素X、Y、Z、E、F,原子序数依次增大.X是非金属元素,且最外层电子数与其周期数相同;Y的最外层电子数是其所在周期数的2倍;Z的最外层电子数与最内层电子数之比为1∶3;E+与Z的最简单离子具有相同的电子数;X单质在F单质中燃烧,有苍白色火焰。回答下列问题:
(1)Z在周期表中的位置是______ 。
(2)E2Z2的电子式为______ 。
(3)XFZ的结构式为______ 。
(4)元素Z、E、F形成的最简单离子的半径由大到小为______ (用离子符号表示)。
(5)Y、Z的最简单气态氢化物的稳定性是:_______>_______(用化学式表示)。______
(6)设计一个简单的实验证明F和Y的非金属性强弱______ (用化学方程式表示)。
(1)Z在周期表中的位置是
(2)E2Z2的电子式为
(3)XFZ的结构式为
(4)元素Z、E、F形成的最简单离子的半径由大到小为
(5)Y、Z的最简单气态氢化物的稳定性是:_______>_______(用化学式表示)。
(6)设计一个简单的实验证明F和Y的非金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】位于前四周期的A、B、C、D、E五种元素。其相关信息如下:
(1)写出E元素原子基态时的电子排布式___________ 。
(2)B的氢化物沸点比同主族下一周期元素的氢化物沸点___________ (填“高”或“低”)。
(3) 分子中C原子的杂化轨道类型是
分子中C原子的杂化轨道类型是___________ 。
(4)A、C、E三种元素可形成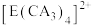 配离子,其中存在的化学键类型
配离子,其中存在的化学键类型___________ (填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若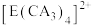 具有对称的空间构型,且当
具有对称的空间构型,且当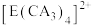 中的两个
中的两个 被两个
被两个 取代时,能得到两种不同结构的产物,则
取代时,能得到两种不同结构的产物,则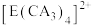 的空间构型为
的空间构型为___________ 填字母)
A.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为___________ ,若该晶体的密度为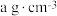 ,则该晶胞的体积是
,则该晶胞的体积是___________  (写出表达式即可)。
(写出表达式即可)。

| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外层上有两个电子 |
| E | E能形成红色(或砖红色)的 和黑色的EO两种氧化物, 和黑色的EO两种氧化物,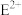 水溶液呈蓝色 水溶液呈蓝色 |
(2)B的氢化物沸点比同主族下一周期元素的氢化物沸点
(3)
 分子中C原子的杂化轨道类型是
分子中C原子的杂化轨道类型是(4)A、C、E三种元素可形成
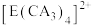 配离子,其中存在的化学键类型
配离子,其中存在的化学键类型①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
若
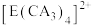 具有对称的空间构型,且当
具有对称的空间构型,且当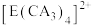 中的两个
中的两个 被两个
被两个 取代时,能得到两种不同结构的产物,则
取代时,能得到两种不同结构的产物,则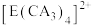 的空间构型为
的空间构型为A.平面正方形 b.正四面体 c.三角锥形 d.V形
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为
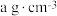 ,则该晶胞的体积是
,则该晶胞的体积是 (写出表达式即可)。
(写出表达式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮、磷、砷是同族元素,该族元素单质及其化合物在农药、化肥等方面有重要应用。请回答下列问题。
(1)砷原子核外电子排布式为________________________________________ 。
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为_________________ ,该化学键能够形成的原因是_______________________________________________________________ 。
(3)已知:
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是__________ 。
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是_________ 。
(1)砷原子核外电子排布式为
(2)K3[Fe(CN)6]晶体中Fe3+与CN-之间的键型为
(3)已知:
| CH4 | SiH4 | NH3 | PH3 | |
| 沸点(K) | 101.7 | 161.2 | 239.7 | 185.4 |
| 分解温度(K) | 873 | 773 | 1073 | 713.2 |
分析上表中四种物质的相关数据,请回答:
①CH4和SiH4比较,NH3和PH3比较,沸点高低的原因是
②CH4和SiH4比较,NH3和PH3比较,分解温度高低的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】请回答下列问题。
(1)基态铁原子的价层电子排布式为_______ 。
(2)元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
① Na的第一电离能小于Li,从原子结构的角度解释其原因_______ 。
② S的第一电离能小于P,解释其原因_______ 。
(3)33As、34Se、35Br三种非金属元素的电负性由大到小的顺序为_______ ;Br可与第三周期Cl元素形成化合物BrCl,其中显正价的元素为_______ ,原因是_______ 。
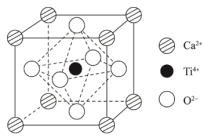
(4)钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。钛酸钙的晶胞如下图所示,1个晶胞中含有O2-的个数是_______ ,离子半径Ca2+大于Ti4+,理由是_______ 。
(5)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞的棱长为a pm,则钛酸钙晶体密度ρ=_______ g·cm-3(列出计算式)。
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是_______ (填字母序号)。
a. BaTiO3 b. MgTiO3 c. BaZrO3
(1)基态铁原子的价层电子排布式为
(2)元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
① Na的第一电离能小于Li,从原子结构的角度解释其原因
② S的第一电离能小于P,解释其原因
(3)33As、34Se、35Br三种非金属元素的电负性由大到小的顺序为
(4)钛酸钙是最典型的钙钛矿型化合物,该类化合物具有特殊的理化性质。钛酸钙的晶胞如下图所示,1个晶胞中含有O2-的个数是

(5)钛酸钙的阴、阳离子均可被半径相近的其它离子替代,从而衍生出多种钙钛矿型化合物。
①已知钛酸钙晶胞的棱长为a pm,则钛酸钙晶体密度ρ=
②若忽略离子替代时的体积变化,下列钙钛矿型化合物中,密度大于钛酸钙的是
a. BaTiO3 b. MgTiO3 c. BaZrO3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】已知A、B、C、D、E、F、G都是元素周期表中短周期主族元素,它们的原子序数依次增大。A原子的电子只有一种自旋取向,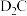 中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
(1)E元素基态原子的简化电子排布式为________ 。E元素原子的第一电离能________ 镁(填“>”“<”或“=”)
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为________ 。离子半径: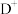
________ (填“<”“>”或“=”)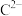 。
。
(3)元素C的简单气态氢化物的沸点________ (填“高于”或“低于”)元素F的简单气态氢化物的沸点,其主要原因是________________________ 。
(4)金属元素H的基态原子核外电子有________ 种空间运动状态。
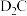 中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:
中阴、阳离子具有相同的电子层结构,B、C均可分别与A形成10电子分子,B、C处于同一周期,两者可以形成许多种共价化合物,C、F处于同一主族,B原子最外p能级上的电子处于半充满状态,C的最外层电子数是内层电子数的3倍,E是的第三周期元素的简单离子中半径最小。元素H原子M能层为全充满状态,且核外只有一个未成对电子的某金属元素,回答下列问题:(1)E元素基态原子的简化电子排布式为
(2)F、G元素对应的最高价含氧酸中酸性较强的化学式为
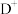
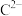 。
。(3)元素C的简单气态氢化物的沸点
(4)金属元素H的基态原子核外电子有
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】已知A、B、C、D是原子序数依次增大的四种短周期主族元素,A的周期数等于其主族序数,B原子的价电子排布为nsnnpn,D是地壳中含量最多的元素,E是第四周期的p区元素且最外层只有2对成对电子,F元素的基态原子第四能层只有一个电子,其它能层均已充满电子。G元素最大能层符号为N,有4个单电子。
(1)基态E原子的价电子排布图___________ 。
(2)B、C、D三元素第一电离能由大到小的顺序为___________ (用元素符号表示)。
(3) 中心原子为
中心原子为___________ 杂化,空间构型为___________ ,键角___________  (用“>、<、=”填空)。
(用“>、<、=”填空)。
(4) 与C2为等电子体结构相似,1mol
与C2为等电子体结构相似,1mol 中含有
中含有 键的数目为
键的数目为___________ 。
(5)D、E元素最简单氢化物的稳定性___________ (填化学式)。
(6)基态G2+离子的电子排布式为:___________ 。
(1)基态E原子的价电子排布图
(2)B、C、D三元素第一电离能由大到小的顺序为
(3)
 中心原子为
中心原子为 (用“>、<、=”填空)。
(用“>、<、=”填空)。(4)
 与C2为等电子体结构相似,1mol
与C2为等电子体结构相似,1mol 中含有
中含有 键的数目为
键的数目为(5)D、E元素最简单氢化物的稳定性
(6)基态G2+离子的电子排布式为:
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解病得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。结合有关知识,回答下列问题:
(1)Cu、N、O、S元素第一电离能由大到小的顺序是_______ (填元素符号);蓝色沉淀溶解时发生反应的离子方程式是________________ 。
(2)Cu(NH3)4SO4·H2O晶体中中心离子是_______ ,配体是_____ ,配位数是_____ ,存在的化学键有____________ (填字母序号)。
a.离子键 b.极性键 c.非极性键 d.配位键
(3)SO42-的空间构型是_____________ ,其中S原子的杂化轨道类型是___________ ,SO3的空间构型是_________ ,其中S原子的杂化轨道类型是_______ ,属于______ 分子(填“极性”或“非极性”)。
(4)已知纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,已知高温下Cu2O比CuO稳定。
①写出基态Cu+的价电子排布式____________ ;按照元素周期表分区,Cu属于____ 区。
②从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因____________ 。
(1)Cu、N、O、S元素第一电离能由大到小的顺序是
(2)Cu(NH3)4SO4·H2O晶体中中心离子是
a.离子键 b.极性键 c.非极性键 d.配位键
(3)SO42-的空间构型是
(4)已知纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,已知高温下Cu2O比CuO稳定。
①写出基态Cu+的价电子排布式
②从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因
您最近一年使用:0次
【推荐1】回答下列问题:
(1)基态碳原子的核外电子排布式为___________ 。非金属元素N的第一电离能大于O的第一电离能,原因是___________ 。
(2)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
下列说法正确的是___________(填序号)。
(3)Mn、Fe均为第四周期过渡金属元素,两元素的部分电离能数据列于下表:
锰元素位于第四周期第ⅦB族。请写出基态Mn2+的价电子排布式:___________ ,比较两元素的I2、I3可知,气态Mn2+和气态Fe2+相比,___________ 更难再失去1个电子。
(4)卤族元素F、Cl、Br、I的电负性由小到大的顺序是___________ 。
(5)基态B原子的价电子轨道表示式为___________ ;B和N相比,电负性较大的是___________ ;BN中B元素的化合价为___________ 。
(1)基态碳原子的核外电子排布式为
(2)下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据。
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A.甲的金属性比乙强 | B.乙有+1价 |
| C.丙不可能为非金属元素 | D.丁一定为金属元素 |
| 元素 | Mn | Fe | |
| 电离能/(kJ·mol-1) | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
(4)卤族元素F、Cl、Br、I的电负性由小到大的顺序是
(5)基态B原子的价电子轨道表示式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】太阳能电池一共可分为三代,请回答下列问题:
(1)第一代太阳能电池为硅基太阳能电池,其中以单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高能层符号为___________ ,电子占据的最高能级的电子云轮廓图为___________ 。
②根据对角线规则,Si的一些化学性质与___________ (填短周期元素名称)相似。
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga___________ As(填“大于”或“小于”,下同),第一电离能:Ga___________ As。
② 分子含有
分子含有___________ (填“ 键”或“
键”或“ 键”),As的最高价氧化物的化学式为
键”),As的最高价氧化物的化学式为___________ 。
③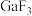 的熔点约为1000℃,
的熔点约为1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是___________ 。
④Ga、F、Cl的电负性由大到小的顺序为___________ 。
(3)第三代太阳能电池—钙钛矿型太阳能电池,它利用有机金属卤化物(组成为 、
、 和有机碱离子
和有机碱离子 )作为吸光材料,其晶胞结构如图所示。
)作为吸光材料,其晶胞结构如图所示。

①该有机碱离子中,C、N原子的杂化轨道类型分别为___________ 、___________ 。
②若晶胞参数为apm,则晶体密度为___________  。(阿伏加德罗常数的值为
。(阿伏加德罗常数的值为 ,列出计算式)
,列出计算式)
(1)第一代太阳能电池为硅基太阳能电池,其中以单晶硅太阳能电池的转化效率最高,技术最为成熟,应用最为广泛。
①在基态Si原子中,电子占据的最高能层符号为
②根据对角线规则,Si的一些化学性质与
(2)第二代太阳能电池是薄膜太阳能电池,如砷化镓电池。
①原子半径:Ga
②
 分子含有
分子含有 键”或“
键”或“ 键”),As的最高价氧化物的化学式为
键”),As的最高价氧化物的化学式为③
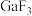 的熔点约为1000℃,
的熔点约为1000℃, 的熔点为77.9℃,其原因是
的熔点为77.9℃,其原因是④Ga、F、Cl的电负性由大到小的顺序为
(3)第三代太阳能电池—钙钛矿型太阳能电池,它利用有机金属卤化物(组成为
 、
、 和有机碱离子
和有机碱离子 )作为吸光材料,其晶胞结构如图所示。
)作为吸光材料,其晶胞结构如图所示。
①该有机碱离子中,C、N原子的杂化轨道类型分别为
②若晶胞参数为apm,则晶体密度为
 。(阿伏加德罗常数的值为
。(阿伏加德罗常数的值为 ,列出计算式)
,列出计算式)
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为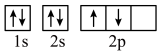 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物的晶体类型为___________ 。
(4)E基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向。
(5)下列关于F原子的价电子轨道表示式是___________ 。
(6)基态Fe3+核外电子排布式为___________ 。过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素是地壳中含量最多的元素 |
| D元素原子的第一至第四电离能分别是:I1=738 kJ·mol-1;I2=1451 kJ·mol-1;I3=7733kJ·mol-1;I4=10540 kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物的晶体类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价电子轨道表示式是
(6)基态Fe3+核外电子排布式为
您最近一年使用:0次



