现有六种元素A、B、C、D、E、F,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)某同学根据上述信息,推断A基态原子的轨道表示式为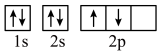 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物的晶体类型为___________ 。
(4)E基态原子中能量最高的电子,其电子云在空间有___________ 个伸展方向。
(5)下列关于F原子的价电子轨道表示式是___________ 。
(6)基态Fe3+核外电子排布式为___________ 。过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应,生成BC气体,该反应的离子方程式为___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| B元素原子的核外p电子数比s电子数少1 |
| C元素是地壳中含量最多的元素 |
| D元素原子的第一至第四电离能分别是:I1=738 kJ·mol-1;I2=1451 kJ·mol-1;I3=7733kJ·mol-1;I4=10540 kJ·mol-1 |
| E原子核外所有p轨道全满或半满 |
| F在周期表的第8纵列 |
(1)某同学根据上述信息,推断A基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了(2)B元素的电负性
(3)C与D形成的化合物的晶体类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)下列关于F原子的价电子轨道表示式是
(6)基态Fe3+核外电子排布式为
更新时间:2023-12-26 21:25:58
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】有五种短周期元素,它们的结构、性质等信息如下表所示:
请根据表中信息回答下列问题:
(1)A元素原子的核外电子排布式为___________ ,D元素原子的核外价电子排布图为___________
(2)B元素在元素周期表中的位置为___________ ;离子半径:___________ (填“>”或“<”)A。
(3)C元素最外层电子有___________ 个未成对电子,能量最高的电子排布在___________ 轨道上,该轨道的形状是___________ 。
(4)C、E元素的第一电离能的大小关系是___________ (用元素符号表示)。
(5)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是___________ (用元素符号表示),CD3与水反应后的产物是___________ (填化学式,反应前后元素化合价不变)。
| 元素 | 结构、性质等信息 |
| A | 是短周期元素(稀有气体元素除外)中原子半径最大的元素,含该元素的某种合金是原子反应堆的导热剂 |
| B | 与A同周期,其最高价氧化物对应的水化物呈两性 |
| C | 其气态氢化物极易溶于水,液态时常用作制冷剂 |
| D | 海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中的杀菌消毒剂 |
| E | 元素原子的2p轨道上有2对成对电子 |
(1)A元素原子的核外电子排布式为
(2)B元素在元素周期表中的位置为
(3)C元素最外层电子有
(4)C、E元素的第一电离能的大小关系是
(5)已知CD3分子中D元素显+1价,则该情况下,C、D元素的电负性大小关系是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】现有A、B、C、D、E、F、G七种短周期主族元素,其原子序数依次增大。已如A、D位于同一主族,D是短周期中原子半径最大的。B、E最外层电子数是最内层电子数的2倍。C、F的最外层电子数相等,且C、F的原子序数之和为A、D原子序数之和的两倍。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是____________ (用离子符号填写)。
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是___________ (用化学式填写)。
(3)由C、D两元素能形成一种原子个数比为1∶1的化合物,该化合物所含的化学键类型有__________ 。
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是______________ 。
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是________________ 。
(1)A、C、D、F形成的简单离子半径由大到小的顺序是
(2)B、E、F、G最高价氧化物对应的水化物酸性最强的是
(3)由C、D两元素能形成一种原子个数比为1∶1的化合物,该化合物所含的化学键类型有
(4)下列事实能说明G元素的非金属性比F元素的非金属性强的是
a. G单质与Na2S溶液反应溶液变浑浊
b. F氢化物的酸性比G的氢化物酸性弱
c. G和F两元素的简单氢化物受热分解,前者的分解温度高
(5)A、C、D、F四种元素形成的化合物M和N在溶液中相互反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】如图为周期表的一小部分,A、B、C、D的位置关系如图所示。且它们均为短周期元素,其中C元素的最外层电子数是电子层数的2倍,回答下列问题:
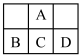
(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是__ (写分子式)。
(2)在A、B、C所形成氢化物中,A的电子式:___ ,其中最稳定的是__ (写分子式)。
(3)写D的单质与C的氢化物反应的化学方程式__ 。
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是__ (用离子方程式表示)。工业上是将氯气通入到30%的NaOH溶液中来制备NaClO溶液,若NaClO溶液中NaOH的质量分数为1%,则生产1000kg该溶液需消耗氯气的质量为___ kg(保留整数)。

(1)在B、C、D最高价氧化物对应水化物中,酸性最强的是
(2)在A、B、C所形成氢化物中,A的电子式:
(3)写D的单质与C的氢化物反应的化学方程式
(4)“84消毒液”的有效成分为NaClO,不可与酸性清洁剂混用的原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为Fe−Sm−As−F−O组成的化合物。回答下列问题:
(1)AsH3的中心原子的杂化轨道类型为___________ ,H2O沸点比H2S的___________ (填“高”或“低”),其判断理由是___________ ,BF3的立体构型为___________ 。
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为___________ 。
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标,例如图1中原子1的坐标为( ),则原子3的坐标分别为
),则原子3的坐标分别为___________ 。

(1)AsH3的中心原子的杂化轨道类型为
(2)Sm的价层电子排布式为4f66s2,Sm3+的价层电子排布式为
(3)一种四方结构的超导化合物的晶胞结构如图1所示,晶胞中Sm和As原子的投影位置如图2所示。图中F−和O2−共同占据晶胞的上下底面位置,若两者的比例依次用x和1−x代表,则该化合物的化学式表示为
 ),则原子3的坐标分别为
),则原子3的坐标分别为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】阅读材料,根据所学知识回答问题:
2022年6月17日,我国第三艘航空母舰命名为“中国人民解放军海军福建舰”,舷号为“18”。航母的甲板用钢具有高强度、大板面、拒磁、高韧性、抗低温(零下38℃)等特性,铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加,是制装甲的好材料。福建舰采用了目前世界上最先进的电磁弹射技术,使中国海军实力大幅提升,改变了亚太地区的军事力量对比。镍等金属因其优良的电磁性质,故而在航母上广泛应用。
(1)基态铬原子的价电子排布图 为_____ ,量子力学上把电子在原子核外的一个空间运动状态称为一个原子轨道,基态铁原子核外有_____ 种空间运动状态的电子。
(2)下列状态的铁中,是基态亚铁离子的为_____ (填编号)。
(3)Cr3+的一种配合物结构如图,配合物中Cr3+的配位原子为_____ ,配位数为_____ 。

(4)铁及其化合物的晶体种类较多。Fe的一种晶体结构如甲、乙(乙由八个甲堆积而成)所示,若按甲中虚线方向切乙,得到的切面图正确的是_____ (填字母)。

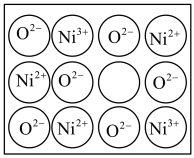
(5)晶体普遍存在各种缺陷。某种NiO晶体中存在如图所示的缺陷:当一个Ni2+空缺,会有两个Ni2+被两个Ni3+所取代,但晶体仍呈电中性。经测定某氧化镍样品的化学式为Ni0.96O,则该样品中Ni3+与Ni2+的离子数之比为_____ 。
2022年6月17日,我国第三艘航空母舰命名为“中国人民解放军海军福建舰”,舷号为“18”。航母的甲板用钢具有高强度、大板面、拒磁、高韧性、抗低温(零下38℃)等特性,铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加,是制装甲的好材料。福建舰采用了目前世界上最先进的电磁弹射技术,使中国海军实力大幅提升,改变了亚太地区的军事力量对比。镍等金属因其优良的电磁性质,故而在航母上广泛应用。
(1)基态铬原子的
(2)下列状态的铁中,是基态亚铁离子的为
A.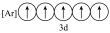 | B.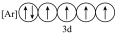 | C.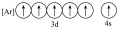 | D.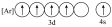 |
(3)Cr3+的一种配合物结构如图,配合物中Cr3+的配位原子为

(4)铁及其化合物的晶体种类较多。Fe的一种晶体结构如甲、乙(乙由八个甲堆积而成)所示,若按甲中虚线方向切乙,得到的切面图正确的是

A. | B.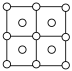 | C.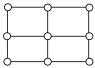 | D.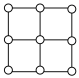 |
(5)晶体普遍存在各种缺陷。某种NiO晶体中存在如图所示的缺陷:当一个Ni2+空缺,会有两个Ni2+被两个Ni3+所取代,但晶体仍呈电中性。经测定某氧化镍样品的化学式为Ni0.96O,则该样品中Ni3+与Ni2+的离子数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】铁及其化合物用途广泛,请回答:
(1)与Fe最外层电子数相同且同周期的过渡元素有____________ 种。
(2)FeSO4·7H2O的结构如图所示。
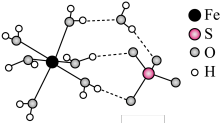
FeSO4·7H2O中H2O与Fe2+、H2O与 的作用力类型分别是
的作用力类型分别是____________ 、____________ 。H2O中H—O—H的键角____________  中O—S—O的键角(填“>”“<”或“=”)。
中O—S—O的键角(填“>”“<”或“=”)。
(3)由铁、钾、硒形成的一种超导材料,其晶胞结构如图1所示。
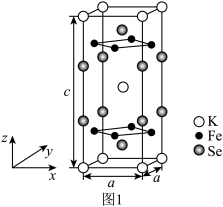
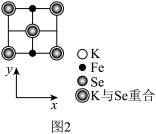
I.该超导材料的化学式是____________ 。
II.该晶胞参数a=0.4nm、c=1.4nm,该晶体密度ρ=____________  。(用
。(用 表示阿伏加德罗常数,写出计算表达式即可)
表示阿伏加德罗常数,写出计算表达式即可)
III.该晶胞在xy平面投影如图2所示,将图2补充完整____________ 。
(1)与Fe最外层电子数相同且同周期的过渡元素有
(2)FeSO4·7H2O的结构如图所示。

FeSO4·7H2O中H2O与Fe2+、H2O与
 的作用力类型分别是
的作用力类型分别是 中O—S—O的键角(填“>”“<”或“=”)。
中O—S—O的键角(填“>”“<”或“=”)。(3)由铁、钾、硒形成的一种超导材料,其晶胞结构如图1所示。


I.该超导材料的化学式是
II.该晶胞参数a=0.4nm、c=1.4nm,该晶体密度ρ=
 。(用
。(用 表示阿伏加德罗常数,写出计算表达式即可)
表示阿伏加德罗常数,写出计算表达式即可)III.该晶胞在xy平面投影如图2所示,将图2补充完整
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】现有属于前四周期的A、B、C、D、E、F、G七种元素,原子序数依次增大。A元素的价电子构型为nsnnpn+1;C元素为最活泼的非金属元素;D元素核外电子有六种空间运动状态,其最高能层容纳的电子数是核外电子总数的 ;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
(1)C元素的电子排布图为___ 。
(2)D元素与氯元素形成的简单化合物的电子式为____ 。
(3)E元素基态原子的价层电子的电子排布式为____ 。
(4)F3+的常见检验方法为取其溶液适量于试管中,滴入____ 溶液形成某种带颜色的配合物。
(5)G元素可能的性质____ 。
 ;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。
;E元素基态原子的未成对电子是第四周期最多的;F元素正三价离子的3d轨道为半充满状态;G元素与A元素位于同一主族,其某种氧化物有剧毒。(1)C元素的电子排布图为
(2)D元素与氯元素形成的简单化合物的电子式为
(3)E元素基态原子的价层电子的电子排布式为
(4)F3+的常见检验方法为取其溶液适量于试管中,滴入
(5)G元素可能的性质
| A.其单质可作为半导体材料 | B.其电负性大于磷 |
| C.其原子半径大于锗 | D.其第一电离能小于硒 |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】元素周期表中第四周期的金属元素在生产和科研中有非常重要的使用价值。
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
4FeCl3+2NH2OH•HCl→4FeCl2+N2O↑+6HCl+H2O
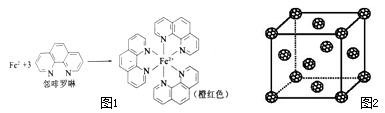
①Fe2+在基态时,核外电子排布式 1 ;
②羟胺中(NH2OH)采用SP3杂化的原子有 2 ;
③Fe2+与邻啡罗啉形成的配合物中,配位数为 3 ;
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是 4 ;
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是 5 ;
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于 6 晶体;
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为 7
(1)测定土壤中铁的含量时需先将三价铁还原为二价铁,再采用邻啡罗啉作显色剂,用比色法测定,若土壤中含有高氯酸盐时会对测定有干扰。相关的反应如下:
4FeCl3+2NH2OH•HCl→4FeCl2+N2O↑+6HCl+H2O

①Fe2+在基态时,核外电子排布式
②羟胺中(NH2OH)采用SP3杂化的原子有
③Fe2+与邻啡罗啉形成的配合物中,配位数为
(2)向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中析出深蓝色的[Cu(NH3)4]SO4晶体,该晶体中含有的化学键类型是
(3)往硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+,已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(4)配合物Ni(CO)4常温下呈液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
(5)如果把晶胞顶点与最近三个面心所围成的空隙叫做四面体空隙,第四周期电负性最小的原子可作为容体掺入C60晶体的空隙中,形成具有良好的超导性的掺杂C60化合物。现把C60抽象成质点,该晶体的晶胞结构如图2所示,若每个四面体空隙填入一个原子,则全部填满C60晶体的四面体空隙后,所形成的掺杂C60化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】前四周期元素X、Y、Z、W、Q的原子序数依次增大,基态X原子核外电子占据3个轨道,基态Y原子核外电子占据3个能级且每个能级上电子数相等,基态Z原子s能级的电子总数比p能级的多1,基态W原子和基态Q原子中成对电子数均是未成对电子数的3倍。回答下列问题:
(1)基态Q原子核外电子占据能量最高的能级符号为______ ,基态W原子核外电子的空间运动状态有_____ 种。
(2)元素X、Y、Z的电负性由大到小的顺序为______ (填元素符号,下同),元素Y、Z、W中第一电离能最大的是______ 。
(3)XCl3、ZCl3中,中心原子采用sp2杂化的是______ (填分子式)。
(4)下列物质中具有旋光性的是______ (填标号)。
(1)基态Q原子核外电子占据能量最高的能级符号为
(2)元素X、Y、Z的电负性由大到小的顺序为
(3)XCl3、ZCl3中,中心原子采用sp2杂化的是
(4)下列物质中具有旋光性的是
| A.乙醇(C2H5OH) | B.1,2-二氯丙烷(CH2ClCHClCH3) |
| C.乙酸(CH3COOH) | D.乳酸(CH3CHOHCOOH) |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐1】某硫与锌元素组成的化合物M不溶于水、易溶于酸,见阳光色变暗。若在该化合物中加入微量的Cu、Mn、Ag做活化剂,经光照后,能发出不同颜色的荧光。回答下列问题:
(1)基态铜原子的价电子排布图为_____ 。第一电离能介于Si、P之间的第三周期元素为_____ (填元素符号)。
(2)SO2中S的杂化类型为_____ ,该分子的空间构型为_____ 。
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为_____ NA,NH3分子在独立存在时H-N-H键角为107°,[Ag(NH3)2]+中H-N-H键角变大的原因:________________ 。
(4)M的晶胞结构如图。
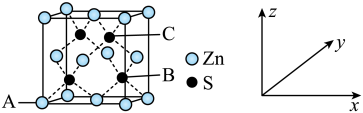
①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为___ 个,M的化学式__ 。
②Zn的第三电离能大于Cu的第三电离能的原因是_____ 。
(1)基态铜原子的价电子排布图为
(2)SO2中S的杂化类型为
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为
(4)M的晶胞结构如图。

①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为
②Zn的第三电离能大于Cu的第三电离能的原因是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】A、B、C、D、E、F为原子序数依次增大的短周期主族元素。其中A与其他元素均不同周期;B的最外层电子数是其内层电子总数的2倍;由C、D组成的化合物D2C和D2C2均为离子晶体;E的内层电子数总和是其最外层电子数的5倍;基态F原子3p轨道上有2个未成对电子且其单质的晶体属于分子晶体。回答下列问题:
(1)基态F的价电子排布式为______ ;D位于第______ 周期______ 族。
(2)与E同周期的元素中,第一电离能小于E的元素有______ (填元素符号)。
(3)BC2分子中,B原子的轨道杂化类型为______ ,BC2属于______ (填“极性”或“非极性”)分子;A2C、A2F中沸点更高的是______ (填化学式),原因是______ ;D与氯元素形成的化合物DCl的熔点比B的氯化物BCl4的熔点高,原因是______ 。
(1)基态F的价电子排布式为
(2)与E同周期的元素中,第一电离能小于E的元素有
(3)BC2分子中,B原子的轨道杂化类型为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐3】在庆祝中华人民共和国成立70周年的阅兵仪式上,最后亮相的DF—31A洲际战略导弹是我国大国地位、国防实力的显著标志。其制作材料中包含了 Fe、Cr、Ni、Na、C等多种元素。回答下列问题:
(1)CaCO3和BaCO3是古代制备蓝色颜料的重要原料。
①CaCO3热分解温度低于BaCO3,其原因可能是___________ 。
②分子中的大π键可用符号Π 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则CO
),则CO 中的大π键应表示为
中的大π键应表示为___________ ,CO 中键角∠OCO =
中键角∠OCO =___________ ,其键角数据可借助晶体___________ 实验获得。
(2)铁钴的配合物常用作催化剂。
①在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”,羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是___________ 。
②Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是___________ 。
(3)快离子导体是一类具有优良离子导电能力的固体电解质。已知氯化钠晶胞参数a=600pm,温度升高时,NaCl晶体出现缺陷(如图1所示,某一个顶点没有Na+,出现空位),成为潜在的快离子导体材料。
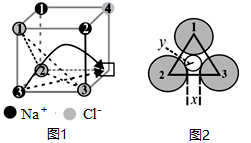
该晶体导电时,离子在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图1中箭头所示):
途径1:在平面内挤过2、3号Cl-之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号Cl-形成的三角形通道(如图2,小圆的半径为y)迁移到空位。已知:r(Na+)=95pm,r(Cl-)=185pm, =1.4,
=1.4,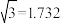 。
。
①x=___________ ,y=___________ ;(保留一位小数)
②迁移可能性更大的途径是___________ 。
(1)CaCO3和BaCO3是古代制备蓝色颜料的重要原料。
①CaCO3热分解温度低于BaCO3,其原因可能是
②分子中的大π键可用符号Π
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π ),则CO
),则CO 中的大π键应表示为
中的大π键应表示为 中键角∠OCO =
中键角∠OCO =(2)铁钴的配合物常用作催化剂。
①在某些过渡金属的羰基化合物中,中心原子的价电子数与配体提供的电子数之和满足“18e-结构规则”,羰基铁与羰基镍的化学式分别为Fe(CO)5和Ni(CO)4,则羰基铬的化学式是
②Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是
(3)快离子导体是一类具有优良离子导电能力的固体电解质。已知氯化钠晶胞参数a=600pm,温度升高时,NaCl晶体出现缺陷(如图1所示,某一个顶点没有Na+,出现空位),成为潜在的快离子导体材料。

该晶体导电时,离子在电场作用下迁移到空位上,形成电流。迁移的途径有两条(如图1中箭头所示):
途径1:在平面内挤过2、3号Cl-之间的狭缝(距离为x)迁移到空位。
途径2:挤过由1、2、3号Cl-形成的三角形通道(如图2,小圆的半径为y)迁移到空位。已知:r(Na+)=95pm,r(Cl-)=185pm,
 =1.4,
=1.4,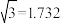 。
。①x=
②迁移可能性更大的途径是
您最近一年使用:0次



