阅读材料,根据所学知识回答问题:
2022年6月17日,我国第三艘航空母舰命名为“中国人民解放军海军福建舰”,舷号为“18”。航母的甲板用钢具有高强度、大板面、拒磁、高韧性、抗低温(零下38℃)等特性,铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加,是制装甲的好材料。福建舰采用了目前世界上最先进的电磁弹射技术,使中国海军实力大幅提升,改变了亚太地区的军事力量对比。镍等金属因其优良的电磁性质,故而在航母上广泛应用。
(1)基态铬原子的价电子排布图 为_____ ,量子力学上把电子在原子核外的一个空间运动状态称为一个原子轨道,基态铁原子核外有_____ 种空间运动状态的电子。
(2)下列状态的铁中,是基态亚铁离子的为_____ (填编号)。
(3)Cr3+的一种配合物结构如图,配合物中Cr3+的配位原子为_____ ,配位数为_____ 。

(4)铁及其化合物的晶体种类较多。Fe的一种晶体结构如甲、乙(乙由八个甲堆积而成)所示,若按甲中虚线方向切乙,得到的切面图正确的是_____ (填字母)。

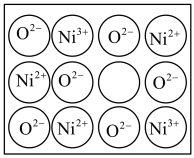
(5)晶体普遍存在各种缺陷。某种NiO晶体中存在如图所示的缺陷:当一个Ni2+空缺,会有两个Ni2+被两个Ni3+所取代,但晶体仍呈电中性。经测定某氧化镍样品的化学式为Ni0.96O,则该样品中Ni3+与Ni2+的离子数之比为_____ 。
2022年6月17日,我国第三艘航空母舰命名为“中国人民解放军海军福建舰”,舷号为“18”。航母的甲板用钢具有高强度、大板面、拒磁、高韧性、抗低温(零下38℃)等特性,铁中掺入铬,铬含量在10.5%以上,它的耐腐蚀性能显著增加,是制装甲的好材料。福建舰采用了目前世界上最先进的电磁弹射技术,使中国海军实力大幅提升,改变了亚太地区的军事力量对比。镍等金属因其优良的电磁性质,故而在航母上广泛应用。
(1)基态铬原子的
(2)下列状态的铁中,是基态亚铁离子的为
A.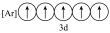 | B.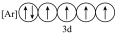 | C.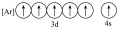 | D.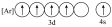 |
(3)Cr3+的一种配合物结构如图,配合物中Cr3+的配位原子为

(4)铁及其化合物的晶体种类较多。Fe的一种晶体结构如甲、乙(乙由八个甲堆积而成)所示,若按甲中虚线方向切乙,得到的切面图正确的是

A. | B.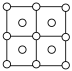 | C.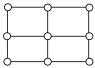 | D.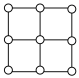 |
(5)晶体普遍存在各种缺陷。某种NiO晶体中存在如图所示的缺陷:当一个Ni2+空缺,会有两个Ni2+被两个Ni3+所取代,但晶体仍呈电中性。经测定某氧化镍样品的化学式为Ni0.96O,则该样品中Ni3+与Ni2+的离子数之比为

更新时间:2023-04-16 22:15:48
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
真题
解题方法
【推荐1】W、X、Y、Z是四种常见的短周期元素,其原子半径随原子序数变化如下图所示。已知W的一种核素的质量数为18,中子数为10;X和Ne原子的核外电子数相差1;Y的单质是一种常见的半导体材料;Z的电负性在同周期主族元素中最大。
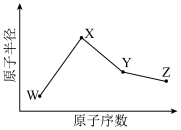
(1) X位于元素周期表中第______ 周期第______ 族;W的基态原子核外有_______ 个未成对电子。
(2)X的单质子和Y的单质相比,熔点较高的是______ (写化学式);Z的气态氢化物和溴化氢相比,较稳定的是_________ (写化学式)。
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是_____________ 。
(4)在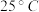 、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是_____________ 。

(1) X位于元素周期表中第
(2)X的单质子和Y的单质相比,熔点较高的是
(3)Y与Z形成的化合物和足量水反应,生成一种弱酸和一种强酸,该反应的化学方程式是
(4)在
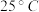 、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
、101 kPa下,已知Y的气态化物在氧气中完全燃烧后恢复至原状态,平均每转移1mol 电子放热190.0kJ,该反应的热化学方程式是
您最近一年使用:0次
【推荐2】W、X、Y、Z、N是短周期元素,它们的核电荷数依次增大。
(1)W单质的化学式为______ ,Z元素原子核外有______ 原子轨道填充了电子。
(2)Y、Z和N三种元素第一电离能由大到小的顺序为__________ (填元素符号)。
(3)X与Z两元素的电负性较大的是_________ (填元素符号)。
(4)Z元素原子共有______ 种不同运动状态的电子。
| 元素 | 元素性质或原子结构 |
| W | 原子核内无中子 |
| X | 在Y的上一周期,原子核外s能级上的电子总数与p能级上的电子总数相等 |
| Y | 元素的离子半径在该周期中最小 |
| Z | 原子核外p能级上的电子总数比s能级上的电子总数多2 |
| N | 最外层电子数比次外层电子数少1 |
(2)Y、Z和N三种元素第一电离能由大到小的顺序为
(3)X与Z两元素的电负性较大的是
(4)Z元素原子共有
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硼材料及含硼化合物的用途非常广泛,如B(C6F5)3可代品Cu催化重氮化合物对杂环分子的修饰、催化吲哚与苯乙炔的区域选择性加成等。回答下列问题:
(1)基态Cu原子的价电子排布式为___________ 。 是一种准晶体,具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性,可通过
是一种准晶体,具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性,可通过___________ 的方法区分晶体与准晶体。
(2)B、C、F的电负性由大到小的顺序为___________ ;Be、B、C是同周期相邻元素,第一电离能: ,这是因为
,这是因为___________ 。
(3)B(C6F5)3分子中所有原子___________ (填“能”或“不能”)处于同一平面。
(4)吲哚(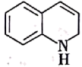 )的沸点为253~254℃,苯乙炔的沸点为142~144℃,前者沸点高得多,其主要原因是
)的沸点为253~254℃,苯乙炔的沸点为142~144℃,前者沸点高得多,其主要原因是_________ 。
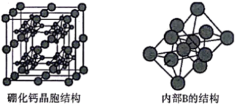
(5)硼化钙的晶胞结构如图所示,晶胞参数为apm,设 为阿伏加德罗常数的值。硼化钙的化学式为
为阿伏加德罗常数的值。硼化钙的化学式为___________ ,其晶体的密度为___________  (列出计算式)。
(列出计算式)。
(1)基态Cu原子的价电子排布式为
 是一种准晶体,具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性,可通过
是一种准晶体,具有与晶体相似的长程有序的原子排列,但是不具备晶体的平移对称性,可通过(2)B、C、F的电负性由大到小的顺序为
 ,这是因为
,这是因为(3)B(C6F5)3分子中所有原子
(4)吲哚(
 )的沸点为253~254℃,苯乙炔的沸点为142~144℃,前者沸点高得多,其主要原因是
)的沸点为253~254℃,苯乙炔的沸点为142~144℃,前者沸点高得多,其主要原因是(5)硼化钙的晶胞结构如图所示,晶胞参数为apm,设
 为阿伏加德罗常数的值。硼化钙的化学式为
为阿伏加德罗常数的值。硼化钙的化学式为 (列出计算式)。
(列出计算式)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】Ⅰ.人类在使用金属的历史进程中,经历了铜、铁、铝之后,第四种将被广泛应用的金属被科学家预测是钛(22Ti),它被誉为“未来世纪的金属”。试回答下列问题:
(1)Ti元素在元素周期表中的位置是第四周期第___ 族;其基态原子的电子排布式为___ 。
(2)在Ti的化合物中,Ti可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好、介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如图所示,则它的化学式是___ ,其中Ti4+的氧配位数为___ ,Ba2+的氧配位数为____ 。

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4是___ 晶体。
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如图a所示,我们通常可以用图b所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体形,它有___ 种同分异构体。

(5)已知过氧化氢分子的空间结构如图c所示,分子中氧原子采取___ 杂化。

(6)24Cr是1~36号元素中未成对电子数最多的原子,Cr3+在溶液中存在如下转化关系:Cr3+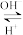 Cr(OH)3
Cr(OH)3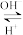 [Cr(OH)4]-。
[Cr(OH)4]-。
①基态Cr原子的价电子排布式为___ 。
②Cr(OH)3是分子晶体,[Cr(OH)4]-中存在的化学键是___ (填标号)。
A.离子键 B.极性键 C.非极性键 D.配位键
(1)Ti元素在元素周期表中的位置是第四周期第
(2)在Ti的化合物中,Ti可以呈现+2、+3、+4三种化合价,其中以+4价的Ti最为稳定。偏钛酸钡的热稳定性好、介电常数高,在小型变压器、话筒和扩音器中都有应用。偏钛酸钡晶体中晶胞的结构示意图如图所示,则它的化学式是

(3)常温下的TiCl4是有刺激性臭味的无色透明液体,熔点-23.2℃,沸点136.2℃,所以TiCl4是
(4)已知Ti3+可形成配位数为6的配合物,其空间构型为正八面体,如图a所示,我们通常可以用图b所示的方法来表示其空间构型(其中A表示配体,M表示中心原子)。配位化合物[Co(NH3)4Cl2]的空间构型也为八面体形,它有

(5)已知过氧化氢分子的空间结构如图c所示,分子中氧原子采取

(6)24Cr是1~36号元素中未成对电子数最多的原子,Cr3+在溶液中存在如下转化关系:Cr3+
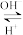 Cr(OH)3
Cr(OH)3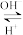 [Cr(OH)4]-。
[Cr(OH)4]-。①基态Cr原子的价电子排布式为
②Cr(OH)3是分子晶体,[Cr(OH)4]-中存在的化学键是
A.离子键 B.极性键 C.非极性键 D.配位键
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】锶(Sr)位于元素周期表的第5周期IIA族。碳酸锶(SrCO3)是制取锶的原料,用天青石固体(主要成分SrSO4,难溶于水)和Na2CO3溶液混合浸泡可制取碳酸锶。完成下列填空:
(1)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号___________ 。写出锶原子的最外层电子排布式___________ 。下列关于锶及其化合物的叙述中,错误的是___________ 。
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(2)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因___________ 。
(3)钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO 3Ba↑+BaO+Al2O3。常温下Al的金属性比Ba的金属性
3Ba↑+BaO+Al2O3。常温下Al的金属性比Ba的金属性___________ (选填“强”“弱”)。利用上述方法可制取Ba的主要原因是___________ 。
a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
(1)已知:锶的原子序数为38,某锶原子的质量数为88,写出能包含这些信息的一种化学符号
a.锶的金属性比镁强 b.氢氧化锶呈两性
c.锶在化合物中呈+2价 d.锶在自然界中以游离态存在
(2)请用溶解平衡移动原理解释工业上可以天青石制取碳酸锶的原因
(3)钡位于元素周期表第六周期IIA族。工业上制备单质钡的原理如下:2Al+4BaO
 3Ba↑+BaO+Al2O3。常温下Al的金属性比Ba的金属性
3Ba↑+BaO+Al2O3。常温下Al的金属性比Ba的金属性a.高温时Al的活泼性大于Ba b.高温有利于BaO分解
c.高温时BaO·Al2O3比Al2O3稳定 d.Ba的沸点比Al的低
您最近一年使用:0次
【推荐1】黄铜矿(CuFeS2)是炼铜的最主要矿物。火法冶炼黄铜矿的过程中,其中一步反应是2Cu2O+Cu2S 6Cu+SO2↑。回答下列问题:
6Cu+SO2↑。回答下列问题:
(1)Cu+的价电子排布图为___________ ;Cu2O与Cu2S熔点较高的是___________ ,原因为___________ 。
(2)离子化合物CaC2的一种晶体结构如图1所示。写出该物质的电子式:___________ 。从钙离子看,属于___________ 堆积;一个晶胞含有的 键平均有
键平均有___________ 个。

(3)奥氏体是碳溶解在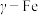 中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为___________ ,若晶体密度为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为___________ pm (阿伏加德罗常数的值用NA表示,写出计算式即可)。
 6Cu+SO2↑。回答下列问题:
6Cu+SO2↑。回答下列问题:(1)Cu+的价电子排布图为
(2)离子化合物CaC2的一种晶体结构如图1所示。写出该物质的电子式:
 键平均有
键平均有
(3)奥氏体是碳溶解在
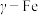 中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为
中形成的一种间隙固溶体,无磁性,其晶胞如图2所示,则该物质的化学式为 ,则晶胞中最近的两个碳原子的距离为
,则晶胞中最近的两个碳原子的距离为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】N、P同属于元素周期表的第VA族元素。
(1)基态磷原子的价电子排布图是____________
(2)NCl3的VSEPR模型名称是__________ ,中心原子杂化轨道类型是__________________ 。
(3)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为原子总数相同、价电子总数相同的粒子即等电子体具有相似的化学键特征,它们的许多性质是接近的。写出N2O的一种有第二周期非金属元素组成的等电子体分子_______________________ 。
(4)沸点比较:PH3___________ NH3(填“>”、“=”、“<”),理由是____________ 。
(5)已知键能:H-H键能为436kJ·mol-1,N-H键能为391kJ·mol-1,N≡N键能为945.6kJ•mol-1。则N2+3H2 2NH3,生成2molNH3时,共放热
2NH3,生成2molNH3时,共放热_________ kJ
(6)NH3极易溶于水,原因是_______________
(1)基态磷原子的价电子排布图是
(2)NCl3的VSEPR模型名称是
(3)“笑气”(N2O)是人类最早应用于医疗的麻醉剂之一。有关理论认为原子总数相同、价电子总数相同的粒子即等电子体具有相似的化学键特征,它们的许多性质是接近的。写出N2O的一种有第二周期非金属元素组成的等电子体分子
(4)沸点比较:PH3
(5)已知键能:H-H键能为436kJ·mol-1,N-H键能为391kJ·mol-1,N≡N键能为945.6kJ•mol-1。则N2+3H2
 2NH3,生成2molNH3时,共放热
2NH3,生成2molNH3时,共放热(6)NH3极易溶于水,原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】单晶边缘纳米催化剂技术为工业上有效利用二氧化碳提供了一条经济可行的途径,其中单晶氧化镁负载镍催化剂表现出优异的抗积碳和抗烧结性能。
(1)基态镍原子的价层电子排布图为___________ 。
(2)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为___________ ;在上述三种物质的分子中碳原子杂化类型不同于其他两种的是______ ,立体构型为正四面体的分子是___________ ,三 种物质中沸点最高的是CH3OH,其原因是___________ 。
(3)Ni与CO在60~80°C时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是___________ ,Ni(CO)4晶体类型是___________ 。
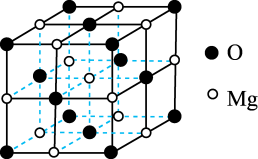
(4)已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞棱长为0.42nm,则MgO的密度为___________ g·cm-3(保留小数点后一位,下同);相邻Mg2+之间的最短距离为___________ nm。(已知 =1.414,
=1.414,  =1.732)
=1.732)
(1)基态镍原子的价层电子排布图为
(2)氧化镁载体及镍催化反应中涉及到CH4、CO2和CH3OH等物质。元素Mg、O和C的第一电离能由小到大排序为
(3)Ni与CO在60~80°C时反应生成Ni(CO)4气体,在Ni(CO)4分子中与Ni形成配位键的原子是
(4)已知MgO具有NaCl型晶体结构,其结构如图所示。已知MgO晶胞棱长为0.42nm,则MgO的密度为
 =1.414,
=1.414,  =1.732)
=1.732)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】三氯化六氨合钴(III){[Co(NH3)6]Cl3}是一种重要的原料。实验室以活性炭为催化剂,用H2O2、CoCl2为原料制备[Co(NH3)6]Cl3,反应过程中会放出大量的热。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线图所示。
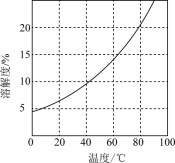
③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
制备[Co(NH3)6]Cl3实验步骤如下:
I.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,控制温度在10℃以下,逐滴加入5mL30%的H2O2溶液。实验装置如图所示。

II.将混合物在水浴1中反应一段时间,再改用水浴2处理,充分结晶后过滤。
III.……
(1)上图中仪器a的名称为_________ 。
(2)步骤I将Co2+转化[Co(NH3)6]3+过程中,先加浓氨水,后加H2O2溶液的目的是_________ 。
(3)步骤II中采用“冰水浴”的是_________ (填“水浴1”或“水浴2”)。制备[Co(NH3)6]Cl3的总反应化学方程式为_________ 。
(4)[Co(NH3)6]Cl3配合物的内界为_________ (用化学式表示)。
已知:①Co2+不易被氧化,Co3+具有强氧化性;[Co(NH3)6]2+具有较强还原性,[Co(NH3)6]3+性质稳定。
②[Co(NH3)6]Cl3在水中的溶解度曲线图所示。

③加入少量浓盐酸有利于[Co(NH3)6]Cl3析出。
制备[Co(NH3)6]Cl3实验步骤如下:
I.称取研细的CoCl2•6H2O10.0g和NH4Cl5.0g于烧杯中溶解,将溶液转入三颈烧瓶,加入25mL浓氨水和适量活性炭粉末,控制温度在10℃以下,逐滴加入5mL30%的H2O2溶液。实验装置如图所示。

II.将混合物在水浴1中反应一段时间,再改用水浴2处理,充分结晶后过滤。
III.……
(1)上图中仪器a的名称为
(2)步骤I将Co2+转化[Co(NH3)6]3+过程中,先加浓氨水,后加H2O2溶液的目的是
(3)步骤II中采用“冰水浴”的是
(4)[Co(NH3)6]Cl3配合物的内界为
您最近一年使用:0次
【推荐2】我国科学家首次报道了双金属Cu/Ni催化剂催化醛亚胺酯的不对称苄基化反应,获得了一系列含有苄基(-CH2C6H5)取代的季碳氨基酸衍生物。这是双金属催化剂在不对称合成领域的重大突破。
(1)基态Cu原子中,电子占据的最高能层的符号为_______ ,该能层具有的原子轨道数为_______ 。CuCl2在火焰上灼烧时火焰的颜色为绿色,从微观角度解释部分金属元素在火焰上灼烧呈现特殊颜色的原因_______ 。
(2)4-氯卞氯(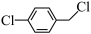 )可用于有机合成中间体。
)可用于有机合成中间体。
①L-苯丙氨酸( )分子中C、N、O三种元素原子的第一电离能由大到小的顺序为
)分子中C、N、O三种元素原子的第一电离能由大到小的顺序为_______ 。
②沸点比较:4-氯卞氯_______ (填“>”、“<”或“=”)L—苯丙氨酸(填“>”、“<”或“=”),主要原因为_______ 。
(3)[Ni(NH3)6]SO4晶体中,1 mol配离子含有的σ键个数为_______ 个, 的空间构型为
的空间构型为_______ 。
(4)Ni和La的合金是目前广泛使用的储氢材料,该合金的晶胞结构如图所示。已知该晶体摩尔质量为M g/mol,密度为d g/cm3,La元素和Ni元素的原子半径分别为r1cm、r2 cm。设NA为阿伏加德罗常数的值,则该晶体中原子的空间利用率(空间利用率:构成晶体的粒子总体积在整个晶体空间所占有的体积百分比)为_______ (写出表达式即可)。

(1)基态Cu原子中,电子占据的最高能层的符号为
(2)4-氯卞氯(
 )可用于有机合成中间体。
)可用于有机合成中间体。①L-苯丙氨酸(
 )分子中C、N、O三种元素原子的第一电离能由大到小的顺序为
)分子中C、N、O三种元素原子的第一电离能由大到小的顺序为②沸点比较:4-氯卞氯
(3)[Ni(NH3)6]SO4晶体中,1 mol配离子含有的σ键个数为
 的空间构型为
的空间构型为(4)Ni和La的合金是目前广泛使用的储氢材料,该合金的晶胞结构如图所示。已知该晶体摩尔质量为M g/mol,密度为d g/cm3,La元素和Ni元素的原子半径分别为r1cm、r2 cm。设NA为阿伏加德罗常数的值,则该晶体中原子的空间利用率(空间利用率:构成晶体的粒子总体积在整个晶体空间所占有的体积百分比)为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】以 、
、 和
和 为主要成分的镀液可在某些材料上镀铜,原理如下:
为主要成分的镀液可在某些材料上镀铜,原理如下: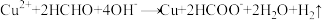
(1)基态 原子的价层电子排布式为
原子的价层电子排布式为_______ 。
(2)根据反应原理分析
①镀铜反应中,利用了 的
的_______ 性。
②选择 进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
进行化学镀铜的原因之一是它易溶于水。下列分析正确的是_______
a. 、
、 均属于极性分子
均属于极性分子
b. 与
与 之间能形成氢键
之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、
、 、
、 三种微粒,空间结构为三角形的是
三种微粒,空间结构为三角形的是_______ 。
(4)为防止 与
与 形成沉淀,可加入
形成沉淀,可加入 使
使 形成配合物。
形成配合物。 能电离出
能电离出 和
和 。
。
 (EDTA4-)
(EDTA4-)
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是_______ 。
(5)铜—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。 位于
位于_______ 区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:

上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①_______ 。
②聚合物有可能与 配位。
配位。
 、
、 和
和 为主要成分的镀液可在某些材料上镀铜,原理如下:
为主要成分的镀液可在某些材料上镀铜,原理如下: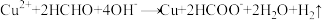
(1)基态
 原子的价层电子排布式为
原子的价层电子排布式为(2)根据反应原理分析
①镀铜反应中,利用了
 的
的②选择
 进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
进行化学镀铜的原因之一是它易溶于水。下列分析正确的是a.
 、
、 均属于极性分子
均属于极性分子b.
 与
与 之间能形成氢键
之间能形成氢键c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、
、 、
、 三种微粒,空间结构为三角形的是
三种微粒,空间结构为三角形的是(4)为防止
 与
与 形成沉淀,可加入
形成沉淀,可加入 使
使 形成配合物。
形成配合物。 能电离出
能电离出 和
和 。
。 (EDTA4-)
(EDTA4-) 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是(5)铜—镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。
 位于
位于(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:

上述方法不适合在该聚酰亚胺基材上直接镀铜。原因是:
①
②聚合物有可能与
 配位。
配位。
您最近一年使用:0次



