某硫与锌元素组成的化合物M不溶于水、易溶于酸,见阳光色变暗。若在该化合物中加入微量的Cu、Mn、Ag做活化剂,经光照后,能发出不同颜色的荧光。回答下列问题:
(1)基态铜原子的价电子排布图为_____ 。第一电离能介于Si、P之间的第三周期元素为_____ (填元素符号)。
(2)SO2中S的杂化类型为_____ ,该分子的空间构型为_____ 。
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为_____ NA,NH3分子在独立存在时H-N-H键角为107°,[Ag(NH3)2]+中H-N-H键角变大的原因:________________ 。
(4)M的晶胞结构如图。
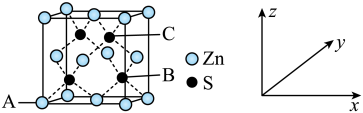
①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为___ 个,M的化学式__ 。
②Zn的第三电离能大于Cu的第三电离能的原因是_____ 。
(1)基态铜原子的价电子排布图为
(2)SO2中S的杂化类型为
(3)1mol[Ag(NH3)2]OH中含有σ键的数目为
(4)M的晶胞结构如图。

①观察图形推测,该晶体中每个Zn2+周围距离相等且最近的Zn2+数目为
②Zn的第三电离能大于Cu的第三电离能的原因是
更新时间:2023-09-12 06:43:09
|
相似题推荐
【推荐1】填写下列空白[第(1)~(3)小题用元素符号填写]。
(1)第三周期原子半径最小的元素___________ ;
(2)电负性最大的元素___________ ;
(3)第四周期中第一电离能最小的元素___________ ;
(4)最外层电子排布为4s24p1的原子的核电荷数为___________ ;
(5)周期表中最活泼的非金属元素原子的轨道表示式为___________ ;
(6)某元素核外有三个电子层,最外层电子数是核外电子总数的 ,写出该元素的离子结构示意图
,写出该元素的离子结构示意图___________ ;
(1)第三周期原子半径最小的元素
(2)电负性最大的元素
(3)第四周期中第一电离能最小的元素
(4)最外层电子排布为4s24p1的原子的核电荷数为
(5)周期表中最活泼的非金属元素原子的轨道表示式为
(6)某元素核外有三个电子层,最外层电子数是核外电子总数的
 ,写出该元素的离子结构示意图
,写出该元素的离子结构示意图
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】C、N化合物对人类生存环境有重要影响。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为_________ 。
(2)C、N、O三种元素的第一电离能由小到大的顺序为_________ 。
(3)键角:NH3__________ (填“>“<”或“=”)H2O;NH3的VSEPR模型为_________ 。
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为_________ 。
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为_________ (填元素符号),原因是_________ 。
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。_________ 。
②2号原子的坐标为_________ 。
③该晶体的密度为__________ g/cm3。
Ⅰ.汽车尾气中的NO和CO在催化剂作用下可生成无毒无害的气体,工业废气中的NO可被NH3在高温催化作用下还原为N2和H2O。
(1)原子序数为N元素两倍的元素的基态原子的外围电子排布图为
(2)C、N、O三种元素的第一电离能由小到大的顺序为
(3)键角:NH3
Ⅱ.NO与血红蛋白中的[Fe(H2O)6]2+结合生成[Fe(NO)(H2O)5]2+可导致人体的血红蛋白丧失携氧能力。
(4)Fe2+的配位数为
(5)在[Fe(NO)(H2O)5]2+中,配体NO提供配位的原子为
Ⅲ.C元素与N元素形成的一种超硬晶体的晶胞结构如图所示(8个碳原子位于立方体的顶点,4个碳原子位于立方体的面心,4个氮原子在立方体内),设晶胞参数为anm,NA为阿伏加德罗常数的值,1号原子的坐标为(0,0,0)、3号原子的坐标为(1,1,1)。
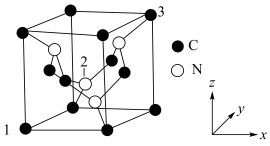
②2号原子的坐标为
③该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】绪(Ge)是半导体元素,应用广泛,回答下列问题:
(1)下列为Ge价电子层电子排布图表示的状态中,能量最低和最高的分别为____ 、_____ (填选项)。
A. B.
B.
C.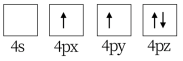 D.
D.
(2)GeH4的空间构型为____ ;比较与同锗族的氢化物的沸点如表所示,分析其变化规律及原因____ 。
(3)有机锗化合物A有一定的医疗保健作用,其结构简式为CF3N=GeH2,则Ge的杂化形式为____ ,碳原子与其它原子结合的键的种类为_____ 。
(4)Li2GeF6可以作为锂电池的电解质,则Li、Ge、F电负性由大到小的顺序为_____ 。
(5)Ge晶胞如下,其中原子坐标参数A为(0,0,0);B为( ,0,
,0, ),D为(
),D为( ,
, ,
, )。则C原子的坐标参数为
)。则C原子的坐标参数为_____ 。
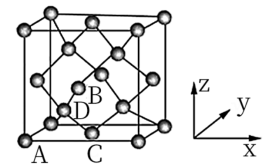

(6)氮化锗具有耐腐蚀、硬度高等优点,晶体中锗原子与氮原子之间存在明显的s-p杂化现象,氮化锗晶体属于____ 晶体。一种氮化锗晶胞的球棍模型如图,晶体中n(Ge)/n(N)=____ ,若晶胞底面正方形的边长为anm,阿伏加 德罗常数值为NA,晶体的密度为ρg/cm3,则长方体的高为____ nm(列出计算式)。
(1)下列为Ge价电子层电子排布图表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(2)GeH4的空间构型为
| CH4 | SiH4 | GeH4 | |
| 沸点/℃ | -161.5 | -119 | -88.1 |
(3)有机锗化合物A有一定的医疗保健作用,其结构简式为CF3N=GeH2,则Ge的杂化形式为
(4)Li2GeF6可以作为锂电池的电解质,则Li、Ge、F电负性由大到小的顺序为
(5)Ge晶胞如下,其中原子坐标参数A为(0,0,0);B为(
 ,0,
,0, ),D为(
),D为( ,
, ,
, )。则C原子的坐标参数为
)。则C原子的坐标参数为

(6)氮化锗具有耐腐蚀、硬度高等优点,晶体中锗原子与氮原子之间存在明显的s-p杂化现象,氮化锗晶体属于
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】无水四氯化锡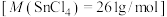 是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成
是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成 ,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水
,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水 ,请回答有关问题:
,请回答有关问题:______ 。
(2)A中盛放 晶体的仪器名称为
晶体的仪器名称为______ ,在其中发生反应的化学方程式是______ 。
(3)整个实验装置的连接顺序是A→______ →B→C→______ (装置可重复选用),若缺少装置F,则收集器C中发生反应的化学方程式为______ 。
(4)收集器C中收集到的液体略显黄色,原因是______ ,C中上方冷水的作用是______ 。
(5)除氯后测定最后产品的纯度。量取 ,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液
,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液 (接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为______ ,产品的纯度为______ %。
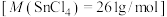 是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成
是一种重要的工业原料,其在常温下为无色液体,沸点114℃,在空气中极易水解生成 ,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水
,液态四氯化锡对很多非极性分子有一定的溶解度。实验室可选用以下装置用熔融的锡与氯气反应制备无水 ,请回答有关问题:
,请回答有关问题:
(2)A中盛放
 晶体的仪器名称为
晶体的仪器名称为(3)整个实验装置的连接顺序是A→
(4)收集器C中收集到的液体略显黄色,原因是
(5)除氯后测定最后产品的纯度。量取
 ,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液
,ag/mL的样品,置于已称重含20mL水的称量瓶中,混合后,移入锥形瓶,加入200mL水和2滴1%甲基橙指示液,用b mol/L的NaOH标准液滴定,消耗标准液 (接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
(接近终点时,每滴加一滴标准液须待沉淀沉降后观察澄清液体的颜色)。滴定到达终点的实验现象为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】第四周期过渡元素Mn,Fe,Ti可与C,H,O形成多种化合物.
(1)H,C,O,N四种元素的电负性由小到大的顺序为___ 。
(2)Mn基态原子的电子排布式可表示为___ ,CO 的空间构型
的空间构型___ (用文字表述)。
(3)下列叙述正确的是___ (填字母)。
A.CH2O与水分子间能形成氢键
B.CH3COOH和苯分子中的碳原子均采用sp2杂化
C.CH2=CH-CHO分子中含有7个σ键和2个π键
D.CO的结构式可表示为:C=O
E.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(4)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为___ 。

(1)H,C,O,N四种元素的电负性由小到大的顺序为
(2)Mn基态原子的电子排布式可表示为
 的空间构型
的空间构型(3)下列叙述正确的是
A.CH2O与水分子间能形成氢键
B.CH3COOH和苯分子中的碳原子均采用sp2杂化
C.CH2=CH-CHO分子中含有7个σ键和2个π键
D.CO的结构式可表示为:C=O
E.CO2晶体的熔点、沸点都比二氧化硅晶体的低
(4)在自然界中TiO2有金红石、板钛矿、锐钛矿三种晶型,其中金红石的晶胞如图所示,则其中Ti4+的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】铜、铁、锌原子结构的特殊性,决定了它们的单质及其化合物在化工生产中发挥着重要的作用,回答下列问题。
(1) 的价电子排布式为
的价电子排布式为___________ ,基态铜原子最高能级电子云轮廓图形状为___________ 。
(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
① 中阴离子的空间构型为
中阴离子的空间构型为___________ 。
② 中
中 的键角比独立
的键角比独立 的键角
的键角___________ (填“大”“小”或“相等”),前10号元素中,第一电离能比N大的元素有___________ 种。
③铜元素会形成多种配离子, 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:___________ 。
(3)一个配体中有两个配位原子的配体叫双齿配体, 就是一种双齿配体。
就是一种双齿配体。 的配位数是6,硫酸铁溶液中加入
的配位数是6,硫酸铁溶液中加入 后生成配离子为
后生成配离子为___________ 。(用化学符号表示)
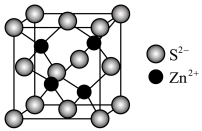
(4)ZnS晶胞如图所示: 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有___________ 个。
②已知该晶胞密度为 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为___________ pm。(列出计算式即可)
(1)
 的价电子排布式为
的价电子排布式为(2)当黄铜受到氨腐蚀时,会出现“龟裂”现象,生成四氨合铜配合物。
①
 中阴离子的空间构型为
中阴离子的空间构型为②
 中
中 的键角比独立
的键角比独立 的键角
的键角③铜元素会形成多种配离子,
 的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:
的氨水溶液在空气中放置迅速由无色变为深蓝色,写出该过程的离子方程式:(3)一个配体中有两个配位原子的配体叫双齿配体,
 就是一种双齿配体。
就是一种双齿配体。 的配位数是6,硫酸铁溶液中加入
的配位数是6,硫酸铁溶液中加入 后生成配离子为
后生成配离子为(4)ZnS晶胞如图所示:
 周围与它最接近且距离相等的
周围与它最接近且距离相等的 有
有②已知该晶胞密度为
 ,阿伏加德罗常数为
,阿伏加德罗常数为 ,则晶胞边长为
,则晶胞边长为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】以NaOH、 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: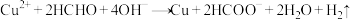
(1)基态Cu原子的价层电子轨道表示式为______
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的______ 性。
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是______ 。
a.HCHO、 均属于极性分子
均属于极性分子
b.HCHO与 之间能形成氢键
之间能形成氢键
c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是______ 。
(4)为防止 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是______ 。
(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于______ 区。
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
①______ 。
②聚酰亚胺在碱性条件下会发生水解。
 和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下:
和HCHO为主要成分的镀液可在某些材料上镀铜,原理如下: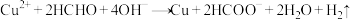
(1)基态Cu原子的价层电子轨道表示式为
(2)根据反应原理分析
①镀铜反应中,利用了HCHO的
②选择HCHO进行化学镀铜的原因之一是它易溶于水。下列分析正确的是
a.HCHO、
 均属于极性分子
均属于极性分子b.HCHO与
 之间能形成氢键
之间能形成氢键c.在醛基的碳氧双键中,电子偏向碳原子
(3)镀液中的
 、HCHO、
、HCHO、 三种微粒,空间结构为平面三角形的是
三种微粒,空间结构为平面三角形的是(4)为防止
 与
与 形成沉淀,可加入EDTA使
形成沉淀,可加入EDTA使 形成配合物。EDTA能电离出
形成配合物。EDTA能电离出 和
和
 (
( )
)
 中除部分O外,还能与
中除部分O外,还能与 配位的原子是
配位的原子是(5)铜―镍镀层能增强材料的耐蚀性。按照核外电子排布,把元素周期表划分为5个区。Ni位于
(6)聚酰亚胺具有高强度、耐紫外线、优良的热氧化稳定性等性质。某聚酰亚胺具有如下结构特征:
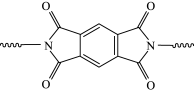
①
②聚酰亚胺在碱性条件下会发生水解。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】第四周期的Cr、Fe、Co、Ni、Cu、Zn等许多金属能形成配合物,单质铁、砷及它们的化合物广泛应用于超导体材料等领域,请回答下列问题:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2) 是一种很好的配体,
是一种很好的配体, 的沸点
的沸点_______ (填“>”“=”或“<”) ,
, 中心原子的杂化类型为
中心原子的杂化类型为_______ ,分子的空间构型为_______ 。
(3)N原子核外有_______ 种不同运动状态的电子。基态N原子中,能量最高的电子所占据的原子轨道的形状为_______ 。
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为_______ 。
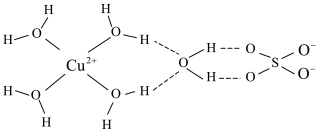
(5)As的卤化物的熔点如下,表中卤化物熔点差异的原因是_______ 。
(6)向 溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表
溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表 ,则
,则 与氮原子之间形成的化学键是
与氮原子之间形成的化学键是_______ , 的配位数为
的配位数为_______ 。

(1)
 的核外电子排布式为
的核外电子排布式为(2)
 是一种很好的配体,
是一种很好的配体, 的沸点
的沸点 ,
, 中心原子的杂化类型为
中心原子的杂化类型为(3)N原子核外有
(4)科学家通过X射线测得胆矾结构示意图可简单表示如图,图中虚线表示的作用力为

(5)As的卤化物的熔点如下,表中卤化物熔点差异的原因是
| 物质 |  | 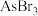 | 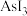 |
| 熔点/K | 256.8 | 304 | 413 |
(6)向
 溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表
溶液中滴入EDTA试剂可得配合物A,其结构如图所示,图中M代表 ,则
,则 与氮原子之间形成的化学键是
与氮原子之间形成的化学键是 的配位数为
的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】有机阳离子是一类带正电荷的粒子,如 (甲铵离子)、
(甲铵离子)、 (二甲基氧正离子)、
(二甲基氧正离子)、 (胍离子)等。
(胍离子)等。
(1)C原子价电子的轨道表示式为________ 。第一电离能N____ O(填“>”或“<”),原因是__________ 。
(2) 中N的杂化方式为
中N的杂化方式为____________________ 。从化学键的角度描述由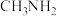 (甲胺)形成
(甲胺)形成 的过程
的过程____________________ 。
(3)分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。
)。 为平面结构,则
为平面结构,则 中的大
中的大 键应表示为
键应表示为__________ 。
(4)某材料中含有机阳离子,其晶胞结构如图所示。
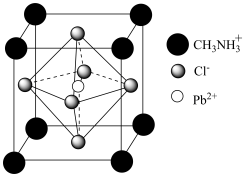
①化学式为____________________ ;其中 周围最临近的
周围最临近的 个数为
个数为__________ 。
②已知晶体密度为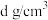 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,列式计算两个
,列式计算两个 之间的最短距离为
之间的最短距离为______  。
。
 (甲铵离子)、
(甲铵离子)、 (二甲基氧正离子)、
(二甲基氧正离子)、 (胍离子)等。
(胍离子)等。(1)C原子价电子的轨道表示式为
(2)
 中N的杂化方式为
中N的杂化方式为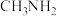 (甲胺)形成
(甲胺)形成 的过程
的过程(3)分子中的大
 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数(如苯分子中的大
键的电子数(如苯分子中的大 键可表示为
键可表示为 )。
)。 为平面结构,则
为平面结构,则 中的大
中的大 键应表示为
键应表示为(4)某材料中含有机阳离子,其晶胞结构如图所示。

①化学式为
 周围最临近的
周围最临近的 个数为
个数为②已知晶体密度为
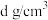 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,列式计算两个
,列式计算两个 之间的最短距离为
之间的最短距离为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】四种短周期主族元素X、Y、Z、R的原子序数与原子半径关系如图1所示,且原子序数均不超过10.由这四种元素组成一种电解质溶剂的分子结构如图2所示。
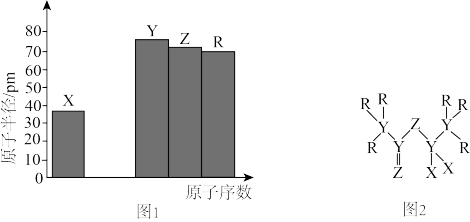
请回答下列问题:
(1)基态Y原子核外电子最高能级的电子云轮廓图为___________ 。
(2)X、Y、Z能组成多种二元或三元化合物。写出一种符合下列条件的结构简式:
①所有原子共直线的烃类且相对分子质量最小:___________ 。
②既能与溴反应,又能与 溶液反应的烃的衍生物:
溶液反应的烃的衍生物:___________ 。
③σ键、π键数目之比等于 的四原子分子:
的四原子分子:___________ 。
④碳原子有3种杂化类型且相对分子质量最小的链状烃:___________ 。
(3)Y和Z组成的简单阴离子空间构型是___________ 。
(4)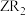 分子的VSEPR模型为
分子的VSEPR模型为___________ 。
(5)R与碱金属元素组成的化合物熔点与碱金属原子序数的关系如图3所示。
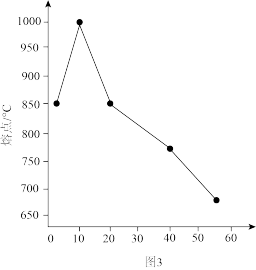
氟化钠、氟化钾、氟化铷、氟化铯的熔点依次降低,其主要原因是___________ 。在上述碱金属元素的氟化物中,离子键百分数最大的是___________ (填名称)。

请回答下列问题:
(1)基态Y原子核外电子最高能级的电子云轮廓图为
(2)X、Y、Z能组成多种二元或三元化合物。写出一种符合下列条件的结构简式:
①所有原子共直线的烃类且相对分子质量最小:
②既能与溴反应,又能与
 溶液反应的烃的衍生物:
溶液反应的烃的衍生物:③σ键、π键数目之比等于
 的四原子分子:
的四原子分子:④碳原子有3种杂化类型且相对分子质量最小的链状烃:
(3)Y和Z组成的简单阴离子空间构型是
(4)
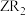 分子的VSEPR模型为
分子的VSEPR模型为(5)R与碱金属元素组成的化合物熔点与碱金属原子序数的关系如图3所示。

氟化钠、氟化钾、氟化铷、氟化铯的熔点依次降低,其主要原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】金刚石、石墨、二氧化碳、氯化铯、氯化钠的结构模型如图所示(石墨仅表示出其中的一层结构):

(1)金刚石属于_______ 晶体,金刚石晶体结构中最小的环为六元环,每个碳与周围四个碳原子构成_______ 结构,键角为_______ 。
(2)石墨属于_______ 晶体,每个六元环平均含有_______ 个碳原子。
(3)金刚石与石墨互为_______ 。
(4) 晶体属于
晶体属于_______ 晶体,每个 分子周围有
分子周围有_______ 个与之紧邻且等距的 分子。
分子。
(5) 晶体属于
晶体属于_______ 晶体,晶体中每个 周围紧邻且等距的
周围紧邻且等距的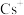 数目为
数目为_______ 。
(6) 晶体属于
晶体属于_______ 晶体,晶体中 的配位数为
的配位数为_______ , 周围紧邻且等距的
周围紧邻且等距的 形成的空何构型为
形成的空何构型为_______ 。

(1)金刚石属于
(2)石墨属于
(3)金刚石与石墨互为
(4)
 晶体属于
晶体属于 分子周围有
分子周围有 分子。
分子。(5)
 晶体属于
晶体属于 周围紧邻且等距的
周围紧邻且等距的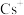 数目为
数目为(6)
 晶体属于
晶体属于 的配位数为
的配位数为 周围紧邻且等距的
周围紧邻且等距的 形成的空何构型为
形成的空何构型为
您最近一年使用:0次




