回答下列问题:
(1)下列物质中,属于电解质的是_____ (填序号,下同),属于非电解质的是_____ ,属于强电解质的是_____ ,属于弱电解质的是_____ 。
①H2SO4②盐酸③氯气④硫酸钡⑤乙醇⑥铜⑦H2CO3⑧氯化氢⑨CH3COOH⑩氨气⑪CO2
(2)根据键能数据计算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热△H=______ 。
(3)泡沫灭火器内装有NaHCO3饱和溶液,该溶液呈碱性的原因是_____ (用离子方程式表示);灭火器内另一容器中装有Al2(SO4)3溶液,该溶液呈酸性的原因是_____ (用离子方程式表示);当意外失火时,使泡沫灭火器倒过来摇动即可使药液混合,喷出大量的白色泡沫,阻止火势蔓延,其相关的离子方程式为______ 。
(1)下列物质中,属于电解质的是
①H2SO4②盐酸③氯气④硫酸钡⑤乙醇⑥铜⑦H2CO3⑧氯化氢⑨CH3COOH⑩氨气⑪CO2
(2)根据键能数据计算CH4(g)+4F2(g)=CF4(g)+4HF(g)的反应热△H=
| 化学键 | C-H | C-F | H-F | F-F |
| 键能/kJ•mol-1 | 414 | 489 | 565 | 155 |
更新时间:2023-03-15 15:14:35
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】请按要求填空。
(1)除去乙醇中溶解的食盐,方法是___ ;除去Ca(OH)2溶液中悬浮的CaCO3颗粒用___ ;除去CO2中少量的HCl通入___ 溶液中洗气。
(2)除去KCl溶液中含有的SO42-离子,依次加入溶液为(填化学式):___ 、___ 、___ 。
(3)①稀硫酸②液态氯化氢③NaOH溶液④蔗糖溶液⑤Na3PO4固体⑥铜丝⑦液氯⑧C2H5OH(酒精)⑨熔融NaCl。其中:上述状态中能导电的是___ ;属于非电解质的是___ 。
(1)除去乙醇中溶解的食盐,方法是
(2)除去KCl溶液中含有的SO42-离子,依次加入溶液为(填化学式):
(3)①稀硫酸②液态氯化氢③NaOH溶液④蔗糖溶液⑤Na3PO4固体⑥铜丝⑦液氯⑧C2H5OH(酒精)⑨熔融NaCl。其中:上述状态中能导电的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】现有以下物质:①氨气② ③
③ ④
④ 胶体⑤
胶体⑤ 溶液⑥S⑦亚硫酸氢钠⑧蔗糖
溶液⑥S⑦亚硫酸氢钠⑧蔗糖
(1)属于非电解质的是_______ (填序号,下同),属于强电解质的是_______
(2)向④中逐滴滴加⑤,可观察到产生红褐色沉淀,后沉淀溶解得到黄色溶液,试写出沉淀溶解的离子方程式:_______ 。
(3)写出⑦在水溶液的电离方程式:_______ 。
(4)②与⑥所对应的元素,非金属性强的是_______ (填元素符号),结合原子结构的知识解释以上结论_______ 。
 ③
③ ④
④ 胶体⑤
胶体⑤ 溶液⑥S⑦亚硫酸氢钠⑧蔗糖
溶液⑥S⑦亚硫酸氢钠⑧蔗糖(1)属于非电解质的是
(2)向④中逐滴滴加⑤,可观察到产生红褐色沉淀,后沉淀溶解得到黄色溶液,试写出沉淀溶解的离子方程式:
(3)写出⑦在水溶液的电离方程式:
(4)②与⑥所对应的元素,非金属性强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】已知下列各物质:
①CO2 ②NaHCO3溶液 ③熔融NaOH ④CaCO3⑤CH3COOH ⑥NH3•H2O ⑦乙醇 ⑧液态氯化氢
I.①能导电的物质___________ ;(请用序号填空,下同,多选错选不给分)
②强电解质______________ ;
③非电解质______________ ;
II.按要求写出方程式。
(1)②的电离方程式:____________
(2)③与⑤在水溶液中反应的化学方程式___________ ;
(3)碳酸钙和盐酸(写出对应的离子方程式)____________
①CO2 ②NaHCO3溶液 ③熔融NaOH ④CaCO3⑤CH3COOH ⑥NH3•H2O ⑦乙醇 ⑧液态氯化氢
I.①能导电的物质
②强电解质
③非电解质
II.按要求写出方程式。
(1)②的电离方程式:
(2)③与⑤在水溶液中反应的化学方程式
(3)碳酸钙和盐酸(写出对应的离子方程式)
您最近一年使用:0次
【推荐1】试从化学键的角度理解化学反应中的能量变化。(以2H2+O2===2H2O为例说明),已知:E反表示反应物(2H2+O2)所具有的总能量,E生表示生成物(2H2O)所具有的总能量。又知:拆开1moL H2中的化学键需要吸收436kJ能量,拆开1moL O2中的化学键需要吸收496kJ能量,形成水分子中的1moLH—O键能够释放463KJ能量。
⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要______ (填“吸收”或“放出”)能量,能量变化值的大小△E=_________ (用E反和E生表示)
⑵从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=______ KJ;形成生成物中的化学键放出的总能量为=______ KJ。E吸______ E放(填“>”或“<”),所以该反应要_____ (填“吸收”或“放出”)能量,能量变化值的大小△E=____ KJ(填数值)
⑶由图可知,化学反应的本质是________________________________ 化学反应中能量变化的主要原因是________________ (从总能量说明)
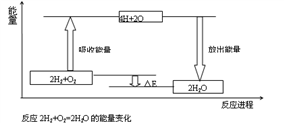
⑴从宏观角度看:反应物所具有的总能量高于生成物所具有的总能量,所以该反应要
⑵从微观角度看:断裂反应物中的化学键吸收的总能量为E吸=
⑶由图可知,化学反应的本质是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业合成氨中氢气的重要来源是水煤气,有关反应如下:① ;②
;② ,它们的能量变化如图所示。
,它们的能量变化如图所示。


(1)写出图1表示的反应的热化学方程式:_______ 。
(2)
_______  。
。
(3)已知几种共价键的键能如表所示:
则a为_______ 。
(4)在恒容密闭容器中发生反应: 。达到平衡后,改变条件使CO的平衡转化率增大,则该反应的
。达到平衡后,改变条件使CO的平衡转化率增大,则该反应的
_______ (填“增大”“减小”或“不变”)。
 ;②
;② ,它们的能量变化如图所示。
,它们的能量变化如图所示。

(1)写出图1表示的反应的热化学方程式:
(2)

 。
。(3)已知几种共价键的键能如表所示:
| 化学键 |  |  | C O O |  |
 | a | 799 | 1076 | 465 |
(4)在恒容密闭容器中发生反应:
 。达到平衡后,改变条件使CO的平衡转化率增大,则该反应的
。达到平衡后,改变条件使CO的平衡转化率增大,则该反应的
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】Ⅰ.(1)在反应A(g)+3B(g)===2C(g)中,若以物质A表示的该反应的化学反应速率为0.2 mol·L-1·min-1,则以物质B的化学反应速率为__________ mol·L-1·min-1。
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=_________ mol·L-1·s-1。
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g) 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有______ mol A,此时C的物质的量浓度为________ ,若此后各物质的量均不再变化,则证明此可逆反应达到了______ 的程度。
A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =________ 。
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)________ 。
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
(2)在2 L的密闭容器中,充入2 mol N2和3 mol H2,在一定条件下发生反应,3 s后测得N2为1.9 mol,则以H2的浓度变化表示的此化学反应速率为vB=
(3)将10 mol A和5 mol B放入容积为10 L的密闭容器中,某温度下发生反应:3A(g)+B(g)
 2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有
2C(g),在最初2 s内,消耗A的平均速率为0.06 mol·L-1·s-1,则在2 s时,容器中有A.反应彻底 B.反应终止 C.化学平衡 D.无法判断
Ⅱ. 已知:①2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1;②N2(g)+O2(g)===2NO(g) ΔH=+180 kJ·mol-1,则2CO(g)+2NO(g)===N2(g)+2CO2(g)的ΔH =
Ⅲ. 下列热化学方程式书写正确的是(ΔH的绝对值均正确)
A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热)
B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=-57.3 kJ·mol-1(中和热)
C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(燃烧热)
D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热)
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】NH4Cl溶液呈酸性的原因是______ (用离子反应方程式表示)。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】已知: CH3COOH 的酸性强于H2CO3。
(1)请写出H2CO3的电离方程式_____________________________ 。
(2)请写出CH3COONa 的水解离子方程式_____________________________ 。
(3)浓度均为0.1mol/L的CH3COONa 溶液和Na2CO3溶液,pH 前者_______ 后者(填“>”、“<”或“=”)。
(1)请写出H2CO3的电离方程式
(2)请写出CH3COONa 的水解离子方程式
(3)浓度均为0.1mol/L的CH3COONa 溶液和Na2CO3溶液,pH 前者
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】亚磷酸(H3PO3)是二元酸,与足量NaOH溶液反应生成Na2HPO3。
(1)PCl3水解可制取亚磷酸,化学方程式为__ 。
(2)H3PO3溶液中存在电离平衡:H3PO3 H2PO
H2PO +H+。
+H+。
①某温度下,0.10mol·L-1的H3PO3溶液pH=1.6,即溶液中c(H+)=2.5×10-2mol·L-1。该温度下上述电离平衡的平衡常数K=__ (H3PO3的第二步电离忽略不计,结果保留两位有效数字)。
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH___ 7(填“>”、“=”或“<”),已知该溶液中离子浓度由大到小的顺序是c(Na+)>c(HPO )>c(OH-)>c(H2PO
)>c(OH-)>c(H2PO )>c(H+)。
)>c(H+)。
(1)PCl3水解可制取亚磷酸,化学方程式为
(2)H3PO3溶液中存在电离平衡:H3PO3
 H2PO
H2PO +H+。
+H+。①某温度下,0.10mol·L-1的H3PO3溶液pH=1.6,即溶液中c(H+)=2.5×10-2mol·L-1。该温度下上述电离平衡的平衡常数K=
②根据H3PO3的性质可推测Na2HPO3稀溶液的pH
 )>c(OH-)>c(H2PO
)>c(OH-)>c(H2PO )>c(H+)。
)>c(H+)。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】正误判断
1.在酒精灯加热条件下,Na2CO3、NaHCO3固体都会分解_____
2.向Na2CO3饱和溶液中通入足量CO2,会有NaHCO3晶体析出_____
3.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液_____
4.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡_____
5.用热的纯碱溶液清洗炊具上的油污时,不涉及化学变化_____
1.在酒精灯加热条件下,Na2CO3、NaHCO3固体都会分解
2.向Na2CO3饱和溶液中通入足量CO2,会有NaHCO3晶体析出
3.用酚酞溶液可鉴别饱和食盐水和饱和碳酸钠溶液
4.将稀盐酸滴入碳酸钠与氢氧化钠的混合溶液中,立即产生气泡
5.用热的纯碱溶液清洗炊具上的油污时,不涉及化学变化
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)在配制AlCl3溶液时,Al3+会部分水解而使溶液呈酸性,水解的离子方程式为___ ;为了防止发生水解,可以加入少量的___ ;溶液加热蒸发灼烧得到固体___ 。
(2)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=__ mol·L-1(Ksp[Cu(OH)2]=2.2×10-20)。若在0.1mol·L-1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是___ mol·L-1。
(3)泡沫灭火剂包括Al2(SO4)3溶液、NaHCO3溶液及起泡剂,使用时发生的离子方程式是___ 。
(1)在配制AlCl3溶液时,Al3+会部分水解而使溶液呈酸性,水解的离子方程式为
(2)在0.10mol·L-1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌,有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时,c(Cu2+)=
(3)泡沫灭火剂包括Al2(SO4)3溶液、NaHCO3溶液及起泡剂,使用时发生的离子方程式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】运用化学反应原理研究氮及其化合物的反应有重要意义。
(1)铵态氮肥不能与含碳酸钾的草木灰混合使用,原因是_______ 。
(2)工业合成氨的反应为 。若在恒温,恒压条件下向平衡体系中通入氩气,平衡
。若在恒温,恒压条件下向平衡体系中通入氩气,平衡_______ (填“向左”、“向右”或“不”)移动;使用催化剂_______ (填“增大”、“减小”或“不改变”)反应的 。
。
(3)合成氨过程中发生的反应机理如下:
I. (慢)
(慢)
II. (快)
(快)
①合成氨反应的速率快慢主要取决于_______ (填“I”或“II”)。
②合成氨反应的催化剂是_______ (填化学式)。
③反应I的活化能_______ (填“>”、“=”或“<”)反应II的活化能。
(4)25℃下,向浓度均为 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成_______ (填化学式)沉淀(25℃时, ,
, )。
)。
(1)铵态氮肥不能与含碳酸钾的草木灰混合使用,原因是
(2)工业合成氨的反应为
 。若在恒温,恒压条件下向平衡体系中通入氩气,平衡
。若在恒温,恒压条件下向平衡体系中通入氩气,平衡 。
。(3)合成氨过程中发生的反应机理如下:
I.
 (慢)
(慢)II.
 (快)
(快)①合成氨反应的速率快慢主要取决于
②合成氨反应的催化剂是
③反应I的活化能
(4)25℃下,向浓度均为
 的
的 和
和 混合溶液中逐滴加入氨水,先生成
混合溶液中逐滴加入氨水,先生成 ,
, )。
)。
您最近一年使用:0次



