镍氢电池是一种新型绿色电池,利用废旧镍氢电池的金属电极芯(主要成分为 Ni(OH)2、Co(OH)2及少量铁、铝的氧化物等)生产硫酸镍、碳酸钴工艺流程如下图:
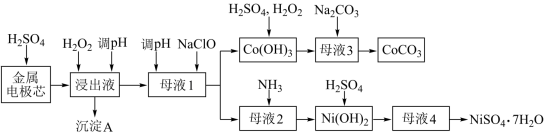
已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
回答下列问题:
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有_______ (写出一种合理方法即可),向 Co(OH)3 中加入H2O2 的目的是_______ 。
(2)沉淀 A 的主要成分是_______ (填化学式),“浸出液”调节 pH 的范围为_______ 。
(3)“母液3”中控制Na2CO3用量使终点pH 为9.5,此时c(Co2+)小于_______ mol∙L-1(已知:Ksp[Co(OH)2]=1.6×10-15)。
(4)用滴定法测定 NiSO4∙7H2O 产品中镍元素含量。取 2.00g 样品,酸溶后配成 100mL 溶液,取 20.00mL 于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为 0.100mol∙L-1 的 Na2H2Y 标准液滴定,重复操作2~3 次,消耗 Na2H2Y 标准液平均值为 12.40mL。
已知:i. Ni2++H2Y2-=[NiY]2-+2H+;ii. 紫脲酸胺:紫色试剂,遇 Ni2+显橙黄色。
①滴定至终点的现象是_______ ;②样品中镍元素的质量分数为_______ %(保留 3 位有效数字)。
(5)NiSO4 在强碱溶液中和 NaClO 反应,可制得碱性镍镉电池电极材料 NiOOH,该反应的离子方程式为_______ 。

已知:部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
| 离子 | Fe2+ | Fe3+ | Al3+ | Ni2+ | Co2+ |
| 开始沉淀时 pH | 6.3 | 1.5 | 3.4 | 6.2 | 7.15 |
| 完全沉淀时 pH | 8.3 | 2.8 | 4.7 | 8.9 | 9.15 |
(1)用硫酸浸取金属电极芯时,提高浸取效率的方法有
(2)沉淀 A 的主要成分是
(3)“母液3”中控制Na2CO3用量使终点pH 为9.5,此时c(Co2+)小于
(4)用滴定法测定 NiSO4∙7H2O 产品中镍元素含量。取 2.00g 样品,酸溶后配成 100mL 溶液,取 20.00mL 于锥形瓶中进行滴定,滴入几滴紫脲酸胺指示剂,用浓度为 0.100mol∙L-1 的 Na2H2Y 标准液滴定,重复操作2~3 次,消耗 Na2H2Y 标准液平均值为 12.40mL。
已知:i. Ni2++H2Y2-=[NiY]2-+2H+;ii. 紫脲酸胺:紫色试剂,遇 Ni2+显橙黄色。
①滴定至终点的现象是
(5)NiSO4 在强碱溶液中和 NaClO 反应,可制得碱性镍镉电池电极材料 NiOOH,该反应的离子方程式为
更新时间:2023-03-17 10:12:20
|
相似题推荐
【推荐1】硫酸锰是一.种重要的化工原料,在农业、电化学和建筑等领域均有广泛应用。以含锰废料(含有MnO2、CuO、Fe和少量CaO)为原料制备MnSO4的一种流程如下:

已知:I .烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:
回答下列问题:
(1)“焙烧”过程加入煤粉的主要作用为___________________________ 。
(2)“酸浸”时所加稀H2SO4不宜过量太多的原因为______________________________ .滤渣1的主要成分为_____________________ (填化学式)。
(3)“氧化”过程中主要反应的离子方程式为__________________ 。
(4)“调pH为4”的目的为______________________ ;若“溶液”中c(Cu2+ )=0.022 mol/L,“滤液2”的体积是“溶液”体积的2倍,则“调pH为4”时Cu2+是否开始沉淀____________ (通过计算说明)。
(5)(NH4)2S的电子式为___________________ 。
(6)已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩_______ 、过滤 、洗涤、干燥;其中用乙醇代替水洗涤的原因为__________ ,需控制温度为____ ( 填选项字母)得到产品最多。
A.10℃ B.40℃ C.60℃ D.100℃


已知:I .烧渣中含有MnO、CuO、Cu、Fe、CaO。
II.难溶电解质的溶度积常数如下表所示:
| 物质 | Mn(OH)2 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| 溶度积常数(Ksp) | 1.9×10-13 | 1.8×10-16 | 2.2×10-20 | 4.0×10-38 |
(1)“焙烧”过程加入煤粉的主要作用为
(2)“酸浸”时所加稀H2SO4不宜过量太多的原因为
(3)“氧化”过程中主要反应的离子方程式为
(4)“调pH为4”的目的为
(5)(NH4)2S的电子式为
(6)已知:(NH4)2SO4与MnSO4的溶解度曲线如图所示。“操作”主要包括蒸发浓缩
A.10℃ B.40℃ C.60℃ D.100℃

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】锰元素在炼钢等方面有着广泛的应用。以纤维素和软锰矿(主要成分为 ,含少量
,含少量 、FeO、
、FeO、 、MgO等杂质)为主要原料,制备
、MgO等杂质)为主要原料,制备 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:

请回答下列问题:
(1)Mn位于元素周期表中________ 区(按电子排布分区)。
(2)“酸浸”过程中,纤维素能将锰元素等还原。“氧化”过程的离子方程式为________________ 。
(3)“沉铁”时,滴入适量氨水充分反应后,需将混合体系煮沸冷却后再过滤、煮沸的目的是________ 。
(4)若“沉镁”前溶液中 浓度为0.002mol/L,取等体积的NaF溶液与该溶液混合(假设混合前后溶液总体积不变),要使
浓度为0.002mol/L,取等体积的NaF溶液与该溶液混合(假设混合前后溶液总体积不变),要使 完全沉淀,则所加NaF溶液的浓度至少为
完全沉淀,则所加NaF溶液的浓度至少为________ mol/L。[已知, ,
,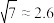 ]
]
(5) 溶液中锰元素含量的测定:取
溶液中锰元素含量的测定:取 溶液于锥形瓶中,滴加2~3滴铬黑
溶液于锥形瓶中,滴加2~3滴铬黑 作指示剂,用
作指示剂,用 标准液滴定至终点,消耗标准液15.00mL.
标准液滴定至终点,消耗标准液15.00mL.
滴定原理如下: (蓝色)
(蓝色) (红色)
(红色)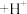
 (无色)
(无色) (无色)
(无色)

①滴定终点的颜色变化为________________ 。
② 溶液中锰元素含量为
溶液中锰元素含量为________ g/L。
(6)锰元素的氧化态—吉布斯自由能图如图所示,该图具有多方面的应用。

①可判断不同氧化态的锰元素在水溶液中的相对稳定性,由图可知,在酸性溶液中 是锰的最稳定态,则在碱性溶液中
是锰的最稳定态,则在碱性溶液中________ (写化学式)是锰的最稳定态。
②可预测歧化反应发生的可能性。若某氧化态位于它相邻两氧化态连线的上方,则该氧化态不稳定,能发生歧化反应,生成其相邻两氧化态。反之,若某氧化态位于它相邻两氧化态连线的下方,则该氧化态是相对稳定的。则由图可知, 在
在________ (填“酸性”或“碱性”)环境中更易发生歧化反应该反应的离子方程式为________________ 。
 ,含少量
,含少量 、FeO、
、FeO、 、MgO等杂质)为主要原料,制备
、MgO等杂质)为主要原料,制备 溶液的工艺流程如图所示:
溶液的工艺流程如图所示:
请回答下列问题:
(1)Mn位于元素周期表中
(2)“酸浸”过程中,纤维素能将锰元素等还原。“氧化”过程的离子方程式为
(3)“沉铁”时,滴入适量氨水充分反应后,需将混合体系煮沸冷却后再过滤、煮沸的目的是
(4)若“沉镁”前溶液中
 浓度为0.002mol/L,取等体积的NaF溶液与该溶液混合(假设混合前后溶液总体积不变),要使
浓度为0.002mol/L,取等体积的NaF溶液与该溶液混合(假设混合前后溶液总体积不变),要使 完全沉淀,则所加NaF溶液的浓度至少为
完全沉淀,则所加NaF溶液的浓度至少为 ,
,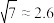 ]
](5)
 溶液中锰元素含量的测定:取
溶液中锰元素含量的测定:取 溶液于锥形瓶中,滴加2~3滴铬黑
溶液于锥形瓶中,滴加2~3滴铬黑 作指示剂,用
作指示剂,用 标准液滴定至终点,消耗标准液15.00mL.
标准液滴定至终点,消耗标准液15.00mL.滴定原理如下:
 (蓝色)
(蓝色) (红色)
(红色)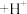
 (无色)
(无色) (无色)
(无色)

①滴定终点的颜色变化为
②
 溶液中锰元素含量为
溶液中锰元素含量为(6)锰元素的氧化态—吉布斯自由能图如图所示,该图具有多方面的应用。

①可判断不同氧化态的锰元素在水溶液中的相对稳定性,由图可知,在酸性溶液中
 是锰的最稳定态,则在碱性溶液中
是锰的最稳定态,则在碱性溶液中②可预测歧化反应发生的可能性。若某氧化态位于它相邻两氧化态连线的上方,则该氧化态不稳定,能发生歧化反应,生成其相邻两氧化态。反之,若某氧化态位于它相邻两氧化态连线的下方,则该氧化态是相对稳定的。则由图可知,
 在
在
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】根据要求,回答下列问题:
I.二氧化氯(ClO2)、高铁酸钠(Na2FeO4)等新型水处理剂可用于城市自来水的处理。ClO2和Na2FeO4在水处理过程中分别被还原为 和Fe3+。
和Fe3+。
(1)如果以单位物质的量的氧化剂所得到的电子数来表示消毒效率,那么ClO2、Cl2、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是___________ 。
(2)工业上以CH3OH和NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体。已知该反应分两步进行,第一步反应为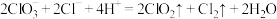 。
。
①第二步反应为___________ (写离子方程式)。
②上述反应中, 的作用是
的作用是___________ 。
II.金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比二价铬毒性高,更易被人体吸收且在体内蓄积。
(3)工业上处理含 的酸性废水的方法如下:
的酸性废水的方法如下:
①向含 的酸性废水中加入FeSO4溶液,使
的酸性废水中加入FeSO4溶液,使 全部转化为Cr3+,反应的离子方程式为
全部转化为Cr3+,反应的离子方程式为___________ 。
②调节溶液的pH,使Cr3+完全沉淀,请问溶液pH的最小理论值为___________ 。(已知常温下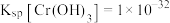 。离子浓度小于
。离子浓度小于 时可认为该离子沉淀完全)
时可认为该离子沉淀完全)
(4)铬元素总浓度的测定:准确移取25.00mL含 和
和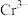 的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成
的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成 。煮沸除去过量的(NH4)2S2O8;上述溶液中加入过量的KI溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加0.015
。煮沸除去过量的(NH4)2S2O8;上述溶液中加入过量的KI溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加0.015 的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mol。
的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mol。
已知测定过程中发生的反应如下:
I.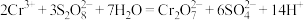
II.
III. ,则废水中铬元素的总浓度为
,则废水中铬元素的总浓度为___________  。
。
I.二氧化氯(ClO2)、高铁酸钠(Na2FeO4)等新型水处理剂可用于城市自来水的处理。ClO2和Na2FeO4在水处理过程中分别被还原为
 和Fe3+。
和Fe3+。(1)如果以单位物质的量的氧化剂所得到的电子数来表示消毒效率,那么ClO2、Cl2、Na2FeO4三种消毒杀菌剂的消毒效率由大到小的顺序是
(2)工业上以CH3OH和NaClO3为原料在酸性条件下制取ClO2,同时产生CO2气体。已知该反应分两步进行,第一步反应为
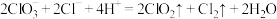 。
。①第二步反应为
②上述反应中,
 的作用是
的作用是II.金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比二价铬毒性高,更易被人体吸收且在体内蓄积。
(3)工业上处理含
 的酸性废水的方法如下:
的酸性废水的方法如下:①向含
 的酸性废水中加入FeSO4溶液,使
的酸性废水中加入FeSO4溶液,使 全部转化为Cr3+,反应的离子方程式为
全部转化为Cr3+,反应的离子方程式为②调节溶液的pH,使Cr3+完全沉淀,请问溶液pH的最小理论值为
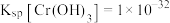 。离子浓度小于
。离子浓度小于 时可认为该离子沉淀完全)
时可认为该离子沉淀完全)(4)铬元素总浓度的测定:准确移取25.00mL含
 和
和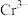 的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成
的酸性废水,向其中加入足量的(NH4)2S2O8溶液将Cr3+氧化成 。煮沸除去过量的(NH4)2S2O8;上述溶液中加入过量的KI溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加0.015
。煮沸除去过量的(NH4)2S2O8;上述溶液中加入过量的KI溶液,充分反应后,以淀粉溶液为指示剂,向其中滴加0.015 的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mol。
的Na2S2O3标准溶液,终点时消耗Na2S2O3溶液20.00mol。已知测定过程中发生的反应如下:
I.
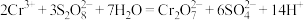
II.

III.
 ,则废水中铬元素的总浓度为
,则废水中铬元素的总浓度为 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】工业上利用某地磷矿(主要成分是磷酸钙,质量分数为80%,另外还含有石英及少量碳酸镁、氧化铝等不含磷杂质)制取磷铵,并用制磷铵排放的废渣磷石膏制取硫酸、水泥。其生产流程如下:

请分析并回答下列问题:
(1)窑气(SO2)进入接触室前需要净化的目的是_________________ ;
(2)实验室完成操作b的方法是__________________ 过滤、洗涤和干燥等;
(3)下图表示接触室和吸收塔的内部构造。吸收塔内安装有许多瓷环作用是_________________ ;

(4)接触室中进行学反应是:2SO2(g) + O2(g) 2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是
2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是____________________ 。图1表示接触室中催化剂随温度变化图象,图2表示SO2的转化率a(SO2)随温度T及压强P的变化图象。你认为接触室中最合适的温度和压强是__________________ 。

图1图2
(5)硫酸厂的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸厂尾气中SO2含量的试剂是______________ (填字母代号):
(6)在述生产过程中循环利用的物质有__________________ (填化学式);
(7)磷铵是一种常用复合肥,经分析其中氮与磷原子数之比为3:2,在生产过程中平均有7%的磷元素损失,该厂日均生产74.1吨磷铵,要维持正常生产,每天需运入这种磷矿至少__________ 吨。

请分析并回答下列问题:
(1)窑气(SO2)进入接触室前需要净化的目的是
(2)实验室完成操作b的方法是
(3)下图表示接触室和吸收塔的内部构造。吸收塔内安装有许多瓷环作用是

(4)接触室中进行学反应是:2SO2(g) + O2(g)
 2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是
2SO3(g) △H=-296.4kJ/mol。接触室内安装热交换器的目的是
图1图2
(5)硫酸厂的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。能用于测定硫酸厂尾气中SO2含量的试剂是
| A.NaOH溶液、酚酞试液 | B.KMnO4溶液、稀H2SO4 |
| C.氨水、酚酞试液 | D.碘水、淀粉溶液 |
(7)磷铵是一种常用复合肥,经分析其中氮与磷原子数之比为3:2,在生产过程中平均有7%的磷元素损失,该厂日均生产74.1吨磷铵,要维持正常生产,每天需运入这种磷矿至少
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】某化学兴趣小组利用如图装置进行“铁与水反应”的实验,并检验产物的性质,请回答下列问题:
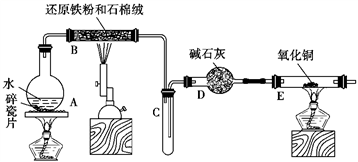
(1)A装置的作用是__________________ 。
(2)B中反应的化学方程式为____________________________ 。
(3)E中的现象是_____________________________ 。
(4)A、B两个装置中应先点燃______ 处的酒精(喷)灯,点燃E处酒精灯之前应进行的操作是__________________________ 。

(1)A装置的作用是
(2)B中反应的化学方程式为
(3)E中的现象是
(4)A、B两个装置中应先点燃
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氯化二硫(S2Cl2)可作硫化剂、氯化剂。常温下是一种黄红色液体,沸点137°C,在空气中剧烈水解而发烟。S2Cl2可通过硫与少量氯气在110~140°C反应制得,氯气过量则会生成SCl2。
(1)选用以下装置制取少量S2Cl2(加热及夹持装置略):

①A中发生反应的化学方程式为_________________________ 。
②装置连接顺序:A→_____ →______ →______ →______ 。
③B中玻璃纤维的作用是________________________________ 。
④D中的最佳试剂是_______ (选填序号)。
a.碱石灰 b.浓硫酸
c.NaOH溶液 d.无水氯化钙
(2)S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
①该反应化学方程式为_________________________ 。
②甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,乙同学认为该方案不可行,原因是______________________ 。
(3)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1. 25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。由此可知产品中________ (填“含有”或“不含有”)SCl2杂质。
(1)选用以下装置制取少量S2Cl2(加热及夹持装置略):

①A中发生反应的化学方程式为
②装置连接顺序:A→
③B中玻璃纤维的作用是
④D中的最佳试剂是
a.碱石灰 b.浓硫酸
c.NaOH溶液 d.无水氯化钙
(2)S2Cl2遇水剧烈水解,生成SO2、HCl和一种常见的固体。
①该反应化学方程式为
②甲同学为了验证两种气体产物,将水解生成的气体依次通过硝酸银与稀硝酸的混合溶液、品红溶液、NaOH溶液,乙同学认为该方案不可行,原因是
(3)乙同学按如下实验方案检验S2Cl2是否含有杂质:
①取1. 25g产品,在密闭容器中依次加入足量水、双氧水、Ba(NO3)2溶液,过滤;
②往①的滤液中加入足量AgNO3溶液,过滤、洗涤、干燥,称得固体质量为2.87g。由此可知产品中
您最近一年使用:0次



