尿素 是人体和动物的代谢产物之一,氨基甲酸铵(
是人体和动物的代谢产物之一,氨基甲酸铵( )是以氨气和二氧化碳为原料合成尿素的中间产物。
)是以氨气和二氧化碳为原料合成尿素的中间产物。
(1)合成尿素的总反应可表示为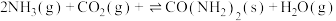 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:
I.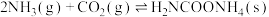
 kJ/mol
kJ/mol
II.
 kJ/mol
kJ/mol
①总反应的
______ 。
②若反应II为慢反应,下列示意图中能体现上述反应能量变化的是______ 。
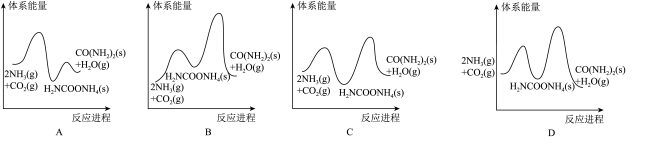
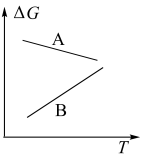
③能定性表示反应I的 随温度变化的曲线是
随温度变化的曲线是______ (填“A”或“B”)。
④尿素中C原子的杂化方式为________________________ 。
(2)尿素废水使水体富营养化,通过电解法处理后可排放,其装置示意图如图所示。
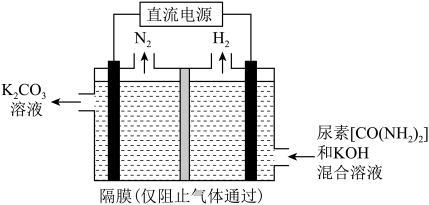
①该装置阳极的电极反应式为__________________ 。
 是人体和动物的代谢产物之一,氨基甲酸铵(
是人体和动物的代谢产物之一,氨基甲酸铵( )是以氨气和二氧化碳为原料合成尿素的中间产物。
)是以氨气和二氧化碳为原料合成尿素的中间产物。(1)合成尿素的总反应可表示为
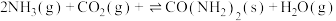 ,该反应一般认为通过如下步骤来实现:
,该反应一般认为通过如下步骤来实现:I.
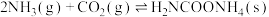
 kJ/mol
kJ/molII.

 kJ/mol
kJ/mol①总反应的

②若反应II为慢反应,下列示意图中能体现上述反应能量变化的是

③能定性表示反应I的
 随温度变化的曲线是
随温度变化的曲线是
④尿素中C原子的杂化方式为
(2)尿素废水使水体富营养化,通过电解法处理后可排放,其装置示意图如图所示。

①该装置阳极的电极反应式为
更新时间:2023-04-03 20:38:12
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】乙酸制氢具有重要意义,发生的反应如下:
热裂解反应:

脱羧基反应:

(1)请写出 与
与 反应生成甲烷的热化学方程式:
反应生成甲烷的热化学方程式:___________ 。
(2)在密闭容器中,利用乙酸制氢,选择的压强为___________ (填“高压”或“常压”)。其中温度与气体产率的关系如图:
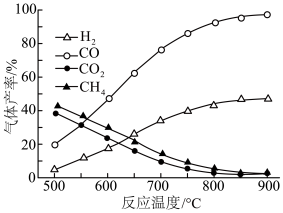
①约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高,热裂解反应速率加快,同时___________ 。
②保持其他条件不变,在乙酸气中掺杂一定量水,氢气产率显著提高而 的产率下降,请分析原因:
的产率下降,请分析原因:___________ 。
(3)若利用合适的催化剂控制其他副反应,温度为T℃时达到平衡,总压强为 ,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%,
,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%, 体积分数为
体积分数为___________ ;脱羧基反应的平衡常数 为
为___________  (
( 为以分压表示的平衡常数,分压=总压×体积分数,计算结果用最简式表示)。
为以分压表示的平衡常数,分压=总压×体积分数,计算结果用最简式表示)。
热裂解反应:


脱羧基反应:


(1)请写出
 与
与 反应生成甲烷的热化学方程式:
反应生成甲烷的热化学方程式:(2)在密闭容器中,利用乙酸制氢,选择的压强为

①约650℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650℃之后氢气产率高于甲烷,理由是随着温度升高,热裂解反应速率加快,同时
②保持其他条件不变,在乙酸气中掺杂一定量水,氢气产率显著提高而
 的产率下降,请分析原因:
的产率下降,请分析原因:(3)若利用合适的催化剂控制其他副反应,温度为T℃时达到平衡,总压强为
 ,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%,
,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%, 体积分数为
体积分数为 为
为 (
( 为以分压表示的平衡常数,分压=总压×体积分数,计算结果用最简式表示)。
为以分压表示的平衡常数,分压=总压×体积分数,计算结果用最简式表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】化学反应都伴随有能量变化。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:
 kJ⋅mol-1
kJ⋅mol-1

 kJ⋅mol-1
kJ⋅mol-1

 kJ⋅mol-1
kJ⋅mol-1
 与
与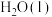 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为___________ 。
(2)如图所示为常温常压下,1mol 和1mol
和1mol 完全反应生成
完全反应生成 和
和 过程中的能量变化。
过程中的能量变化。
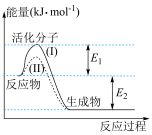
①曲线II表示___________ (填“有”或“无”)催化剂作用时的能量变化。
②若能量变化如曲线I所示,该反应逆反应的活化能为___________ kJ⋅mol-1。
③若常温常压下,1mol 完全燃烧放出的热量为
完全燃烧放出的热量为 kJ,则
kJ,则

___________ kJ⋅mol-1。
(3)工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。键能如下表所示,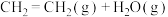
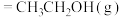 反应的
反应的
___________ kJ⋅mol-1。
(1)以甲烷为原料制取氢气是工业上常用的制氢方法。
已知:

 kJ⋅mol-1
kJ⋅mol-1
 kJ⋅mol-1
kJ⋅mol-1
 kJ⋅mol-1
kJ⋅mol-1 与
与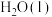 反应生成
反应生成 和
和 的热化学方程式为
的热化学方程式为(2)如图所示为常温常压下,1mol
 和1mol
和1mol 完全反应生成
完全反应生成 和
和 过程中的能量变化。
过程中的能量变化。
①曲线II表示
②若能量变化如曲线I所示,该反应逆反应的活化能为
③若常温常压下,1mol
 完全燃烧放出的热量为
完全燃烧放出的热量为 kJ,则
kJ,则

(3)工业上,在一定条件下利用乙烯和水蒸气反应制备乙醇。键能如下表所示,
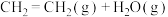
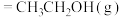 反应的
反应的
| 化学键 |  |  |  |  |  |
| 键能/(kJ·mol-1) | 413 | 615 | 463 | 348 | 351 |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是_______ 。
(2)已知:25℃时,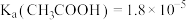 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
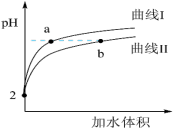
①曲线I代表_______ 溶液(填“ ”或“
”或“ ”)。
”)。
②a、b两点对应的溶液中,水的电离程度a_______ b(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
③向上述 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
_______  (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。
④酸度( )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=_______ 。
(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
①三种酸的酸性由强到弱的顺序为_______ (填标号)。
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是_______ (填标号)。
A.通入氨气 B.加入Na C.加入苯甲酸钠 固体 D.加热至90℃
固体 D.加热至90℃
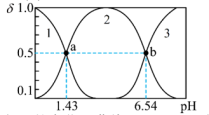
(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。
①写出亚磷酸H3PO3的第一步电离方程式_______ 。
② 随溶液pH的变化用曲线
随溶液pH的变化用曲线_______ (填“1”、“2”或“3”)表示。
③反应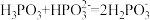 的平衡常数K=
的平衡常数K=_______ 。
(1)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101kPa时:
CaO(s)+H2SO4(l)=CaSO4(s)+H2O(l) ΔH= -271 kJ·mol-1
5CaO(s)+3H3PO4(l)+HF(g)= Ca5(PO4)3F(s)+5H2O(l) ΔH= -937 kJ·mol-1
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是
(2)已知:25℃时,
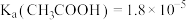 常温下,将pH和体积均相同的
常温下,将pH和体积均相同的 和
和 溶液分别稀释,溶液pH随加水体积的变化如图:
溶液分别稀释,溶液pH随加水体积的变化如图:
①曲线I代表
 ”或“
”或“ ”)。
”)。②a、b两点对应的溶液中,水的电离程度a
 ”、“
”、“ ”或“
”或“ ”)。
”)。③向上述
 溶液和
溶液和 溶液分别滴加等浓度的
溶液分别滴加等浓度的 溶液,当恰好中和时,消耗
溶液,当恰好中和时,消耗 溶液体积分别为
溶液体积分别为 和
和 ,则
,则
 (填“
(填“ ”、“
”、“ ”或“
”或“ ”)。
”)。④酸度(
 )也可表示溶液的酸碱性,
)也可表示溶液的酸碱性, 。常温下,
。常温下, 的硝酸溶液AG=
的硝酸溶液AG=(3)雪碧是一款柠檬味汽水饮料,其中所含酸性物质包括:碳酸、柠檬酸、苯甲酸。25℃时,上述三种酸的电离常数如表所示:
| 化学式 | 苯甲酸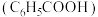 | 碳酸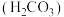 | 柠檬酸 |
| 电离常数 | 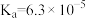 | 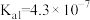  | 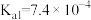 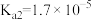 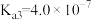 |
a.苯甲酸 b.碳酸 c.柠檬酸
②欲使水的平衡向右移动,且溶液显碱性,下列符合条件的方法是
A.通入氨气 B.加入Na C.加入苯甲酸钠
 固体 D.加热至90℃
固体 D.加热至90℃(4)亚磷酸H3PO3是一种二元弱酸,可用作还原剂、尼龙增白剂、亚磷酸盐原料、农药中间体以及有机磷水处理药剂的原料。常温下,已知H3PO3溶液中含磷粒子的浓度之和为0.1mol·L-1,溶液中含磷粒子的物质的量分数(δ)与溶液pH的关系如图所示。

①写出亚磷酸H3PO3的第一步电离方程式
②
 随溶液pH的变化用曲线
随溶液pH的变化用曲线③反应
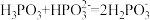 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
【推荐1】CO2加氢制化工原料对实现“碳中和”有重大意义。部分CO2加氢反应的热化学方程式如下:
反应Ⅰ:CO2(g)+H2(g)⇌HCOOH(g) ΔH1=+35.2kJ·mol−1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-24.7kJ·mol−1
反应Ⅲ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3
反应IV:CO2(g)+3H2(g)⇌ CH3OCH3(g)+
CH3OCH3(g)+ H2O(g) ΔH4
H2O(g) ΔH4
回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH5=-483.6kJ·mol−1。
CH3OH(g)+O2(g)⇌HCOOH(g)+H2O(g) ΔH6=__________ kJ·mol−1。
(2)CO2催化加氢体系中,部分反应的lnKp与温度(T)关系如图1所示:
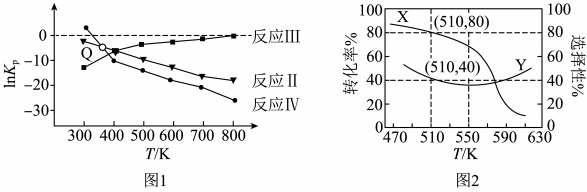
①300K时,反应进行趋势最大的是__________ (填“Ⅱ”、“Ⅲ”或“IV”)。
②图1中Q点时,反应2CH3OH(g)⇌CH3OCH3(g)+H2O(g)的Kp=___________ 。
③实验测得CO2平衡转化率(曲线Y)和平衡时CH3OH的选择性(曲线X)随温度变化如图2所示。CO2加氢制CH3OH时,温度选择510~550K的原因为__________ 。(已知:CH3OH的选择性=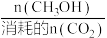 ×100%)
×100%)
④510K时,往刚性容器中通入nmolCO2和一定量H2,tmin达到平衡,tmin内CH3OH的平均生成速率为___________ mol·min−1。
(3)我国科学家以Bi为电极在酸性水溶液中可实现电催化还原CO2,两种途径的反应机理如下图所示,其中,TS表示过渡态、数字表示微粒的相对总能量。
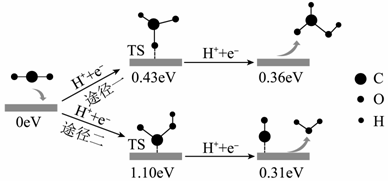
①途径一,CO2电还原经两步反应生成HCOOH:第一步为CO2+e−+H+=HCOO*(*表示微粒与Bi的接触位点);第二步为_____________ 。
②CO2电还原的选择性以途径一为主,理由是_______________ 。
反应Ⅰ:CO2(g)+H2(g)⇌HCOOH(g) ΔH1=+35.2kJ·mol−1
反应Ⅱ:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH2=-24.7kJ·mol−1
反应Ⅲ:CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH3
反应IV:CO2(g)+3H2(g)⇌
 CH3OCH3(g)+
CH3OCH3(g)+ H2O(g) ΔH4
H2O(g) ΔH4回答下列问题:
(1)已知:2H2(g)+O2(g)=2H2O(g) ΔH5=-483.6kJ·mol−1。
CH3OH(g)+O2(g)⇌HCOOH(g)+H2O(g) ΔH6=
(2)CO2催化加氢体系中,部分反应的lnKp与温度(T)关系如图1所示:

①300K时,反应进行趋势最大的是
②图1中Q点时,反应2CH3OH(g)⇌CH3OCH3(g)+H2O(g)的Kp=
③实验测得CO2平衡转化率(曲线Y)和平衡时CH3OH的选择性(曲线X)随温度变化如图2所示。CO2加氢制CH3OH时,温度选择510~550K的原因为
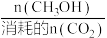 ×100%)
×100%)④510K时,往刚性容器中通入nmolCO2和一定量H2,tmin达到平衡,tmin内CH3OH的平均生成速率为
(3)我国科学家以Bi为电极在酸性水溶液中可实现电催化还原CO2,两种途径的反应机理如下图所示,其中,TS表示过渡态、数字表示微粒的相对总能量。

①途径一,CO2电还原经两步反应生成HCOOH:第一步为CO2+e−+H+=HCOO*(*表示微粒与Bi的接触位点);第二步为
②CO2电还原的选择性以途径一为主,理由是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】碳是形成化合物种类最多的元素,其单质及其化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:M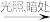 N ∆H=+88.6kJ/mol,则M、N相比,较稳定的是
N ∆H=+88.6kJ/mol,则M、N相比,较稳定的是_______ 。
(2)已知CH3OH(l)的燃烧热为-726.5kJ/mol,CH3OH(l)+ O2(g)=CO2(g)+2H2O(g) ∆H=-akJ/mol,则a
O2(g)=CO2(g)+2H2O(g) ∆H=-akJ/mol,则a____ 726.5(填“<”“>”或“=”)
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应生成1molCO2时的热化学方程式:_______ 。
(4)在微生物作用的条件下, 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
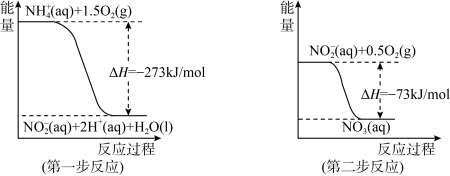
①第一步反应是_______ (填“放热”或“吸热”)反应,判断依据是_______ 。1mol (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是_______ 。
(5)已知H2(g)+Br2(1)=2HBr(g) △H=-72kJ·mol⁻¹,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
则表中a=_______ 。
(1)有机物M经过太阳光光照可转化成N,转化过程如下:M
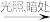 N ∆H=+88.6kJ/mol,则M、N相比,较稳定的是
N ∆H=+88.6kJ/mol,则M、N相比,较稳定的是(2)已知CH3OH(l)的燃烧热为-726.5kJ/mol,CH3OH(l)+
 O2(g)=CO2(g)+2H2O(g) ∆H=-akJ/mol,则a
O2(g)=CO2(g)+2H2O(g) ∆H=-akJ/mol,则a(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应生成1molCO2时的热化学方程式:
(4)在微生物作用的条件下,
 经过两步反应被氧化成
经过两步反应被氧化成 。两步反应的能量变化示意图如下:
。两步反应的能量变化示意图如下:
①第一步反应是
 (aq)全部氧化成
(aq)全部氧化成 (aq)的热化学方程式是
(aq)的热化学方程式是(5)已知H2(g)+Br2(1)=2HBr(g) △H=-72kJ·mol⁻¹,蒸发1molBr2(l)需要吸收的能量为30kJ,其他相关数据如下表:
| 物质 | H2(g) | Br2(g) | HBr(g) |
| 1mol分子中的化学键断裂时需要吸收的能量(kJ) | 436 | 200 | a |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】有效去除大气中的NOx和水体中的氮是环境保护的重要课题。
(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=_______ 。
(2)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
①生成磷酸铵镁沉淀的离子反应方程式为_______ 。
②测得反应pH对氨氮去除率的影响如图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是_______ 。

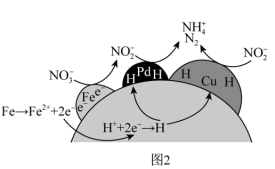
(3)纳米零价铁(NZVI)/BC与(CuPd)/BC联合作用可去除水体中的硝态氮。在NZVI/BC和(CuPd)/BC复合材料联合作用的体系中,生物炭(BC)作为NZVI、Cu、Pb的载体且减少了纳米零价铁的团聚,纳米零价铁作为主要还原剂,Cu和Pd作为催化剂且参与吸附活性H。
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如图2所示,NO 转化为N2或NH
转化为N2或NH 的过程可描述为
的过程可描述为_______ 。
②实验测得体系初始pH对NO 去除率的影响如图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是_______ 。

(1)已知:①2CO(g)+O2(g)=2CO2(g);ΔH1=-566.0kJ·mol-1
②N2(g)+2O2(g)=2NO2(g);ΔH2=+64kJ·mol-1
反应2NO2(g)+4CO(g)=N2(g)+4CO2(g);ΔH3=
(2)磷酸铵镁(MgNH4PO4)沉淀法可去除水体中的氨氮(NH
 和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH
和NH3)。实验室中模拟氨氮处理:1L的模拟氨氮废水(主要含NH ),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。
),置于搅拌器上,设定反应温度为25℃。先后加入MgCl2和Na2HPO4溶液,用NaOH调节反应pH,投加絮凝剂;开始搅拌,反应30min后,取液面下2cm处清液测定氨氮质量浓度。①生成磷酸铵镁沉淀的离子反应方程式为
②测得反应pH对氨氮去除率的影响如图1所示,当pH从7.5增至9.0的过程中,水中氨氮的去除率明显增加,原因是

(3)纳米零价铁(NZVI)/BC与(CuPd)/BC联合作用可去除水体中的硝态氮。在NZVI/BC和(CuPd)/BC复合材料联合作用的体系中,生物炭(BC)作为NZVI、Cu、Pb的载体且减少了纳米零价铁的团聚,纳米零价铁作为主要还原剂,Cu和Pd作为催化剂且参与吸附活性H。
①NZVI/BC和(CuPd)/BC复合材料还原硝酸盐的反应机理如图2所示,NO
 转化为N2或NH
转化为N2或NH 的过程可描述为
的过程可描述为
②实验测得体系初始pH对NO
 去除率的影响如图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
去除率的影响如图3,前200min内,pH=9.88时的去除率远低于pH=4.05时,其可能的原因是
您最近一年使用:0次
【推荐1】红土镍矿渣主要成分包含铁、钴、镍、锰、铬、硅的氧化物,为节约和充分利用资源,利用如下流程进行分离回收。已知该温度下Co(OH)2、Fe(OH)3的溶度积分别是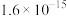 、
、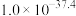 。回答下列问题:
。回答下列问题:
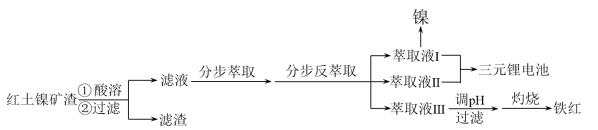
(1)酸溶时,需将红土镍矿渣研成粉末,目的是_______ 。
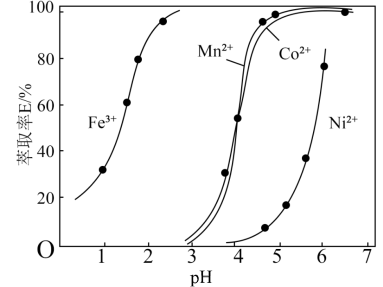
(2)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是_______ ,分步萃取浸出金属离子先后顺序为_______ 、_______ 、_______ ,当调pH=4.60时,溶液中
_______ 。
(3)萃取液I电解制取镍的阴极电极反应式为_______ 。
(4)三元锂电池化学式为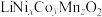 ,其中
,其中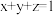 ,Ni、Co、Mn的化合价分别为+2、+3、+4,则
,Ni、Co、Mn的化合价分别为+2、+3、+4,则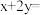
_______ (用含z的代数式表示)。
(5)写出铁红的一种用途:_______ 。
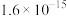 、
、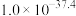 。回答下列问题:
。回答下列问题:
(1)酸溶时,需将红土镍矿渣研成粉末,目的是
(2)各种离子萃取率与pH关系如图。分步萃取前需通入适量氧气,目的是


(3)萃取液I电解制取镍的阴极电极反应式为
(4)三元锂电池化学式为
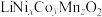 ,其中
,其中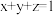 ,Ni、Co、Mn的化合价分别为+2、+3、+4,则
,Ni、Co、Mn的化合价分别为+2、+3、+4,则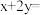
(5)写出铁红的一种用途:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】高锰酸钾(KMnO4)在工业中广泛用作为氧化剂,工业上常用软锰矿(主要成分是MnO2)为原料制备高锰酸钾晶体。制备高锰酸钾分两个阶段进行。
阶段一:制备锰酸钾(K2MnO4),工艺流程流程如下:
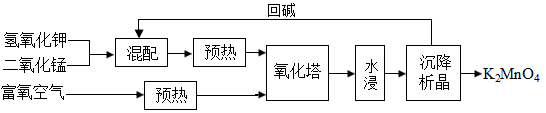
(1)原料加入氧化塔前必须粉碎、预热,目的是_______ 。
(2)在氧化塔,反应分两步进行:
第一步反应生成K3MnO4,反应方程式为_______ 。
第二步反应方程式为4K3MnO4+O2+2H2O 4K2MnO4+4KOH
4K2MnO4+4KOH
阶段二:制备高锰酸钾(KMnO4)
工业中,用锰酸钾制备高锰酸钾有两种方法。
(3)方法一:电解法
工业上采用惰性电极电解锰酸钾溶液,电解反应的化学方程式为2K2MnO4+2H2O 2KMnO4+H2↑+2KOH,阴极上电极反应为
2KMnO4+H2↑+2KOH,阴极上电极反应为_______ 。
(4)方法二:歧化法
相关资料:锰酸钾在强碱性溶液中稳定,在酸性、中性和弱碱性环境下, 会发生歧化反应。20℃时下列各物质溶解度如下表。
会发生歧化反应。20℃时下列各物质溶解度如下表。
工业中常用CO2歧化法制备高锰酸钾,工艺流程如下:
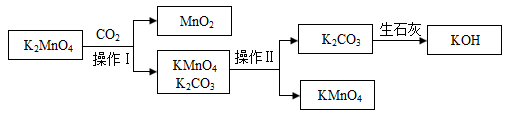
①在该制备过程可循环使用的物质有_______ 、_______ (写化学式)
②操作Ⅱ是将混合液_______ 、_______ 、过滤。
③在酸性条件下,锰酸钾发生歧化反应,工业中用歧化法制高锰酸钾时,用CO2进行酸化,而不用硫酸或盐酸酸化的原因是_______ 。
(5)高锰酸钾是实验室重要试剂,可用于硫酸亚铁样品纯度的测定。取1.000克硫酸亚铁样品溶于蒸馏水,用容量瓶配成100毫升溶液,取出其中20.00mL溶液注入锥形瓶中,加入适量的稀硫酸酸化,用0.0100mol/L的KMnO4标准液进行滴定,当溶液变为微红色且半分钟不褪色时,消耗KMnO4标准液20.00mL,则样品中硫酸亚铁的纯度为_______ 。
阶段一:制备锰酸钾(K2MnO4),工艺流程流程如下:

(1)原料加入氧化塔前必须粉碎、预热,目的是
(2)在氧化塔,反应分两步进行:
第一步反应生成K3MnO4,反应方程式为
第二步反应方程式为4K3MnO4+O2+2H2O
 4K2MnO4+4KOH
4K2MnO4+4KOH阶段二:制备高锰酸钾(KMnO4)
工业中,用锰酸钾制备高锰酸钾有两种方法。
(3)方法一:电解法
工业上采用惰性电极电解锰酸钾溶液,电解反应的化学方程式为2K2MnO4+2H2O
 2KMnO4+H2↑+2KOH,阴极上电极反应为
2KMnO4+H2↑+2KOH,阴极上电极反应为(4)方法二:歧化法
相关资料:锰酸钾在强碱性溶液中稳定,在酸性、中性和弱碱性环境下,
 会发生歧化反应。20℃时下列各物质溶解度如下表。
会发生歧化反应。20℃时下列各物质溶解度如下表。| 物质 | KMnO4 | K2CO3 | K2SO4 |
| 溶解度 | 6.38 | 111 | 11.1 |
工业中常用CO2歧化法制备高锰酸钾,工艺流程如下:

①在该制备过程可循环使用的物质有
②操作Ⅱ是将混合液
③在酸性条件下,锰酸钾发生歧化反应,工业中用歧化法制高锰酸钾时,用CO2进行酸化,而不用硫酸或盐酸酸化的原因是
(5)高锰酸钾是实验室重要试剂,可用于硫酸亚铁样品纯度的测定。取1.000克硫酸亚铁样品溶于蒸馏水,用容量瓶配成100毫升溶液,取出其中20.00mL溶液注入锥形瓶中,加入适量的稀硫酸酸化,用0.0100mol/L的KMnO4标准液进行滴定,当溶液变为微红色且半分钟不褪色时,消耗KMnO4标准液20.00mL,则样品中硫酸亚铁的纯度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】低碳转化是当今世界重要科研课题之一,科学家们提出了多种途径来实现低碳转化。
(1)CO2可以转化为甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=−184 kJ·mol−1。该转化过程正反应的活化能为a kJ·mol−1,则逆反应的活化能为
CH3OH(g)+H2O(g) ΔH=−184 kJ·mol−1。该转化过程正反应的活化能为a kJ·mol−1,则逆反应的活化能为_______ kJ·mol−1(用含a的式子表示);与该反应有关的化学键的键能数据如下表,则表中x=_______ 。
(2)CO2与H2在一定条件下还能转化为CH4,同时发生副反应产生CO,有关图象如下。CO2与H2转化为CH4适宜的条件为_______ 。

(3)中科院上海高等研究院将CO2在Na−Fe3O4/HZSM−5催化下转变为汽油(C5~C11的烃),辛烷值最高含量可达78%左右,该研究成果在《Nature Chemistry》上发表,并已申报中国发明专利和国际PCT专利。反应过程如下图所示。

①若CO2在该条件下转化为辛烷,请写出该反应的化学方程式_______ 。
②催化剂中的Fe3O4可用铁做电极,稀硫酸为电解质,然后通过电解来制备,写出电解时的阳极反应式:_______ 。
③下列关于该转化方法的说法合理的是_______ (填标号)。
a.Na−Fe3O4/HZSM−5不参与反应过程,可以降低反应的活化能
b.CO2在该条件下转化为戊烷或辛烷,均需三步反应
c.反应过程中有非极性键的断裂,没有非极性键的生成
d.该方法有助于减少CO2排放,同时减轻对化石燃料的依赖
(1)CO2可以转化为甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH=−184 kJ·mol−1。该转化过程正反应的活化能为a kJ·mol−1,则逆反应的活化能为
CH3OH(g)+H2O(g) ΔH=−184 kJ·mol−1。该转化过程正反应的活化能为a kJ·mol−1,则逆反应的活化能为| 化学键 | C=O | C–O | C–H | H–H | O–H |
| 键能/kJ·mol−1 | x | 351 | 415 | 436 | 462 |

(3)中科院上海高等研究院将CO2在Na−Fe3O4/HZSM−5催化下转变为汽油(C5~C11的烃),辛烷值最高含量可达78%左右,该研究成果在《Nature Chemistry》上发表,并已申报中国发明专利和国际PCT专利。反应过程如下图所示。

①若CO2在该条件下转化为辛烷,请写出该反应的化学方程式
②催化剂中的Fe3O4可用铁做电极,稀硫酸为电解质,然后通过电解来制备,写出电解时的阳极反应式:
③下列关于该转化方法的说法合理的是
a.Na−Fe3O4/HZSM−5不参与反应过程,可以降低反应的活化能
b.CO2在该条件下转化为戊烷或辛烷,均需三步反应
c.反应过程中有非极性键的断裂,没有非极性键的生成
d.该方法有助于减少CO2排放,同时减轻对化石燃料的依赖
您最近一年使用:0次



