为研究金属与酸反应的实质,室温下将金属镁与不同酸反应,具体条件如下:
实验测得的气体体积、pH变化如下图1、2

已知,室温时,CH3COOHKa≈1.0×10-5
(1)镁与CH3COOH反应的离子方程式为___________ 。
(2)计算实验ⅡCH3COOH溶液的c(H+)≈___________ mol·L-1。
(3)对比Ⅱ、ⅡI反应的初始阶段可以看出,c(H+)___________ (填“是”或“不是”)产生气体速率差异的主要因素。
(4)探究镁与醋酸溶液中哪种微粒进行反应,进行如下实验方案
①实验Ⅳ可以证明CH3COOH分子可以与Mg直接反应的理由是___________ 。
②pH均为5时,V和Ⅵ溶液中CH3COOH分子浓度分别约为___________ mol/L和___________ mol/L,对比实验V和Ⅵ,可以证明与Mg反应的主要微粒为CH3COOH分子,其理由是___________ 。
| 序号 | 金属 | 酸 | V(酸)/mL | C(酸)/mol·L-1 |
| I | 0.1g光亮的镁屑 | HCl | 10 | 0.10 |
| Ⅱ | 0.1g光亮的镁屑 | CH3COOH | 10 | 0.10 |
| Ⅲ | 0.1g光亮的镁屑 | HCl | 10 | 0.001 |

已知,室温时,CH3COOHKa≈1.0×10-5
(1)镁与CH3COOH反应的离子方程式为
(2)计算实验ⅡCH3COOH溶液的c(H+)≈
(3)对比Ⅱ、ⅡI反应的初始阶段可以看出,c(H+)
| 序号 | 实验方案 | 现象 | 结论 |
| Ⅳ | 取0.1g光亮的镁屑,投入10ml冰醋酸中 | 立即产生大量气泡 | 证明CH3COOH分子可以与Mg直接反应 |
| Ⅴ | 取0.1g光亮的镁屑,投入10ml0.10mol·L-1CH3COOH中,测定初始反应速率va及pH=5时的反应速率vb | va=2.3mL·min-l vb=0.8mL·min-l | 1.镁与醋酸溶液反应时,CH3COOH分子、H+均能与镁反应产生氢气 2.CH3COOH分子是与Mg反应产生气体的主要微粒 |
| Ⅵ | 取0.1g光亮的镁屑,投入10ml含0.10mol·L-1的CH3COOH与0.10mol·L-1CH3COONa混合液(pH=5),测定pH=5时的反应速率vc | vc=2.1mL·min-l |
①实验Ⅳ可以证明CH3COOH分子可以与Mg直接反应的理由是
②pH均为5时,V和Ⅵ溶液中CH3COOH分子浓度分别约为
2023·广东汕头·一模 查看更多[2]
更新时间:2023-04-06 15:50:25
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
【推荐1】近十几年来,化学界掀起研究二氧化碳与氢气反应的热潮。回答下列问题:
(1)已知CoO(s)有下列两个反应:
I.CoO(s)+H2(g) Co(s)+H2O(g) △H=-3.9 kJ·mol-1
Co(s)+H2O(g) △H=-3.9 kJ·mol-1
II.CoO(s)+CO(g) Co(s)+CO2(g) △H=-45.1 kJ·mol-1
Co(s)+CO2(g) △H=-45.1 kJ·mol-1
①根据焓变判断,还原CoO(s)为Co(s)的倾向是CO_______ H2(填“大于”或“小于”)。
②反应CO2(g)+H2(g) CO(g)+H2O(g) △H=
CO(g)+H2O(g) △H=_______ kJ·mol-1。
(2)在723 K、10.0 kPa的甲装置中发生反应I,在723 K、12.0 kPa的乙装置中发生反应II,得到部分气体的分压随时间的变化关系如下图所示。

①在甲装置中,10~40 min内反应的平均速率v(H2)=_______ kPa·min-1。
②已知甲、乙两装置中的反应分别在40 min、31 min达到平衡状态,则在723 K时,反应 的平衡常数Kp=
的平衡常数Kp=_______ (保留三位有效数字)。
(3)向装置丙中充入0.10 mol H2和0.20 mol CO2,在一定温度和12.0 kPa下进行反应: ,平衡时水蒸气体积分数为0.10。再向达到平衡后的装置丙中加入足量的CoO(s)和Co(s),得到如下图象。
,平衡时水蒸气体积分数为0.10。再向达到平衡后的装置丙中加入足量的CoO(s)和Co(s),得到如下图象。

①上表中的a、b两条线分别代表的气体物质是_______ (填化学式)。
②可作为 的催化剂的是
的催化剂的是_______ (填标号)。
A.Co(s) B.CoO(s) C.CoO(s)和Co(s)
(4)科学家设计了如下光电池,常温下在水溶液中完成 反应。
反应。

①装置中的电解质参与了多个反应,在使用过程中电解质的量_______ (填标号)。
A.增大 B.减少 C.基本不变 D.无法确定
②已知电极X上的电极反应为 ,结合总反应式,写出Y电极上的电极反应式:
,结合总反应式,写出Y电极上的电极反应式:_______ 。
(1)已知CoO(s)有下列两个反应:
I.CoO(s)+H2(g)
 Co(s)+H2O(g) △H=-3.9 kJ·mol-1
Co(s)+H2O(g) △H=-3.9 kJ·mol-1II.CoO(s)+CO(g)
 Co(s)+CO2(g) △H=-45.1 kJ·mol-1
Co(s)+CO2(g) △H=-45.1 kJ·mol-1①根据焓变判断,还原CoO(s)为Co(s)的倾向是CO
②反应CO2(g)+H2(g)
 CO(g)+H2O(g) △H=
CO(g)+H2O(g) △H=(2)在723 K、10.0 kPa的甲装置中发生反应I,在723 K、12.0 kPa的乙装置中发生反应II,得到部分气体的分压随时间的变化关系如下图所示。

①在甲装置中,10~40 min内反应的平均速率v(H2)=
②已知甲、乙两装置中的反应分别在40 min、31 min达到平衡状态,则在723 K时,反应
 的平衡常数Kp=
的平衡常数Kp=(3)向装置丙中充入0.10 mol H2和0.20 mol CO2,在一定温度和12.0 kPa下进行反应:
 ,平衡时水蒸气体积分数为0.10。再向达到平衡后的装置丙中加入足量的CoO(s)和Co(s),得到如下图象。
,平衡时水蒸气体积分数为0.10。再向达到平衡后的装置丙中加入足量的CoO(s)和Co(s),得到如下图象。
①上表中的a、b两条线分别代表的气体物质是
②可作为
 的催化剂的是
的催化剂的是A.Co(s) B.CoO(s) C.CoO(s)和Co(s)
(4)科学家设计了如下光电池,常温下在水溶液中完成
 反应。
反应。
①装置中的电解质参与了多个反应,在使用过程中电解质的量
A.增大 B.减少 C.基本不变 D.无法确定
②已知电极X上的电极反应为
 ,结合总反应式,写出Y电极上的电极反应式:
,结合总反应式,写出Y电极上的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】科学家研究出一种以天然气为燃料的“燃烧前捕获系统”,其简单流程如图所示部分(条件及物质未标出)。

(1)已知:CH4、CO、H2的燃烧热分别为890.3kJ·mol-1、283.0kJ·mol-1、285.8kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=_______ 。
(2)工业上可用H2和CO2制备甲醇,其反应为:CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH<0,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)+H2O(g) ΔH<0,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
①用H2表示前2h平均反应速率v(H2)=_______ 。
②该温度下CO2的平衡转化率为_______ 。
③达到平衡后,改变下列条件,能够提高CO2转化率的是_______ 。
A.加入催化剂 B.压缩体积 C.升高温度 D.分离出水蒸气
(3)在300℃、8MPa下,将二氧化碳和氢气按物质的量之比为1∶3通入一密闭容器中发生(2)中反应,达到平衡时,测得二氧化碳的平衡转化率为50%,则该反应条件下的平衡常数Kp=_______ MPa-2 (计算结果用分数表示,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。

(1)已知:CH4、CO、H2的燃烧热分别为890.3kJ·mol-1、283.0kJ·mol-1、285.8kJ·mol-1,则上述流程中第一步反应2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH=
(2)工业上可用H2和CO2制备甲醇,其反应为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) ΔH<0,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:
CH3OH(g)+H2O(g) ΔH<0,某温度下,将1molCO2和3molH2充入体积不变的2L密闭容器中,发生上述反应,测得不同时刻反应前后的压强关系如下:| 时间/h | 1 | 2 | 3 | 4 | 5 | 6 |
 | 0.90 | 0.85 | 0.83 | 0.81 | 0.80 | 0.80 |
②该温度下CO2的平衡转化率为
③达到平衡后,改变下列条件,能够提高CO2转化率的是
A.加入催化剂 B.压缩体积 C.升高温度 D.分离出水蒸气
(3)在300℃、8MPa下,将二氧化碳和氢气按物质的量之比为1∶3通入一密闭容器中发生(2)中反应,达到平衡时,测得二氧化碳的平衡转化率为50%,则该反应条件下的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】氮的氧化物是大气污染物之一,研究它们的反应机理,对于消除环境污染,促进社会可持续发展有重要意义。回答下列问题:
(1)已知:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H1=-907.0kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1269.0kJ/mol
写出NH3与NO反应生成N2和H2O(g)的热化学方程式:_______ 。
(2)氢气选择性催化还原NO是一种比NH3还原NO更为理想的方法,备受研究者关注。以Pt-HY为催化剂,氢气选择性催化还原NO在催化剂表面的反应机理如图:
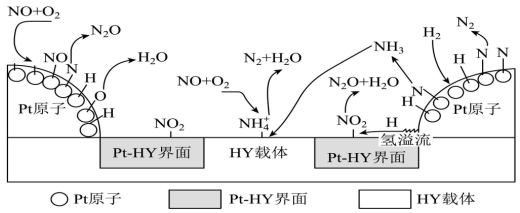
Pt原子表面上发生的反应除N+N=N2、2H+O=H2O外还有_______ 。
(3)在密闭容器中充入4molNO和5molH2,发生反应:2NO(g)+2H2(g) N2(g)+2H2O(g) △H<0,平衡时NO的体积分数随温度、压强的变化关系如图。
N2(g)+2H2O(g) △H<0,平衡时NO的体积分数随温度、压强的变化关系如图。
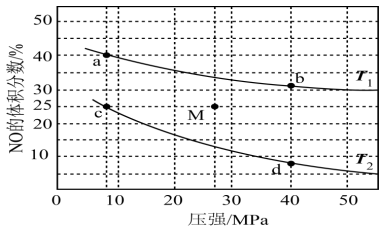
①下列物理量中,图中d点大于b点的是_______ (填字母)。
A.正反应速率 B.H2的转化率
C.N2(g)的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为_______ 。
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的点:_______ 。
(4)T℃时,向容积为2L的恒容容器中充入0.4molNO、0.8molH2发生反应:2NO(g)+2H2(g) N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
①0~20min内该反应的平均反应速率v(NO)= _______ mol/(L·min)。
②该温度下反应的平衡常数Kp=_______ kPa-1(用平衡分压代替平衡浓度,平衡分压=总压×物质的量分数)。
(1)已知:
①4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H1=-907.0kJ/mol
②4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H2=-1269.0kJ/mol
写出NH3与NO反应生成N2和H2O(g)的热化学方程式:
(2)氢气选择性催化还原NO是一种比NH3还原NO更为理想的方法,备受研究者关注。以Pt-HY为催化剂,氢气选择性催化还原NO在催化剂表面的反应机理如图:

Pt原子表面上发生的反应除N+N=N2、2H+O=H2O外还有
(3)在密闭容器中充入4molNO和5molH2,发生反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g) △H<0,平衡时NO的体积分数随温度、压强的变化关系如图。
N2(g)+2H2O(g) △H<0,平衡时NO的体积分数随温度、压强的变化关系如图。
①下列物理量中,图中d点大于b点的是
A.正反应速率 B.H2的转化率
C.N2(g)的浓度 D.对应温度的平衡常数
②c点NO的平衡转化率为
③若在M点对反应容器升温的同时扩大容器体积使体系压强减小,重新达到的平衡状态可能是图中a、b、c、d中的点:
(4)T℃时,向容积为2L的恒容容器中充入0.4molNO、0.8molH2发生反应:2NO(g)+2H2(g)
 N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:
N2(g)+2H2O(g),体系的总压强p随时间t的变化如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 |
| p/kPa | 240 | 226 | 216 | 210 | 210 |
②该温度下反应的平衡常数Kp=
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】碘及其化合物在生产生活中有重要作用。
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 2:1 的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)=2HI(g),反应经过 5 分钟测得碘化氢的浓度为 0.1mol·L-1,碘蒸气的浓度为 0.05mol·L-1。
①前 5 分钟平均反应速率 v(H2)=_______ ,H2的初始浓度是_______ 。
②下列能说明反应已达平衡状态的是_______ (填序号)。
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的 H-H 键数目与断裂的 H-I 键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
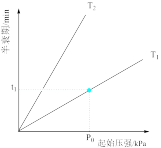
(2)已知:2N2O=2N2 +O2,不同温度(T)下,N2O 分解半衰期随起始压强的变化关系如图所示( 图中半衰期指任一浓度 N2O消耗一半时所需的相应时间) ,则 T1_______ T2(填“>”、“=”或“<”)。当温度为 T1、起始压强为p0,反应至 t1min 时,此时体系压强 p=_______ (用 p0 表示)。
(3)某小组同学在室温下进行“碘钟实验”:将浓度均为 0.01mol·L-1的 H2O2、H2SO4、HI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为 H2O2+2S2O +2H+=S4O
+2H+=S4O +2H2O
+2H2O
反应分两步进行:
反应 A:……反应 B:I2+2S2O =2I-+S4O
=2I-+S4O
①反应 A 的离子方程式是_______ 。对于总反应,I-的作用是_______
②为探究溶液变蓝快慢的影响因素,进行实验 Ⅰ、Ⅱ(溶液浓度均为 0.01mol·L-1)。
溶液从混合时的无色变为蓝色的时间:实验 Ⅰ是 30min、实验 Ⅱ是 40min。实验Ⅱ中,x、y、z 所对成的数值分别是_______ ;对比实验 Ⅰ、Ⅱ,可得出的实验结论是________
(1)单质碘可与氢气反应生成碘化氢。将物质的量比为 2:1 的氢气和碘蒸气放入密闭容器中进行反应:H2(g)+I2(g)=2HI(g),反应经过 5 分钟测得碘化氢的浓度为 0.1mol·L-1,碘蒸气的浓度为 0.05mol·L-1。
①前 5 分钟平均反应速率 v(H2)=
②下列能说明反应已达平衡状态的是
a.氢气的生成速率等于碘化氢的消耗速率
b.单位时间内断裂的 H-H 键数目与断裂的 H-I 键数目相等
c.c(H2):c(I2):c(HI)=1:1:2
d.2v(I2)正=v(HI)逆
e.反应混合体系的颜色不再发生变化
(2)已知:2N2O=2N2 +O2,不同温度(T)下,N2O 分解半衰期随起始压强的变化关系如图所示( 图中半衰期指任一浓度 N2O消耗一半时所需的相应时间) ,则 T1

(3)某小组同学在室温下进行“碘钟实验”:将浓度均为 0.01mol·L-1的 H2O2、H2SO4、HI、Na2S2O3溶液及淀粉混合,一定时间后溶液变为蓝色。
已知:“碘钟实验”的总反应的离子方程式为 H2O2+2S2O
 +2H+=S4O
+2H+=S4O +2H2O
+2H2O反应分两步进行:
反应 A:……反应 B:I2+2S2O
 =2I-+S4O
=2I-+S4O
①反应 A 的离子方程式是
②为探究溶液变蓝快慢的影响因素,进行实验 Ⅰ、Ⅱ(溶液浓度均为 0.01mol·L-1)。
| 试剂 用量(mL) 序号 | H2O2溶液 | H2SO4溶液 | Na2S2O3溶液 | KI 溶液(含淀粉) | H2O |
| 实验 Ⅰ | 5 | 4 | 8 | 3 | 0 |
| 实验 Ⅱ | 5 | 2 | x | y | z |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐2】某兴趣小组探究外界因素对化学反应的影响,设计了下面两组实验。
I.探究反应物浓度对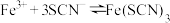 的影响
的影响
(1).在小烧杯中加入10mL蒸馏水,再滴入5滴0.05 FeCl3溶液、5滴0.15
FeCl3溶液、5滴0.15 KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为
KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为 。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
①配制100mL0.15 KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和
KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和____________ 。
②试管a和c是为了验证____________________________________ ,预测两支试管吸光度的大小关系:
η1__________ η3(填“>”“<”或“=”)。
③已知η2<η0,试用平衡移动原理解释此现象___________________________________________________ 。
II.用0.50 KI溶液、0.2%淀粉溶液、0.20
KI溶液、0.2%淀粉溶液、0.20 K2S2O8溶液、0.10
K2S2O8溶液、0.10 Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
已知: (慢)
(慢) 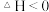

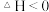
(2).向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色, 与
与 初始的物质的量需满足的关系为:
初始的物质的量需满足的关系为:
_______________ 。
(3).为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
表中Vx=__________ mL,理由是_______________________________________________________ 。
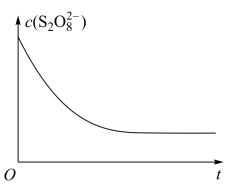
(4).已知某条件下,浓度 ~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时
~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时 ~t的变化曲线示意图(注意要进行必要的标注)
~t的变化曲线示意图(注意要进行必要的标注)___________ 。
I.探究反应物浓度对
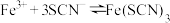 的影响
的影响(1).在小烧杯中加入10mL蒸馏水,再滴入5滴0.05
 FeCl3溶液、5滴0.15
FeCl3溶液、5滴0.15 KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为
KSCN溶液,用玻璃棒搅拌,使其充分混合,此时测得溶液吸光度为 。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):
。然后将溶液平均注入a、b、c三支试管中。按下列方案进行实验并记录溶液的吸光度(溶液颜色越深,吸光度越大):试管编号 | 加入试剂 | 吸光度 |
a | 5滴m1 | η1 |
b | 少量还原铁粉 | η2 |
c | 5滴蒸馏水 | η3 |
 KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和
KSCN溶液所需要用到的玻璃仪器有100mL容量瓶、烧杯和②试管a和c是为了验证
η1
③已知η2<η0,试用平衡移动原理解释此现象
II.用0.50
 KI溶液、0.2%淀粉溶液、0.20
KI溶液、0.2%淀粉溶液、0.20 K2S2O8溶液、0.10
K2S2O8溶液、0.10 Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。
Na2S2O3溶液等试剂,探究反应条件对化学反应速率的影响。已知:
 (慢)
(慢) 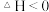

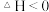
(2).向KI、Na2S2O3与淀粉的混合溶液中加入一定量的K2S2O8溶液,当溶液中的Na2S2O3耗尽后,溶液颜色将由无色变为蓝色,为确保能观察到蓝色,
 与
与 初始的物质的量需满足的关系为:
初始的物质的量需满足的关系为:
(3).为探究反应物浓度对化学反应速率的影响,设计的实验方案如下表:
实验序号 | 体积V/mL | ||||
K2S2O3溶液 | 水 | KI溶液 | Na2S2O3溶液 | 淀粉溶液 | |
① | 10.0 | 0.0 | 4.0 | 4.0 | 2.0 |
② | 9.0 | 1.0 | 4.0 | 4.0 | 2.0 |
③ | 8.0 | Vx | 4.0 | 4.0 | 2.0 |
(4).已知某条件下,浓度
 ~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时
~反应时间t的变化曲线如图,若保持其他条件不变,请在坐标图中,画出降低反应温度时 ~t的变化曲线示意图(注意要进行必要的标注)
~t的变化曲线示意图(注意要进行必要的标注)
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】乙酸亚铬水合物是红棕色晶体,其化学式为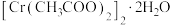 ,不溶于冷水、乙醇、乙醚,易溶于盐酸,非常不稳定,能够迅速被空气中的氧气氧化为三价铬。实验室常用锌粒、
,不溶于冷水、乙醇、乙醚,易溶于盐酸,非常不稳定,能够迅速被空气中的氧气氧化为三价铬。实验室常用锌粒、 和醋酸钠制备乙酸亚铬水合物,装置甲中依次观察到溶液中发生暗绿→绿→蓝绿→亮蓝一系列颜色变化,实验装置如图所示。请回答下列问题:
和醋酸钠制备乙酸亚铬水合物,装置甲中依次观察到溶液中发生暗绿→绿→蓝绿→亮蓝一系列颜色变化,实验装置如图所示。请回答下列问题:
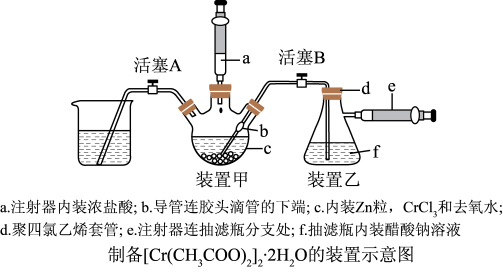
(1)装置甲中仪器c的名称为_______ 。
(2)装置乙中发生反应的离子方程式为_______ 。
(3)检查气密性良好后装入药品,活塞A和活塞B均为闭合状态,滴入浓盐酸时,应打开活塞_______ ,当_______ (描述实验现象)时,应关闭该活塞,打开另一个活塞。
(4)装置甲中的液体能够快速流入装置乙中的原因是_______ 。
(5)反应结束后,用布氏漏斗将所得混合物减压抽滤,先用去氧水洗3次,然后用少量乙醇、乙醚各洗涤3次,将产品铺于表面皿上,室温下干燥。用乙醇、乙醚洗涤的原因_______ 。
(6)某实验室探究减少盐酸的用量对实验进行改进,实验结果如表。试分析实验①产率较低的原因_______ 。实验⑤的优点有节约药品、_______ 。
稀释浓盐酸后的实验结果对比
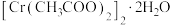 ,不溶于冷水、乙醇、乙醚,易溶于盐酸,非常不稳定,能够迅速被空气中的氧气氧化为三价铬。实验室常用锌粒、
,不溶于冷水、乙醇、乙醚,易溶于盐酸,非常不稳定,能够迅速被空气中的氧气氧化为三价铬。实验室常用锌粒、 和醋酸钠制备乙酸亚铬水合物,装置甲中依次观察到溶液中发生暗绿→绿→蓝绿→亮蓝一系列颜色变化,实验装置如图所示。请回答下列问题:
和醋酸钠制备乙酸亚铬水合物,装置甲中依次观察到溶液中发生暗绿→绿→蓝绿→亮蓝一系列颜色变化,实验装置如图所示。请回答下列问题:
(1)装置甲中仪器c的名称为
(2)装置乙中发生反应的离子方程式为
(3)检查气密性良好后装入药品,活塞A和活塞B均为闭合状态,滴入浓盐酸时,应打开活塞
(4)装置甲中的液体能够快速流入装置乙中的原因是
(5)反应结束后,用布氏漏斗将所得混合物减压抽滤,先用去氧水洗3次,然后用少量乙醇、乙醚各洗涤3次,将产品铺于表面皿上,室温下干燥。用乙醇、乙醚洗涤的原因
(6)某实验室探究减少盐酸的用量对实验进行改进,实验结果如表。试分析实验①产率较低的原因
稀释浓盐酸后的实验结果对比
 盐/g | 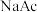 /g | 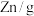 | 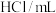 | 去氧水 /m | 产品 颜色 | 剩余 Zn/g | 理论 产量/g | 实际 产量/g | 产率 /% | |
①浓 ②  去氧水 去氧水③  去氧水 去氧水④  去氧水 去氧水⑤  去氧水 去氧水 | 2.5 2.5 2.5 2.5 2.5 | 2.5 2.5 2.5 2.5 2.5 | 4 3 3 3 3 | 5 4 3 2 1 | 0 1 2 3 4 | 深红棕 红棕 砖红 砖红 砖红 | 2 1.4 1.7 2.1 2.4 | 1.76 1.76 1.76 1.76 1.76 | 1.01 1.31 1.44 1.50 1.61 | 57 74 82 85 91 |
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐1】醋酸是常见的一元弱酸。请运用化学反应原理回答下列问题:
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=___________ mol·L-1该醋酸和pH=2的盐酸溶液相比,导电性___________ (填“相同”“不同”或“无法判断”)。
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是___________ 。
(3)向 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是___________ (填字母)。
a.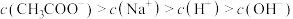
b.
c.
d.
(4)常温下,将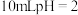 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
___________ (填“>”“<”或“=”)4;在醋酸稀释过程中下列数值变大的是___________ 。
A. B.
B. C.
C. D.
D.
(5)醋酸中存在平衡: ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。
(1)室温下,pH=2的醋酸中,水电离出的c(H+)=
(2)pH相同的盐酸和醋酸分别与足量的锌粒反应,生成等量的H2时所需时间较短的是
(3)向
 醋酸溶液中滴入
醋酸溶液中滴入 溶液,下列浓度大小顺序不可能出现的是
溶液,下列浓度大小顺序不可能出现的是a.
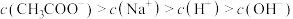
b.

c.

d.

(4)常温下,将
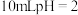 的醋酸溶液稀释至
的醋酸溶液稀释至 ,溶液的
,溶液的
A.
 B.
B. C.
C. D.
D.
(5)醋酸中存在平衡:
 ,下列措施可使醋酸的
,下列措施可使醋酸的 增大,并且电离平衡向右移动的是___________。
增大,并且电离平衡向右移动的是___________。A.加入 溶液 溶液 | B.加入盐酸 | C.加水稀释 | D.对醋酸溶液加热 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】甲、乙两同学设计确定HA为弱酸的实验方案如下:
甲:①称取一定质量的NaA,配制成0.1 mol·L-1的溶液100mL;
②室温下,用pH计测其pH,根据结果即可判定HA为弱酸。
乙:①量取一定体积的HA浓溶液,配制成0.1mol· L-l的溶液100mL;
②将上述溶液稀释100倍,室温下,用pH计测定稀释前后的pH,根据结果即可判定HA为弱酸。
(1)两个方案的步骤①中都要用到的定量仪器 是___________ 。
(2)甲方案若测得溶液的pH___________ 7(填写“>”、”<”或“=”),即可说明HA为弱酸,用离子方程式解释原因___________ 。
(3)乙方案中能说明HA为弱酸的依据是___________ 。
A.稀释后溶液的pH值大于稀释前的
B.稀释后溶液的pH值增大不到两个单位
C.稀释后,水的电离程度更大
(4)丙同学取乙同学配制的溶液和同浓度的盐酸,用如图所示的装置,控制相同条件,做两溶液的导电性实验,根据灯泡的亮度也可得出HA为弱酸的结论,其依据的实验现象是___________ 。

(5)请参考上述方案,改进乙同学的方案。要求只用乙配制的溶液,不用其他任何试剂(仪器任选)。你的方案(包括:操作、现象、结论)是___________ 。
甲:①称取一定质量的NaA,配制成0.1 mol·L-1的溶液100mL;
②室温下,用pH计测其pH,根据结果即可判定HA为弱酸。
乙:①量取一定体积的HA浓溶液,配制成0.1mol· L-l的溶液100mL;
②将上述溶液稀释100倍,室温下,用pH计测定稀释前后的pH,根据结果即可判定HA为弱酸。
(1)两个方案的步骤①中都要用到的
(2)甲方案若测得溶液的pH
(3)乙方案中能说明HA为弱酸的依据是
A.稀释后溶液的pH值大于稀释前的
B.稀释后溶液的pH值增大不到两个单位
C.稀释后,水的电离程度更大
(4)丙同学取乙同学配制的溶液和同浓度的盐酸,用如图所示的装置,控制相同条件,做两溶液的导电性实验,根据灯泡的亮度也可得出HA为弱酸的结论,其依据的实验现象是

(5)请参考上述方案,改进乙同学的方案。要求只用乙配制的溶液,不用其他任何试剂(仪器任选)。你的方案(包括:操作、现象、结论)是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】一定温度下,有 盐酸;
盐酸; 硫酸;
硫酸; 醋酸三种酸的稀溶液
醋酸三种酸的稀溶液 用a、b、c、
用a、b、c、 、
、 、
、 号填写
号填写
 当其物质的量浓度相同时,
当其物质的量浓度相同时, 由大到小的顺序是
由大到小的顺序是____________ ,
 同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是
同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是____________ ,
 当其
当其 相同时,物质的量浓度由大到小的顺序为
相同时,物质的量浓度由大到小的顺序为____________ ,
 当
当 相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气
相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气 相同状况
相同状况 ,则开始时反应速率的大小关系是
,则开始时反应速率的大小关系是____________ .
 将
将 相同的三种酸均加水稀释至原来的10倍,
相同的三种酸均加水稀释至原来的10倍, 由大到小的顺序为
由大到小的顺序为_____________ .
 盐酸;
盐酸; 硫酸;
硫酸; 醋酸三种酸的稀溶液
醋酸三种酸的稀溶液 用a、b、c、
用a、b、c、 、
、 、
、 号填写
号填写
 当其物质的量浓度相同时,
当其物质的量浓度相同时, 由大到小的顺序是
由大到小的顺序是 同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是
同体积同物质的量浓度的三种酸,中和NaOH能力由大到小的顺序是 当其
当其 相同时,物质的量浓度由大到小的顺序为
相同时,物质的量浓度由大到小的顺序为 当
当 相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气
相同、体积相同时,同时加入形状、质量、密度相同的锌,若产生相同体积的氢气 相同状况
相同状况 ,则开始时反应速率的大小关系是
,则开始时反应速率的大小关系是 将
将 相同的三种酸均加水稀释至原来的10倍,
相同的三种酸均加水稀释至原来的10倍, 由大到小的顺序为
由大到小的顺序为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】化学兴趣小组对某品牌牙膏中的摩擦剂成分及其含量进行以下探究:查得资料:该牙膏摩擦剂由碳酸钙、氢氧化铝组成;牙膏中其它成分遇到盐酸时无气体产生。利用下图所示装置(图中夹持仪器略去)进行牙膏样品中碳酸钙的定量测定实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:____
(2)C中反应生成BaCO3的化学方程式是__________________ 。
(3)下列各项措施中,不能提高测定准确度的是_________ (填标号)。
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为__________ 。
(5)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是_____
(6)上述实验中用到的氢氧化钠以食盐为原料进行生产的。食盐在生产生活中应用广泛,下图是以食盐为原料并综合利用的某些过程如下图所示。
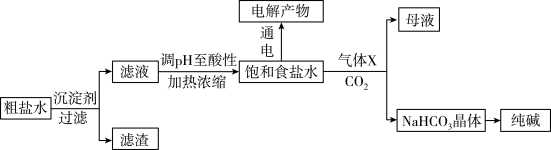
I.除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是(填字母)__________ 。
a.Na2CO3 b.NaOH c.BaCl2
Ⅱ.电解饱和食盐水可得到H2和另外两种产物,这两种物质相互反应的离子方程式为____________ ,欲从饱和食盐水中获得食盐晶体,可采用的实验方法是__________ 。
Ⅲ.气体X可增大饱和食盐水吸收CO2的量,有利于NaHCO3晶体的生成和析出,X的化学式是________ 。
Ⅳ.下列有关NaHCO3和纯碱的说法正确的是__________ (填字母)
A.NaHCO3属于盐类,纯碱属于碱
B.分别往同浓度的NaHCO3溶液和纯碱溶液中滴加稀盐酸,产生气泡的速率相同
C.常温下在水中的溶解度,NaHCO3大于纯碱
D.除去NaHCO3溶液中的纯碱,应往溶液中通入足量的CO2

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气。其作用除了可搅拌B、C中的反应物外,还有:
(2)C中反应生成BaCO3的化学方程式是
(3)下列各项措施中,不能提高测定准确度的是
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(4)实验中准确称取8.00 g样品三份,进行三次测定,测得BaCO3平均质量为3.94 g。则样品中碳酸钙的质量分数为
(5)有人认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以确定碳酸钙的质量分数。实验证明按此方法测定的结果明显偏高,原因是
(6)上述实验中用到的氢氧化钠以食盐为原料进行生产的。食盐在生产生活中应用广泛,下图是以食盐为原料并综合利用的某些过程如下图所示。

I.除去粗盐中的Ca2+、Mg2+和SO42-离子,加入下列沉淀剂的顺序是(填字母)
a.Na2CO3 b.NaOH c.BaCl2
Ⅱ.电解饱和食盐水可得到H2和另外两种产物,这两种物质相互反应的离子方程式为
Ⅲ.气体X可增大饱和食盐水吸收CO2的量,有利于NaHCO3晶体的生成和析出,X的化学式是
Ⅳ.下列有关NaHCO3和纯碱的说法正确的是
A.NaHCO3属于盐类,纯碱属于碱
B.分别往同浓度的NaHCO3溶液和纯碱溶液中滴加稀盐酸,产生气泡的速率相同
C.常温下在水中的溶解度,NaHCO3大于纯碱
D.除去NaHCO3溶液中的纯碱,应往溶液中通入足量的CO2
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】二氯化二硫 可作硫化剂、氯化剂。常温下,
可作硫化剂、氯化剂。常温下, 是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。
(1)选用以下装置制取少量 (加热及夹持装置略)。
(加热及夹持装置略)。

①写出A中发生反应的化学方程式_______ 。
②装置连接顺序:A→_______ 。
③B中玻璃纤维的作用是什么_______ ?
④D中盛放的试剂是什么_______ ?
(2) 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。

①W溶液可以是下列溶液中的_______ (填标号)。
a. 溶液 b.酸性
溶液 b.酸性 溶液 C.氯水 d.
溶液 C.氯水 d. 溶液
溶液
②计算混合气体中 的体积分数
的体积分数______ (用含 、
、 的代数式表示,不要求计算过程)。
的代数式表示,不要求计算过程)。
 可作硫化剂、氯化剂。常温下,
可作硫化剂、氯化剂。常温下, 是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。
是一种黄红色液体,沸点137℃,在潮湿的空气中剧烈水解而发烟。 可通过硫与少量氯气在110~140℃反应制得。
可通过硫与少量氯气在110~140℃反应制得。(1)选用以下装置制取少量
 (加热及夹持装置略)。
(加热及夹持装置略)。
①写出A中发生反应的化学方程式
②装置连接顺序:A→
③B中玻璃纤维的作用是什么
④D中盛放的试剂是什么
(2)
 遇水会生成
遇水会生成 、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中
、HCl两种气体,某同学设计了如下实验方案来测定该混合气体中 的体积分数。
的体积分数。
①W溶液可以是下列溶液中的
a.
 溶液 b.酸性
溶液 b.酸性 溶液 C.氯水 d.
溶液 C.氯水 d. 溶液
溶液②计算混合气体中
 的体积分数
的体积分数 、
、 的代数式表示,不要求计算过程)。
的代数式表示,不要求计算过程)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】在Al2O3催化剂和加热的条件下,丁烷发生完全裂解: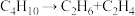 ,
,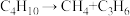 .某实验小组通过下列实验装置定性、定量测定丁烷裂解产物及其含量.
.某实验小组通过下列实验装置定性、定量测定丁烷裂解产物及其含量.
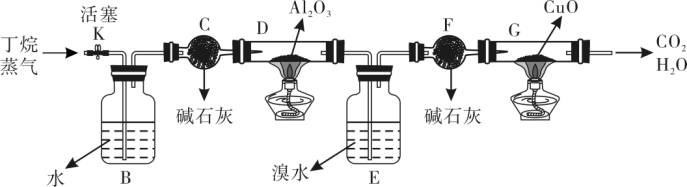
(1)C和F玻璃仪器的名称是________ ,F装置的作用是______ 。
(2)参考上述装置图,连接好各仪器,________ ,加入各试剂,排除装置中的空气,加热D和G装置…….B装置所起的作用是________ 。
(3)E装置中的实验现象是________ ;写出反应的化学方程式_______ 。(写出一个即可)
(4)E和F装置的总质量比反应前增加了0.7g,G装置的质量减少了1.28g,则丁烷的裂解产物中,甲烷的摩尔分数是x=_____ %
(提示1: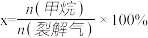 ;提示2:假定流经D、G装置中的气体能完全反应)
;提示2:假定流经D、G装置中的气体能完全反应)
(5)对E装置中的混合物再按以下流程实验:
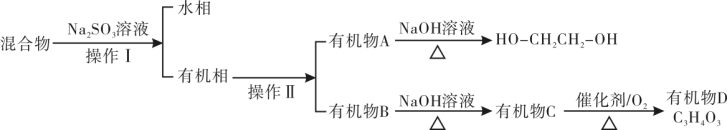
①Na2SO3溶液的作用是(用离子方程式表示)_________ ,分离操作Ⅱ名称是__________ 。
②有机物C的系统命名为_________ ,写出有机物C转变为D的化学反应方程式 ________ 。
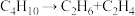 ,
,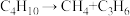 .某实验小组通过下列实验装置定性、定量测定丁烷裂解产物及其含量.
.某实验小组通过下列实验装置定性、定量测定丁烷裂解产物及其含量.
(1)C和F玻璃仪器的名称是
(2)参考上述装置图,连接好各仪器,
(3)E装置中的实验现象是
(4)E和F装置的总质量比反应前增加了0.7g,G装置的质量减少了1.28g,则丁烷的裂解产物中,甲烷的摩尔分数是x=
(提示1:
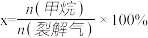 ;提示2:假定流经D、G装置中的气体能完全反应)
;提示2:假定流经D、G装置中的气体能完全反应)(5)对E装置中的混合物再按以下流程实验:

①Na2SO3溶液的作用是(用离子方程式表示)
②有机物C的系统命名为
您最近一年使用:0次



