第三代永磁体材料——钕铁硼(NdFeB)因其优异的综合磁性能,被广泛应用于计算机、通信信息等高科技产业
(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,NiO、FeO的晶体结构类型与氯化钠相同。基态钴原子价电子轨道表示式为___________ ,熔、沸点:NiO___________ (填“<”“>”或“=”)FeO
(2)新型储氢材料氨硼烷(NH3BH3)常温下以固体形式稳定存在,极易溶于水
①氨硼烷分子中B原子采取___________ 杂化
②氨硼烷晶体中存在的作用力有范德华力、极性键、___________ 和___________
(3)氨硼烷受热析氢的过程之一如图甲所示
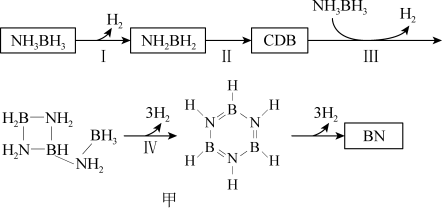
①NH2BH2的氮硼键键能大于NH3BH3,其原因为___________
②CDB的结构简式为___________
③立方氮化硼(BN)晶体的晶胞结构如图乙所示。设阿伏加德罗常数的值为NA,该晶体的密度为___________ g·cm-3(用含a和NA的最简式表示)。图丙是立方氮化硼晶胞的俯视投影图,请在图中用“ ”标明B原子的相对位置
”标明B原子的相对位置___________

(1)铁、钴、镍元素性质非常相似,原子半径接近但依次减小,NiO、FeO的晶体结构类型与氯化钠相同。基态钴原子价电子轨道表示式为
(2)新型储氢材料氨硼烷(NH3BH3)常温下以固体形式稳定存在,极易溶于水
①氨硼烷分子中B原子采取
②氨硼烷晶体中存在的作用力有范德华力、极性键、
(3)氨硼烷受热析氢的过程之一如图甲所示

①NH2BH2的氮硼键键能大于NH3BH3,其原因为
②CDB的结构简式为
③立方氮化硼(BN)晶体的晶胞结构如图乙所示。设阿伏加德罗常数的值为NA,该晶体的密度为
 ”标明B原子的相对位置
”标明B原子的相对位置
2023高三·全国·专题练习 查看更多[1]
(已下线)01 物质结构与性质综合题型集训(1) (解析)-备战2023年高考化学大题逐空突破系列(全国通用)
更新时间:2023-05-08 16:56:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】 是元素周期表前四周期中的四种常见元素,其相关信息如下表:
是元素周期表前四周期中的四种常见元素,其相关信息如下表:
(1)元素X的原子中能量最高的是_______ 电子,其电子云在空间有_______ 方向;它的氢化物的电子式是_______
(2)元素Y位于元素周期表的第三周期_______ 族。该原子的价电子排布图为_______ 。
(3)元素Z的原子最外层共有_______ 种不同运动状态的电子。
(4)元素Y与元素Z相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ 。
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
 是元素周期表前四周期中的四种常见元素,其相关信息如下表:
是元素周期表前四周期中的四种常见元素,其相关信息如下表: | 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且最高能级是半充满状态 |
| Y | 第三周期元素,它的单质是良好的半导体材料 |
| Z | Z和Y同周期,Z是本周期原子半径最小的主族元素 |
| W | W的一种核素的质量数为63,中子数为34 |
(2)元素Y位于元素周期表的第三周期
(3)元素Z的原子最外层共有
(4)元素Y与元素Z相比,非金属性较强的是
a.常温下,Y的单质与Z的单质状态不同
b.等物质的量浓度的氢化物水溶液的酸性不同
c.Z的电负性大于Y
d.Z的氢化物比Y的氢化物稳定
e.在反应中,Y原子得电子数比Z原子得电子数多
f.Z元素最高价氧化物对应水化物的酸性比Y元素最高价氧化物对应水化物的酸性强
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】自然界中存在大量的金属元素和非金属元素,它们在工农业生产中有着广泛的应用。
(1)纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,已知高温下Cu2O比CuO稳定。
①画出基态Cu原子的价电子轨道排布图_______ ;
②从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因_______ 。
(2)CuSO4溶液常用作农药、电镀液等,向CuSO4溶液中滴加足量浓氨水,直至产生的沉淀恰好溶解,再向其中加入适量乙醇,可析出深蓝色的Cu(NH3)4SO4·H2O晶体。
①Cu(NH3)4SO4·H2O晶体中存在的化学键有_______ (填字母序号)。
a.离子键 b.极性键 c.非极性键 d.配位键
② 的立体构型是
的立体构型是_______ ,其中S原子的杂化轨道类型是_______ 。
③已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是_______ 。
(3)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是_______ 。
(4)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),该反应是:
[Cu(NH3)2]Ac+CO+NH3 [Cu(NH3)3CO]Ac(醋酸羰基三氨合铜)(I) △H<0
[Cu(NH3)3CO]Ac(醋酸羰基三氨合铜)(I) △H<0
①C、N、O三种元素的第一电离能由小到大的顺序为_______ ;
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为_______ 。
(5)铜的化合物种类很多,如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a cm,则氯化亚铜密度的计算式为: =
=_______ g/cm3(用NA表示阿伏伽德罗常数)。

(1)纳米氧化亚铜(Cu2O)是一种用途广泛的光电材料,已知高温下Cu2O比CuO稳定。
①画出基态Cu原子的价电子轨道排布图
②从核外电子排布角度解释高温下Cu2O比CuO更稳定的原因
(2)CuSO4溶液常用作农药、电镀液等,向CuSO4溶液中滴加足量浓氨水,直至产生的沉淀恰好溶解,再向其中加入适量乙醇,可析出深蓝色的Cu(NH3)4SO4·H2O晶体。
①Cu(NH3)4SO4·H2O晶体中存在的化学键有
a.离子键 b.极性键 c.非极性键 d.配位键
②
 的立体构型是
的立体构型是③已知NF3与NH3的空间构型都是三角锥形,但NF3不易与Cu2+形成配离子,其原因是
(3)NaCl和MgO都属于离子化合物,NaCl的熔点为801.3℃,MgO的熔点高达2800℃。造成两种晶体熔点差距的主要原因是
(4)合成氨工业中,原料气(N2、H2及少量CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜(I)溶液来吸收原料气体中的CO(Ac-代表CH3COO-),该反应是:
[Cu(NH3)2]Ac+CO+NH3
 [Cu(NH3)3CO]Ac(醋酸羰基三氨合铜)(I) △H<0
[Cu(NH3)3CO]Ac(醋酸羰基三氨合铜)(I) △H<0①C、N、O三种元素的第一电离能由小到大的顺序为
②配合物[Cu(NH3)3CO]Ac中心原子的配位数为
(5)铜的化合物种类很多,如图是氯化亚铜的晶胞结构,已知晶胞的棱长为a cm,则氯化亚铜密度的计算式为:
 =
=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。
(1)画出A基态原子的核外电子排布图___________ 。
(2)C的基态原子的核外电子排布图 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背___________ 。
(3)D的基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(4)写出C原子的电子排布式___________ ;写出E原子的电子简化排布式___________ 。
(5)请写出F元素价电子排布式___________ 。
(6)写出微粒的核外电子排布式:28Ni___________ ;26Fe3+___________ ;
| A元素原子的核外p电子数比s电子数少3 |
| B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| C元素基态原子p轨道有3个未成对电子 |
| D原子核外所有p轨道全满或半满 |
| E在该周期中未成对电子数最多 |
| F能形成红色(或砖红色)和黑色的两种氧化物 |
(1)画出A基态原子的核外电子排布图
(2)C的基态原子的核外电子排布图
 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背(3)D的基态原子中能量最高的电子,其电子云在空间有
(4)写出C原子的电子排布式
(5)请写出F元素价电子排布式
(6)写出微粒的核外电子排布式:28Ni
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素符号A:___________ B:___________ G___________ ,写出元素B的基态原子的轨道表示式:___________ 。
(2)C、D、E三种元素的原子半径由大到小的顺序___________ 。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:___________ ,___________ ,___________ ,其中C的简单气态氢化物的键角为:___________ 。
(4)已知元素A、B形成的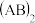 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为___________ 。
(5)F元素的简单阴离子结构示意图___________ 。电解D与F形成的化合物的水溶液在工业上有着重要应用,试写出其电解的总的化学反应方程式:___________ 。
(6)元素G位于周期表的___________ 区,其价电子的排布式为:___________ ,该元素可形成 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是___________ 。
(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是___________ 化合物(填“离子”或“共价”)。推测M的最高价氧化物对应水化物___________ (填“能”或“不能”)与D的最高价氧化物对应水化物发生反应。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属 |
(2)C、D、E三种元素的原子半径由大到小的顺序
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,其空间构型分别为:
(4)已知元素A、B形成的
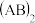 链状分子中所有原子都满足8电子稳定结构,则其分子中
链状分子中所有原子都满足8电子稳定结构,则其分子中 键与
键与 键之比为
键之比为(5)F元素的简单阴离子结构示意图
(6)元素G位于周期表的
 、
、 ,其中较稳定的是
,其中较稳定的是 ,原因是
,原因是(7)短周期元素M与元素E在周期表中的位置呈现对角线关系,已知元素M、F的电负性分别为1.5和3.0,预测它们形成的化合物是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】周期表中的七种元素T、X、Y、Z、Q、R、W原子序数依次递增,其中,W为第四周期元素,其余均为短周期主族元素。相关信息如下:
(1)X、Y、Q三种元素的电负性由大到小的顺序是___________ (用元素符号表示)。
(2)Y、R两元素电负性接近,但Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是___________ 。
(3)W的最高价含氧酸的分子式为___________ 。
(4)T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为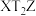 ,该分子空间构型为
,该分子空间构型为___________ ,是___________ (填“极性”或“非极性”)分子。
(5)X与Y原子结合形成的X3Y4晶体,其晶体结构与金刚石类似,但硬度比金刚石大,请解释原因是___________ 。
| 元素 | 原子结构信息 |
| T | 原子所处的周期数、族序数分别与其原子序数相等 |
| X | 基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同 |
| Z | 基态原子价电子排布为ns2npn+2 |
| Q | 在该元素所在周期中,其基态原子的第一电离能最小 |
| R | 单质常温常压下是气体,其基态原子的层上有1个未成对的p电子 |
| W | 与R同主族,单质常温下是液体 |
(2)Y、R两元素电负性接近,但Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是
(3)W的最高价含氧酸的分子式为
(4)T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为
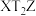 ,该分子空间构型为
,该分子空间构型为(5)X与Y原子结合形成的X3Y4晶体,其晶体结构与金刚石类似,但硬度比金刚石大,请解释原因是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】有A、B、C、D、E五种元素。其相关信息如下:
请回答下列问题:
(1)写出E元素原子基态时的电子排布式_______ 。
(2)C元素的第一电离能比氧元素的第一电离能_____ (填“大”或“小”)。
(3)CA3分子中C原子的杂化轨道类型是______ ,CA3分子的空间构型是_____ 。
(5)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有________ (填序号)。
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
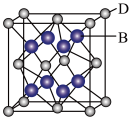
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为_______ 。
| 元素 | 相关信息 |
| A | A原子的1s轨道上只有1个电子 |
| B | B是电负性最大的元素 |
| C | C的基态原子2p轨道中有三个未成对电子 |
| D | D是主族元素且与E同周期,其最外能层上有两个运动状态不同的电子 |
| E | E能形成红色(或砖红色)的E2O和黑色的EO两种氧化物 |
请回答下列问题:
(1)写出E元素原子基态时的电子排布式
(2)C元素的第一电离能比氧元素的第一电离能
(3)CA3分子中C原子的杂化轨道类型是
(5)A、C、E三种元素可形成[E(CA3)4]2+配离子,其中存在的化学键类型有
①配位键 ②金属键 ③极性共价键 ④非极性共价键 ⑤离子键 ⑥氢键
(5)B与D可形成离子化合物,其晶胞结构如图所示。其中D离子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硫、钒化合物在药物化学及催化化学等领域应用广泛。回答下列问题:
(1)基态钒原子的价层电子排布图为_______ ,钒有+2、+3、+4、+5等多种化合价,其中最稳定的化合价是_______ , 的空间构型为
的空间构型为_______ 。
(2)2-巯基烟酸氧钒配合物(图甲)是副作用小的有效调节血糖的新型药物:
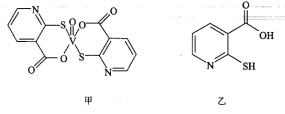
该药物中N原子的杂化方式是_______ ;2-巯基烟酸(图乙)水溶性优于2-巯基烟酸氧钒配合物(图甲)的原因是_______ 。
(3)某六方硫钒化合物晶体的晶胞如图丙所示,该晶胞的化学式为_______ 。图丁为该晶胞的俯视图,该晶胞的密度为_______  (列出计算式即可)。
(列出计算式即可)。

(1)基态钒原子的价层电子排布图为
 的空间构型为
的空间构型为(2)2-巯基烟酸氧钒配合物(图甲)是副作用小的有效调节血糖的新型药物:

该药物中N原子的杂化方式是
(3)某六方硫钒化合物晶体的晶胞如图丙所示,该晶胞的化学式为
 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】利用物质的结构与性质对周期表进行研究,有助于我们更好地掌握同类知识。
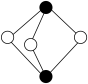
(1)基态砷原子中,价电子占用_____ 个原子轨道;雌黄分子式为As2S3,分子结构如图所示,则砷原子的杂化方式为______ 。
(2)现代化学中,常利用_______ 上的特征谱线来鉴定元素,Ga的价层电子排布式为________ 。
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,该配离子中含有的化学键类型有______ (填字母序号)。
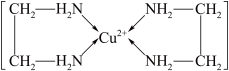
A.配位键 B.极性键 C.离子键 D.非极性键
(4)元素的基态气态原子得到一个电子形成气态-l价离子时所放出的能量称作第一电子亲和能(E),-l价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如表所示。
下列说法正确的是________ 。
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O-时放出141kJ的能量
C.氧元素的第二电子亲和能是-780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(5)铁和氨气在640°C可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式__ 。
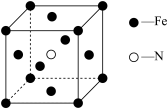
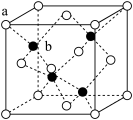
(6)立方硫化锌晶胞与金刚石晶胞类似,结构如图,其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位数为___ ,若晶体的密度为ρg•cm-3,则晶胞的体积为____ cm3
(1)基态砷原子中,价电子占用

(2)现代化学中,常利用
(3)Cu2+能与乙二胺(H2N—CH2—CH2—NH2)形成配离子如图,该配离子中含有的化学键类型有

A.配位键 B.极性键 C.离子键 D.非极性键
(4)元素的基态气态原子得到一个电子形成气态-l价离子时所放出的能量称作第一电子亲和能(E),-l价阴离子再获得一个电子的能量变化叫做第二电子亲和能,部分元素或离子的电子亲和能数据如表所示。
| 元素 | Cl | Br | I | O | O- |
| 电子亲和能(kJ/mol) | 349 | 343 | 295 | 141 | -780 |
下列说法正确的是
A.电子亲和能越大,说明越难得到电子
B.一个基态的气态氧原子得到一个电子成为O-时放出141kJ的能量
C.氧元素的第二电子亲和能是-780kJ/mol
D.基态的气态氧原子得到两个电子成为O2-需要吸收能量
(5)铁和氨气在640°C可发生置换反应,产物之一的晶胞结构如图所示,写出该反应的化学方程式

(6)立方硫化锌晶胞与金刚石晶胞类似,结构如图,其中a代表S2-,b代表Zn2+。则该晶胞中S2-的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】现有A、B、C、D、E五种短周期非金属元素,其原子序数依次增大。A是原子半径最小的元素,B元素的一种核素可用于考古断代,D元素的s轨道和p轨道上的电子数相等。C、E是同主族元素,它们的核外均有3个未成对电子。请回答下列问题:
(1)基态E原子有_____ 种能量不同的电子。
(2)六种元素中,电负性最大的是_______ ,第一电离能最大的是________ (均填元素符号)。
(3)化合物CA3的沸点比化合物BA4的沸点高,其主要原因是____________ 。
(4)CD2-的立体构型是________ ,其中C原子的杂化类型为___________ 。
(5)C2A4溶于水电离方程式与CA3溶于水电离方程式相似,试写出C2A4在水溶液中的电离方程式____ (写一步即可,要求用化学符号表示)。
(6)开发金属储氢材料是氢能的重要研究方向。MgA2是一种储氢材料,其晶胞结构如下图所示:
已知该晶胞的体积为Vcm3,则该晶胞的密度为_______ g·cm-3(用V和NA表示)。
(1)基态E原子有
(2)六种元素中,电负性最大的是
(3)化合物CA3的沸点比化合物BA4的沸点高,其主要原因是
(4)CD2-的立体构型是
(5)C2A4溶于水电离方程式与CA3溶于水电离方程式相似,试写出C2A4在水溶液中的电离方程式
(6)开发金属储氢材料是氢能的重要研究方向。MgA2是一种储氢材料,其晶胞结构如下图所示:
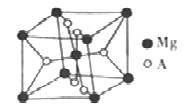
已知该晶胞的体积为Vcm3,则该晶胞的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)基态Fe原子有______ 个未成对电子,Fe3+的电子排布式为______ 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为______ 。
(2)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。1mol乙醛分子中含有的键的数目为______ 。乙醛中碳原子的杂化轨道类型为______ ,乙酸的沸点明显高于乙醛,其主要原因是______ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______ 个铜原子。
(3)Al单质为面心立方晶体,其晶胞边长a0.405nm,晶胞中铝原子的配位数为______ 。列式表示Al单质的密度______ gcm-3。(阿伏加 德罗常数用NA表示)
(1)基态Fe原子有
(2)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。1mol乙醛分子中含有的键的数目为
(3)Al单质为面心立方晶体,其晶胞边长a0.405nm,晶胞中铝原子的配位数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____ ,与钛同周期的元素中,基态原子的未成对电子数与钛相同的元素分别是____ (填元素符号)。
(2)在浓的TiCl 3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配合物的化学式为______ ; 1mol该配合物中含有σ键的数目_______ 。
(3)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。
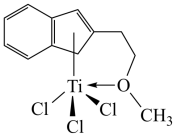
①组成M的元素中,电负性最大的是_________ (填名称)。
②M中非金属元素的第一电离能大小顺序_________ 。
③M中不含________ (填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(4)金红石(TiO 2)是含钛的主要矿物之一。其晶胞是典型的四方晶系,结构(晶胞中相同位置的原子相同)如图所示。
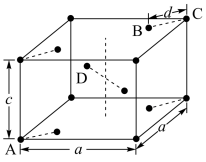
若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____ ,___ );钛氧键的键长d=______ (用代数式表示)。
(1)基态钛原子的价电子排布式为
(2)在浓的TiCl 3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1∶5,则该配合物的化学式为
(3)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是
②M中非金属元素的第一电离能大小顺序
③M中不含
a.π键 b.σ键 c.离子键 d.配位键
(4)金红石(TiO 2)是含钛的主要矿物之一。其晶胞是典型的四方晶系,结构(晶胞中相同位置的原子相同)如图所示。

若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】东晋《华阳国志·南中志》卷四中关于白铜的记载——云南镍白铜(铜镍合金),曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)Ni基态原子的电子排布式为___________ ;它在元素周期表中的位置___________ 。
(2)单质铜及镍都是由___________ 键形成的晶体;元素铜与镍的第二电离能分别为:Icu=1958kJ•mol-1、INi=1753kJ•mol-1,Icu>INi的原因是___________ 。
(3)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。
2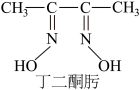 +Ni2+→
+Ni2+→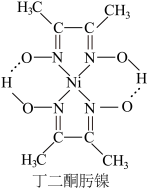 ↓+2H+
↓+2H+
①1mol丁二酮肟分子中含有σ键的数目为___________ mol。
②丁二酮肟镍分子中碳原子的杂化轨道类型为___________ 。
(4)Ni的晶胞结构如图所示,镍晶体配位数目是___________ ;若Ni的原子半径为dpm,Ni的密度计算表达式是___________ g/cm3(Ni的相对原子量用Mr表示)。
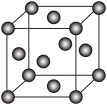 (Ni的晶胞结构)
(Ni的晶胞结构)
(1)Ni基态原子的电子排布式为
(2)单质铜及镍都是由
(3)Ni2+与丁二酮肟生成鲜红色丁二酮肟镍沉淀,该反应可用于检验Ni2+。
2
 +Ni2+→
+Ni2+→ ↓+2H+
↓+2H+①1mol丁二酮肟分子中含有σ键的数目为
②丁二酮肟镍分子中碳原子的杂化轨道类型为
(4)Ni的晶胞结构如图所示,镍晶体配位数目是
 (Ni的晶胞结构)
(Ni的晶胞结构)
您最近一年使用:0次



